制取甲烷的最佳反應溫度探究
闕榮輝+李嵌+吳鳳兮+熊言林

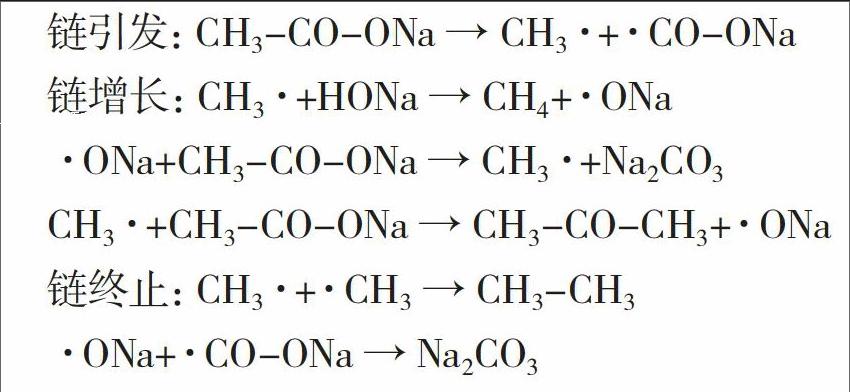
摘要:針對制取甲烷的傳統實驗方法存在的不足進行了實驗探究。2.5g的反應混合物,用高溫熱電偶傳感器直接探測實時反應溫度,通過記錄反應的溫度變化曲線和反應的產氣速率確定反應的最佳溫度。實驗結果表明,采用反應物配比為無水醋酸鈉:堿石灰:氫氧化鈉=2:1:1時,反應產生氣體的最佳溫度在500℃上下,整個氣體制備過程約5min左右。本實驗溫度探測、數據記錄直接,用時短,實驗結果可靠性強。能指導并幫助教師和學生方便有效地制備甲烷氣體并進行甲烷的性質實驗。
關鍵詞:甲烷;制取;反應溫度;熱電偶;傳感器
文章編號:1005-6629(2015)11-0059-04 中圖分類號:G633.8 文獻標識碼:B
甲烷作為最簡單的有機化合物,是中學生認識有機化合物的起點,因而,其制備和性質教學在中學化學教學中具有重要意義。傳統實驗方法采用無水醋酸鈉與堿石灰以1:3混合,反應速度慢,產氣率低,副產物多且容易失敗。國內研究者對于反應物配比、實驗裝置的優化、催化劑的選擇、副反應的影響等進行了多次探究,但都未對甲烷制備反應的最佳溫度進行深入探討。在有機化學反應中,溫度是非常重要的條件,也是實驗過程中不易控制的。而且,固體反應物溫度實時探測和氣體產生速率確定的困難也是鮮有人探究的重要原因之一。鑒于此,本文將使用高溫熱電偶傳感器直接探測反應的實時溫度,有效消除了反應時加熱強度不易控制帶來的影響;通過收集反應產生的甲烷氣體速率與反應溫度的變化曲線確定甲烷制備的最佳反應溫度。為甲烷制備與性質實驗提供指導與幫助,以期獲得理想的實驗教學效果。
1 反應物準備與實驗儀器選擇
1.1反應物的準備
總結國內一些研究者的研究結果可以歸納出以下影響實驗成功的因素:
(1)市售堿石灰的成分氫氧化鈉的含量較低不適合本實驗;
(2)適量的反應物比例才能促進反應進行;
(3)實驗的副反應生成了丙酮,影響甲烷的性質實驗;
(4)實驗的堿石灰和無水醋酸鈉不干燥,影響了甲烷的制備;
(5)加熱方式、副產物的冷凝、堿在強熱下腐蝕玻璃易導致試管的炸裂;
(6)使用鋁箔小舟裝載反應物可以防止堿與試管直接接觸導致試管損壞。
根據以上因素分析,本實驗結合優秀的研究成果給出最佳的反應物配比,無水醋酸鈉:堿石灰:氫氧化鈉=2:1:1,堿石灰使用前在蒸發皿內由淺紅色灼燒至灰白色,再先后與無水醋酸鈉、氫氧化鈉一起混合,研磨后備用。
1.2實驗條件及熱源的選擇
甲烷制備反應原理為:
堿石灰中的生石灰CaO起到了干燥劑和使反應物疏松甲烷易于逸出的作用。關于甲烷制備的反應機理有兩種理解,一種認為反應為離子型反應,甲基碳負離子奪取水中的氫生成甲烷;另一種認為反應為游離基反應。
無論哪種機理都需要將反應物加熱至熔融狀態,且反應體系中須盡可能要保持無水狀態才能使反應順利進行。
1.2.1最佳反應溫度推測
無水醋酸鈉的熔點為324℃,氫氧化鈉的熔點為327.6℃,基于以上分析估計反應在溫度達到二者熔點之后才開始進行。該反應是吸熱反應,當反應物達到熔融狀態之后仍需要加熱。隨著溫度的上升,反應速度加快,產生的氣體增多,直到反應結束。
由上面推測可知,反應開始的溫度應該在330℃以上,反應溫度較高,通過沙浴、油浴加熱已不能滿足實驗需要;若改用控溫效果好的馬沸爐卻不能收集反應產生的氣體,反應體系的實時溫度也不易探測;改用酒精噴燈則溫度過高,試管不能承受。最后選擇酒精燈作為加熱源,這更接近教師實驗教學時的反應環境,希望所得的實驗結果能幫助教師在教學過程中更好地完成實驗。
1.2.2高溫熱電偶傳感器校驗
在室溫為15.8℃時,使用高溫熱電偶溫度傳感器測試沸騰的水的溫度,兩次分別顯示穩定在99.0℃和99.1℃。說明傳感器測試正常。
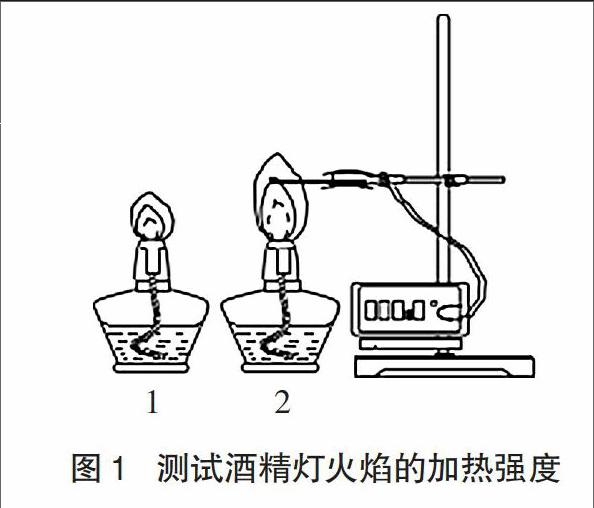
1.2.3酒精燈加熱強度討論
實驗中用到以下兩個酒精燈,1號酒精燈燈芯比較細短,火焰比較小;2號酒精燈燈芯比較粗長,火焰比較大。分別用高溫熱電偶傳感器探測兩個酒精燈的外焰溫度,見圖1。發現兩個酒精燈的外焰加熱溫度都能達到850℃左右,1號酒精燈由室溫加熱到850℃平均用時約11秒左右,而2號酒精燈需要約7秒。2號酒精燈的加熱強度略高于1號酒精燈。實驗中將討論加熱強度不同時對甲烷制備實驗產生的影響。
1.3實驗儀器與裝置
反應裝置中使用鋁箔槽防止試管破裂。將高溫熱電偶埋人平鋪在鋁箔槽(小舟)上的反應混合物中,另一端連接數據采集器以探測實時反應的溫度,氣體的收集用排水集氣法收集于倒扣在水槽中的500mL大量筒中,實驗裝置見圖2。
2 實驗步驟和現象
2.1排除實驗中可能出現的鋁箔與氫氧化鈉反應
鋁在氫氧化鈉溶液中能發生劇烈的反應:2AI+2NaOH+2H2O=2NaAlO2+3H2↑。為了排除該反應的影響進行如下表1實驗。
實驗用的堿石灰全部都由淺紅色塊狀研磨成粉末后灼燒至灰白色,反應物按照無水醋酸鈉:堿石灰:氫氧化鈉=2:1:1的比例混合,經由同一個酒精燈加熱。
比較反應后實驗1和實驗4的鋁箔小舟發現兩者基本保持原有的金屬光澤,沒有受到腐蝕。實驗1的反應物結塊成一體,實驗4的反應物基本保持在反應前的粉末狀,僅有少量結塊。在實驗4加熱后的小舟和反應物中滴加少量水,立即發生劇烈反應,鋁箔小舟被腐蝕放出大量氣泡和熱量,反應最后鋁箔小舟被嚴重腐蝕,表面也失去金屬光澤呈灰黑色。
由實驗1、2、3、4可知:
(1)在反應體系無水情況下即使加熱到400℃,氫氧化鈉與鋁箔也不發生反應,可以排除鋁箔小舟與混合物中氫氧化鈉發生反應的可能。
(2)甲烷的制備反應在350℃左右開始有氣體生成,是否與反應物的質量和加熱源的強弱有關還需要進一步的實驗驗證。
2.2甲烷制備反應溫度隨時間變化的探究
針對上一組實驗中存在的問題,進行了第二組對比實驗,見表2。反應物配比等同上。
實驗5、6、7分別用不同質量的反應物和不同加熱強度的酒精燈來進行實驗,并記錄反應溫度在200℃之后到反應結束不再產生氣體這段時間內變化,然后繪制溫度隨時間變化的曲線,見圖3。
根據以上實驗結果可知:
(1)實驗選擇酒精燈加熱強度不同,會影響反應的總時間和反應速度的快慢,其中熱源加熱強度越大,反應體系溫度上升越快,氣體生成速率越快,反應結束越早;
(2)反應物質質量的多少會影響反應的總時間,反應物質質量越多需要的反應時間越長,反應的總時間受到熱源和反應物質質量多少的共同影響;
(3)反應的熱源加熱強度不會影響反應發生開始產生氣體的溫度與結束溫度,反應物質質量的多少也不會改變反應的開始與結束溫度。通過數據采集器的記錄可知開始產生氣體的溫度在350℃左右,反應結束的溫度在510℃左右。
2.3
甲烷制備反應氣體生成速率隨溫度變化的探究
根據以上結果設計了第三組實驗,探究不同溫度區間氣體生成的速率,見表3。
用500mL大量筒收集產生的氣體,記錄不同溫度區間內產生的氣體體積和溫度區間內經過的時間,其中從開始產生氣體到不再產生氣體的這段時間記錄為反應總時間。計算不同溫度區間內反應的氣體生成速率并繪制條形統計表見圖4。
由實驗結果可以看出,在熱源加熱強度不同和反應物質量不同的條件下,實驗開始產生氣體溫度和實驗結束的溫度符合前兩組實驗的結果:即在350℃左右開始產生氣體,在510℃左右反應結束。由圖4可以看出在不同的溫度區間內反應的氣體生成速率表現出以下幾點規律:
(1)隨著溫度的上升氣體的生成速率逐漸增大,且在440℃之后增大的幅度明顯加快,在500℃附近氣體生成速率出現了峰值,在出現峰值之后氣體生成速率開始下降至反應結束。
(2)實驗表明甲烷的氣體生成速率與加熱強度有關,由圖4可見,加熱強度大的實驗9氣體產生速率明顯高于實驗8的氣體產生速率,但兩個實驗的速率增長趨勢相同。
(3)實驗8、9同時表現出均勻產氣的時間約為120s左右,且在到達500℃氣體生成速率峰值之后實驗也趨于結束。整個實驗的加熱時間約在五分鐘左右,時間較短適合在課堂進行演示實驗。
3 實驗結果與討論
3.1實驗結果
從上述系列實驗的結果可知:
(1)反應開始產生氣體的溫度(350℃)和反應結束的溫度(510℃)不受熱源加熱強度和反應物質量多少的影響;
(2)甲烷氣體的生成速率與熱源的加熱強度呈正相關;
(3)甲烷制備過程中均勻產氣時間約為120s左右,整個加熱制備過程約5min左右。
3.2甲烷制備實驗副反應產物的影響
影響實驗的副產物主要是乙烷和丙酮。研究表明反應的主要副產物為丙酮(乙烷的量很少),采用排水集氣法收集后可以除去。所以實驗的副反應產物對甲烷產氣速率的影響可以基本排除。
3.3實驗結論
甲烷制備實驗的最佳條件是:當反應物配比為無水醋酸鈉:灼燒除水的堿石灰:氫氧化鈉=2:1:1時,試管內使用鋁箔小舟裝載混合反應物2.5g左右,反應產生氣體的最佳溫度在500℃左右。
本系列實驗利用高溫熱電偶傳感器直接探測反應物的實時溫度,突破了固體反應物溫度探測的難點。更重要的是,本實驗通過反應溫度隨加熱時間的變化曲線和反應產氣速率的統計來確定反應最佳溫度,有效地保障了實驗結果的科學性。該實驗結論對于課堂演示或探究甲烷的制備和性質實驗過程有很好的指導作用,能夠幫助教師和學生更好地完成整個實驗,對于甲烷及相關知識的學習起到了有效的促進作用。

