黃芩莖葉總黃酮對阿爾茨海默病大鼠海馬神經元Bax和Bcl-2蛋白表達的影響
王瑞婷 董雅潔 左彥珍 關麗華 丁 實
(承德醫學院藥理教研室,河北 承德 067000)
黃芩莖葉總黃酮對阿爾茨海默病大鼠海馬神經元Bax和Bcl-2蛋白表達的影響
王瑞婷董雅潔左彥珍關麗華丁實
(承德醫學院藥理教研室,河北承德067000)
〔摘要〕目的探討黃芩莖葉總黃酮(SSTF)對大鼠海馬注射淀粉樣蛋白Aβ25~35所致神經元Bax和Bcl-2蛋白表達的影響。方法40只雄性Wistar大鼠按隨機數字表法分為對照組、模型組、SSTF 50 mg/kg、100 mg/kg組,每組10只。模型組、SSTF組大鼠于灌胃第8天雙側海馬注射Aβ 10 μg,對照組大鼠海馬注射生理鹽水,大鼠于灌胃20 d后處死。采用TUNEL法觀察大鼠海馬神經元凋亡;免疫組化、Western印跡檢測海馬組織中Bax、Bcl-2的表達,采用光密度值(IOD)表示實驗結果。結果模型組大鼠海馬細胞凋亡IOD較對照組明顯升高(P<0.01),50、100 mg/kg給藥組IOD較模型組明顯降低(P<0.01);免疫組化及Western印跡結果顯示模型組Bax表達較對照組明顯升高(P<0.01),SSTF 50、100 mg/kg組Bax表達較模型組明顯降低(P<0.01);模型組Bcl-2較對照組明顯降低(P<0.01),SSTF 50、100 mg/kg組Bcl-2表達較模型組明顯升高(P<0.01)。結論大鼠海馬注射Aβ25~35可引起海馬神經元凋亡,其機制可能與Aβ 上調凋亡基因Bax表達、降低抗凋亡基因Bcl-2表達有關。SSTF可減輕Aβ引起的神經元凋亡,其機制可能與其調控Bax、Bcl-2表達有關。
〔關鍵詞〕阿爾茨海默病;淀粉樣蛋白;黃芩莖葉總黃酮;神經元凋亡;Bax;Bcl-2
淀粉樣蛋白(Aβ)作為阿爾茨海默病(AD)發病的始動因子已得到廣泛的認可〔1〕。前期研究已顯示黃芩莖葉總黃酮(SSTF)能減輕海馬注射Aβ引起的大鼠學習記憶能力減退,減輕海馬CA1區神經元的脫失和超微結構損傷,且其效應與SSTF的抗氧化作用有關〔2,3〕。體內凋亡和抗凋亡失衡與神經退行性疾病有關,有研究報道Aβ體內、體外均可引起神經元凋亡〔4,5〕,也有實驗研究黃酮類化合物的體內、體外抗神經元凋亡作用〔6〕,但SSTF體內對神經元凋亡的影響未見報道。本研究探討SSTF對Aβ致AD大鼠海馬神經元凋亡及與凋亡相關蛋白Bax、Bcl-2表達的影響。
1材料與方法
1.1實驗動物雄性Wistar大鼠40只,10~12周齡,體質量(280±20)g,動物證號0289310,北京華阜康生物科技股份有限公司提供,許可證號SCXK(京)2009-0004,SPF級,全部實驗在SPF動物實驗室進行,實驗室合格證號:SYXK(冀2009-0022)。動物室溫度(22±2)℃,濕度(50±5)%,自由攝食飲水。
1.2試劑Aβ25~35購自Sigma公司,HPLC≥97%,SSTF由承德醫學院中藥研究所提供,純度61.88%。脫氧核糖核苷酸末端轉移酶介導的缺口末端標記法(TUNEL)細胞凋亡檢測試劑盒購自羅氏公司,山羊抗兔Bcl-2多抗(Lot:K2206)、山羊抗兔Bax多抗(Lot:E1607)、小鼠β-actin 單抗購自 SANTA CRUZ公司。SP9000、SP9002免疫組化試劑盒、山羊抗兔IgG/辣根過氧化物酶標記(Lot:73399)購自中杉金橋公司。RIPA強裂解液購自碧云天生物技術研究所,BCA蛋白定量試劑盒購自上海炎彬化工科技有限公司。ECL超敏發光液購自北京普利萊基因技術有限公司,PVDF膜Millipore 公司產品。
1.3試劑的配制Aβ25~351 mg溶于500 μl無菌生理鹽水(2 g/L),-20℃保存,臨用前置于37℃孵育5~7 d成凝膠態。黃芩莖葉總黃酮溶于蒸餾水中,調pH值為中性,現用現配,用前置室溫,搖勻。
1.4方法
1.4.1實驗動物分組及AD模型制作雄性Wistar 大鼠40只,隨機數字表法分為對照組、模型組、SSTF 50、100 mg/kg組,每組10只。對照組和模型組大鼠給予蒸餾水灌胃,給藥組灌胃總黃酮,1次/d,連續20 d,于大鼠前囟后(AP)-3.5 mm,左右旁開(ML)±2 mm,進針深度(DV)2.7 mm定位海馬CA1區,灌胃第8天對照組雙側海馬各注射5 μl的無菌生理鹽水,其他組雙側海馬各注射Aβ25~355 μl含10 μg制作AD模型。所有動物于灌胃第20天處死,每組取4只大鼠腦組織制作石蠟標本。
1.4.2TUNEL檢測石蠟切片脫蠟、水合,細胞通透,加入TUNEL反應液,加converter-POD,DAB顯色,蘇木素復染,梯度酒精脫水,二甲苯透明,中性樹膠封片。以胞質或胞核著棕黃色為凋亡陽性細胞。
1.4.3免疫組化切片經二甲苯脫蠟,梯度酒精水合,95℃水浴抗原修復,滴加Ⅰ抗孵育37℃ 2.5 h,Ⅰ抗濃度分別為兔抗Bax多抗(1∶100)、兔抗Bcl-2多抗(1∶75)。Ⅱ抗孵育37℃ 15 min,DAB顯色,蘇木素復染,中性樹膠封片,用PBS液代替一抗為陰性對照。
1.4.4TUNEL、免疫組化陽性細胞累積光密度測定每組選取4只大鼠腦組織石蠟標本,光鏡下每個標本選注射部位附近海馬CA1區2張切片,400倍視野下采用image-pro plus軟件進行光密度測定。
1.4.5Western印跡蛋白提取及定量:稱取每組6只大鼠的海馬組織0.15~0.2 g加1 ml PBS-NaF,研磨(冰上操作)、離心、裂解、蛋白定量采用BCA試劑盒,按說明書操作。制膠、上樣、凝膠電泳、轉膜、封閉過夜,Ⅰ抗孵育,Ⅰ抗濃度分別為兔抗Bax多抗(1∶200)、兔抗Bcl-2多抗(1∶100)、β-actin單抗(1∶1 000),Ⅱ抗孵育2 h,Ⅱ抗濃度山羊抗兔IgG/辣根過氧化物酶標記1∶3 000,顯影、定影。 光密度值測定:膠片掃描后采用Gelpro4軟件測定灰度值,每個組織每個指標的灰度值與該組織的β-actin灰度值相比。
1.5統計學方法采用SPSS11.5軟件進行單因素方差分析。
2結果
2.1SSTF對大鼠海馬神經元凋亡的影響TUNEL檢測發現模型組大鼠海馬神經元多數細胞核呈棕黃色,對照組大鼠海馬神經元核著色細胞少,著色淺,SSTF組較模型組著色淺,著色細胞少,見圖1。模型組IOD〔(40.41±9.1)×103〕較對照組〔(7.77±1.8)×103〕明顯升高(P<0.01);SSTF 50 mg/kg和100 mg/kg組IOD〔(20.80±4.4)×103vs(12.56±4.5)×103〕明顯低于模型組(P<0.01)。
2.2SSTF對大鼠海馬神經元Bax、Bcl-2表達的影響(免疫組化)模型組大鼠海馬CA1區Bax免疫組化IOD較對照組明顯升高;SSTF組IOD較模型組明顯降低,見表1。Bax在大鼠海馬神經元胞質呈棕黃色顆粒狀,模型組海馬CA1區多數神經元胞質黃染,較對照組著色深,SSTF組較模型組著色淺,見圖2。Bcl-2在大鼠海馬神經元胞質中呈棕黃色,模型組海馬CA1區著色細胞數比對照組少,著色淺,SSTF組較模型組著色細胞多,著色深,見圖3。模型組海馬CA1區Bcl-2免疫組化IOD明顯低于對照組,SSTF組IOD明顯高于模型組,見表1。
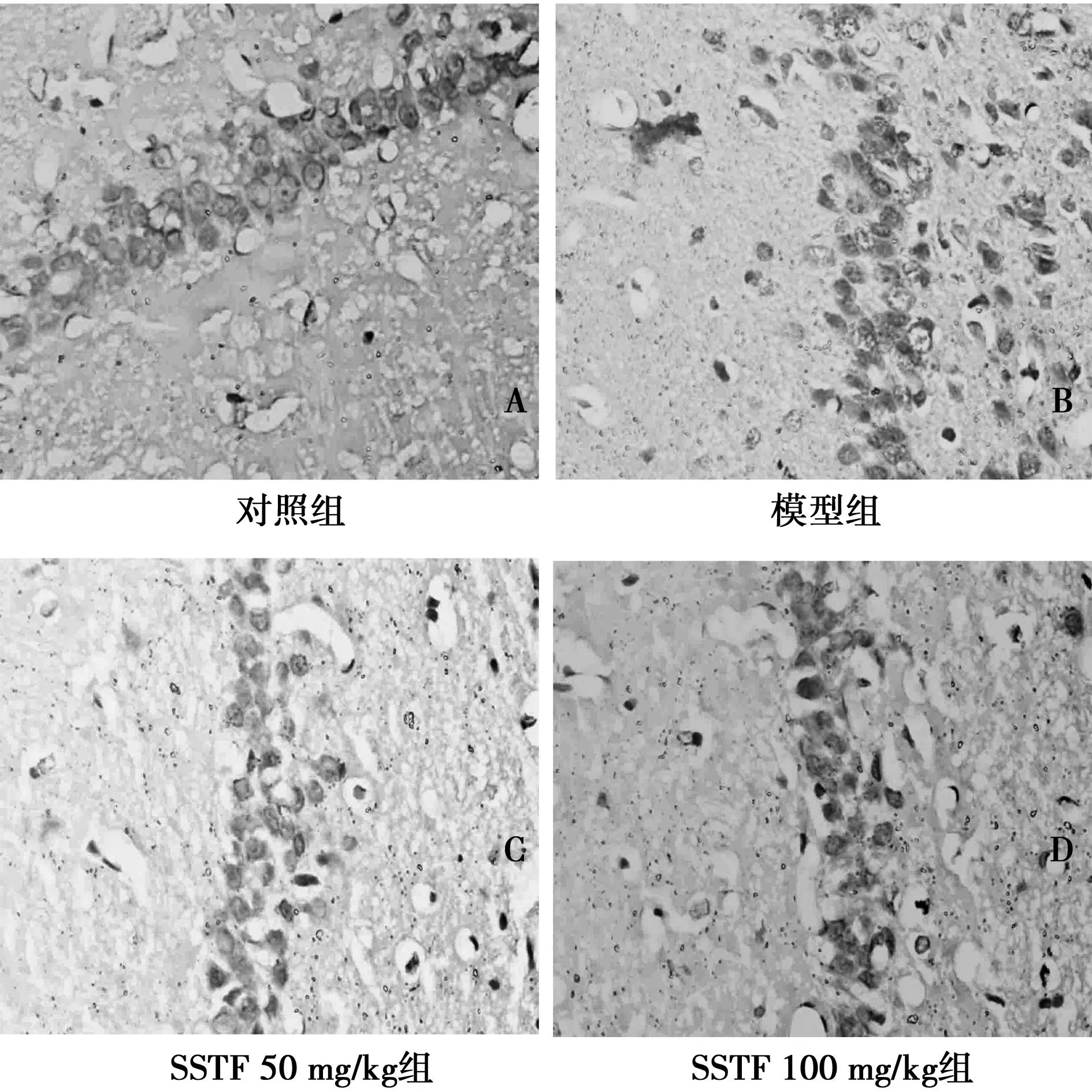
圖1 大鼠海馬CA1區神經元凋亡(TUNEL,×400)
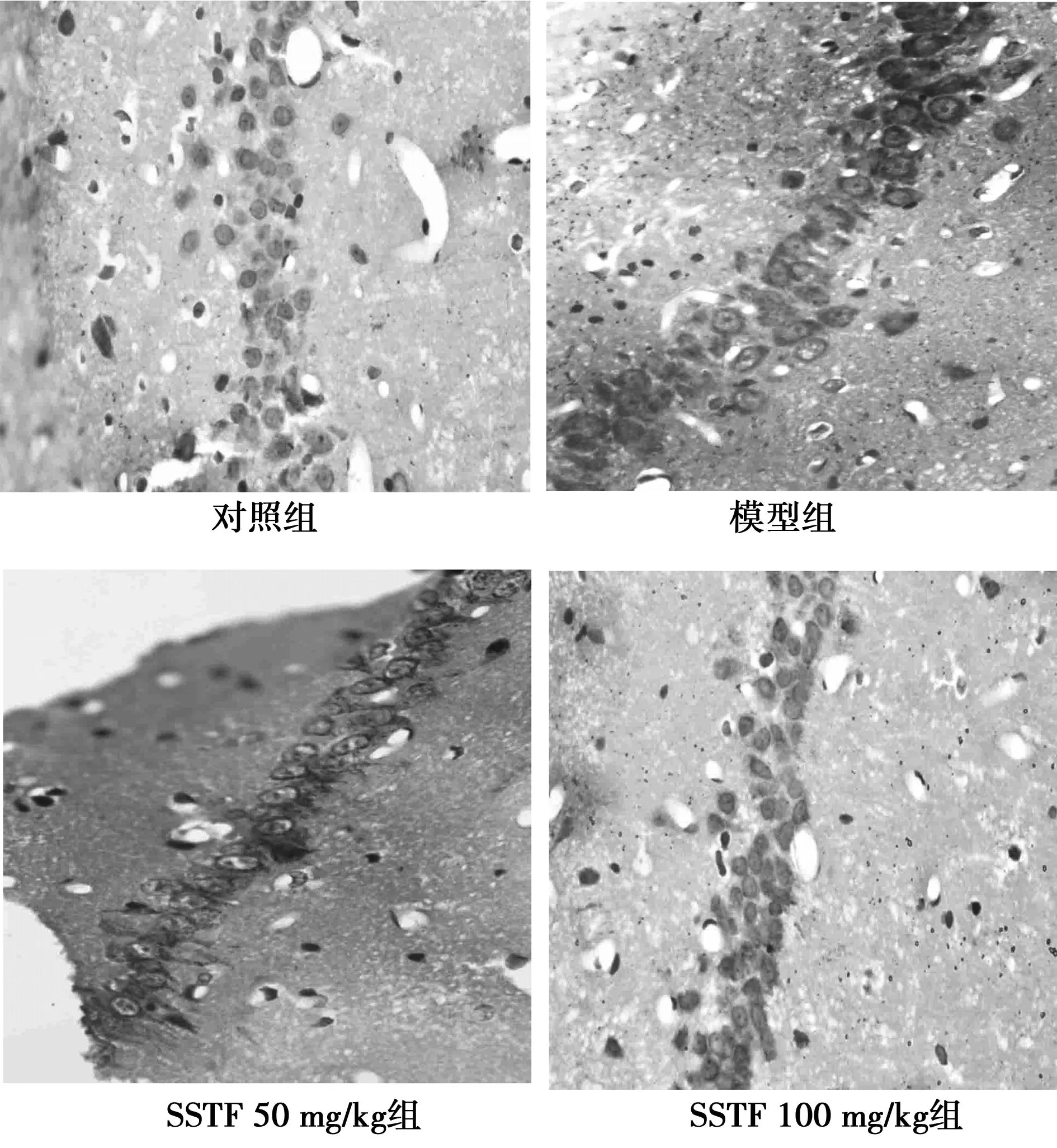
圖2 大鼠海馬CA1區Bax表達(DAB,×400)

組別BaxBcl-2對照組20.78±5.17115.24±24.56模型組144.51±30.451)21.45±5.271)SSTF50mg/kg組87.65±24.562)46.27±8.372)SSTF100mg/kg組52.17±12.782)76.74±18.192)
與對照組比較:1)P<0.01;與模型組比較:2)P<0.01
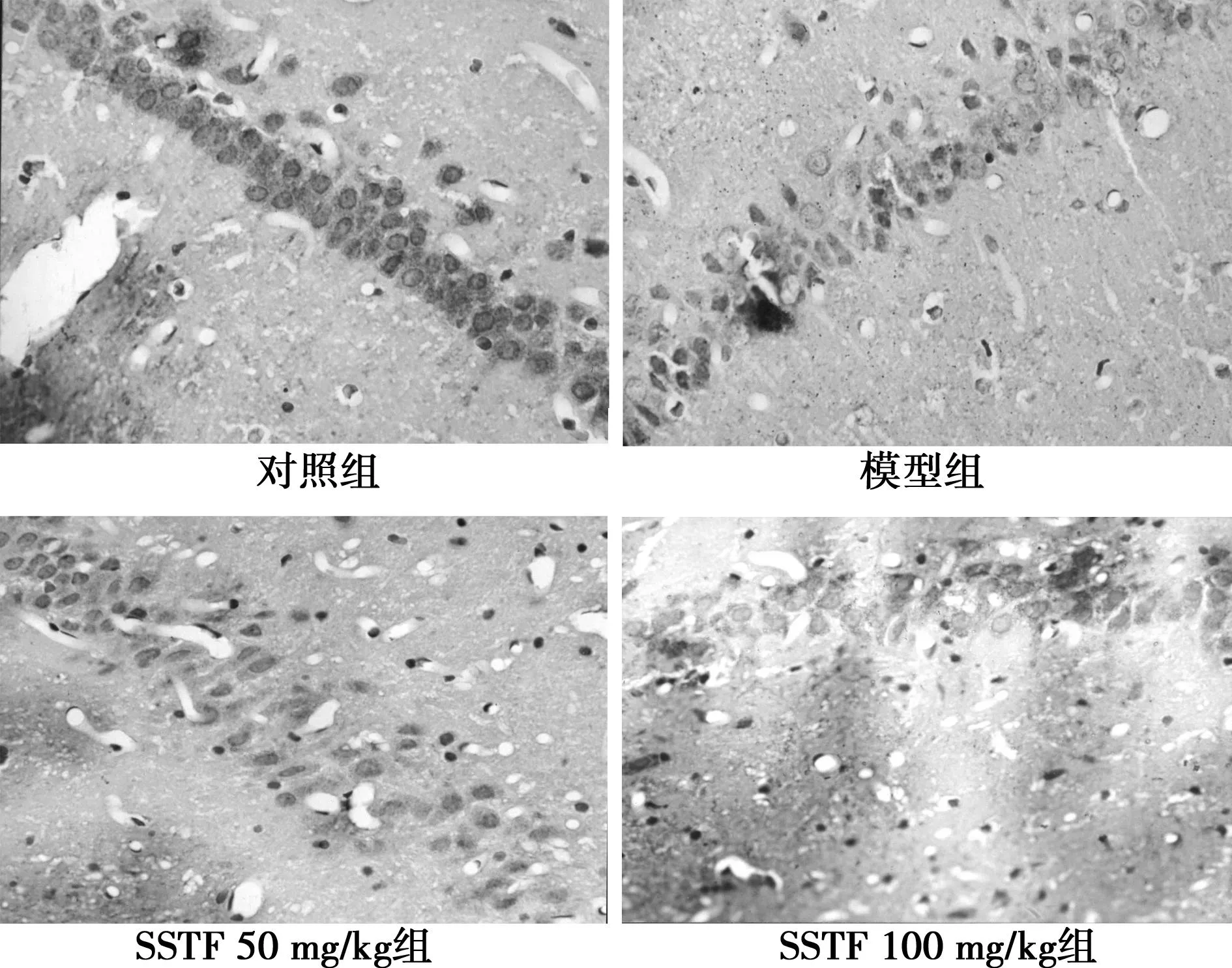
圖3 大鼠海馬CA1區神經元Bcl-2表達(IHC,×400)
2.3SSTF對大鼠海馬組織中Bax、Bcl-2表達量的影響(Western印跡)模型組大鼠海馬組織中Bax/β-actin明顯高于對照組;SSTF組明顯低于模型組;模型組大鼠海馬組織中Bcl-2/β-actin明顯低于對照組,SSTF組明顯高于模型組;模型組Bax/bcl-2較對照組明顯升高,SSTF組較模型組明顯降低,見表2,圖4。
表2 黃芩莖葉總黃酮對大鼠海馬CA1區神經元Bax,Bcl-2
與對照組比較:1)P<0.01;與模型組比較:2)P<0.05,3)P<0.01
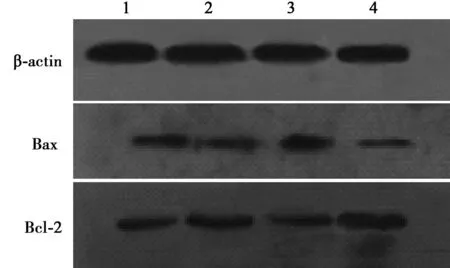
1~4:SSTF 50、100 mg/kg組、模型組、對照組圖4 大鼠海馬組織中Bax,Bcl-2 的表達(Western印跡)
3討論
線粒體凋亡途徑主要有P53蛋白、Bax蛋白、Bcl-2蛋白及caspase的參與〔7,8〕。Caspase-3是凋亡執行的關鍵因子,它的激活與細胞色素C(cyt-c)自線粒體釋放、線粒體損傷、神經元凋亡密切相關〔9〕。Bcl-2基因家族中Bcl-2蛋白與Bax蛋白是一對互相拮抗的蛋白,Bcl-2具有明顯抑制凋亡作用,而Bax則促進凋亡,Bax,Bcl-2 通過影響線粒體外膜通透性來調節cyt-c 釋放,Bax占優勢時,cyt-c自線粒體釋放,導致凋亡發生一系列瀑布反應〔10〕。Aβ也可引起線粒體呼吸鏈的復合體Ⅲ(泛醌-細胞色素C-還原酶)、Ⅳ(細胞色素C氧化酶,COX)活性降低〔11〕,其活性降低會導致ATP產生下降,過多的電子直接使氧分子O2產生超氧陰離子O2-和其他ROS〔14〕,線粒體內膜上的心肌磷脂作為線粒體膜的唯一磷脂也是ROS的靶點,ROS的升高引起心肌磷脂過氧化,氧化的心肌磷脂與cyt-c結合力下降,引起cyt-c完全釋放〔12〕。本實驗結果提示Aβ可能通過影響Bax,Bcl-2表達,影響線粒體外膜通透性,調節cyt-c釋放,引起神經元凋亡;Silva等〔13〕研究發現AD患者線粒體內Aβ寡聚體含量增加,加速了線粒體損傷。TAT-XIAP可通過減少Aβ引起的海馬神經元凋亡而改善大鼠學習記憶能力〔14〕。前期實驗結果證明Aβ可以引起ROS增多〔15〕,因此Aβ也可能通過ROS引起cyt-c釋放,誘導凋亡。本文結果顯示SSTF較模型組大鼠海馬神經元凋亡明顯減少,Bax表達下調,Bcl-2上調,Bax/Bcl-2比值明顯降低,提示SSTF通過對抗Aβ引起的凋亡相關基因改變來減輕神經元凋亡。前期研究結果顯示SSTF具有明顯的抗氧化作用〔2〕,因此推測SSTF的抗凋亡作用也可能通過抗氧化,降低ROS產生而減輕神經元凋亡。有研究報道通過上調超氧化物歧化酶、谷胱甘肽過氧化物酶活性可減少細胞的凋亡〔16〕。Zhu等〔17〕研究發現一種黃酮糖苷Hibifolin能夠抑制Aβ引起的皮層神經元中caspase-3,7的激活,抑制Ca2+流動,減少DNA斷裂。丁振禹等〔18〕研究發現三羥基異黃酮可影響APP695基因轉染PCI2細胞Bax和Bcl-2蛋白表達。
黃酮類化合物除了從抗氧化、抗凋亡機制減輕Aβ引起的神經毒性外,也有研究顯示通過影響Aβ生成、Aβ原纖維形成起到保護神經元作用。Jung等〔19〕研究了從槐屬植物中提取的總黃酮能抑制β分泌酶活性,淀粉樣蛋白前體(APP)通過β、γ分泌酶裂解產生Aβ,因此抑制β分泌酶活性可減少Aβ生成。Naiki等〔20〕采用離體實驗研究了五種黃酮類化合物的作用,能夠抑制Aβ原纖維的形成及增強原纖維的不穩定性。Aβ在體內以可溶性狀態存在時沒有毒性,形成原纖維絲后會產生毒性。Lemkul等〔21〕也證實桑黃素可以結合到原纖維的末端阻斷新的肽附著,能滲入到疏水中心在天冬氨酸與賴氨酸處裂解,干擾主鏈上的氫鍵而影響原纖維絲的形成。
本文顯示SSTF可減輕Aβ引起的神經元凋亡,其作用機制與其影響凋亡相關基因表達、抗氧化作用有關,本研究結果為進一步研發黃芩莖葉總黃酮用于神經退行型疾病的預防和治療提供了實驗依據。黃芩莖葉總黃酮的抗凋亡作用與凋亡通路中信號轉導間關系仍需進一步研究。
4參考文獻
1Lv G,Cui B,Lan H,etal.Diarylethene based fluorescent switchable probes for the detection of amyloid-β pathology in Alzheimer's disease〔J〕.Chem Commun(Camb),2015;51(1):125-8.
2王瑞婷,張建新,董雅潔.黃芩莖葉總黃酮對AD大鼠模型海馬神經元超微結構的影響及抗氧化作用〔J〕.中國老年學雜志,2010;30(7):926-8.
3金春慧,袁建民,程灶火.漆黃素改善阿爾茨海默病模型小鼠學習記憶障礙的細胞內信號通路〔J〕.中華行為醫學與腦科學雜志,2012;21(10):865-8.
4Javier Miguel-Hidalgo J,Paul IA,Wanzo V,etal.Memantine prevents cognitive impairment and reduces Bcl-2 and caspase 8 immunoreactivity in rats injected with amyloid β(1-40)〔J〕.Eur J Pharmacol,2012;692(1-3):38-45.
5Xu J,Zhang R,Zuo P,etal.Aggravation effect of isoflurane on Aβ(25-35)-induced apoptosis and tau hyperphosphorylation in PC12 cells〔J〕.Cell Mol Neurobiol,2012;32(8):1343-51.
6Huang HC,Xu K,Jiang ZF,etal.Curcumin-mediated neuroprotection against amyloid-β-induced mitochondrial dysfunction involves the inhibition of GSK-3β〔J〕.J Alzheimers Dis,2012;32(4):981-96.
7Kazuchika Nishitsuji,Takami Tomiyama,Kenichi Ishibashi,etal.The E693Δ mutation in amyloid precursor protein increases intracellular accumulation of amyloid β oligomers and causes endoplasmic reticulum stress-induced apoptosis in cultured cells〔J〕.Am J Pathol,2009;174(3):957-69.
8Silva DF,Selfridge JE,Lu J,etal.Mitochondrial abnormalities in Alzheimer's disease:possible targets for therapeutic intervention〔J〕.Adv Pharmacol,2012;64:83-126.
9Musatov A,Robinson NC.Susceptibility of mitochondrial electron-transport complexes to oxidative damage.Focus on cytochrome c oxidase〔J〕.Free Radic Res,2012;46(11):1313-26.
10Todt F,Cakir Z,Reichenbach F,etal.Differential retrotranslocation of mitochondrial Bax and Bak〔J〕.EMBO J,2015;34(1):67-80.
11Evstafieva AG,Garaeva AA,Khutornenko AA,etal.A sustained deficiency of mitochondrial respiratory complex Ⅲ induces an apoptotic cell death through the p53-mediated inhibition of pro-survival activities of the activating transcription factor 4〔J〕.Cell Death Dis,2014;5:e1511.
12Jacquemin G,Margiotta D,Kasahara A,etal.Granzyme B-induced mitochondrial ROS are required for apoptosis〔J〕.Cell Death Differ,2015;22(5):862-74.
13Silva DF,Santana I,Esteves AR,etal.Prodromal metabolic phenotype in MCI cybrids:implications for Alzhermer’s disease〔J〕.Curr Alzheimer Res,2013;10(2):180-90.
14夏春波,蔣常文,劉源劫,等.TAT-XIAP融合蛋白對學習記憶障礙大鼠的影響及其機制〔J〕.中華行為醫學與腦科學雜志,2013;22(7):587-90.
15王瑞婷,關麗華,周健,等.黃芩莖葉總黃酮對Aβ25~35致大鼠學習記憶損傷及海馬抗氧化酶活性的影響〔J〕.神經藥理學報,2011;1(2):14-8.
16Zhao J,Xu S,Song F,etal.2,3,5,4'-tetrahydroxystilbene-2-O-β-d-glucoside protects human umbilical vein endothelial cells against lysophosphatidylcholine-induced apoptosis by upregulating superoxide dismutase and glutathione peroxidase〔J〕.UBMB Life,2014;66(10):711-22.
17Zhu JT,Choi RC,Xie HQ,etal.Hibifolin,a flavonol glycoside,prevents beta-amyloid-induced neurotoxicity in cultured cortical neurons〔J〕.Neurosci Lett,2009;461(2):172-6.
18丁振禹,趙翠香,王鳳斌,等.三羥基異黃酮對APP695基因轉染PCI2細胞Bax和Bcl-2蛋白表達的影響〔J〕.中華行為醫學與腦科學雜志,2013;22(9):791-3.
19Jung HA,Yokozawa T,Kim BW,etal.Selective inhibition of prenylated flavonoids from Sophora flavescens against BACE1 and cholinesterases〔J〕.Am J Chin Med,2010;38(2):415-29.
20Naiki H,Hasegawa K,Ono K,etal.A search for antiamyloidogenic compounds based on a nucleation-dependent polymerization model〔J〕.Yakugaku Zasshi,2010;130(4):503-9.
21Lemkul JA,Bevan DR.Destabilizing Alzheimer's A beta 42 protofibrils with morin:mechanistic insights from molecular dynamics simulations〔J〕.Biochemistry,2010;49(18):3935-46.
〔2015-03-17修回〕
(編輯苑云杰/曹夢園)
基金項目:河北省科技廳資助項目(08276101D-21)
〔中圖分類號〕R962
〔文獻標識碼〕A
〔文章編號〕1005-9202(2016)10-2337-04;
doi:10.3969/j.issn.1005-9202.2016.10.011
第一作者:王瑞婷(1969-),女,教授,博士,碩士生導師,主要從事植物藥抗癡呆作用研究。

