HPLC-MS/MS法測定人血漿及尿液中奧普力農濃度
梅亞君,秦永平,毛銳,張梅,余勤,向瑾,南峰,梁茂植
?
HPLC-MS/MS法測定人血漿及尿液中奧普力農濃度
梅亞君1,2,秦永平2,毛銳2,張梅1,余勤2,向瑾2,南峰2,梁茂植2
[摘要]目的:建立準確、靈敏的HPLC-MS/MS法測定人血漿及尿液中奧普力農(OLP)的濃度,以用于OLP的藥代動力學研究。方法:采用API3000 LC-MS/MS液質聯用系統,Phenomenex Gemini C18柱(50×3.0 mm, 5μm),流動相為乙腈∶2 mmol.L-1甲酸銨(30∶70),流速0.2 mL.min-1,血漿及尿液樣本在pH7.5的弱堿性環境下分別用二氯甲烷∶異丙醇(95∶5)、二氯甲烷萃取后進樣,采用ESI源,正離子MRM模式檢測,米力農(MIL)作內標。結果:OLP和內標MIL的保留時間分別為1.91 min和1.88 min。OLP的血漿標準曲線在(0.05~100) ng.mL-1范圍內線性良好(r=0.9960),定量下限為0.05 ng.mL-1。日內精密度在2.0%~4.1%之間,日間精密度在4.2%~5.5%之間。方法回收率在(91.78±1.24)%~(103.12±2.64)%之間。萃取回收率在56.9%~68.1%之間。基質效應在-13.9~3.4%之間。OLP的尿液標準曲線在(1~1000) ng.mL-1范圍內線性良好(r=0.9954),定量下限為1 ng.mL-1。日內精密度在2.0%~5.8%之間,日間精密度在2.7%~9.4%之間。方法回收率在(90.28±1.80)%~(97.82±5.68)%之間。萃取回收率在67.4%~82.3%之間;基質效應在-13.9%~-12.0%之間。穩定性各項數據均符合相關要求。結論:本法具有快速、簡便、靈敏、準確等特點,適用于OLP血藥濃度及尿藥濃度的測定及其藥代動力學研究。
[關鍵詞]HPLC-MS/MS;奧普力農;血藥濃度;尿藥濃度
[作者單位]1.成都中醫藥大學藥學院 中藥材標準化教育部重點實驗室 中藥資源系統研究與開發利用省部共建國家重點實驗室培育基地,四川 成都 611137;2.四川大學華西醫院國家藥物臨床試驗機構臨床藥理研究室,四川 成都 610041
鹽酸奧普力農(Olprinone Hydrochloride ,OLP)是一種選擇性磷酸二酯酶Ⅲ(PDE)抑制劑。研究發現奧普力農能顯著提高心輸出量、降低左心室舒張壓及體循環血管阻力指數、減小心肌梗塞區域、降低肌酸激酶和肌鈣蛋白-I水平[1~4]。由于OLP體內濃度水平較低,對檢測靈敏度要求較高,文獻中均采用液質聯用法進行測定。Jie Sun等[5]以流動相梯度洗脫,建立了LC-MS測定大鼠血漿中OLP濃度的測定方法。Ping Zhu等[6]以米力農(Milrinone,MIL)為內標,樣品經液液萃取技術建立了LC-MS/MS測定人血漿中OLP 濃度的分析方法。倪穗琴等[7-8]采用尿液直接稀釋法建立了LC-MS/MS測定人尿液中奧普力農濃度的測定方法。本文采用液-液萃取法,同時建立了靈敏準確的測定血漿及尿液中OLP濃度的HPLCMS/MS分析方法,并已用于其人體藥代動力學實驗研究。
1 儀器與試藥
1.1 儀器
SL-HTC系列HPLC儀(含系統控制器,全自動進樣器,日本島津公司);API 3000型LC-MS/MS液質聯用系統(含Analyst1.4色譜工作站,美國ABI公司);Eppendorf Centrifuge 5810R 型臺式低溫離心機(Gene Company Limited)。
1.2 試藥
OLP對照品(北京福瑞康正醫藥技術研究所,含量99.4%,批號:130901);MIL對照品(中國藥品生物制品檢定所,含量99.0%,批號101065-201001);乙腈、甲酸銨、異丙醇為色譜純;其余試劑為分析純。實驗用純水由Millipore公司Milli-Q型超純水器制備所得。
2 方法與結果
2.1 色譜與質譜條件
采用Phenomenex Gemini C18(50×3.0 mm,5 μm)色譜柱,流動相為乙腈∶2 mmol.L-1甲酸銨(30∶70),流速0.2 mL.min-1,柱溫40 ℃。質譜檢測采用電噴霧離子源(ESI),多反應離子監測模式(MRM)檢測,噴霧電壓(IS)為2000V,溫度(TEM)為450℃,CAD=12,NEB=13,CUR=8;碰撞入口電壓(EP)10.5V,碰撞室射出電壓(CXP)為12V,環形聚焦電壓(FP)為100V;OLP和內標的監測離子對m/z分別為251.2 /155.2和212.2/140.2,離子去簇電壓(DP)分別為21V,46V,碰撞誘導解離電壓(CE)分別為48V和43V。
2.2 溶液配制
2.2.1 OLP儲備液的配制 精密稱取OLP對照品0.01225 g(相當于OLP10 mg)置50 mL棕色容量瓶中,用50%乙腈定容至刻度,即得OLP儲備液(200 μg.mL-1),置4℃冰箱避光保存。
2.2.2 MIL(內標)儲備液及工作液的配制 精密稱取MIL對照品0.01010 g (相當于MIL10.0 mg)置50 mL棕色容量瓶中,用50%乙腈定容至刻度,即得內標儲備液(200 μg.mL-1),置4 ℃冰箱避光保存。臨用前用50%乙腈稀釋到所需濃度即可。
2.2.3 OLP血漿和尿液標準曲線工作液配制 取OLP儲備液(200 μg.mL-1),用50%乙腈依次稀釋可得血漿和尿液標準曲線各管工作液。血漿最高管工作液(OLP 500 ng.mL-1),尿液最高管工作液(OLP 2000 ng.mL-1)。
2.3 樣品測定
兩組術前NIHSS評分比較差異無統計學意義(P>0.05),術后14 d的NIHSS評分均較術前顯著降低,但觀察組比對照組改善更明顯(P<0.05)。見表3。
2.3.1 血漿樣品 取空白血漿500 μL,加入100 μL內標工作液(160 ng.mL-1)及100 μL 相應濃度的標準曲線系列工作液或質控工作液,再加入200 μL 0.25 mol.L-1磷酸鹽緩沖液(pH 7.5),混勻后加入3.5 mL二氯甲烷-異丙醇(95∶5,v/v)渦旋萃取5 min,低溫離心6 min(8 ℃,3000 rpm),抽棄上層水相,轉移下層有機相于尖底管內,置45℃水浴通空氣流揮干。殘渣用50 μL流動相復溶,進樣10 μL。記錄色譜峰面積,以藥物與內標的峰面積比在當日標準曲線上求出血樣中OLP濃度。
2.3.2 尿液樣品 取空白尿液200 μL,加入100 μL內標工作液(800 ng.mL-1)及100 μL相應濃度的標準曲線系列工作液或質控工作液,再加入100 μL 0.25 mol.L-1磷酸鹽緩沖液(pH 7.5),混勻后加入3.5 mL二氯甲烷渦旋萃取5 min,低溫離心6 min( 8℃,3000 rpm),抽棄上層水相,轉移下層有機相于尖底管內,置45 ℃水浴通空氣流揮干。殘渣用100 μL流動相復溶,進樣10μL。記錄色譜峰面積,以藥物與內標的峰面積比在當日標準曲線上求出尿樣中OLP濃度。
2.4 專屬性
對照品、空白血漿、空白血漿加對照品及血漿樣品的色譜圖見圖1;對照品、空白尿液、空白尿液加對照品及尿液樣品的色譜圖見圖2。OLP和內標的保留時間分別為1.91 min和1.88 min。結果顯示藥物及內標出峰處無雜質干擾,本方法的專屬性符合方法學評價要求。
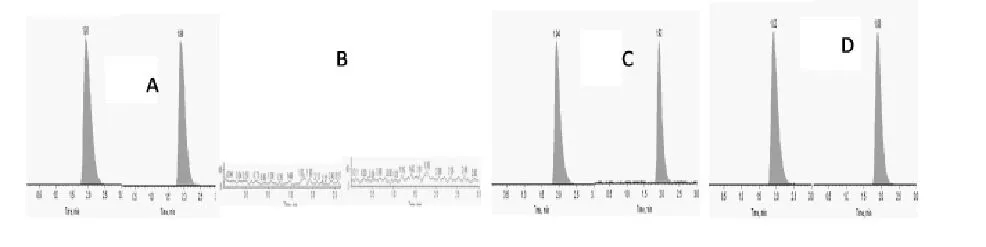
圖1 OLP及IS代表性色譜圖 A:標液 B:空白血漿C:空白血漿+標液 D:樣品

圖2 OLP及IS代表性色譜圖 E:標液 F:空白尿液G:空白尿液+標液 H:樣品
2.5 標準曲線及最低定量限考察
2.5.1 血漿 分別取空白血漿500μL10份,依次加入OLP血漿標準系列工作液各100 μL,使其血漿藥物濃度分別為:100,50,20,5,2,1,0.5,0.2,0.1,0.05 ng.mL-1,再加入內標工作液 (160 ng.mL-1)100 μL,按2.3.1項下自“再加入200 μL 0.25 mol.L-1磷酸鹽緩沖液(pH 7.5)”操作,進樣10 μL。記錄藥物及內標的色譜峰面積,以二者峰面積之比(Y)對OLP血漿濃度(X)進行加權(1/c2)線性回歸,得OLP血漿標準曲線方程:Y=0.0736X + 0.00257(r= 0.9960)。結果顯示,OLP在0.05~100 ng.mL-1范圍線性良好。血漿中最低定量限為0.05 ng.mL-1,其測定5次的平均準確度為102.32%,RSD為1.5%。
2.5.2 尿液 分別取空白尿液200 μL 8份,依次加入OLP尿液標準系列工作液各100 μL,使其尿藥濃度分別為:1000,500,200,50,20,5,2,1 ng. mL-1,再加入內標工作液 (800 ng.mL-1)100 μL,按“2.3.2”項下自“再加入100 μL 0.25 mol.L-1磷酸鹽緩沖液(pH 7.5)”操作,進樣10 μL。記錄藥物及內標的色譜峰面積,以二者峰面積之比(Y)之比對OLP尿液濃度(X)進行加權(1/c2)線性回歸,得OLP尿液標準曲線方程:Y=0.0361 X + 0.0464(r= 0.9954)。結果顯示,OLP在1~1000ng.mL-1范圍線性良好。尿液中最低定量限為1.0ng.mL-1,其測定5次的平均準確度為97.87%,RSD為5.2%。
2.6.1 血漿 取空白血漿加OLP配成的含OLP濃度分別為(LL)0.1 ng.mL-1、(L)0.2 ng.mL-1、(M)10 ng. mL-1、(H)80 ng.mL-1四個濃度樣品,于同日內連續測定5次,計算其方法回收率分別為(100.00±4.12)%、(103.12±2.64)%、(94.90±1.90)%、(91.78±1.24)%;批內RSD分別為4.1%、2.6%、2.0%、1.4%;于一周內測定3批每批5次,計算其批間RSD分別為4.5%、5.5%、5.4%、5.2%。
2.6.2 尿液 取空白尿液加OLP配成的含OLP濃度分別為(L)2 ng.mL-1、(M)100 ng.mL-1和(H)800 ng.mL-1三個濃度樣品。于同日內連續測定5次,計算其方法回收率分別為(97.82±5.68)%、(97.01±3.91)%、(90.28±1.80)%;批內RSD分別為5.8%、4.0%、2.0%;于一周內測定3批每批5次,計算其批間RSD分別為9.4%、4.1%、2.7%。
2.7 萃取回收率及基質效應
2.7.1 血漿 取空白血漿加OLP配成的LL、 L 、M和H四個濃度樣品,每種濃度3份。按“2.3.1”項下操作進樣,得到OLP與內標的峰面積B;同時取與血漿樣品LL、L、M、H四個濃度相同量的OLP標準工作液及內標工作液于尖底管揮干,流動相復溶,先直接進樣得OLP的峰面積C,再將復溶液加入預處理后的空白血漿管,充分混合后進樣得OLP的峰面積A。將所得峰面積B與峰面積A比較(B/C×100%)得血漿樣品OLP及內標的萃取回收率,結果分別為56.9~68.1% 和57.2~77.9%之間。峰面積A與峰面積C比較,計算OLP及內標的基質效應[ME=(A-C)/C×100%],血漿樣品OLP及內標的基質效應分別為-13.9~3.4% 和-14.3~-10.5%之間。
2.7.2 尿液 取空白尿液加OLP配成L、M和H三個濃度樣品,每種濃度3份。按“2.3.2”項下操作進樣,記錄藥物和內標的峰面積為B;同時取與尿液樣品L、M和H三個濃度相同量的OLP標準工作液及內標工作液于尖底管揮干,流動相復溶,先直接進樣得OLP的峰面積C;再將復溶液加入預處理后的空白尿液管,充分混合后進樣得OLP的峰面積A。將所得峰面積B與峰面積A較(B/A×100%),尿液樣品OLP及內標的萃取回收率分別為67.4%~82.3% 和65.7~79.8%之間;將峰面積A與峰面積C比較[ME=(A-C)/C×100%],計算藥物及內標的基質效應分別為-12.0~-13.9%之間和-14.4~10.7%之間。
2.8 樣品穩定性考察
分別取空白血漿、尿液加OLP配制成L、M、H三個濃度樣品,根據實際樣品測定過程中可能涉及到的樣品穩定性,分別考察了樣品在室溫放置0h、3h、6h,-35℃冰箱中放置0d、29d、37d,反復凍融0、1、2、3次取樣測定,萃取物在4℃冰箱放置0 h、12 h、24 h、36 h,樣品處理后立即進樣溶解與重復進樣1、2次、樣品經處理后進樣室(8℃)放置0 h,6 h,12 h,4℃低溫下室內光照3h、6h后進樣的穩定性。結果表明:血漿和尿液樣品在-35℃冰箱冷凍保存37d,反復凍融3次,在室溫放置6h后測定與未保存、未凍融和未放置樣品測定結果無明顯差異,處理后的樣品在進樣室(8°C)放置16h進樣、萃取物在冰箱(4°C)中放置36h進樣,重復進樣測定2次與0時刻值比較變化率均<15%,穩定性符合要求。同時血漿和尿液樣品在室內光照6h穩定。
2.9 方法應用
本文建立的方法已用于12例健康受試者在3個周期分別單次靜脈推注低(5 μg.kg-1)、中(10 μg. kg-1)、高(20 μg.kg-1)負荷劑量鹽酸奧普力農葡萄糖注射液的藥代動力學研究,其均值藥時曲線見圖2,由圖可知藥物濃度隨劑量增加而增大,低、中、高劑量藥時曲線變化趨勢一致。
靜脈推注中劑量鹽酸奧普力農葡萄糖注射液后,尿液中奧普力農平均累積排泄率-時間曲線見圖3。結果表明鹽酸奧普力農靜脈推注后主要經腎臟清除,且多集中于給藥后2小時內。
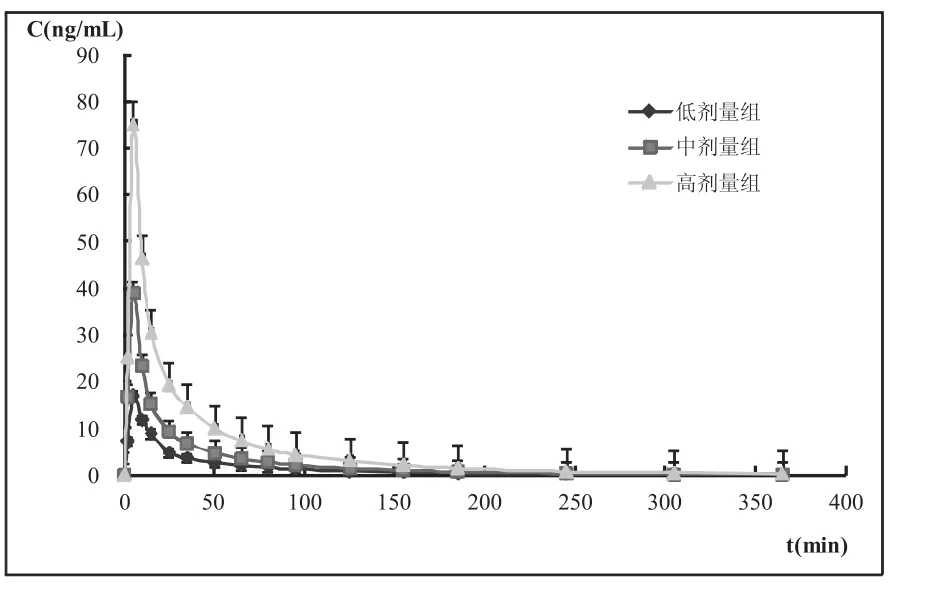
圖3 低、中、高劑量組均值血藥濃度-時間曲線
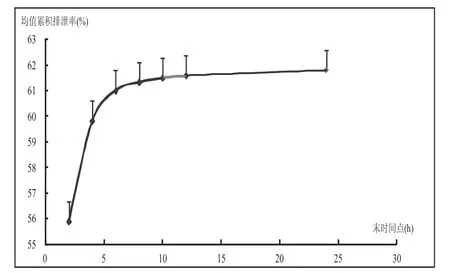
圖4 靜脈推注中劑量OLP后均值尿藥累積排泄率曲線圖
3 討論
3.1 流動相的選擇
在相同的質譜條件下,比較了不同流動相系統(甲醇-水、乙腈-水、乙腈-水-甲酸、甲醇-水-甲酸、乙腈-甲酸銨、甲醇-甲酸銨)OLP的出峰情況。結果顯示:甲醇系統,峰展寬較嚴重且靈敏度較低;乙腈-2 mmol.L-1甲酸銨系統下OLP離子響應最強,且峰形較好,故選用乙腈為有機相,2 mmol.L-1甲酸銨緩沖液為流動相添加劑。在乙腈-2 mmol.L-1甲酸銨系統下,考察了不同乙腈比例對奧普力農及內標保留時間、色譜峰峰型和基質效應的影響。當乙腈比例為30%時,藥物與內標的基質效應最小,滿足≤15%的要求,且保留時間短、色譜峰峰形好,最終確定本文所用流動相。
3.2 光照穩定性考察
文獻報道奧普力農儲備液應避光保存,內標米力農的凍干粉在自然光或強光照射下易發生變色現象,對照品也應避光保存。為了給工作液及生物樣品的儲存條件、樣品采集及測定過程的環境控制提供科學依據,我們對藥物及內標的光照穩定性進行了考察。結果顯示藥物及內標的工作液在室內普通光照下36h穩定、血漿及尿液樣品在室內普通光照下6h藥物濃度均穩定。但為了保證測定結果的準確性,在工作液貯存及樣品測定過程中仍進行了避光處理。
3.3 萃取環境的選擇
奧普力農具有兩性離子性質,查閱資料得知該化合物在pH6~10范圍內油水分布系數較高,因而本實驗分別考察了以pH10和pH8.5的1 mol.L-1碳酸鹽緩沖液、pH7.5和pH6.0的0.25 mol.L-1磷酸鹽緩沖液作為萃取用緩沖液。結果表明:在pH7.5和pH6.0的0.25 mol.L-1磷酸鹽緩沖液條件下藥物的萃取回收率較高,但在pH6.0的酸性環境下血漿中被提取出的內源性雜質較多,藥物的基質效應較高,因此選擇以pH7.5的0.25 mol.L-1磷酸鹽緩沖液作為萃取用緩沖液。
[參考文獻]
[1]Kentaro Setoyama, Ryozo Kamimura, Makoto Fujiki, et al. Effects of olprinone on myocardial ischemia-reperfusioninjury in dogs [J]. Journal of veterinary medical science, 2006, 68 (8): 865.
[2]杜崗,李自成,張濤.鹽酸奧普力農治療充血性心力衰竭的隨機對照觀察[J].暨南大學學報(醫學版),2010,31(6):592.
[3]楊建民,方楚葵.奧普力農改善心力衰竭療效的臨床觀察[J].臨床醫學工程,2009,16(6):34.
[4]Akimura S, Yoshino J, Izumi K, et al. Comparison of the effects of phosphodiesterase III inhibitors, milrinone and olprinone, in infant corrective cardiac surgery [J]. The Japanese Journal of Anesthesiology,2013,62(5):583.
[5]Jie Sun, Yan Liang, Lin Xie, et al. Simple, Sensitive and rapid LC-ESI-MS method for the quantitation of olprinone in rat plasma [J]. Chromatographia, 2007,66:49.
[6]Ping Zhu, Yu-Guan Wen, Ji-Mei Chen, et al. Determination of olprinone in human plasma utilizing liquid chromatography tandem mass spectrometry [J]. Journal of Pharmaceutical and Biomedical Analysis,2011,54:198.
[7]倪穗琴,溫預關.液相色譜- 串聯質譜測定尿液中奧普力農的濃度[J].今日藥學,2008,18(3):24.
[8]Hongbo Wang, Baochang Zhang, Xilin Sun, et al. Method development and validation of olprinone in human plasma by HPLC coupled with ESI-MS-MS: application to a pharmacokinetic study [J]. Journal of Chromatographic Science,2014,52(5):400.
(責任編輯:李蕓霞)
HPLC-MS/MS determination of olprinone in human plasma and urine
M
EI Ya-jun1,2,QIN Yong-ping2,MAO Rui2, ZHANGMei1, YU Qin2,XIANG Jin2, NAN Feng2, LIANG Mao-zhi2// (1 School of Pharmacy, Chengdu University of Traditional Chinese Medicine, Key Laboratory of Standardization of Chinese Herbal Medicines of Ministry of Education, State Key Laboratory Breeding Base of Systematic research, development and Utilization of Chinese Medicine Resources, Chengdu 611137, Sichuan;2 Department of Clinical Pharmacology, West China Hospital, Sichuan University, Chengdu 610041, Sichuan)
[Abstract]Objective: To develop an accurate and sensitive method for the determination of olprinone in human plasma and urine, which can be used in the pharmacokinetic study of OLP. Method: API3000 LC - MS/MS system was used. The mobile phase consisted of a mixture of acetonitrile-2mmol.L-1ammonium formate (30:70) was delivered at a flow rate of 0.2 mL.min-1. Plasma samples and urine samples were respectively extracted by dichloromethane: isopropanol (95:5, v/v) and dichloromethane in the condition of pH=7.5, and then separated on a Phenomenex Gemini C18column (50×3.0mm, 5μm). The sample were subsequently analyzed by mass spectrometry with an ESI source and quantified by multiple reaction monitoring (MRM) mode. Milri-none was used as the internal standard. Result: The retention time of olprinone and internal standard were 1.91 min and 1.88 min, respectively. The calibration curve for plasma samples was in the range of 0.05~100 ng.mL-1. The limit of quantification was 0.05 ng.mL-1. Methodological recovery was (91.78±1.24)% ~(103.12±2.64)%. Pretreatment recovery was 56.9%~68.1%. Matrixes effect was -13.9%~3.4%. The calibration curve for urine samples was in the range of 1~1000 ng.mL-1. The limit of quantification was 1ng.mL-1.Methodological recovery was (90.28±1.80) % ~ (97.82±5.68)%. Pretreatment recovery was 67.4%~82.3%. Matrixes effect was -12.0%~ -13.9%. Data about all stability study fitted the request. Conclusion: The developed method is found to be simple, rapid, sensitive and accurate for the determination of olprinone in human plasma and urine samples and to be suitable for the pharmacokinetic study.
[Key words]HPLC-MS/MS; olprinone; plasma concentration; urine concentration
[中圖分類號]R 917
[文獻標識碼]A
[文章編號]1674-926X(2016)02-017-04
[作者簡介]梅亞君(1990-),女,在讀碩士,主要從事生物藥物分析方向研究Tel:15184443565 Email:327699932@qq.com
[通訊作者]張梅,女,教授,主要從事中藥有效成分研究Tel:13882126775 Email:zhangmei63@126.com秦永平,男,研究員,主要從事生物藥物分析Tel:18980601665 Email:qinyongping1@163.com
[收稿日期]2015-12-30/

