pH值對處理電鍍含銀廢水的影響關系分析
楊濱瑜+陳明
摘 要 本文簡述了氫氧化鈉沉淀法處理電鍍含銀廢水的原理,通過實驗對pH值的調節來達到對銀離子的最佳沉淀率,對于提高電鍍含銀廢水治理效果及提高環境質量都具有非常重要的現實意義。
關鍵詞 pH值;含銀廢水;沉淀率
中圖分類號 X8 文獻標識碼 A 文章編號 1674-6708(2016)161-0181-01
電鍍含銀廢水的水質成分非常的復雜。但總的來講,銀離子是電鍍含銀廢水中的主要污染物,即使銀離子的濃度很小,它都會對人體和環境造成很大的危害,因此,含有銀離子的污染廢水必須嚴格治理,治理達標后才能排放,否則后果將不堪設想。本文通過不同pH值下氫氧化鈉對銀的沉淀率影響,找出最佳pH值,達到對銀的最佳沉淀效果。
1 用氫氧化鈉沉淀法處理含銀廢水的原理
用氫氧化鈉沉淀法的原理為:通過加入一定量的沉淀劑,使其與銀離子發生化學反應,生成難溶的物質從而呈沉淀析出。平衡關系如下:
[X+][Y-]=Ksp(溶度積) (1)
上式中,Ksp為溶度積,不同的兩種離子(X+、Y-)可以出現以下3種情況:第一種情況為:當[X+][Y-]
A(OH)n=nOH-+An+
Ksp=[An+][OH-]n (2)
在這里需要指出的是,以上計算方法得出的金屬氫氧化物沉淀所需的pH值條件是理論計算值,不能作為廢水處理的依據。因為實際廢水成分非常復雜,受諸多因素的影響(如:攪拌時間、溫度、、靜置時間、pH),所以最佳PH值的確定就需要通過實驗來確定。
2 實驗方法與數據處理
通過模擬含銀廢液的方法,取一定體積事先模擬配置好的含銀廢液,一邊攪拌一邊加入氫氧化鈉溶液(20%),同時用酸度計測量溶液的pH值,隨著氫氧化鈉的不斷加入,pH值不斷升高,當溶液pH值到了一個比較合理的一個數值時,然后再對該溶液進行過濾,過濾后分析濾液中的含離子的銀量,計算出銀離子的沉淀率。
本實驗采用的是氫氧化鈉沉淀法處理含銀廢液,準確量取300ml已配制好的銀離子廢水模擬溶液,置于500ml燒杯內,一邊攪拌一邊加入氫氧化鈉溶液(20%)[2,3],同時用酸度計測量溶液的pH值,當溶液的pH值為10.6左右時,然后靜置該溶液一段時間,等待溶液完全分層,然后進行過濾,分析濾液中銀離子的含量,通過計算得知此種方法銀的回收率。在實驗過程中,一邊攪拌一邊用酸度計測得的pH值,記錄好數據,數據如表1。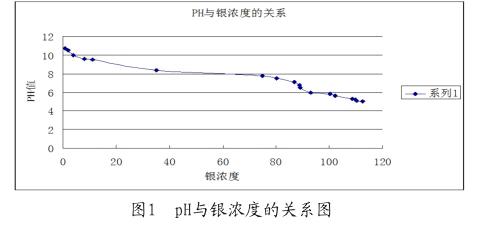
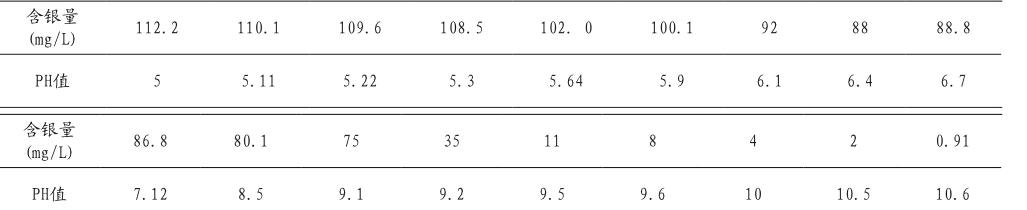
由表1和圖1可以看出,剛開始反應時,隨著氫氧化鈉(20%)的不斷加入,溶液的pH值不斷增加,溶液的pH值為5~8.5之間的時候,濾液中銀離子含量變化較小,當溶液pH值為9.1~10.05之間的時候,濾溶液中銀離子含量變化明顯下降。當溶液pH值達到10.5左右時,濾液中銀離子的含量非常小。隨著氫氧化鈉的不斷加入,溶液pH的也不斷上升,當pH值大于10.6左右時,濾液中的銀含量變化量就很小了。
3 結論
由本文實驗可以看出,要采用氫氧化鈉(20%)中和沉淀法來處理含銀廢水,最關鍵的就是要控制好pH值,在實際處理過程中,我們要根據不同的水質,不同的金屬種類,去選擇最恰當的pH值。本實驗結果可以得知,使用氫氧化鈉(20%)中和沉淀法來處理含銀廢水的最佳pH值為10.5左右。
參考文獻
[1]葛麗穎.含銅/鎳電鍍廢水的處理與分離研究[D].貴陽:貴州大學,2007.
[2]李盼盼.酸浸電解法回收電鍍污泥中銅和鎳的工藝研究[D].青島:中國海洋大學,2009.
[3]陳思寧,等.利用硅烷螯合樹脂處理重金屬廢水[J].廣東化工,2001,28(5):18-20.

