山茱萸紅色素穩定性的研究
吳海霞,馬國剛
(運城學院生命科學系,山西運城 044000)
山茱萸紅色素穩定性的研究
吳海霞,馬國剛
(運城學院生命科學系,山西運城044000)
以A440 nm吸光度為指標,研究pH值、溫度、光照、金屬離子、氧化劑、還原劑及常用食品添加劑等對山茱萸紅色素穩定性的影響。結果表明,山茱萸紅色素在酸性條件下較為穩定,但隨著酸性減弱,其顏色變淺;在一定的溫度范圍內(0~90℃)對熱比較穩定;不同光照條件對其具有一定程度的降解作用;Na+,Ca2+,Mg2+,Al3+,Zn2+,K+,Cu2+等金屬離子對色素影響不大,但Fe3+的存在會使色素變色而不穩定,而Ba2+會使色素溶液產生部分沉淀而渾濁;氧化劑H2O2和還原劑Na2SO3可使色素褪色;蔗糖、葡萄糖、抗壞血酸、苯甲酸鈉等食品添加劑對色素穩定性影響不大,檸檬酸和食鹽對色素具有一定的增色作用。
山茱萸;紅色素;穩定性
色素是常用的食品添加劑,有合成色素和天然色素之分。與合成色素相比,天然色素作為生物體內原有的組成成分,其安全性較高,有的還具有增加消化液的分泌、促進食欲的功效[1]。但是,天然色素在著色性和穩定性方面還略遜于合成色素,同時由于其較高的原料價格及提取成本也使其在生產中的應用受到限制。山茱萸是一種傳統中藥材,其果實呈鮮艷紅色,并含有豐富的營養成分和生理活性成分,目前的研究均側重于對其中有效成分的研究利用[2-3],而對其色素的研究較少[4]。本試驗在提取山茱萸紅色素的基礎上,對山茱萸紅色素的穩定性進行研究分析,為新型天然色素的開發及山茱萸資源的深度利用提供思路。
1 材料與方法
1.1試驗原料與主要試劑
山茱萸,采自山西臨汾市浮山縣。
甲醇、丙酮、抗壞血酸、苯甲酸鈉、檸檬酸、過氧化氫、三氯化鋁、鄰苯二甲酸氫鉀、三氯化鐵等,均為分析純。
1.2儀器設備
微型高速萬能粉碎機,天津泰斯特儀器有限公司產品;101A-1E型思安熱恒溫鼓風干燥箱,上海實驗儀器總廠產品;LXJ-II型離心沉淀機,上海醫分儀器制造有限公司產品;WFZ UV-2100型紫外可見分光光度計,尤尼柯(上海)儀器有限公司產品;PHS-3C型精密酸度計,上海大普儀器有限公司產品。
1.3試驗方法
1.3.1山茱萸紅色素提取工藝流程
山茱萸粉→按料液比1∶20加入80%乙醇→超聲波輔助提取(60℃,400 W,15 min)→離心(3 000 r/min,20 min)→取上清液→上清液即為色素溶液。
1.3.2最大吸收波長的確定
將提取所得色素溶液稀釋后,用0.05 mol/L鄰苯二甲酸氫鉀-鹽酸緩沖液將其pH值分別調至1.0,2.0,3.0,于400~500 nm下測其吸光度[5],確定其最適作用pH值及最大吸收波長。
1.3.3光照對色素穩定性影響
取山茱萸紅色素樣液,稀釋1倍后調至pH值3.0,分別置于暗光、室內、L66強光下,每隔90 min取出,測定A440 nm。
1.3.4pH值對色素穩定性影響
取山茱萸紅色素溶液,稀釋1倍后分別用0.05mol/L的鄰苯二甲酸氫鉀-鹽酸緩沖液、磷酸氫二鈉-檸檬酸緩沖液及硼砂-氫氧化鈉緩沖液,依次調溶液pH值至1.0~10.0,并測定A440 nm[6-8]。
1.3.5溫度對色素穩定性影響
(1)溫度和時間對色素穩定性影響。取5 mL色素溶液6份,稀釋后調pH值至3.0,分別放入40,50,60,70,80,90℃的恒溫水浴鍋,每隔30 min測定A440 nm。
(2)溫度和pH值對色素穩定性影響。取pH值1.0,2.0,3.0,4.0,5.0,6.0,7.0,8.0,9.0,10.0的色素溶液各1份,放入溫度為40,50,60,70,80,90℃的恒溫水浴鍋內,30 min后測定A440 nm。
1.3.6金屬離子對色素穩定性影響
分別配置含NaCl,CaCl2,MgCl2,AlCl3,ZnCl2,KCl,CuSO4,BaCl2(0.01,0.02,0.03 mol/L),FeCl3(0.001,0.002,0.003 mol/L) 的金屬離子溶液,各取1 mL分別加入pH值3.0的色素溶液中,測定A440nm[6-8]。
1.3.7氧化劑對色素穩定性影響
配制含H2O2濃度為0,0.1%,0.5%的pH值3.0色素溶液,于室溫暗置24 h,測其于400~500 nm波長范圍內的吸光度[6-8]。
1.3.8還原劑對色素穩定性影響
配制含Na2SO3濃度為0,0.012,0.06 mg/mL的pH值3.0色素溶液,分別于室溫暗置24 h,繪制于400~500 nm波長范圍內吸光度,繼續放置至7 d后,繪制吸光度[6-8]。
1.3.9食品添加劑對色素穩定性影響
分別配制含蔗糖(0,0.5%,5.0%,10.0%),葡萄糖(0,5%,10%,15%)以及檸檬酸(0,0.5%,1.0%,1.5%),抗壞血酸(0,0.5%,1.0%,1.5%),苯甲酸鈉(0,0.01%,0.10%,0.50%),食鹽(0,0.5%,1.0%,2.0%)的pH值3.0色素溶液,測定A440 nm[6-8]。
2 結果與分析
2.1山茱萸紅色素最大波長的確定
最大吸收波長的確定見圖1。
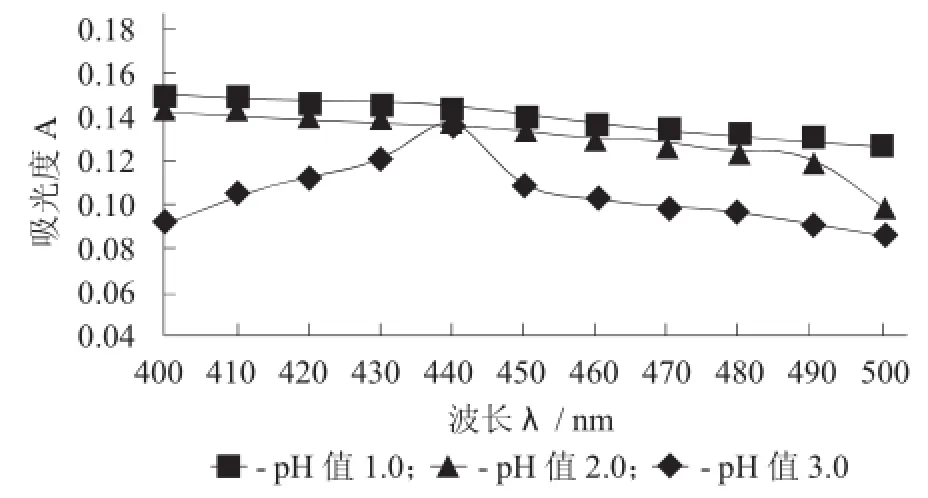
圖1 最大吸收波長的確定
由圖1可知,色素溶液在pH值3.0下,于400~ 500 nm間有1個最大吸收波峰,處于440 nm波長處。于400~440 nm范圍內,隨著波長的增大吸光度有所增大;當波長大于440 nm時,隨著波長的增大吸光度反而有所降低。這是因為在不同的波長下,山茱萸紅色素的選擇性吸收所導致。因此,之后試驗均將色素溶液pH值調至3.0,并且選擇440 nm作為測定吸光度的最佳波長。
2.2光照對山茱萸紅色素穩定性影響
光照對山茱萸紅色素穩定性的影響見圖2。

圖2 光照對山茱萸紅色素穩定性的影響
由圖2可知,1.5 h內,暗光下放置的色素溶液隨時間的延長吸光度下降不明顯;在室內和L66強光下放置的色素溶液吸光度迅速下降,色素溶液顏色變淡。之后,暗置色素溶液的吸光度也開始迅速下降,3 h后3種溶液的吸光度趨于恒定,L66強光下溶液的顏色較其他2種放置條件下的稍淡。由此認為,山茱萸紅色素對光照比較敏感,但在一定貯藏時間內,其穩定性較好。建議在對山茱萸紅色素或其相關產品進行包裝、儲運、使用時,要注意光照對制品色澤的影響,建議采用深色包裝或避光保存的方式進行貯藏。
2.3pH值對色素穩定性影響
pH值對色素穩定性的影響見表1。
溶液中不同濃度的H+和OH-會使色素的發色基團及化學結構發生變化,從而引起變色。由表1可知,山茱萸色素在pH值1.0~4.0的酸性溶液中比較穩定,呈鮮亮的紅色;pH值5.0~6.0范圍內,顏色略微變淺。在中性及堿性條件下,其顏色發生改變,逐漸由淺紫色變為紫色,pH值10.0時變為棕黃色。由于本色素在酸性條件下相對穩定,呈明亮鮮紅色,故適宜應用于果汁、飲料等酸性食品中。

表1 pH值對色素穩定性的影響
2.4溫度對色素穩定性影響
2.4.1溫度與時間對色素穩定性的影響
溫度與時間對色素穩定性影響見表2。

表2 溫度與時間對色素穩定性影響
由表2可知,在相同溫度下,色素溶液隨著時間的延長其吸光度略有降低,但變化不明顯;在不同的溫度下放置相同的時間,色素溶液吸光度會隨著溫度的升高逐漸增大,但變化幅度也不大,溶液顏色變化不明顯。說明山茱萸紅色素對熱的穩定性較好,并且可以較長時間放置,這與長時間光照下的變化一致。
2.4.2溫度與pH值對色素穩定性影響
溫度與pH值對色素穩定性影響見表3。
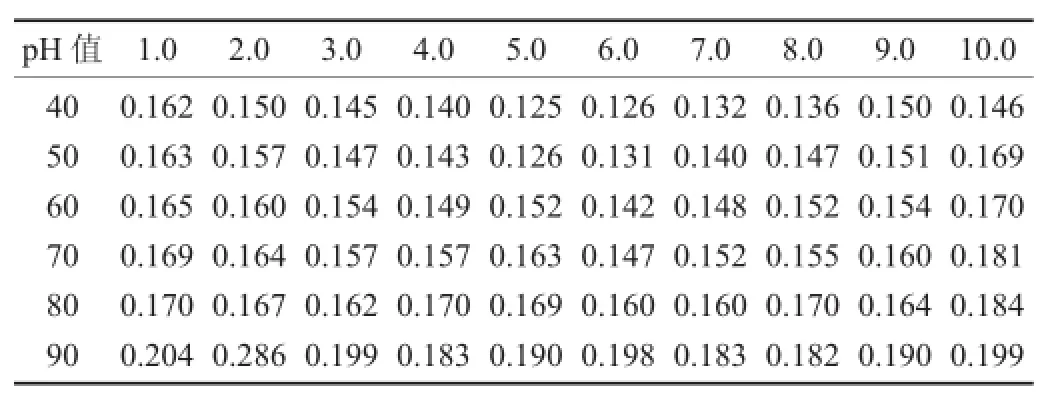
表3 溫度與pH值對色素穩定性影響
由表3可知,在相同的pH值下,隨著溫度的升高,色素溶液的吸光度逐漸升高,但變化不明顯;在任何溫度下,不同pH值色素溶液顏色變化與2.3中的現象一致,均表現為隨著溶液由酸到堿的變化,顏色會由紅變紫。結果證明,該色素對熱比較穩定,而pH值對其影響較大。
2.5金屬離子對色素穩定性影響
金屬離子對色素穩定性影響見表4。

表4 金屬離子對色素穩定性影響
由表4可知,含Na+,Ca2+,Mg2+,Al3+,Zn2+,K+,Cu2+的色素溶液與對照液相比,其吸光度均有不同程度的增加,但顏色變化不大;試驗中觀察到Fe3+會使色素溶液的顏色發生變色而變為淡紫色,說明該金屬離子可能會與此色素中的某些基團反應而使其結構發生變化,或者通過影響溶液酸堿性而使色素結構改變,故在加工與儲運中產品應避免與鐵器接觸;同時,不同濃度Ba2+的存在會使色素溶液變渾濁,這可能是由于Ba2+和山茱萸色素溶液中的某些成分反應生成沉淀的緣故。
2.6氧化劑對色素穩定性影響
H2O2對山茱萸紅色素穩定性的影響見圖3。
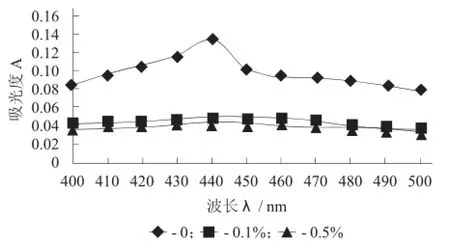
圖3 H2O2對山茱萸紅色素穩定性的影響
由圖3可知,H2O2使色素溶液的吸收峰消失,紫外吸收特征的變化說明色素在氧化劑的作用下結構改變。同時,試驗中觀察到色素溶液的顏色隨著H2O2濃度增大逐漸變淺,直至消失,可見色素對氧化劑極為敏感。
2.7還原劑對色素穩定性影響
Na2SO3對山茱萸紅色素穩定性影響見圖4。
由圖4可知,加入Na2SO3暗置24 h的色素溶液,不同波長下的吸光度均明顯降低,吸收峰也幾近消失,同時色素溶液褪色,可見還原劑可以使色素發生還原反應而對其穩定性產生影響。繼續暗置7 d后,色素溶液吸光度又有較大幅度回升,440 nm處又出現明顯吸收峰,溶液的顏色也由淡紅色逐漸又轉變為紅色。這可能是由于室溫放置條件下SO2從溶液中溢出,使還原劑部分失效而引起。

圖4 Na2SO3對山茱萸紅色素穩定性影響
2.8食品添加劑對色素穩定性影響
食品添加劑對色素穩定性的影響見表5。
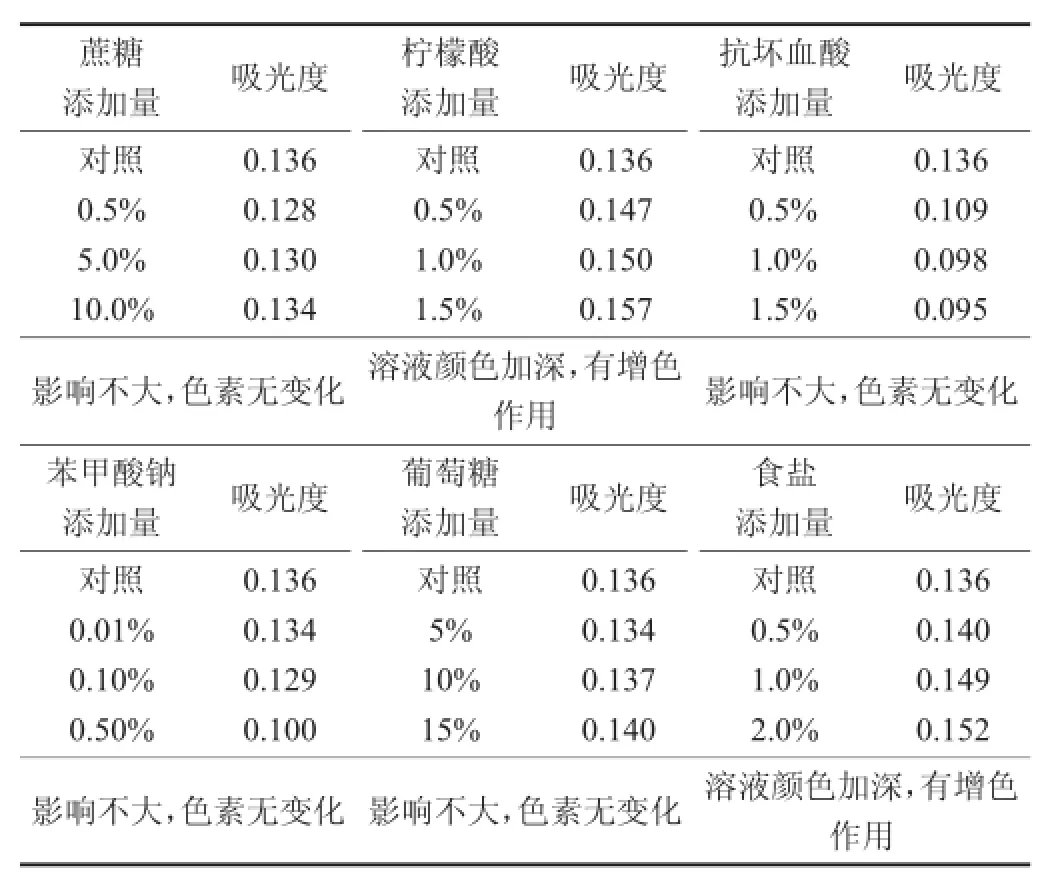
表5 食品添加劑對色素穩定性的影響
由表5可知,與對照相比,添加了不同濃度檸檬酸和食鹽后,溶液的吸光度均較對照增大,溶液顏色也明顯加深;添加了蔗糖、葡萄糖的色素溶液,其吸光度與對照差別不大,顏色基本沒有變化;添加了抗壞血酸和苯甲酸鈉的色素溶液,其吸光度均有降低,且濃度越高吸光值越小,但色素溶液的顏色變化不明顯。因此,蔗糖、葡萄糖、抗壞血酸和苯甲酸鈉對山茱萸紅色素的穩定性影響不大,而檸檬酸和食鹽對山茱萸紅色素具有不同程度的增色作用。
3 結論
pH值3.0時,山茱萸紅色素在可見光區440 nm處有最大吸收峰;山茱萸紅色素在強酸性溶液(pH值1.0~4.0)中比較穩定,呈現鮮亮紅色;0~90℃范圍內山茱萸紅色素對熱比較穩定;山茱萸紅色素對光不穩定,隨光照強度增大,色素溶液顏色變淺;Na+,Ca2+,Mg2+,Al3+,Zn2+,K+,Cu2+對山茱萸紅色素影響不大,Fe3+對該色素具有破壞作用,使色素顏色由紅色變為淡紫色,而Ba2+可使色素溶液產生沉淀而渾濁;還原劑Na2SO3可使山茱萸紅色素褪色,但脫硫后,色素顏色能基本復原;該色素對氧化劑極為敏感,不同濃度氧化劑均可使其褪色,甚至無色;常用食品添加劑蔗糖、葡萄糖、抗壞血酸、苯甲酸鈉等對山茱萸紅色素穩定性影響不大,檸檬酸和食鹽則對該色素有一定的增色作用。
[1]喬華,張生萬,李美萍,等.天然色素穩定性研究及其新的類型劃分 [J].食品科學,2006,27(9):69-72.
[2]劉洪.山茱萸及其主要成分的藥理學研究進展 [J].南京中醫藥大學學報,2003,19(4):254-255.
[3]李小平,陳錦屏.山茱萸果皮紅色素穩定性的研究 [J].食品研究與開發,2002,23(4):25-28.
[4]皮文霞,蔡寶昌.HPLC法及UV法共同監控山茱萸制劑提取純化工藝 [J].現代中藥研究與實踐,2003,17(4):58-59.
[5]徐固華,王欣,等.山楂紅色素提取及穩定性研究 [J].安徽農業科學,2007,35(28):8 785-8 786.
[6]陳存社,董銀卯,陸辛玫,等.食用天然色素的提取及其穩定性研究 [J].天然產物研究與開發,2001,13(6):39-41.
[7]謝程程,王勇,宮立晶.天然食用色素紫甘薯花青素的穩定性研究 [J].食品工業,2012(6):99-102.
[8]耿敬章.香樟籽色素的超聲波輔助提取及其穩定性研究 [J].江西農業大學學報,2009,31(1):119-123.◇
Study on the Stability of the Red Pigment in Cornus officinalis
WU Haixia,MA Guogang
(Department of Life Science,Yuncheng University,Yuncheng,Shanxi 044000,China)
Taking absorbance at 400 nm as standard,the influences of some factors on the stability of the red pigment in Cornus officinalis are discussed.Such as pH value,temperature,light,metal ions,oxidant,reducer and some food additives.The results show that the red pigment is stable relatively for acid and heat,the color faded as the light intensity enhanced,metal ions of low thickness such as Na+,Ca2+,Mg2+,Al3+,Zn2+,K+,Cu2+had no influence on the pigment,but it is unstable if there are Fe3+and Ba2+in solutions.The oxidants and reducers had significant impact on its stability and common food additives had little influence,but citric acid and salt had hyperchromic effect on the pigment.
Cornus officinalis;red pigment;stability
TS202
A
10.16693/j.cnki.1671-9646(X).2016.06.030
1671-9646(2016)06b-0012-04
2016-05-19
運城學院博士啟動基金(YQ-2014031)。
吳海霞(1980— ),女,博士,講師,研究方向為生物活性成分。

