PTP1B及瘦素信號通路在奧曲肽抗大鼠肝纖維化中的作用
陳元淦,張 超,李方躍,牛森森
PTP1B及瘦素信號通路在奧曲肽抗大鼠肝纖維化中的作用
陳元淦,張 超,李方躍,牛森森
目的 研究蛋白酪氨酸磷酸酶1B(PTP1B)在奧曲肽(OCT)治療大鼠肝纖維化過程中的作用機制,及其對瘦素和JAK2-STAT3信號通路的影響。方法 將大鼠隨機分為:空白組、OCT組、模型組。模型組和OCT組采用皮下注射四氯化碳(CCl4)法建立肝纖維化模型。飼養8周后,采集標本,全自動生化分析儀測定血清肝臟生化指標:總膽紅素(TBIL)、丙氨酸氨基轉移酶(ALT)、天冬氨酸氨基轉移酶(AST)及大鼠血清白蛋白(ALB)。ELISA法測定瘦素水平,HE染色觀察肝臟病理,免疫組化法檢測肝組織瘦素及瘦素受體(Ob-Rb)的表達,堿水解法測定肝臟中羥脯氨酸(Hyp)含量。Western blot法檢測肝組織內PTP1B、JAK2、STAT3、p-JAK2、p-STAT3的表達。結果 與空白組比較,模型組和OCT組大鼠血清中TBIL、ALT、AST水平上升(P<0.05),ALB水平明顯降低(P<0.05),血清瘦素、肝組織內瘦素及瘦素受體表達增加(P<0.001)。肝組織中Hyp含量明顯升
網絡出版時間:2016-3-8 8:29:01 網絡出版地址:http://www.cnki.net/kcms/detail/34.1065.R.20160308.0829.020.htm l高(P<0.05)。模型組及OCT組JAK2、STAT3磷酸化水平較空白組升高(P<0.001)。OCT組與模型組比較,肝臟生化指標改善明顯,病理改變較輕,血清瘦素含量減少(P<0.05),肝組織內瘦素、Ob-Rb及Hyp含量降低(P<0.05),JAK2、STAT3磷酸化水平較模型組均有降低(P<0.05),而PTP1B表達增加(P<0.001)。結論 應用OCT能一定程度上減輕大鼠肝維化程度,減輕肝臟損傷。推測其機制是OCT通過上調PTP1B,抑制了瘦素及JAK2/STAT3信號通路的促肝纖維化效應,最終達到抗肝纖維化的目的。
瘦素;奧曲肽;蛋白酪氨酸磷酸酶1B;JAK2/STAT3
肝星狀細胞(hepatic stellate cell,HSC)被認為在肝纖維化的發展過程中有重要地位。各種因素導致肝臟的損傷,使HSC被激活并產生細胞外機制[1]。瘦素與瘦素受體(obese receptor,Ob-Rb)結合,激活下游信號通路JAK2/STAT3,參與了HSC的增殖和活化[2-3]。蛋白酪氨酸磷酸酶1B(protein tyrosine phosphatase 1B,PTP1B)是JAK2/STAT3的負性調控因子。生長抑素是一種能抑制細胞因子合成與分泌的多肽,能夠調節炎癥、免疫過程。其可通過上調HSC內的PTP1B,抑制JAK2/STAT3磷酸化,從而抑制HSC的激活[4]。生長抑素類似物奧曲肽(octreotide,OCT),可被用于治療門靜脈高壓癥[5]。前期實驗[6]顯示,OCT能降低肝纖維化大鼠中瘦素及其受體的表達,減輕肝臟的損害。該實驗通過建立肝纖維化模型,觀察OCT對瘦素及其信號通路和PTP1B表達的影響,探究OCT在抗肝纖維化中的作用機制。
1 材料與方法
1.1 材料與試劑
1.1.1 實驗動物 清潔級成年雄性SD大鼠45只,200~250 g,購自安徽醫科大學實驗動物中心,實驗前在標準環境下適應性飼養。
1.1.2 藥物試劑 四氯化碳(CCl4)及橄欖油購自國藥集團有限公司。將CCl4與橄欖油配成40%的混合溶液(容積比4∶6)。5%乙醇溶液用于造模大鼠唯一飲水。OCT(0.1 mg/ml)購自瑞士Novartis Phama Schwaiz公司,將其稀釋成200 ng/m l用于皮下注射;羥脯氨酸(hydroxyproline,Hyp)測試盒購自南京建成生物工程研究所;瘦素ELISA試劑盒購自上海源葉生物科技有限公司;兔抗鼠瘦素、瘦素受體抗體購自北京博奧森公司;ECL試劑盒、β-actin以及相應二抗均購自北京中杉金橋公司;Western blot所需一抗(JAK2、STAT3、p-JAK2、p-STAT3、PTP1B)購自英國abcam公司。
1.2 實驗方法
1.2.1 動物分組及造模 將大鼠分為:空白組、OCT組、模型組,每組15只。OCT組給予腹部皮下注射OCT 100 ng/100 g,每天2次。空白組和模型組皮下注射等量生理鹽水。肝硬化模型建立:模型組和治療組于左右后肢交替注射40%的CCl4、橄欖油混合溶液(造模3周后出現注射部位潰爛,視情況更改為背部、頸部等部位皮下注射),注射后棉簽按壓,防止溢出。首次注射劑量為0.5 ml/100 g,維持劑量為0.3 ml/100 g(每隔3 d注射1次)。使用動物實驗中心提供的普通飼料用于喂養,5%乙醇溶液為唯一飲用水(飲水狀況不佳時調整乙醇溶液濃度以避免大鼠脫水)。空白組注射等量橄欖油及生理鹽水,普通飼料及飲水喂養。造模時間為8周,實驗過程中每3 d測量體重,用于調節藥物劑量。
1.2.2 標本采集 末次給藥24 h后,戊巴比妥鈉腹腔麻醉后,腹主動脈采血,4℃冰箱靜置120 min后,14 000 r/min離心,取上層血清保存,用于后續檢測。肝左葉取1 cm×1 cm×1 cm肝組織,10%中性甲醛固定。肝右葉取相同大小肝組織,-80℃保存。
1.2.3 血清學檢測 全自動生化分析儀(安徽醫科大學第一附屬醫院檢驗科提供)測定總膽紅素(total bilirubin,TBIL)、丙氨酸氨基轉移酶(alanine aminotransferase,ALT)、天冬氨酸氨基轉移酶(aspartate aminotransferase,AST)及大鼠血清白蛋白(serum albumin,ALB)的含量。
1.2.4 形態學及病理學觀察 甲醛固定后,肝臟組織常規石蠟包埋、切片、HE染色,普通光學顯微鏡下觀察肝臟病理學改變。
1.2.5 檢測肝臟組織瘦素和Ob-Rb的表達 免疫組織化學法測定大鼠肝臟瘦素及Ob-Rb的表達。將切片置于Leica DM4000光學顯微鏡下觀察,400倍下每張切片隨機選取5個不連續視野,將觀察到的明顯棕黃色顆粒視為陽性細胞。Leica DM4000進行拍攝,拍攝后的圖片使用Image ProPlus 6.0圖像分析系統測平均光密度(optical density,OD)值。
1.2.6 組織蛋白提取及測定 取大鼠肝組織20 mg,加入500μl RIPA細胞裂解液,玻璃勻漿器勻漿,置于冰上裂解30 min,離心機預冷至4℃,14 000 r/min離心10 min,取上清液。BCA法測定蛋白濃度,將樣本蛋白總量調成一致。依據不同蛋白分子量,制備8%~10%SDS-PAGE進行蛋白電泳,120~160 min將蛋白轉移到PVDF膜上,3%~5%脫脂奶粉37℃封閉2 h,一抗4℃搖床孵育過夜。一抗濃度分別為PTP1B(1∶500)、JAK2(1∶1 000)、p-JAK2(1∶1 000)、STAT3(1∶1 000)、p-STAT3(1∶1 000);TBST洗膜3次,TBS洗膜1次后將膜置于二抗中,常溫下孵育1~2 h。TBST洗膜3次,TBS洗膜1次后,用ECL發光試劑盒發光。Quantity One軟件分析條帶灰度值。
1.2.7 ELISA法測定血清瘦素含量 按照試劑盒說明書進行操作,用酶標儀在450 nm波長下測定樣本的吸光度值,隨后對照標準曲線測出血清瘦素含量。
1.2.8 堿水解法測定肝臟Hyp含量 按照試劑盒說明書進行操作,用酶標儀在550 nm下測定樣本吸光度值后計算出Hyp含量。
1.3 統計學處理 采用SPSS 17.0軟件進行分析,數據以±s表示。單因素方差分析行多組間差異統計,LSD法進行組間兩兩比較。
2 結果
2.1 大鼠狀況 模型組3只大鼠因感染和營養狀況極差而死亡;OCT組死亡1只;空白組大鼠活動、飲食飲水無異常,精神狀況好,體重逐漸增加;解剖見肝臟無腫大或萎縮,色澤紅潤,表面光滑,邊緣銳利,脾臟色紅潤,無腫大。模型組大鼠于注射CCl4當天開始,精神狀況逐漸變差,毛發干枯,飲食飲水逐漸減少;解剖見肝臟顏色較淺,表面欠光滑,邊緣鈍,可見大小不等的結節,脾臟明顯腫大。OCT組大鼠精神,飲食飲水較模型組有明顯改善;解剖見肝臟表面欠光滑,色澤較淺,表面結節較模型組明顯減少,少數大鼠脾臟輕度腫大。
2.2 大鼠血清相關指標變化及肝組織中Hyp含量的變化 與空白組比較,模型組和OCT組血清AST、ALT、TBIL、肝組織中Hyp含量升高,ALB降低,差異有統計學意義(P<0.05);與模型組比較,OCT組TBIL、AST、ALT和Hyp均有改善,差異有統計學意義(P<0.05)。與空白組比較,模型組和OCT組瘦素表達水平均有升高,差異有統計學意義(P<0.05);與模型組比較,OCT組瘦素水平降低,差異有統計學意義(P<0.05)。見表1。
2.3 肝臟形態學檢測 HE染色顯示,與空白組比較,模型組肝細胞排列紊亂,部分肝細胞氣球樣變、脂肪樣變以及點狀壞死;結締組織廣泛增生包繞肝小葉,正常肝小葉被假小葉取代,中央靜脈偏位或缺如。OCT組較模型組有明顯改善,纖維間隔包繞的假小葉減少,炎性細胞浸潤程度明顯改善,肝細胞變性壞死明顯減少。見圖1。
2.4 瘦素及Ob-Rb的表達 瘦素及Ob-Rb的表達見于HSC的胞質和胞膜,為黃褐色細顆粒沉積。空白組肝細胞內無表達,或僅在肝竇間隙的間質細胞中及匯管區有極少量表達甚至是不表達;模型組瘦素及Ob-Rb表達明顯增加,主要見于HSC中。在肝臟的匯管區、肝竇、血管周圍瘦素及Ob-Rb表達增多。與模型組比較,OCT組陽性表達則明顯減少。空白組瘦素表達量為(0.37±0.07),模型組(0.57 ±0.39)和OCT組(0.49±0.24)均比空白組明顯增加,差異有統計學意義(F=25.204,P<0.001);與模型組比較,OCT組瘦素表達降低,差異有統計學意義(0.57±0.39 vs 0.49±0.24,P<0.05)。空白組Ob-Rb表達量為(0.38±0.09),模型組(0.55± 0.04)和 OCT組(0.46±0.05)均比空白組明顯增加,差異有統計學意義(F=10.899,P<0.001);與模型組比較,OCT組Ob-Rb表達降低,差異有統計學意義(0.55±0.04 vs0.46±0.05,P<0.05),見圖2。
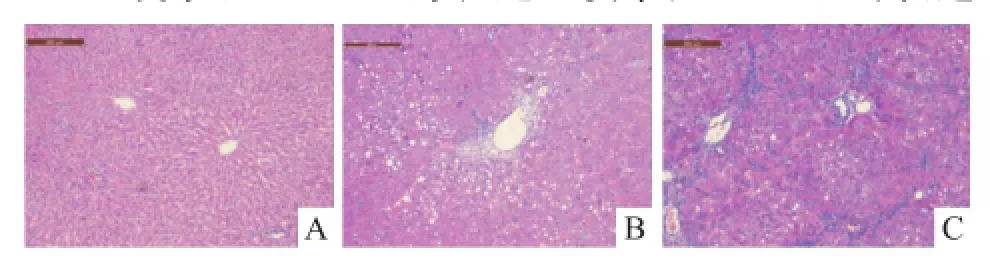
圖1 肝組織 HE染色 ×100A:空白組;B:OCT組;C:模型組
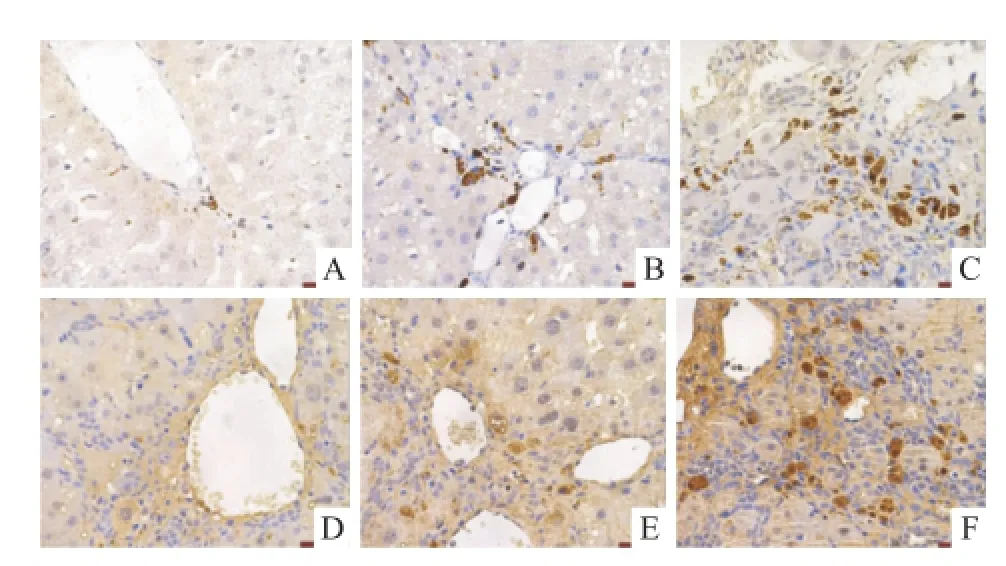
圖2 肝組織瘦素及Ob-Rb表達 ×400A:空白組;B:OCT組;C:模型組;1:瘦素;2:Ob-Rb
表1 大鼠血清TBIL、AST、ALT、ALB、瘦素及肝組織中Hyp含量(n=12,±s)

表1 大鼠血清TBIL、AST、ALT、ALB、瘦素及肝組織中Hyp含量(n=12,±s)
與空白組比較:*P<0.05;與 OCT組比較:#P<0.05
項目 空白組 OCT組 模型組 F值TBIL(μmol/L) 0.61±0.07 1.62±0.33* 2.01±0.31*#75.043 AST(U/L) 101±13 370±57* 470±50*# 185.036 ALT(U/L) 37±5 196±60* 294±51*# 81.375 ALB(g/L) 36.19±1.73 26.68±1.84* 26.49±1.69* 99.977瘦素(ng/m l) 8.24±0.37 10.62±0.87* 11.75±0.95*# 53.398 Hyp(mg/g) 5.43±0.65 9.45±0.78* 11.12±0.93*#136.328
2.5 肝組織內相關蛋白的表達 模型組PTP1B顯著低于其他兩組(P<0.001),OCT組PTP1B表達高于空白組(P<0.05);模型組和OCT組 p-JAK2較空白組明顯升高(P<0.001),而OCT組的表達較模型組降低(P<0.05);模型組和OCT組p-STAT3表達較空白組明顯升高(P<0.001),OCT組較模型組降低(P<0.05)。見圖3、4。
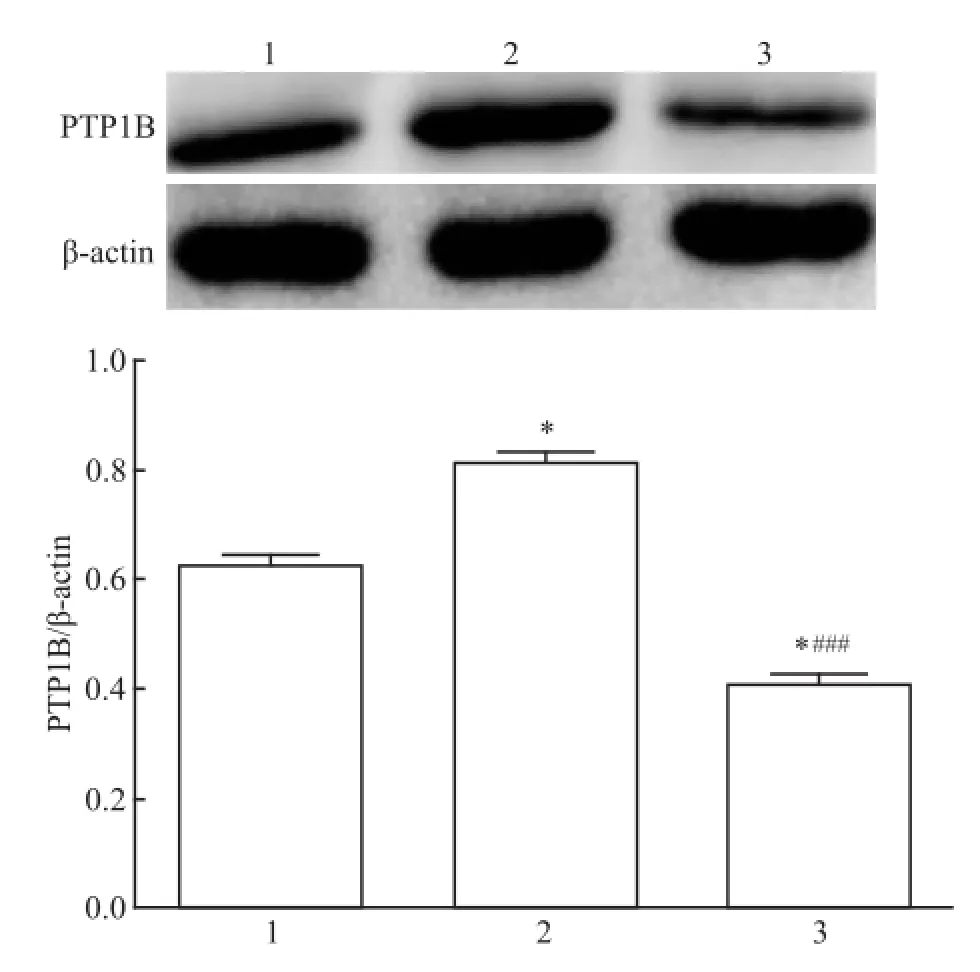

圖3 PTP1B表達水平1:空白組;2:OCT組;3:模型組;與空白組比較:*P<0.05;與OCT組比較:###P<0.001
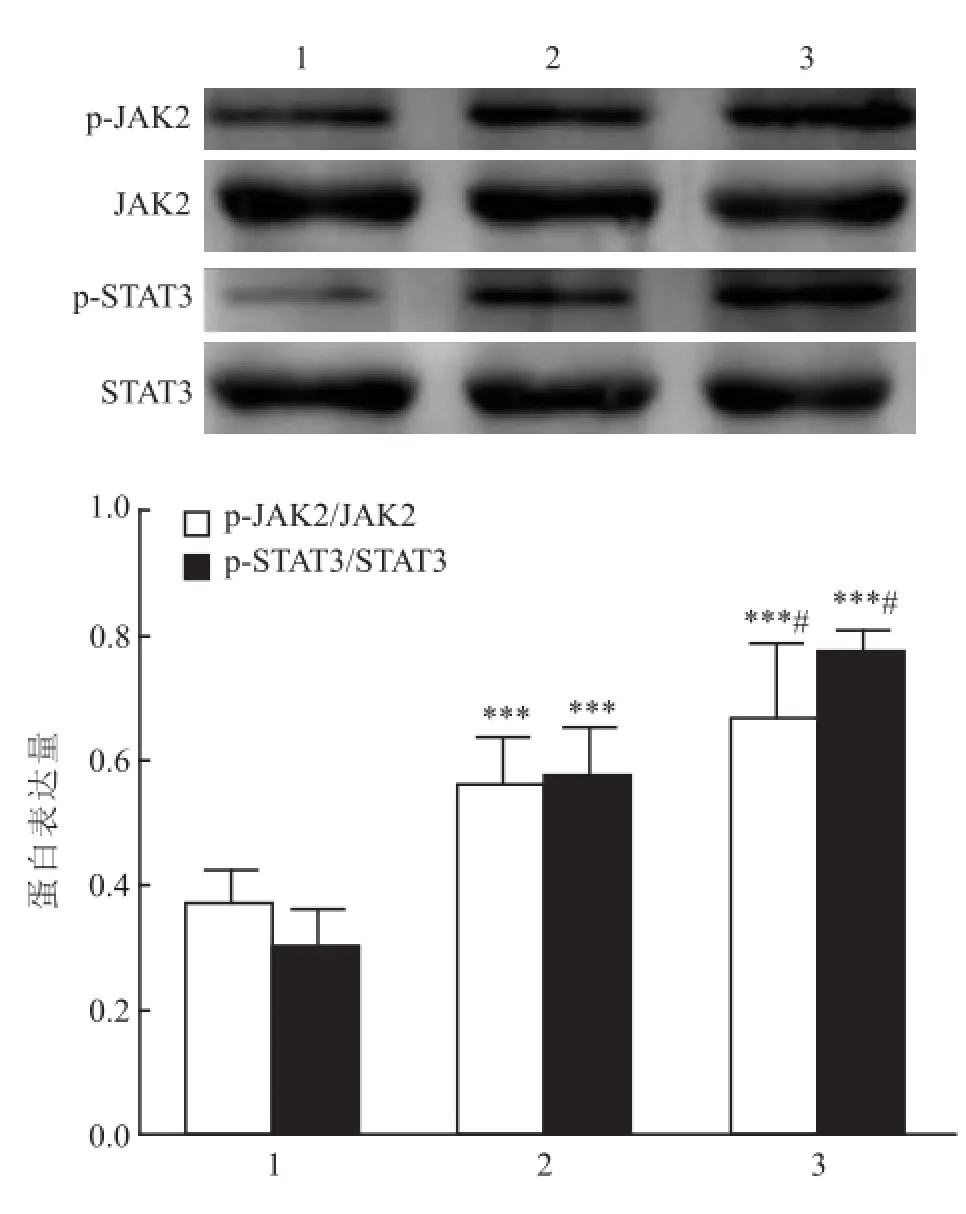

圖4 STAT3、p-STAT3、JAK 2、p-JAK 2表達水平1:空白組;2:OCT組;3:模型組;與空白組比較:***P<0.001;與OCT組比較:#P<0.05
3 討論
CCl4誘導形成肝纖維化模型是最經典和廣泛的建模方法。本實驗利用該方法可制備有效的肝纖維化模型[7]。TBIL、ALT、AST和ALB是反應肝臟功能的重要指標。Hyp為膠原纖維中特有的氨基酸,由于肝纖維化時肝內主要增加的成分為膠原纖維,測量肝Hyp的含量可以反應肝纖維的程度。實驗結果顯示,與模型組比較,OCT組大鼠生存狀態較好,解剖可見肝臟、脾臟外觀有明顯改善;肝臟血清指標提示TBIL、ALT、AST降低明顯,肝 Hyp含量顯著降低,肝臟病理改變較輕,纖維間隔包繞的假小葉明顯減少。在大鼠肝纖維化模型中應用OCT,能明顯改善大鼠生存質量,一定程度上減輕肝纖維化程度,緩解肝纖維化所致的肝功能損害。肝纖維化是病毒、藥物、毒物等各種因素導致的慢性肝損傷,HSC增殖活化是肝纖維化發生發展的重要環節。前期實驗[4]顯示:生長抑素能夠抑制HSC的增殖和活化。推測OCT作為生長抑素類似物,能一定程度上抑制HSC的增殖活化,從而具有一定的抗肝纖維化作用,進而緩解了肝臟的損傷。瘦素是近年來發現的調控HSC的重要因子,HSC也能夠參與合成和分泌瘦素[8]。實驗結果顯示,模型組和OCT組大鼠肝臟內Hyp含量增加,血清瘦素、肝組織中瘦素及其受體表達水平升高,證實了瘦素與肝纖維化程度密切相關。與OCT組比較,模型組大鼠肝功能指標TBIL、ALT、AST明顯升高,肝纖維化指標Hyp增加,血清瘦素水平增加,肝組織瘦素和Ob-Rb表達增加。說明OCT緩解肝纖維化所致的肝功能損害,可能是基于其抑制了瘦素及其受體的表達。瘦素與Ob-Rb結合后,JAK2-STAT3是主要的下游信號轉導通路[9],而PTP1B是調節JAK2-STAT3磷酸化的重要因子。Western blot法檢測顯示,OCT組PTP1B的表達較模型組和空白組均明顯增加,且JAK2/ STAT3的磷酸化程度減小。提示OCT可能上調了PTP1B的表達,較高表達的PTP1B使瘦素下游通路JAK2/STAT3的磷酸化程度降低,這與相關文獻[10]報道相一致。
綜上所述,在CCl4誘導的肝纖維化模型中應用OCT,能夠上調體內PTP1B水平,抑制瘦素下游信號通路JAK2/STAT3的磷酸化。結合前期細胞水平的研究,推測OCT通過該作用機制,抑制HSC的增殖與活化,最終能一定程度上抑制肝纖維化并減輕肝臟損害。但是OCT促進PTP1B的表達是否是其保護作用的唯一機制,以及其是否具有時間和劑量依賴性等問題仍然值得進一步研究。
[1] Lee U E,Friedman SL.Mechanisms of hepatic fibrogenesis[J]. Best Pract Res Clin Gastroenterol,2011,25(2):195-206.
[2] De Minicis S,SekiE,Oesterreicher C,etal.Reduced nicotinamide adenine dinucleotide phosphate oxidase mediates fibrotic and inflammatory effects of leptin on hepatic stellate cells[J].Hepatology,2008,48(6):2016-26.
[3] Handy JA,Fu PP,Kumar P,etal.Adiponectin inhibits leptin signaling via muLtiple mechanisms to exert protective effects against hepatic fibrosis[J].Biochem J,2011,440(3):385-95.
[4] 牛森森,張 超,李方躍,等.生長抑素阻斷瘦素誘導肝星狀細胞增殖及基質分泌的分子機制[J].實用醫學雜志,2014,30 (20):3216-9.
[5] Zhang C,Xu JM,Kong D R,etal.Immediate effects of different schedules of somatostatin on portal pressure in patients with liver cirrhosis[J].JClin Pharm Ther,2008,38(3):206-11.
[6] 姚 磊,張 超,李方躍,等.奧曲肽對實驗性肝纖維化大鼠瘦素及功能性瘦素受體表達的影響[J].安徽醫科大學學報,2012,47(7):800-4.
[7] Vanheule E,Geerts A M,Reynaert H,et al.Influence of somatostatin and octreotide on livermicrocirculation in an experimental mousemodel of cirrhosisstudied by intravital fluorescencemicroscopy[J].Liver Int,2008,28(1):107-16.
[8] Saxena N K,Titus M A,Ding X,et al.Leptin as a novel profibrogenic cytokine in hepatic stellate cells:mitogenesis and inhibition of apoptosis mediated by extracelluLar reguLated kinase (Erk)and Akt phosphorylation[J].FASEB J,2004,18(13):1612-4.
[9] Park H K,Ahima R S.Leptin signaling[J].F1000Prime Reports,2014,6:73.
[10]White S J,Taylor M J,Hurt R T,et al.Leptin-based adjuvants:an innovative approach to improve vaccine response[J].Vaccine,2013,31(13):1666-72.
Octriotide promotes PTP1B expression to protect carbon tetrachloride-induced hepatic fibrogenesis rats
Chen Yuangan,Zhang Chao,Li Fangyue,et al
(Dept of Liver and Biliary Pancreatic Surgery,
The First Affiliated Hospital of AnhuiMedical University,Hefei 230022)
Objective To investigate the mechanisms of octriotide(OCT)protecting carbon tetrachloride-induced hepatic fibrogenesis rats and the effects of protein tyrosine phosphatase 1B(PTP1B)on leptin and JAK2/STAT3 signaling.Methods Adultmale SD ratswere divided into three groups:control,OCT and model group.The liver fibrosismodelswere induced with carbon tetrachloride(CCl4).The levels of total bilirubin(TBIL),alanine aminotransferase(ALT),aspartate aminotransferase(AST),serum albumin(ALB)and leptin in serum and Hyp in liver were tested and histopathology changes were observed.Leptin and obese receptor(Ob-Rb)expressions were observed by immunohistochemical staining.The expressions of the phosphorylation of Janus kinase2(JAK2),signal transducers and activators of transcription 3(STAT3)and PTP1B were tested by Western blot.Resu lts In model and OCT group,compared with the control group,the levels of TBIL,ALT,AST and leptin in serum increased and serum ALB decreased(P<0.05).Compared with the control group,in model and OCT group,the expressions of Hyp,p-JAK2,p-STAT3,leptin and Ob-Rb in liver increased(P<0.05).In OCT group,with lower leptin,OBRb and Hyp expression,the injury of hepatic histopathology was less serious than that in model group.In model group,the expressions of p-JAK2 and p-STAT3 rosemore evidently than OCT group(P<0.05),while PTP1B expressions were lower(P<0.001).Conclusion OCT can ease the CCl4-induced hepatic injury and relieve liver fibrosis.OCT dampens leptin signaling by stimulating PTP1B expression,which is a negative regulator of JAK2/ STAT3,and thus inhibits liver fibrosis.
leptin;octreotide;protein tyrosine phosphatase;JAK2/STAT3
2016-01-18接收
安徽省教育廳自然科學基金(編號:KJ2014A117)
安徽醫科大學第一附屬醫院肝膽胰外科一病區,合肥230022
陳元淦,男,碩士研究生;
張 超,男,副教授,主任醫師,碩士生導師,責任作者,E-mail:smallcloud2@hotmail.com
R 575.2
A
1000-1492(2016)04-0501-05

