采用DNA條形碼技術檢測馬鈴薯4種細菌病害
魏 琪,閔凡祥,張 抒,高云飛,董學志,王文重,楊 帥
(黑龍江省農業科學院植物脫毒苗木研究所,黑龍江哈爾濱150086)
病蟲防治
采用DNA條形碼技術檢測馬鈴薯4種細菌病害
魏琪*,閔凡祥,張抒,高云飛,董學志,王文重,楊帥
(黑龍江省農業科學院植物脫毒苗木研究所,黑龍江哈爾濱150086)
馬鈴薯易受到多種細菌病害的侵染,特別是檢疫性病害和土傳性病害,對馬鈴薯種薯進行全面的細菌病害檢測勢在必行。將檢測檢疫性細菌病害的DNA條形碼技術應用在馬鈴薯4種細菌性病害(環腐病、青枯病、瘡痂病和黑脛病)的檢測中,探討該項技術的應用可行性。采用已知菌株以明確該項技術的應用效果,結果表明,該項DNA條形碼技術檢測馬鈴薯環腐病和瘡痂病的結果良好;檢測青枯病可以確定到屬;檢測黑脛病時配合特異性基因,可獲得良好的檢測結果。該DNA條形碼技術是標準性操作規程與測序技術相結合的一種方法,檢測結果的準確性高,同時可以在大規模樣品的檢測工作中縮減工作量,提高檢測效率。
DNA條形碼技術;馬鈴薯;環腐病;青枯病;瘡痂病;黑脛病
中國是世界第一大馬鈴薯生產國。馬鈴薯在實際生產中會受到多種病原細菌的影響而導致減產、甚至絕產。這些病原細菌引起的馬鈴薯病害分為2類:一類為允許率為“0”檢疫性病害,如馬鈴薯環腐病和青枯病;另一類為非檢疫性病害,但嚴重影響馬鈴薯生產的病害,如馬鈴薯黑脛病、軟腐病及瘡痂病。馬鈴薯種薯傳播方式是上述細菌性病害大范圍傳播的重要途徑之一。因此,對于馬鈴薯種薯進行主要細菌病害的檢測勢在必行。
1 材料與方法
1.1材料
供試菌株及待檢馬鈴薯樣品來源見表1。

表1 樣品來源Table 1Source of sample
1.2方法
1.2.1DNA提取、PCR擴增及測序
采用北京天根生化科技(北京)有限公司的新型植物基因組提取試劑盒(DP320)提取所有樣品的DNA。分子生物學試劑均為Takara公司產品。
擴增及測序引物、擴增體系及擴增條件參考歐盟內檢疫性有害生物的DNA Barcoding數據庫網站(www.q-bank.eu)內細菌鑒定流程中所推薦的方法,并進行必要的調整。所用引物均由英濰捷基(上海)貿易有限公司合成,其序列見表2和表3。
獲得的擴增序列由英濰捷基(上海)貿易有限公司和華大基因科技股份有限公司進行測序。
根據最新流行病學資料顯示[7-8],全球糖尿病患者人數在3.8億左右,是目前最為嚴重的代謝性疾病之一,嚴重影響患者的生活質量和生活健康。糖尿病患者往往存在多飲、多食、多尿以及身體消瘦等臨床癥狀,對糖尿病患者進行中醫護理具有重要意義。中醫認為人體是一個有機的整體,強調人與自然、環境的相互統一,中醫學中,糖尿病(消渴)病機是陰津虧損、稟賦不足以及燥熱偏盛等,所以強調在疾病的治療和康復中保證患者的生活護理質量,從整體的角度出發。其次,中醫特色護理具有個性化特征,針對不同個體患者和患者疾病的不同階段[9],在中醫辨證的基礎上進行個體化指導,能夠讓治療具有針對性,促進患者的康復。
1.2.2病害檢測流程
本研究中主要檢測的馬鈴薯細菌性病害種類有環腐病、青枯病、黑脛病和瘡痂病,引起這4種病害的病原菌分別來自Clavibacter屬、Ralstonia屬、Pectobacterium屬和Streptomyces屬。研究中采用歐盟內檢疫性有害生物的DNA Barcoding數據庫網站(www.q-bank.eu)推薦的病害檢測流程見圖1。首先,根據16S rDNA的測序及Blast比對結果,初步判斷各樣品所含病原菌的屬。在這個結果的基礎上,分別使用其他基因,進行病原菌的進一步鑒定。其中,Clavibacter屬和Streptomyces屬采用DNA促旋酶B亞單位基因(GyrB);Ralstonia屬采用DNA錯配修復基因(mutS),Pectobacterium屬采用基因組的基因。
1.2.3序列比對及同源性分析
由于采用的檢測樣品存在多種病原菌共同侵染的情況以及馬鈴薯塊莖組織內含物相對復雜等情況,因此在DNA提取、PCR擴增和測序的過程中,均有可能會出現結果不佳的情況,所以本研究對結果不佳的樣品進行汰出,以最終獲得有效的病原菌基因序列的個體來進行分析。

表2 3種細菌擴增引物及測序引物Table 2Three kinds of primers used for PCR-sequencing bacteria

表3 Pectobacterium屬細菌擴增引物及測序引物Table 3Primers used for PCR-sequencing Pectobacterium
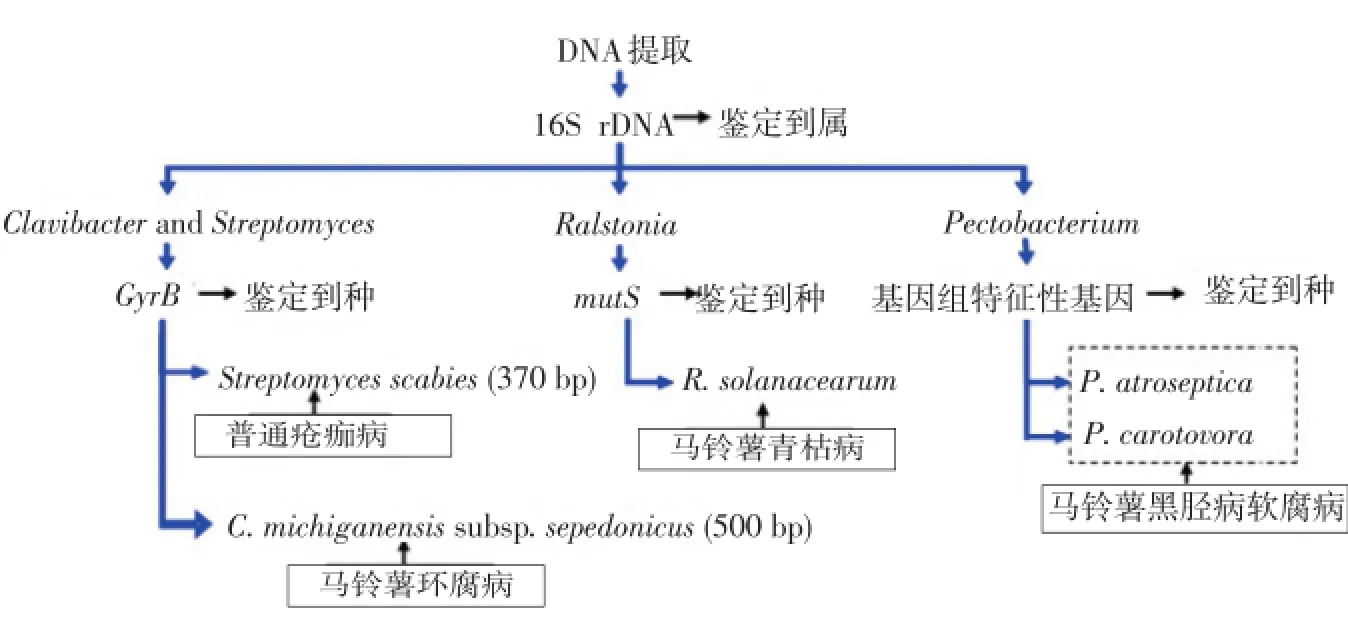
圖1 馬鈴薯細菌病害檢測方案Figure 1Detection scheme for potato bacterial diseases
采用Chromas軟件對獲得的堿基序列進行峰值圖的檢查,確定序列的準確性及截取有效片段長度,將確定有效測序結果與GenBank中的現有數據庫進行Blast比對和分類學比較,判斷被測樣品中病原菌的屬。利用MEGA6軟件分析序列間的相似度,并構建系統發生樹。
2 結果與分析
2.116S rDNA檢測結果及分析
將供試樣品進行16S rDNA序列擴增,YA-6無PCR產物,其他樣品經瓊脂糖凝膠電泳檢測PCR產物情況(圖2)。每個樣品的PCR產物分別經過2條引物進行測序后,分析二者的重合序列,用該重合序列進行Blast比對,比對結果見表4。其中,樣品1-1、HJ1、QK3、YA-4、ZN-1的測序結果不能獲得有效的重合序列,因此不能進行16S rDNA的比對分析。
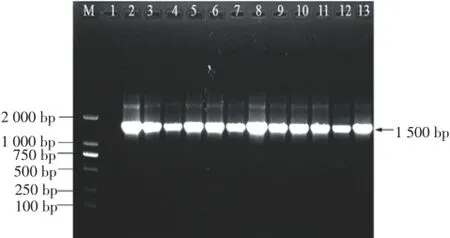
圖2 供試樣品16S rDNA-PCR結果Figure 216S rDNA-PCR results
2.2后續基因擴增及測序
根據表4中所示的16S rDNA序列比對結果,進行后續基因檢測分析。
2.2.1Clavibacter屬和Streptomyce屬的GyrB基因擴增
樣品HF1、YA-3、YA-5、28-2、YA-4進行550 bp的GyrB基因擴增,電泳結果見圖3,從圖3中可知,Streptomyce屬的28-2也獲得了擴增產物,其條帶大小明顯小于500 bp;Clavibacter屬的HF1、YA-3、YA-5及YA-4均獲得了550 bp左右的產物。YA-4的16S rDNA未獲得重合序列,因此,僅進行GyrB基因的PCR擴增,未測序。樣品HF1、YA-3、YA-5以及28-2進行GyrB基因序列測定。

表4 7個樣品的16S rDNA序列比對結果Table 4Blast comparison with 16S rDNA sequences of seven samples

圖3 Clavibacter屬和Streptomyce屬的GyrB基因擴增Figure 3GyrB-PCR results of Clavibacter and Streptomyce
2.2.2Ralstonia屬的mutS基因擴增
樣品QK1、QK3及1-1進行767 bp的mutS基因擴增,電泳結果見圖4,從圖4中可知,1-1未產生目的條帶,而QK1和QK3均獲得了與預期相似的目的條帶,其中對QK1的mutS基因擴增產物進行測序分析。

圖4 Ralstonia屬的mutS基因擴增Figure 4mutS-PCR results of Ralstonia
2.2.3Pectobacterium屬的基因擴增
樣品HJ2和FL-1分別進行P.atrosepticum基因組和P.carotovorum基因組的特異性引物擴增及測序,電泳結果見圖5和圖6。從電泳圖5中可知,HJ2擴增出P.atrosepticum基因組的特異性目的片段,而FL-1并未獲得任何PCR產物。因此,HJ2的P.atrosepticum-PCR產物進行測序。從電泳圖6中可知,樣品HJ2和FL-1均未擴增出P.carotovorum基因組的特異性片段。

圖5 P.atrosepticum基因組特異性擴增Figure 5PCR of P.atrosepticum by special primers
2.2.4序列比對分析
將樣品HF1、YA-3、YA-5和28-2的GyrB基因序列測定結果、QK1的mutS基因測序結果和HJ2的P.atrosepticum基因組PCR產物的測序結果在GenBank進行Blast的比對分析,分析結果見表5。從表5可知,樣品HF1、YA-3、YA-5的病害類型均為C.michiganensis subsp.sepedonicus;樣品QK1為R.pickettii;樣品HJ2為P.atrosepticum;樣品28-2為S.scabiei。

圖6 P.carotovorum基因組特異性擴增Figure 6PCR of P.carotovorum by special primers
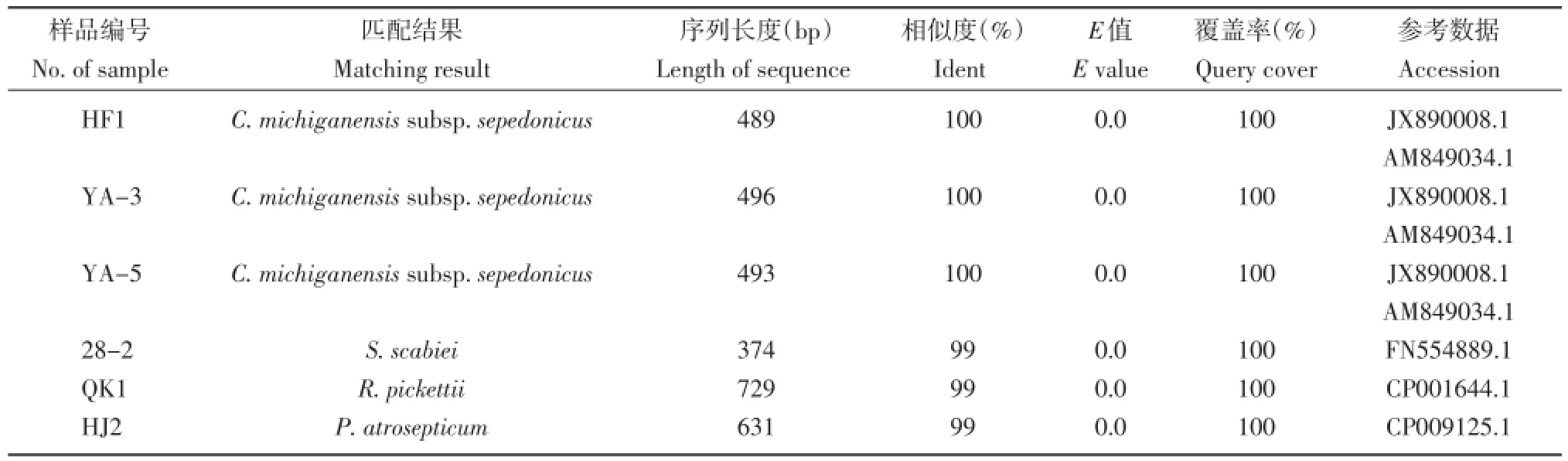
表5 6個樣品的其他基因序列比對結果Table 5Blast comparison with other gene sequences of six samples
3 討論
3.1DNA條形碼技術檢測結果的比較
4種病害的已知菌液中,HF1、HJ2和28-2的16S rDNA序列比對結果、GyrB基因鑒定結果與已知結果相一致;QK1的樣品原為R.solanacearum,而本研究所使用的條碼技術鑒定結果卻為R.pickettii,該樣品在“種”鑒定方面存在差異。
在病害待檢的樣品鑒定中,YA-3的16S rDNA序列比對結果與GyrB基因擴增及測序結果差異很大,YA-5的16S rDNA序列比對結果是未知菌株,但是,YA-3和YA-5的GyrB基因擴增的電泳圖中可明顯看出二者與HF1一致,經過測序后比對發現,二者確實為C.michiganensis subsp.sepedonicus,與HF1結果一致。而且,YA-3、YA-4和YA-5經環腐病Real-Time PCR方法驗證均為C.michiganensis subsp.sepedonicus[14],與應用DNA條形碼技術的檢測結果一致。因此,本研究應用的DNA條形碼技術檢測C.michiganensis subsp.sepedonicus時,采用16S rDNA序列與GyrB基因相結合,其中GyrB基因鑒定結果良好,田茜等[12]的分析認為cpn60基因具備作為Clavibacter屬內亞種級別區分鑒定用基因的潛力。但是,在實際應用中,GyrB基因即可滿足馬鈴薯病害檢測的要求。主要原因是,該基因可以將2種革蘭氏陽性菌引起的馬鈴薯環腐病和瘡痂病區分開來,獲得準確的馬鈴薯瘡痂病檢測結果。
3.2復合侵染樣品對DNA條形碼技術檢測結果的影響
DNA條形碼技術在應用的過程中對被測樣品的DNA質量要求較高,特別是在16S rDNA序列的比對中[12]。在本研究中,采用的供試馬鈴薯塊莖樣品可能存在多種細菌病害復合侵染的情況,導致16S rDNA序列的測定后無法獲得足夠長度的重合序列。因此,在應用該DNA條形碼技術檢測馬鈴薯細菌病害時,需要對待檢樣品提取DNA時應確保是單一菌株侵染并保證提取的DNA質量良好。如果無法保證待檢樣品是單一病害侵染時,應先對待檢樣品進行菌株的分離培養,再逐一挑取病原菌進行16S rDNA序列的擴增等檢測工作。同時,在檢測過程中務必設立空白對照,以保證PCR反應未發生污染現象。
3.3DNA條形碼技術檢測馬鈴薯細菌病害的可行性
本文所應用DNA條形碼技術是根據歐盟地區的檢疫性細菌病害DNA條形碼技術進行必要的改良后建立的。在本研究中,該技術在馬鈴薯環腐病檢測的應用效果良好,可以作為馬鈴薯環腐病的一種檢測體系在實際工作中應用。然而,該DNA條形碼技術檢測馬鈴薯青枯病時,可以獲得“屬”的鑒定結果,但是在“種”的鑒定中未能獲得理想的檢測結果,因此,該方法需要進一步對mutS基因或其他特異性基因進行篩選研究后,以獲得更加準確的檢測鑒定結果。
在馬鈴薯瘡痂病的檢測上,借鑒了馬鈴薯環腐病的檢測方法,本研究發現該方法可檢測S.scabiei(馬鈴薯普通瘡痂病菌),而對于其他種的馬鈴薯瘡痂病菌還將繼續進行應用研究。在馬鈴薯黑脛病的檢測中,雖然已知樣品在16S rDNA序列中獲得了準確的檢測結果,但是在待檢樣品的檢測中未獲得良好的檢測結果,因此,該DNA條形碼技術在馬鈴薯黑脛病檢測中應用需要配合以該病原菌特異性基因。
除2種馬鈴薯檢疫性病害之外,本研究拓展了該DNA條形碼技術的檢測范圍,將其應用在非檢疫性病害的病原細菌(瘡痂病和黑脛病菌)等方面。本研究初步構建的馬鈴薯4種細菌病害DNA條形碼技術檢測流程使得馬鈴薯種薯質量檢測中獨立的待檢樣品進行多種細菌性病害檢測得以實施,待檢樣品首先經過16S rDNA序列的分類后,再進行具體病原菌種類的鑒定。而且標準操作和測序技術的相結合使得檢測結果準確性高,還可以避免待檢樣品按照不同病害種類多次進行特異性PCR擴增的工作,大大縮減工作量。該項技術既可保證操作的標準性和結果的準確性,還大大提高馬鈴薯病害的檢測效率,因此,該項技術在馬鈴薯種薯生產中應用潛力巨大。
[1]Hebert P D,Ratnasingham S,Waard J R.Barcoding animal life:cytochrome coxidase subunit 1 divergences among closely related species[J].Proc Biol Sci,2003,270(s1):96-99.
[2]Jordaens K,Goergen G,Virgilio M,et al.DNA barcoding to improve the taxonomy of the Afrotropical hoverflies(Insecta: Diptera:Syrphidae)[J].PLoS One,2015,10:1-15.
[3]Sizhu Z,Jialin L,Yihan W,et al.DNA barcoding identification of Dermestidae species[J].Mitochondrial DNA,2015,5:1-5.
[4]朱惠敏,連一陽,王中鐸,等.基于cox1條形碼的魚肚DNA分子鑒定[J].廣東海洋大學學報,2014,34(6):1-5.
[5]周美玉,陳驍,楊圣云.采用DNA條形碼技術對廈門海域魚卵、仔稚魚種類的鑒定[J].海洋環境科學,2015,34(1): 120-125,135.
[6]王曉明,姬可平,牛憲力,等.DNA條形碼與動植物分類學的研究[J].生物信息學,2012,10(2):83-86.
[7]陳士林,龐曉慧,羅焜,等.生物資源的DNA條形碼技術[J].生命科學,2013,25(5):458-466.
[8]Liu Y,Sun W,Liu C,et al.Identification of Hippophae species (Shaji)through DNA barcodes[J].Chin Med,2015,10:1-11.
[9]Andreakis N,Hθj L,Kearns P,et al.Diversity of marine-derived fungal cultures exposed by DNA barcodes:the algorithm matters[J]. PLoS One,2015,10:1-22.
[10]陳巖,張立,劉力,等.我國檢疫性有害生物DNA條形碼信息系統建設[J].植物檢疫,2014,28(1):1-5.
[11]張穗生,陳英,陳小玲.微生物DNA條形碼技術的研究進展[J].廣西科學,2015,22(1):27-30.
[12]田茜,張美,胡潔,等.植物病原細菌DNA條形碼檢測技術[J].植物檢疫,2014,28(6):1-7.
[13]Humphris S N,Cahill G,Elphinstone J G,et al.Detection of the bacterial potato pathogens Pectobacterium and Dickeya spp.using conventional and Real-time PCR[J].Plant Pathology:Method in Molecular Biology,2015,1302:1-16.
[14]魏琪,胡林雙,董學志,等.馬鈴薯環腐病菌Real-time Taqman-PCR檢測體系的建立[J].中國馬鈴薯,2010,24(5): 301-305.
Detection of Four Bacterial Diseases of Potato by DNA Barcoding
WEI Qi*,MIN Fanxiang,ZHANG Shu,GAO Yunfei,DONG Xuezhi,WANG Wenzhong,YANG Shuai
(Virus-free Seedling Research Institute,Heilongjiang Academy of Agricultural Sciences,Harbin,Heilongjiang 150086,China)
ract:Potato is vulnerable to infection by a variety of bacterial diseases,especially quarantine diseases and soil-borne diseases,and to advance a comprehensive detection of bacterial diseases for seed potato bacterial disease is imperative.In this research,four bacterial diseases of potato,including potato ring rot,bacterial wilt,potato common scab, and black leg,were detected using DNA barcoding technique to investigate the application feasibility of the technology for potato bacterial disease testing.Known strains were used to assess the detection results.The DNA barcoding technique was good for potato ring rot and potato scab detection.Bacterial wilt was determined to genus level.Black leg could also be detected by combination of DNA barcode technology and specific gene.The DNA barcoding technique includes a standard method of operating procedures,and sequencing technology,which could achieve high accuracy of testing,reduce the workload of large-scale work in potato bacterial diseases testing,and improve the detection efficiency.
rds:DNA barcoding;potato;ring rot;bacterial wilt;common scab;black leg
S532
A
1672-3635(2016)02-0105-07
2016-01-15
黑龍江省青年科學基金項目(QC2012C063);現代農業產業技術體系專項資金資助(CARS-10-P14);國際合作項目(2013DFA31970);國家科技支撐項目(2012BAD06B02);公益性行業科研專項經費項目(201303015-9)。
魏琪(1981-),女,博士,副研究員,主要從事馬鈴薯病害檢測技術的研發工作。
(Corresponding author):魏琪,E-mail:weiqi1981917@126.com。

