不同產地白術藥材中白術內酯I和II的含量測定
吳梓春 何兆錦(廣東省佛山市第一人民醫院(中山大學附屬佛山醫院)藥學部 佛山 528000)
不同產地白術藥材中白術內酯I和II的含量測定
吳梓春何兆錦(廣東省佛山市第一人民醫院(中山大學附屬佛山醫院)藥學部佛山528000)
目的:探討不同產地白術藥材中白術內酯I和白術內酯II的高效液相測定方法。方法:選擇浙江、安徽、甘肅、江西四個產地的白術藥材,色譜柱采用Hypersil 0DS(4.6mm×250mm,2.5μm),流動相為乙腈∶水=55∶45,流速為1.0ml/min,柱溫為30℃,檢測波長223nm。結果:白術內酯I的線性關系方程為:Y=3.546×104+0.524×104(r=0.9998),在0.5~500μg范圍內線性關系良好;白術內酯II的線性關系方程為:Y=4.746×104+0.949×104(r=0.9997),在0.5~500μg范圍內線性關系良好。白術內酯I的平均加樣回收率為99.74%,RSD1.32%,白術內酯II平均加樣回收率為99.68%,RSD為2.01%。浙江產白術藥材中兩種有效成分含量最高,江西產白術藥材的兩種有效成分含量較低。結論:高效液相色譜法測定不同產地白術中的有效成分,方法簡單易操作,靈敏度高,準確性好,重復性強,可以作為白術質量控制的定量指標。
白術內酯I白術內酯II高效液相色譜 不同產地
中藥白術為菊科(Composetae)蒼術屬(Atractylodes)植物白術(Atractylodes macrocephala Koidz)的干燥根莖[1],多數分布于我國的浙江、安徽、甘肅、湖南以及江西等產地[2]。白術味苦、甘,性溫,主要歸脾胃經,功能健脾益氣,燥濕利水,為補益類的補氣中藥材[3]。由于我國白術的產地較多,藥材的質量也有一定的差異,我國各個地域的生態環境、氣候等不同,導致了不同產地白術藥材有效成分的含量存在差異。為了加強白術藥材的質量控制,本研究以白術中白術內酯I、白術內酯II的含量作為觀察指標,采用高效液相色譜法觀察不同產地白術中上述兩種有效成分的含量。
1 儀器與試藥
1.1實驗儀器:日本島津LC-10AT型單泵高效液相色譜儀,SPD-10AVP型紫外檢測器,島津CBM色譜工作站。手提式高速萬能粉碎機DFD-100、4號篩,電熱恒溫鼓風干燥箱,KQ-500E型超聲波清洗儀,美國梅特勒電子分析天平(精密度為0.0001g),PL-80離心沉淀機。
1.2實驗試藥:白術藥材采自浙江、安徽、甘肅、江西四個產地,藥材均經專家鑒定分別為菊科(Compositae)植物白術(Atractylodes macrocephala koidz)的干燥根莖和菊科植物Atractylades macrocephalacv.Yuzhu的干燥根莖。乙腈為色譜純,水為三蒸水,其他試劑均為分析純。
2 方法與結果
2.1色譜條件的選擇:色譜柱采用Hypersil 0DS(4.6mm×250mm,2.5μm),流動相為乙腈∶水=55∶45,流速為1.0ml/min,柱溫為30℃,檢測波長223nm,進樣量為20μL。以白術內酯I作為參考,色譜柱的理論塔板數>5000。
2.2對照品溶液的制備:精密稱定白術內酯I對照品0.4mg,置于5ml容量瓶中,甲醇溶液定溶至刻度后搖勻,靜置;取白術內酯II對照品0.45mg精密稱定后置于5ml容量瓶中,甲醇溶液定溶至刻度后搖勻,靜置。兩種對照品溶液置于-20℃冰箱中保存,備用。
2.3供試品溶液的制備:取白術藥材2.0g置于粉碎機中粉碎后過4號篩,精密稱定后置于加塞錐形瓶中,加入甲醇溶液50ml后稱定重量,超聲處理40min。放冷后再次稱定重量,甲醇溶液將減少的重量補足后以塞蓋住錐形瓶,搖勻,過0.45μm微孔濾膜后,置于3000轉/min的離心機中離心10min,取上清液即得供試品溶液。
2.4標準曲線的繪制:將分別溶解于甲醇溶液中的白術內酯I、白術內酯II對照品溶液稀釋成0.5、1.0、5.0、10.0、20.0、50.0、80.0、100.0μg/ml的白術內酯I、II標準溶液,按照“2.1”項下的色譜條件,分別進樣20μL,以白術內酯I、II色譜峰面積作為縱坐標,白術內酯I、II對照品質量濃度為橫坐標繪制標準曲線,得到回歸方程以及相關系數。白術內酯I的線性關系方程為:Y= 3.546×104+0.524×104(r=0.9998),在0.5~500μg范圍內線性關系良好;白術內酯II的線性關系方程為:Y=4.746×104+0.949×104(r=0.9997),在0.5~500μg范圍內線性關系良好。
2.5穩定性考察:取同一批次的樣品藥材,按照“2.3”項下供試品溶液的制備方法進行操作,制備供試品溶液后精密吸取同一供試品溶液,按照“2.1”項下的色譜條件進樣,分別在配制溶液后0、1、4、6、8、12、24h吸取20μL進樣分析,按照線性關系方程計算白術內酯I、白術內酯II在供試品溶液中的穩定性,結果表明白術內酯I的RSD值為2.14%,白術內酯II的RSD值為2.01%,表明溶液在24h內較為穩定。
2.6精密度考察:將:2.5:項下配制的同一批次供試品溶液,吸取20μL,按照“2.1”項下的色譜條件重復進樣5次,計算峰面積值,結果表明其RSD值為1.36%,表明該儀器的精密度良好。
2.7重現性考察:取同一白術樣品粉末,精密稱取5份,每份為1.245g,按照“2.3”項下的供試品溶液的制備方式進行配制,按照“2.1”項下的色譜條件進樣后得到白術內酯I、白術內酯II的RSD分別為1.84%、1.76%,表明該色譜條件下測定結果的重現性良好。
2.8加樣回收率試驗:精密稱取已知白術內酯I、白術內酯II含量的白術粉末,精密稱定5份,精密加入白術內酯I、II對照品適量,按照“2.3”項下供試品溶液的制備方式進行供試品溶液的配制,按照“2.1”項下的色譜條件進行色譜圖的分析,計算平均加樣回收率,結果見表1、表2。
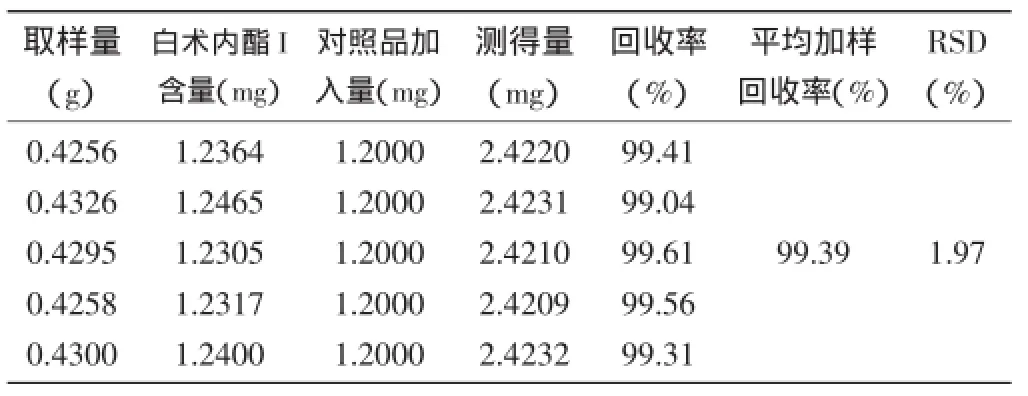
表1 白術內酯I加樣回收率測定結果(n=5)

表2 白術內酯II 加樣回收率測定結果(n=5)
2.9不同產地白術含量測定結果:取浙江、安徽、甘肅、江西白術樣品約1.0g,精密稱定后按照“2.3”項下的供試品溶液制備溶液并進行處理測定,按照“2.1”項下的色譜條件進樣,計算不同產地白術藥材中白術內酯I、II的含量并進行比較,結果見表3。
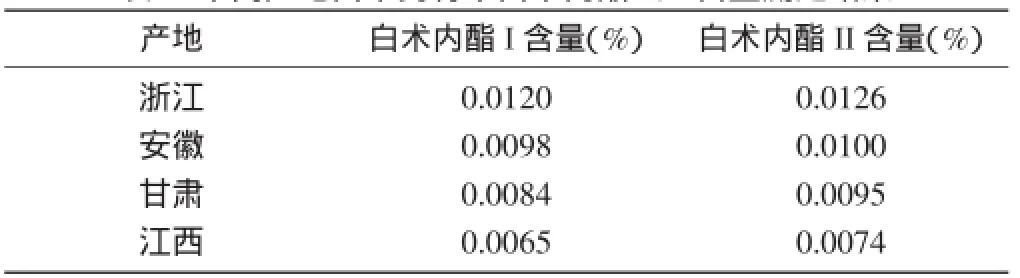
表3 不同產地白術藥材中白術內酯I、II含量測定結果
3 討論
3.1流動相的選擇:本研究中采用了乙腈:水,甲醇:水等按照不同比例流動相系統,結果顯示在乙腈∶水=55∶45時色譜系統可以獲得較好的峰形,同時色譜峰分離較好。因此實驗中選擇乙腈:水作為流動相。
3.2檢測波長的選擇:采用Agilent 1100DAD三維圖譜進行分析得到白術內酯類化合物在223nm處有最大的吸收峰,為了在同一條件下進行檢測,選擇同時檢測兩個波長的信號[4]。
不同產地的白術內酯含量具有一定的差異[5],在相同的測定條件下,分離得到的白術內酯I、II含量,浙江產地的白術藥材中最多,江西產地的藥材則偏少,因此如果要獲得較多含量的白術內酯可以選擇浙江產的白術中藥材。
[1]趙桂芝,洪學智.白術內酯的藥理學研究進展[J].中國藥房,2012,20(3):230-231.
[2]曾志,周育妹.3個不同產地白術的揮發性化學成分比較[J].華南師范大學學報,2012,47(5):78-83.
[3]趙紅紅.三產地白術揮發油氧化分解后化學成分的變化[J].山西大學學報,2015,38(3):516-521.
[4]田穎.不同產地白術藥材中白術內酯II和III的含量測定[J].海峽藥學,2012,24(8):65-67.
[5]姜東京,徐志偉.浙江道地藥材於術與白術的質量對比研究[J].中華中醫藥學刊,2014,32(12):2864-2866.
R284.1
A
1672-8351(2016)09-0010-02

