共聚物接枝蛋白離子交換色譜介質制備及性能
張素玲,楊葳,余林玲,白姝,孫彥,史清洪
?
共聚物接枝蛋白離子交換色譜介質制備及性能
張素玲,楊葳,余林玲,白姝,孫彥,史清洪
(天津大學化工學院生物化工系,系統生物工程教育部重點實驗室,天津 300354)
高容量蛋白質色譜介質是色譜過程高效化的材料基礎和重要前提。采用原子轉移自由基聚合(ATRP)技術,以甲基丙烯酸3-磺酸丙酯鉀和甲基丙烯酸甲酯(MMA)為單體化合物合成了多種無規共聚物接枝離子交換色譜介質,并對其蛋白質吸附性能進行研究。單體總濃度一定情況下共聚物接枝色譜介質孔道半徑(pore)隨MMA濃度升高而增大,反映出接枝共聚物鏈漸趨塌陷的特征。蛋白質吸附結果表明,溶菌酶吸附容量取決于介質的離子交換容量;而抗體吸附容量則與pore及相應的聚合物層厚度變化密切相關。隨著聚合物層厚度的增大,聚合物層對抗體的空間排阻作用增強,抗體吸附容量下降。此外,引入MMA優化共聚物分子鏈可顯著提高蛋白質吸附量,在SEP-S30/M30介質中抗體和溶菌酶的飽和吸附量分別達到237 mg·g-1和380 mg·g-1。無規共聚物接枝離子交換色譜介質孔道內聚合物層厚度和蛋白質吸附也受無機鹽濃度調控。
共聚物接枝離子交換色譜介質;原子轉移自由基聚合;蛋白質;吸附;高容量;抗體
引 言
蛋白質離子交換色譜介質是蛋白質色譜技術的核心構件和技術創新的物質基礎,開發高容量的蛋白質離子交換色譜介質成為色譜過程高效化的重要前提。
20世紀90年代起,以POROS灌注介質[1]、超大孔色譜介質[2-3]和整體柱介質[4-5]為代表的新型色譜材料相繼問世。上述色譜介質的共同特征是引入微米級對流孔道強化色譜介質內蛋白質的傳質速率,實現對介質結合位點的更有效利用,提高蛋白質結合容量。但傳統色譜介質中蛋白質的結合僅發生在介質孔道的表面,飽和吸附容量受限于介質的比表面積[6]。HyperD[7]和Fractogel EMD[8]等雜化色譜介質通過引入聚丙烯酰胺凝膠或聚合物分子在介質孔道內構建“腳手架”,修飾于聚丙烯酰胺凝膠或聚合物分子上的色譜配基分布于整個孔道空間而非僅限于孔道表面,由此提供了更多的有效結合位點,顯著提升了蛋白質的飽和吸附容量。作為此類介質的一個成功范例,Sepharose XL離子交換色譜介質是將葡聚糖分子接枝在瓊脂糖凝膠粒子上,繼而偶聯離子交換配基,在介質孔道內獲得三維的配基分布[9]。Ljunglof等研究表明SP Sepharose XL的Fab抗體飽和吸附容量和動態吸附容量(dynamic binding capacity, DBC)分別可達295 mg·ml-1和180 mg·ml-1 [10],并在其綜述中對截至2011年的聚合物接枝離子交換色譜介質的研究進行了系統總結[9]。近來,Yu等[11-13]報道了聚乙烯亞胺直接接枝的瓊脂糖離子交換色譜介質的制備方法,其牛血清白蛋白的飽和吸附容量達到274 mg·ml-1。鑒于介質孔道的空間位阻作用和聚合物分子多分散性及其在介質孔道內的多位點結合屬性,前述介質孔道內聚合物接枝過程和接枝聚合物層特性都是難以控制的。本課題組公開了利用原子轉移自由基聚合(ATRP)技術在瓊脂糖色譜介質表面接枝單體化合物甲基丙烯酸3-磺酸丙酯鉀(SPM)制備鏈結構可控的聚合物接枝離子交換色譜介質的方法[14],該介質的溶菌酶飽和吸附容量高達413 mg·ml-1。但上述介質的抗體飽和吸附容量隨接枝聚合物鏈長度增大而急劇下降至32 mg·ml-1。
為了獲得高抗體吸附容量的聚合物接枝離子交換色譜介質,本課題組引入甲基丙烯酸甲酯(MMA),通過其與單體化合物SPM摻雜合成了不同配基分布密度的無規共聚物接枝離子交換色譜介質,系統地研究了離子交換色譜介質中聚合物鏈長和配基分布密度對溶菌酶和抗體離子吸附行為的影響。
1 實驗材料和方法
1.1 材料
瓊脂糖凝膠Sepharose Fast Flow,購于通用醫療公司(Uppsala, Sweden);抗體(來源于牛血清,≥99%,w約155×103)、溶菌酶(來源于雞蛋白,≥90%,w約14.3×103)、-溴異丁酰溴(BIBB)、MMA和SPM,Sigma-Aldrich公司(St. Louis, USA)試劑;,′-二甲基甲酰胺(DMF),購于天津大學江天化工科技開發公司;三乙胺(TEA)、溴化亞銅(CuBr)、溴化銅(CuBr2)和2,2′-聯吡啶(Bpy),購自天津市光復精細化工研究所。化學試劑均為分析純試劑。
1.2 方法
1.2.1 無規共聚物接枝離子交換色譜介質的合成
無規共聚物接枝離子交換色譜介質的合成工藝如圖1所示。瓊脂糖凝膠Sepharose Fast Flow置于G3漏斗中,經蒸餾水反復沖洗并抽干后,稱取15 g抽干介質,并將溶劑置換為DMF。處理好的介質轉入250 ml三口燒瓶,依次加入95 ml DMF和3 ml TEA后,置于冰浴中攪拌均勻。將含20%(體積分數)BIBB的12.5 ml DMF溶液置于恒壓漏斗中,逐滴加入三口燒瓶,滴加結束后升溫至30℃,反應12 h。產物依次經DMF、乙醇和去離子水清洗后,得到溴化Sepharose Fast Flow介質,記為SEP-Br。
SEP-Br介質的共聚物接枝反應在100 ml錐形瓶中進行。稱取3g SEP-Br介質,轉移至裝有50 ml 50%(體積分數)甲醇水溶液的錐形瓶中,然后依次加入SPM、MMA、Bpy和CuBr2。化學試劑的加入量見表1。上述的錐形瓶連續通入純氮30 min后,迅速加入CuBr,并繼續通入純氮30 min以完全排空氧氣。錐形瓶密封后置于25℃水浴搖床中,在170 r·min-1下反應4 h,然后錐形瓶敞口暴露于空氣中,直至溶液變為墨綠色。反應結束后,產物經0.1 mol·L-1EDTA溶液清洗除去Cu2+,再依次用大量乙醇和去離子水清洗,獲得不同種類的無規共聚物接枝離子交換色譜介質,用于蛋白質吸附行為的實驗研究。

表1 聚合物接枝離子交換色譜介質制備單體用量和介質性質參數 Table 1 SPM and MMA contents in synthesis of random copolymer-grafted cation-exchangers and properties of cation-exchangers
1.2.2 共聚物接枝離子交換色譜介質的表征
無規共聚物接枝離子交換色譜介質、溴化SEP-Br介質和Sepharose Fast Flow的紅外光譜采用Nicolet 6700傅里葉紅外光譜儀(MA, USA)測定。測試樣品采用冷凍干燥24 h獲得。色譜介質的粒徑采用Mastersizer2000U 粒徑分析儀(Malvern instruments, UK)測定。測定過程重復3次,得到色譜介質的平均粒徑p。共聚物接枝離子交換色譜介質的離子交換容量IC采用酸堿滴定法測定[15]。
色譜介質的平均孔道半徑pore是以不同分子量的葡聚糖為探針,采用逆體積排阻色譜(iSEC)方法測量[11,16]。待測色譜介質填充于TricornTM5/50色譜柱中,柱高控制在5.5 cm±0.2 cm。色譜柱用20 mmol·L-1Tris-HCl緩沖液(pH 8.0)平衡至少15個柱體積(CV),直至示差檢測器(RID)的信號穩定并調零。葡聚糖溶液同樣采用20 mmol·L-1Tris-HCl緩沖液制備后,在0.25 ml·min-1流速下上樣20 μl。上樣結束后,采用同一緩沖液沖洗色譜柱,記錄不同葡聚糖的保留體積R。
利用式(1)計算出不同分子量溶質的分配系數D
式中,0為色譜柱空隙體積,ml,由分子量為521×103的葡聚糖分子測得;T為色譜柱總體積,ml,由葡萄糖分子測得。
iSEC實驗數據采用單一圓柱孔模型擬合,得到介質的孔道半徑pore
式中,s為不同溶質分子半徑,nm,用黏性半徑η表示;glu為葡萄糖分子半徑,nm。
1.2.3 蛋白質靜態吸附實驗
無規共聚物接枝離子交換色譜介質的靜態吸附實驗在25 ml錐形瓶中進行[17]。離子交換色譜介質經蒸餾水清洗并抽濾后,用吸附緩沖液平衡不少于12 h。在本研究中,溶菌酶靜態吸附實驗采用20 mmol·L-1Tris-HCl緩沖液(pH 8.0)為吸附緩沖液,抗體靜態吸附實驗采用20 mmol·L-1醋酸鹽緩沖液(pH 5.0)為吸附緩沖液。平衡后的色譜介質經G3漏斗抽干后,稱取0.05 g介質,分別置于25 ml錐形瓶中,隨后向錐形瓶中加入5 ml不同濃度的蛋白質溶液。錐形瓶置于25℃水浴搖床中,在170 r·min-1下振蕩24 h后取出,在4000 r·min-1下離心5 min收集上清液。最后,以吸附緩沖液為參比,在280 nm下測定上清液中蛋白質濃度。
根據式(3),求得蛋白質的吸附量
式中,0為蛋白質溶液初始濃度,mg·ml-1;為蛋白質溶液體積,ml;為蛋白質吸附量,mg·g-1;為色譜介質濕重,g。
靜態吸附實驗數據與Langmuir吸附等溫線[式(4)]擬合,可得到蛋白質飽和吸附量m和解離常數d
1.2.4 蛋白質吸附動力學實驗
蛋白質在色譜介質上的吸附動力學實驗采用間歇攪拌法測定[18],具體實驗方法如下:100 ml蛋白質溶液置于100 ml三口圓底燒瓶中,并插入半月形攪拌槳后,燒瓶置于25℃水浴中,在100 r·min-1條件下勻速攪拌至恒溫。燒瓶內蛋白質溶液在蠕動泵驅動下以25 ml·min-1的流速經孔徑2 μm的不銹鋼濾頭流入UV-900紫外檢測器的檢測池,在280 nm下測定蛋白質濃度,檢測池流出的溶液返回燒瓶中。本研究中,溶菌酶濃度為1 mg·ml-1,抗體濃度為0.3 mg·ml-1。當吸光度值穩定后,稱取0.22 g經吸附緩沖液平衡并抽濾后的介質加入三口燒瓶中,在線測量蛋白質溶液吸光度值隨時間變化情況。實驗數據用本課題組此前建立的有效孔擴散模型分析[11],求解得到蛋白質在離子交換色譜介質中的有效孔擴散系數e。
1.2.5 動態吸附容量測定
蛋白質的DBC采用迎頭分析法,在?KTA FPLC快速液相色譜系統中測定[15, 19]。在本研究中,溶菌酶的穿透實驗色譜流動相為含有不同濃度NaCl的20 mmol·L-1Tris-HCl緩沖液(pH 8.0),抗體的穿透實驗流動相為含有不同濃度NaCl的20 mmol·L-1醋酸鹽緩沖液(pH 5.0);原料液為溶于色譜流動相的濃度0為2.0 mg·ml-1的蛋白質溶液。填充在Tricorn5/50色譜柱中的色譜介質經流動相平衡至少10個柱體積后,溶菌酶溶液以1 ml·min-1的流速、抗體溶液以0.2 ml·min-1的流速向色譜柱內連續輸入,直至蛋白質在色譜柱出口處完全穿透。蛋白質穿透體積(10,ml)根據色譜柱出口處蛋白質濃度達到原料液濃度10%時的色譜進料體積;色譜柱死體積(0,ml)為蛋白非保留條件下的穿透體積。
抗體的DBC(10,mg·ml-1)可根據式(5)計算
式中,B為色譜介質填充體積,ml。
本研究的介質的動態吸附容量均重復5次,以評估合成色譜介質的實用性。
2 結果與討論
2.1 共聚物接枝離子交換色譜介質的表征
本研究合成的無規共聚物接枝離子交換色譜介質的粒徑見表1。可以看出,離子交換色譜介質的平均粒徑介于92~103 μm之間,而且與合成過程中單體化合物無明確的關聯。此外,離子交換色譜介質的平均粒徑與本課題組此前測定的Sepharose Fast Flow平均粒徑(92 μm±2 μm)相當[14]。這說明接枝過程對瓊脂糖凝膠Sepharose Fast Flow結構沒有顯著的影響。
Sepharose Fast Flow、SEP-Br和共聚物接枝離子交換色譜介質SEP-S/M的紅外光譜如圖2所示。可以看出,SEP-Br的IR光譜[圖2(b)]的1729 cm-1波數下存在BIBB分子羰基的不對稱振動吸收峰,而Sepharose Fast Flow的IR光譜[圖2(a)]對應波數處并無此吸收峰,這表明BIBB固定在Sepharose Fast Flow上。因單體化合物MMA和SPM均含有羰基基團,故圖2(c)中共聚物接枝色譜介質SEP-S30/M60的1729 cm-1波數下羰基吸收峰顯著增強,并在610 cm-1和523 cm-1波數下出現了磺酸基的伸縮振動峰。IR光譜結果表明單體化合物SPM和MMA通過ATRP方法已經成功接枝于Sepharose Fast Flow表面。
本研究制備的離子交換色譜介質的IC結果亦列于表1。IC結果顯示,單體化合物總濃度一定條件下,隨著單體化合物SPM的增大,共聚物分子鏈上SPM配基密度增大,離子交換色譜介質的IC值升高。IC的最大值(456 μmol·g-1)出現在SEP-S60介質上,為SEP-S06/M54介質IC值的7.2倍。在單體化合物SPM濃度一定的情況下,單體化合物MMA用量由0增至9 μmol時,表1中IC值僅在214~263 μmol·g-1之間變化。這說明引入MMA對離子交換色譜介質IC的影響是有限的。
表1列出了本研究合成的聚合物接枝離子交換色譜介質的pore。本研究測得Sepharose Fast Flow的pore為19.8 nm±1.4 nm。對比接枝前、后色譜介質pore的變化可知介質孔道因聚合物接枝而變小。單體化合物總濃度一定的條件下,SEP-S60具有最小的pore(12.8 nm)。這歸因于SEP-S60中聚合物鏈上較高的SPM配基密度引發聚合物鏈間強烈的靜電排斥作用。由此,聚合物分子鏈向孔道中心充分伸展,聚合物層厚度增大,介質pore減小。隨著MMA的引入,共聚物鏈間的靜電排斥作用逐漸減弱,分子鏈的柔性增加。這引起分子鏈塌陷,漸趨卷曲線團狀[20],直接的表現就是色譜介質的pore增大。MMA含量高的兩種介質SEP-S06/M54和SEP-S12/ M48具有最大的pore(表1),說明兩種介質孔道內的共聚物鏈的塌陷最為顯著。當SPM濃度一定時,隨著MMA濃度的升高,單體化合物總濃度提高,因此接枝的共聚物具有更長的分子鏈。表1結果顯示介質的pore由16.6 nm逐步降至9.3 nm。
2.2 離子交換配基密度對蛋白質吸附的影響
圖3給出了初始蛋白質濃度為5 mg·ml-1條件下溶菌酶和抗體在不同IC值的共聚物接枝離子交換色譜介質內的吸附量。可以看出,SEP-S60介質上溶菌酶吸附量最大,抗體吸附量最小。這與本課題組此前的結果一致[14]。接枝過程中MMA的引入也對蛋白質的吸附量產生了顯著影響。圖3顯示,SEP-S06/M54和SEP-S12/M48介質上溶菌酶和抗體的吸附量均較小,與非接枝離子交換色譜介質SP Sepharose FF的實驗結果相當[14, 21]。SP Sepharose FF的IC值通常在200 μmol·ml-1左右[10],遠高于本研究中SEP-S06/M54和SEP-S12/M48介質的63~81 μmol·g-1。兩者相近的蛋白質吸附量與其在IC值上的差異反映出共聚物接枝離子交換色譜介質中孔道內三維的配基空間分布在蛋白質吸附上的優勢。
隨著IC的增大,溶菌酶和抗體的吸附量顯著提高。在SEP-S24/M36中,溶菌酶和抗體的吸附量均達到220 mg·g-1以上。該吸附量也高于溶菌酶在Fractogel EMD介質上的吸附量[22],屬于典型的蛋白質多層吸附。這也從蛋白質吸附角度印證了SEP-S24/M36介質中離子交換配基呈現空間分布的特征。當IC進一步增大至228 μmol·g-1及以上時,溶菌酶吸附量再次階躍提升,在SEP-S30/M30、SEP-S36/M24和SEP-S48/M12中達到382~440 mg·g-1。與IC值增大相對應的是,此時pore并未發生改變(表1)。這意味著介質孔道內聚合物層中離子交換配基密度增加,可視為溶菌酶吸附量在SEP-S30/M30、SEP-S36/M24和SEP-S48/ M12介質中升高的直接原因。在上述介質IC值增大的同時,介質pore和抗體吸附量并未明顯變化,各自維持在14.6~15.3 nm和231~262 mg·g-1。而在IC值最大的SEP-S60介質中抗體吸附量急劇降低至78 mg·g-1。與之相應的是介質pore降至12.8 nm。上述結果充分說明抗體的吸附量很大程度上與pore和聚合物層厚度的變化相關。已有研究表明[23],接枝聚合物層對蛋白質分子的空間排阻作用隨聚合物層厚度和蛋白質分子量增大而增強。聚合物層厚度增大表現為SEP-S60介質pore下降,進而導致抗體(w約155×103)吸附量降低。在單體化合物總濃度一定的情況下,這種聚合物層的空間排阻作用對溶菌酶(w約14.3×103)等小蛋白質而言可基本忽略[23]。因此,高容量聚合物接枝離子交換色譜介質的設計應當IC和pore并重,同時具備高離子交換配基密度和一定孔道半徑的色譜介質(如SEP-S30/M30、SEP-S36/M24和SEP-S48/M12)更加適合于蛋白質的高容量吸附。
2.3 共聚物鏈長對介質吸附性能的影響
進一步研究了共聚物鏈長對蛋白質在離子交換色譜介質內吸附平衡的影響,結果如圖4所示。可以看出,溶菌酶在SEP-S30中有最小的吸附量,而抗體正好相反。表2中Langmuir吸附等溫線擬合的蛋白質飽和吸附容量也驗證了這一點。這一結果與SEP-S60介質中抗體吸附量(78 mg·g-1)形成鮮明的對照,體現介質孔道內較大厚度的聚合物層對抗體強烈的空間排阻作用[23]。隨著MMA濃度的增大,介質pore減小及對應的聚合物層厚度增大,與之相伴的是介質的抗體吸附量降低[圖4(b)]。表2的結果顯示抗體飽和吸附容量最終降至77 mg·g-1。實驗結果進一步驗證了抗體在聚合物接枝離子交換色譜介質內的吸附容量與介質pore和聚合物層厚度密切相關。在IC值穩定條件下,單體化合物MMA濃度增大引起SEP-S30/M30、SEP-S30/M60和SEP-S30/M90 3種介質內溶菌酶的吸附容量由380 mg·g-1逐漸降低至276 mg·g-1(表2)。這一結果也展現了聚合物層對溶菌酶排阻作用隨其厚度增大而逐漸顯現。
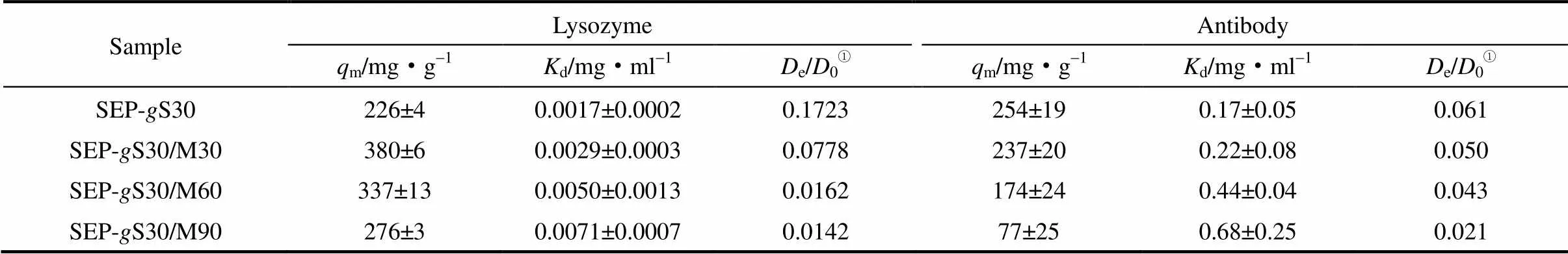
表2 溶菌酶和抗體在聚合物接枝離子交換色譜介質上的吸附等溫線和動力學參數 Table 2 Langmuir parameters and effective diffusivities of lysozyme and antibody adsorption on copolymer-grafted cation-exchangers
①0is the diffusivity of proteins in free solution.
2.4 鹽濃度對蛋白質吸附的影響
進一步考察了無機鹽濃度對蛋白質在SEP-S30/M30上吸附的影響,結果如圖5所示。隨著無機鹽濃度的增大,溶菌酶在SEP-S30/M30上的吸附量下降[圖5(a)]。隨著無機鹽濃度的增加,蛋白質與離子交換配基間的親和力降低,并且聚合物分子鏈塌陷。后者的影響已見諸此前的研究報道[13-14]。因此,溶菌酶吸附容量隨無機鹽濃度增大而降低。對于抗體吸附而言,由此帶來聚合物層厚度的降低,弱化了聚合物層對抗體的空間排阻作用,有利于改善抗體的吸附,結果如圖5(b)所示。進一步增大無機鹽濃度,溶菌酶和抗體吸附量均降低。上述結果表明,無機鹽對蛋白質在聚合物接枝離子交換色譜介質中吸附的調控作用不僅反映在對蛋白質結合作用的影響上,也表現在其對聚合物層的調控以及由此帶來的對蛋白質吸附的影響上。
2.5 吸附動力學
溶菌酶和抗體在SEP-S30、SEP-S30/M3、SEP-S30/M60和SEP-S30/M902上的吸附動力學結果如圖6所示。有效孔擴散系數的擬合結果列于表2。從圖6可以看出,介質吸附蛋白質的動力學曲線均緩慢下降,100 min后才趨于穩定。由表2中擬合得到的參數可以看出介質孔道內聚合物層厚度增加引起介質內蛋白質有效擴散系數下降。溶菌酶在共聚物接枝離子交換色譜介質內的有效擴散系數也明顯小于SP Sepharose FF和由SPM單體合成的離子交換色譜介質的有效擴散系數[14]。
2.6 蛋白質的動態吸附
基于上述結果進一步測量了溶菌酶和抗體在介質SEP-S30和SEP-S30/M30上的DBC值,實驗結果如圖7所示。從圖7(a)可以看出,當鹽濃度在0~100 mmol·L-1范圍時,溶菌酶在兩種介質上的DBC值都在135 mg·ml-1左右;當鹽濃度增加到200 mmol·L-1時,溶菌酶在介質SEP-S30上的DBC值降到43 mg·ml-1,在介質SEP-S30/M30上的DBC值降到88 mg·ml-1,后者為SEP-S30介質DBC的2倍并表現出更強的鹽的耐受性。從圖7(b)可以看出,抗體在介質SEP-S30上的DBC值隨鹽濃度增加而下降,而抗體在介質SEP-S30/M30上的DBC值隨鹽濃度增加呈現先增加后降低的趨勢,并且最大值達到33 mg·ml-1。從中可以看出,SEP-S30/M3色譜介質具有較高的抗體DBC值,展現了較好的應用潛力。
3 結 論
引入新單體化合物MMA,利用ATRP技術合成了不同離子交換配基密度和共聚物鏈長的無規共聚物接枝離子交換色譜介質,系統地研究了溶菌酶和抗體在離子交換色譜介質內的吸附行為。在單體化合物總濃度一定的情況下,單體化合物MMA濃度增大導致無規共聚物接枝離子交換色譜介質IC下降及pore增大,后者反映出介質孔道內共聚物鏈逐漸塌陷的特征。蛋白質的吸附表明,溶菌酶的吸附主要取決于介質的離子交換配基密度,抗體的吸附則在更大程度上與pore和共聚物層厚度相關。這主要體現在聚合物層對抗體的空間排阻作用。蛋白質在不同鏈長的共聚物接枝離子交換色譜介質中的吸附結果也證實了這一結論,而且進一步表明優化無規共聚物分子鏈可顯著提高蛋白質吸附量。此外,蛋白質的吸附和介質孔道內聚合物層厚度均受無機鹽濃度調控。吸附動力學的結果反映出pore導致介質內蛋白質有效擴散系數下降。上述研究結果對設計和開發高容量聚合物接枝離子交換色譜介質具有重要的指導意義。
符 號 說 明

c——蛋白質溶液濃度,mg·ml-1 c0——蛋白質溶液初始濃度,mg·ml-1 De——介質內蛋白質有效擴散系數 D0——溶液中蛋白質擴散系數 dp——色譜介質粒徑,μm IC——離子交換容量,μmol·g-1 KD——葡聚糖分子分配系數 Kd——解離常數,mg·ml-1 Mw——蛋白質分子量 m——色譜介質濕重,g q——蛋白質吸附量,mg·g-1 qm——蛋白質飽和吸附容量,mg·g-1 q10——蛋白質動態結合容量,mg·ml-1 rglu——葡萄糖分子半徑,nm rpore——介質孔道半徑,nm rs——葡聚糖分子半徑,nm VB——色譜柱介質填充體積,ml VR——葡聚糖分子在色譜柱內保留體積,ml VT——色譜柱總體積,ml V0——色譜柱空隙體積,ml V10——10%穿透條件下色譜進樣體積,ml
References
[1] AFEYAN N B, GORDON N F, MAZSAROFF I,. Flow-through particles for the high-performance liquid chromatographic separation of biomolecules: perfusion chromatography [J]. Journal of Chromatography, 1990, 519(1): 1-29.
[2] SHI Q H, ZHOU X, SUN Y. A novel superporous agarose medium for high-speed protein chromatography [J]. Biotechnology and Bioengineering, 2005, 92(5): 643-651.
[3] WANG D M, HAO G, SHI Q H,. Fabrication and characterization of superporous cellulose bead for high-speed protein chromatography [J]. Journal of Chromatography A, 2007, 1146(1): 32-40.
[4] SVEC F, FRECHET J M. New designs of macroporous polymers and supports: from separation to biocatalysis [J]. Science, 1996, 273(5272): 205-211.
[5] SVEC F. Porous polymer monoliths: amazingly wide variety of techniques enabling their preparation [J]. Journal of Chromatography A, 2010, 1217(6): 902-924.
[6] PARHI P, GOLAS A, BARNTHIP N,. Volumetric interpretation of protein adsorption: capacity scaling with adsorbate molecular weight and adsorbent surface energy [J]. Biomaterials, 2009, 30(36): 6814-6824.
[7] HORVATH J, BOSCHETTI E, GUERRIER L,. High-performance protein separations with novel strong ion exchangers [J]. Journal of Chromatography A, 1994, 679(1): 11-22.
[8] HAHN R, SCHULZ P M, SCHAUPP C,. Bovine whey fractionation based on cation-exchange chromatography [J]. Journal of Chromatography A, 1998, 795(2): 277-287.
[9] LENHOFF A M. Protein adsorption and transport in polymer-functionalized ion-exchangers [J]. Journal of Chromatography A, 2011, 1218(49): 8748-8759.
[10] LJUNGLOF A, LACKI K M, MUELLER J,. Ion exchange chromatography of antibody fragments [J]. Biotechnology and Bioengineering, 2007, 96(3): 515-524.
[11] YU L L, TAO S P, DONG X Y,. Protein adsorption to poly(ethylenimine)-modified Sepharose FF (Ⅰ): A critical ionic capacity for drastically enhanced capacity and uptake kinetics [J]. Journal of Chromatography A, 2013, 1305: 76-84.
[12] HONG Y, LIU N, WEI W,. Protein adsorption to poly(ethylenimine)-modified Sepharose FF (Ⅲ): Comparison between different proteins [J]. Journal of Chromatography A, 2014, 1342: 30-36.
[13] YU L L, SUN Y. Protein adsorption to poly(ethylenimine)-modified Sepharose FF (Ⅱ): Effect of ionic strength [J]. Journal of Chromatography A, 2013, 1305: 85-93.
[14] 王宏燕. 基于ATRP的聚合物接枝瓊脂糖色譜介質合成及其性能表征 [D]. 天津: 天津大學, 2015.
WANG H Y. Synthesis and characterization of agarose-based polymer-grafted chromatographic gelsatom transfer radical polymerization [D]. Tianjin: Tianjin University, 2015.
[15] SHI Q H, JIA G D, SUN Y. Dextran-grafted cation exchanger based on superporous agarose gel: adsorption isotherms, uptake kinetics and dynamic protein adsorption performance [J]. Journal of Chromatography A, 2010, 1217(31): 5084-5091.
[16] YAO Y, LENHOFF A M. Pore size distributions of ion exchangers and relation to protein binding capacity [J]. Journal of Chromatography A, 2006, 1126(1/2): 107-119.
[17] SHI Q H, SHEN F F, SUN S. Studies of lysozyme binding to histamine as a ligand for hydrophobic charge induction chromatography [J]. Biotechnology Progress, 2010, 26(1): 134-141.
[18] ZHANG S P, SUN Y. Ionic strength dependence of protein adsorption to dye-ligand adsorbents [J]. AIChE Journal, 2002, 48(1): 178-186.
[19] SHI Q H, CHENG Z, SUN Y. 4-(1-imidazol-1-yl)aniline: a new ligand of mixed-mode chromatography for antibody purification [J]. Journal of Chromatography A, 2009, 1216(33): 6081-6087.
[20] 李海普, 李星, 張莎莎, 等. 高分子在固液界面吸附構象的研究方法及手段 [J]. 化學通報, 2011, 74(5): 417-423.
LI H P, LI X, ZHANG S S,. Methods and techniques for studying the adsorption conformation of polymers at solid/liquid interface [J]. Chemistry Bulletin, 2011, 74(5): 417-423.
[21] DISMER F, PETZOLD M, HUBBUCH J. Effects of ionic strength and mobile phase pH on the binding orientation of lysozyme on different ion-exchange adsorbents [J]. Journal of Chromatography A, 2008, 1194(1): 11-21.
[22] DISMER F, HUBBUCH J. A novel approach to characterize the binding orientation of lysozyme on ion-exchange resins [J]. Journal of Chromatography A, 2007, 1149(2): 312-320.
[23] SHI Q H, JIA G D, XU L,. Effect of electric field on the partitioning behavior of solutes in entropic interaction chromatography [J]. Journal of Separation Science, 2013, 36(18): 3075-3085.
Synthesis and characterization of copolymer-grafted cation-exchangers for protein adsorption
ZHANG Suling, YANG Wei, YU Linling, BAI Shu, SUN Yan, SHI Qinghong
(Key Laboratory of System Bioengineering of Ministry of Education, Department of Biochemical Engineering, School of Chemical Engineering and Technology, Tianjin University, Tianjin 300354, China)
High-capacity chromatographic packings for protein adsorption are the material prerequisite for the development of efficient protein chromatography processes. In this work, random copolymer-grafted cation-exchangers for protein adsorption were synthesized by grafting 3-sulfopropyl methacrylate and methyl methacrylate (MMA) to Sepharose Fast Flowatom transfer radical polymerization, and lysozyme and antibody adsorption on to these cation-exchangers was investigated. In case of a given total concentration of the monomers for the grafting reaction, the pore radii of the copolymer-grafted cation-exchangers increased with an increase of MMA concentration, indicating a typical characteristic of a decreasing depth of polymer layer and gradual collapse of the random copolymers. Adsorption equilibria showed that the adsorption capacity for lysozyme was dominated by ionic capacity of the cation-exchangers whilst for antibody it was related to pore radius and corresponding the change in depth of polymer layer. With an increase in depth of polymer layer, there was stronger steric excluded interaction between antibody and polymer layer, and thus decreasing the adsorption capacity for antibody. Moreover, the results demonstrated that the adsorption capacities for proteins on random copolymer-grafted cation-exchangers were improved by optimizing the conformation of random copolymer chains. The adsorption capacities for antibody and lysozyme reached 237 and 380 mg·g-1 in the optimized random copolymer-grafted cation exchangers, respectively. The research revealed that both layer depth of copolymer and protein binding were also regulated by ionic strength in copolymer-grafted cation-exchangers.
copolymer-grafted cation-exchanger; atom transfer radical polymerization; protein; adsorption; high-capacity; antibody
supported by the National Natural Science Foundation of China (21476166, 21236005) and the Natural Science Foundation of Tianjin (15JCYBJC48500).
date: 2016-03-28.
Prof. SHI Qinghong, qhshi@tju.edu.cn
TQ 936.2
A
0438—1157(2016)09—3738—09
10.11949/j.issn.0438-1157.20160349
國家自然科學基金項目(21476166,21236005);天津市應用基礎與前沿技術研究計劃一般項目(15JCYBJC48500)。
2016-03-28收到初稿,2016-05-09收到修改稿。
聯系人:史清洪。第一作者:張素玲(1989—),女,碩士研究生。

