芒柄花素抑制乳腺癌細胞HIF-1α/CXCR4信號以及細胞增殖和遷移
葛新 李林 王芳 郭廣成 李靖若 谷元廷
(鄭州大學第一附屬醫院 乳腺外科 河南 鄭州 450052)
?
芒柄花素抑制乳腺癌細胞HIF-1α/CXCR4信號以及細胞增殖和遷移
葛新李林王芳郭廣成李靖若谷元廷
(鄭州大學第一附屬醫院 乳腺外科河南 鄭州450052)
目的研究芒柄花素對乳腺癌細胞行為的影響及其作用機制。方法利用不同濃度(5、10、15、20 μM)的芒柄花素處理MDA-MB-231細胞,分別處理48 h。應用qRT-PCR法檢測細胞中低氧誘導因子-1α(HIF-1α)和CXC趨化因子受體4(CXCR4)mRNA的表達,利用Western blot方法檢測細胞中HIF-1α和CXCR4蛋白的表達。構建pShuttle-HIF-1α過表達載體并轉染MDA-MB-231細胞。利用噻唑藍(MTT)法檢測細胞增殖,利用Transwell法檢測細胞體外遷移。結果相比于對照組,芒柄花素顯著降低MDA-MB-231細胞中HIF-1α和CXCR4 mRNA和蛋白的表達水平(P<0.05),并且具有劑量依賴性。過表達HIF-1α提高芒柄花素處理后細胞中HIF-1α和CXCR4的表達水平(P<0.05),促進癌細胞增殖(P<0.05),并促進癌細胞體外遷移(P<0.05)。結論芒柄花素可能通過調控乳腺癌細胞中HIF-1α/CXCR4信號轉導影響癌細胞增殖和遷移。
芒柄花素;乳腺癌;低氧誘導因子-1α;CXC趨化因子受體4;增殖;遷移
芒柄花素是黃芪的有效成分之一,具有抑制腫瘤細胞生長和增殖的作用[1]。研究發現,芒柄花素能夠通過下調乳腺癌細胞中Akt磷酸化抑制細胞增殖[2]。低氧誘導因子-1α(hypoxia-inducible factor-1α,HIF-1α)和CXC趨化因子受體4(CXC chemokine receptor 4,CXCR4)在乳腺癌細胞生長、增殖、遷移、上皮間充質化中具有重要作用[3-4]。目前,芒柄花素是否能夠通過調控HIF-1α和CXCR4影響乳腺癌細胞行為還不清楚。本研究通過探索芒柄花素在乳腺癌中的作用機制,從而為其在臨床治療中的應用提供理論基礎。
1 材料與方法
1.1實驗材料MDA-MB-231細胞購自于美國模式培養物保藏所;芒柄花素(C16H12O4,分子量268.264 08,純度≥98%)購自上海純優生物;胎牛血清、DMEM培養基、Trizol試劑盒、噻唑藍(MTT)、二甲基亞砜、硝酸纖維素膜購自大連寶生物公司;DNA Engine OpticonTM2熒光檢測系統和DyNAmo SYBR Green qPCR試劑盒購自美國Invitrogen公司;抗HIF-1α單抗、抗CXCR4單抗和酶標羊抗鼠二抗購自美國Sigma公司。
1.2實驗方法
1.2.1細胞培養與分組處理將MDA-MB-231細胞孵育于含10%胎牛血清的DMEM培養基中,置于37 ℃恒溫、5%CO2的飽和濕度培養箱中培養。將細胞隨機分為對照組、芒柄花素組、空載體組、HIF-1α過表達組。芒柄花素組分別用5、10、15、20 μM芒柄花素處理48 h。空載體組和HIF-1α過表達組細胞轉染pShuttle空載質粒和pShuttle-HIF-1α質粒24 h后,利用20 μM芒柄花素處理48 h。
1.2.2構建pShuttle-HIF-1α表達載體將人HIF-1α cDNA克隆至pGEMTEasy載體,測序鑒定質粒。重組質粒pGEM-HIF-1α及表達空載體pShuttle用限制性內切酶NotⅠ和ApaⅠ雙酶切,將HIF-1α片段與表達載體pShuttle連接,然后將重組表達載體pShuttle-HIF-1α轉染MDA-MB-231細胞,應用Western分析方法檢測HIF-1α的表達。
1.2.3噻唑藍(MTT)法檢測細胞增殖收集對數生長期細胞,按每孔3×104個接種于96孔培養板。細胞達到80%融合時用于MTT實驗。MTT實驗檢測分別在細胞培養24、48、72、96 h后進行。按實驗分組情況,每孔加入20 μl MTT(5 mg/ml)后培養4 h。去掉上清,按照每孔150 μl加入二甲基亞砜(dimethyl sulfoxide,DMSO)。混勻后用酶標儀(Bio-tek Instruments/USA)測定(測量波長為570 nm)。實驗重復3次,取平均數作為實驗結果。
1.2.4Transwell法檢測細胞遷移用胰蛋白酶消化細胞,細胞計數3×105,轉移至Transwell 上層小室中,每孔鋪200 μl細胞,加入200 μl無血清培養基。下層板孔中加入600 μl完全培養基,37 ℃、5%CO2培養箱中培養24 h,隨后取出小室用90%乙醇固定,0.1%結晶紫溶液染色,置于顯微鏡下觀察并拍照,隨機選取4個低倍視野(100×)進行細胞計數,并計算平均值。
1.2.5qRT-PCR檢測利用Trizol試劑盒提取培養細胞系總RNA,按照步驟反轉錄合成cDNA。查找Genbank序列設計并合成HIF-1α和CXCR4基因引物序列。HIF-1α上游引物:5’-CCT GAG CCT AAT AGT CCC-3’;下游引物:5’-GGT GGC ATT AGC AGT AGG-3’。CXCR4上游引物:5’-GGT GGT CTA TGT TGG CGT CT;下游引物: 5’-TGG AGT GTG ACA GCT TGG AG-3’。采用DNA Engine OpticonTM 2熒光檢測系統和DyNAmo SYBR Green qPCR 試劑盒進行基因表達的測定。取3次重復的平均值,靶基因的相對表達量的計算由目的基因的拷貝數除以β-actin的拷貝數。
1.2.6Western blot檢測提取MDA-MB-231細胞中總蛋白,取30 μg蛋白樣品進行SDS-PAGE電泳。電泳結束后,將凝膠上的蛋白轉移到硝酸纖維素膜上,并用1%麗春紅染色檢測轉移效果。將膜放在10 ml封閉液中(2%脫脂奶粉)1 h;加入抗HIF-1α單抗(1∶800)和抗CXCR4單抗(1∶1 000),4 ℃過夜孵育;加入酶標羊抗鼠二抗抗體(1∶10 000),室溫孵育2 h,利用化學發光法(ECL),并在暗盒曝光。用凝膠圖像分析系統拍照并分析,比較蛋白條帶的相對積分吸光度(OD)值。
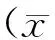
2 結果
2.1芒柄花素抑制HIF-1α mRNA和CXCR4 mRNA表達水平相比于對照組細胞,芒柄花素組MDA-MB-231細胞中HIF-1α mRNA和CXCR4 mRNA的表達水平下調。 當芒柄花素劑量≥10 μM時,差異具有統計學意義(P<0.05),且劑量為20 μM時效果最為明顯。見圖1。
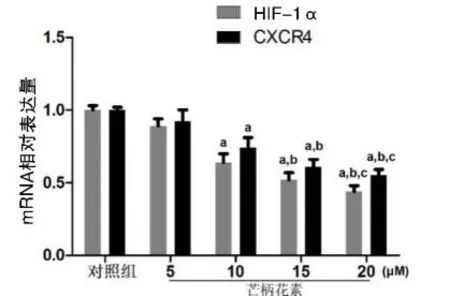
圖1 芒柄花素處理后MDA-MB-231細胞HIF-1α和CXCR4 mRNA的表達
2.2芒柄花素抑制HIF-1α蛋白和CXCR4蛋白表達水平芒柄花素劑量≥10 μM時,MDA-MB-231細胞中HIF-1α蛋白和CXCR4蛋白的表達顯著下調(P<0.05);當藥物劑量為20 μM時,效果最明顯。見圖2和圖3。
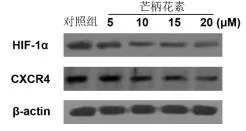
圖2 芒柄花素處理后MDA-MB-231細胞HIF-1α和CXCR4蛋白的表達
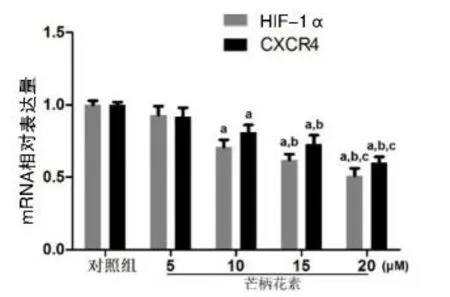
圖3 HIF-1α和CXCR4蛋白條帶定量分析
2.3過表達HIF-1α拮抗芒柄花素對CXCR4蛋白的影響與對照組比較,20 μM芒柄花素顯著抑制細胞中HIF-1α蛋白和CXCR4蛋白的表達(P<0.05)。與空載體+芒柄花素組比較,HIF-1α過表達+芒柄花素組中HIF-1α蛋白和CXCR4蛋白明顯升高,差異有統計學意義(P<0.05)。見圖4和圖5。
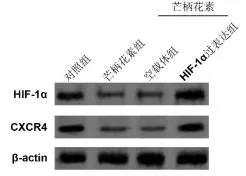
圖4 過表達HIF-1α后MDA-MB-231細胞HIF-1α和CXCR4蛋白的表達

圖5 HIF-1α和CXCR4蛋白條帶定量分析
2.4過表達HIF-1α拮抗芒柄花素對細胞增殖的影響相比于對照組細胞,芒柄花素處理后的細胞增殖速率顯著降低(P<0.05)。轉染pShuttle-HIF-1α后,MDA-MB-231細胞增殖速率明顯上升(P<0.05)。見圖6。
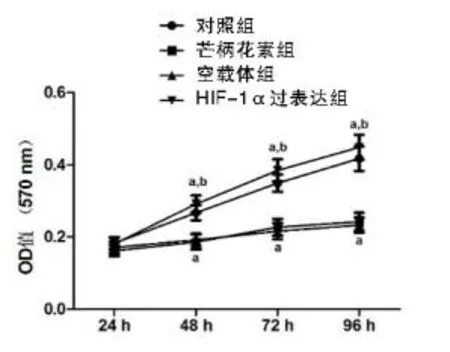
圖6 MTT法檢測MDA-MB-231細胞增殖
2.5過表達HIF-1α拮抗芒柄花素對細胞遷移的影響芒柄花素處理后的細胞遷移數目相比于對照組顯著降低(P<0.05)。轉染pShuttle-HIF-1α后,細胞遷移數目顯著增加(P<0.05)。見圖7和圖8。
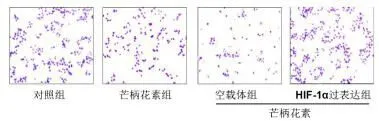
圖7 Transwell法檢測MDA-MB-231細胞遷移
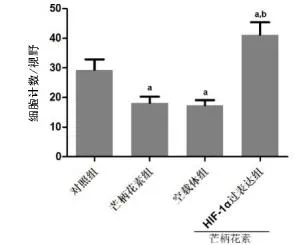
圖8 MDA-MB-231細胞遷移數目分析
3 討論
HIF-1α/CXCR4信號異常活化被證明與多種惡性腫瘤的發生有關,其中包括乳腺癌[5-6]。芒柄花素的抑癌作用也在多個研究中得到報道[7]。Wu等[8]發現芒柄花素可抑制內皮細胞增殖、遷移、微血管形成,并在體內抑制乳腺癌進展相關的新血管形成。本研究利用不同劑量(5、10、15、20 μM)的芒柄花素體外處理乳腺癌細胞系MDA-MB-231,隨后檢測細胞中HIF-1α和CXCR4的mRNA和蛋白水平的變化。結果發現芒柄花素能夠顯著抑制HIF-1α和CXCR4的表達,并且具有劑量依賴性,說明芒柄花素可能通過調控HIF-1α和CXCR4的表達影響乳腺癌疾病進展。
本研究構建了pShuttle-HIF-1α過表達載體,并在體外轉染pShuttle-HIF-1α及其空載體對照。結果發現,過表達HIF-1α可以顯著上調乳腺癌細胞中HIF-1α蛋白和CXCR4蛋白的表達水平。隨后,本研究發現芒柄花素可抑制細胞增殖,而過表達HIF-1α則可以拮抗芒柄花素的作用,促進細胞增殖。同時,本研究也檢測了芒柄花素對癌細胞遷移的影響,結果顯示芒柄花素可抑制癌細胞的體外遷移,而過表達HIF-1α則可以促進細胞遷移,拮抗芒柄花素的作用。
綜上所述,芒柄花素能夠抑制人乳腺癌細胞中HIF-1α和CXCR4的表達,過表達HIF-1α可抵消芒柄花素對CXCR4的表達調控以及對癌細胞增殖和遷移的抑制作用。因此,HIF-1α可能是芒柄花素的重要調控靶基因,進而影響癌細胞的增殖和遷移能力。
[1]Zhou R, Xu L, Ye M, et al. Formononetin inhibits migration and invasion of MDA-MB-231 and 4T1 breast cancer cells by suppressing MMP-2 and MMP-9 through PI3K/AKT signaling pathways[J]. Horm Metab Res, 2014, 46(11): 753-760.
[2]鄧櫻, 陳紅風. 黃芪注射液及其有效成分對乳腺癌細胞增殖和Akt磷酸化的影響[J]. 中西醫結合學報, 2009, 7(12): 1174-1180.
[3]Wang W, He Y F, Sun Q K, et al. Hypoxia-inducible factor 1α in breast cancer prognosis[J]. Clin Chim Acta, 2014, 428: 32-37.
[4]Xu T P, Shen H, Liu L X, et al. The impact of chemokine receptor CXCR4 on breast cancer prognosis: a meta-analysis[J]. Cancer Epidemiol, 2013, 37(5): 725-731.
[5]Andreou K, Rajendran R, Krstic-Demonacos M, et al. Regulation of CXCR4 gene expression in breast cancer cells under diverse stress conditions[J]. Int J Oncol, 2012, 41(6): 2253-2259.
[6]Guan G, Zhang Y, Lu Y, et al. The HIF-1alpha/CXCR4 pathway supports hypoxia-induced metastasis of human osteosarcoma cells[J]. Cancer Lett, 2015, 357(1): 254-264.
[7]周瑞娟, 陳紅風, 葉媚娜, 等. 芒柄花素對不同亞型乳腺癌細胞增殖及細胞周期的影響[J]. 腫瘤防治研究, 2012, 39(9): 1051-1055.
[8]Wu X Y, Xu H, Wu Z F, et al. Formononetin, a novel FGFR2 inhibitor, potently inhibits angiogenesis and tumor growth in preclinical models[J]. Oncotarget, 2015, 6(42): 44563-44578.
Formononetin regresses HIF-1α/CXCR4 signaling and cell proliferation and migration in breast cancer cells
Ge Xin, Li Lin, Wang Fang, Guo Guangcheng, Li Jingruo, Gu Yuanting
(DepartmentofBreastSurgery,theFirstAffiliatedHospitalofZhengzhouUniversity,Zhengzhou450052,China)
ObjectiveTo investigate the effect of formononetin on breast cancer cell behavior as well as its mechanism. MethodsMDA-MB-231 cells were exposed to different doses (5, 10, 15, 20 μM) of formononetin for 48 h respectively. The expression of hypoxia-inducible factor-1α (HIF-1α) mRNA and CXC chemokine receptor 4 (CXCR4) mRNA were analyzed by qRT-PCR. The expression of HIF-1α and CXCR4 protein were analyzed by Western blot method. Furthermore, pShuttle-HIF-1α overexpression vector was constructed and transfected into MDA-MB-231 cells. Cell proliferation was determined by MTT assay. Cell migration was evaluated by Transwell assay. ResultsCompared with the control, exposure of formononetin significantly decreased both mRNA and protein expression of HIF-1α and CXCR4 (P<0.05) in a dose dependent way. Overexpression of HIF-1α raised HIF-1α and CXCR4 expression in cancer cells after formononetin treatment (P<0.05), promoting cell proliferation (P<0.05) and enhancing cell migration (P<0.05). ConclusionFormononetin might affect breast cancer cell proliferation and migration through modulation of HIF-1α/CXCR4 signaling transduction.
formononetin; breast cancer; hypoxia-inducible factor-1α; CXC chemokine receptor 4; proliferation; migration
谷元廷,E-mail:zzyuantinggu@126.com。
R 737.9doi: 10.3969/j.issn.1004-437X.2016.09.003
2016-03-04)

