替比夫定治療乙型肝炎肝硬化失代償療效分析及對腎臟功能的影響
高得勇 王迎迎 汪妍妍 徐國榮 吳劍琴 夏利萍 劉亮明
?
·論著·
替比夫定治療乙型肝炎肝硬化失代償療效分析及對腎臟功能的影響
高得勇王迎迎汪妍妍徐國榮吳劍琴夏利萍劉亮明
目的評價替比夫定治療乙型肝炎肝硬化失代償患者的療效及對腎臟功能的影響。方法回顧性分析2012年4月至2015年11月在上海市松江區中心醫院感染科就診的失代償期乙型肝炎肝硬化患者72例, 給予替比夫定抗病毒治療,在治療后24周、48周觀察血清丙氨酸氨基轉移酶(ALT)、血清總膽紅素(TBil) 、白蛋白(Alb)、凝血酶原時間(PT) 、Child-Pugh積分、腹水、HBV DNA、陰轉率及耐藥變異率;比較治療后24周、48周血清肌酐(CR),估算腎小球濾過率(eGFR)較基線的變化情況。計量資料比較采用獨立樣本t檢驗,治療前后比較采用配對t檢驗,計數資料采用χ2檢驗。 結果治療24周時,血清ALT、TBil、HBV DNA載量均值分別為:46.12 U/L、44.31 μmol/L和1.89 lg拷貝/mL,HBV DNA陰轉率為75.00%,均較治療前有明顯改善(P<0.05)。2例患者出現耐藥變異,但未發現有腹水消失的病例;隨著治療時間延長至48周,Alb水平和PT均值分別為:34.16 g/L和15.09 s,Child-Pugh積分也較治療前進一步明顯改善(P<0.05),有3例患者腹水消失且耐藥變異病例增加至5例。治療48周時eGFR及CR分別為:108.48 mL/(min·1.73 m2)和0.83 mg/dL,均較治療前明顯改善(P<0.05),39例基線腎功能輕度受損[eGFR 60~90 mL/ (min·1.73 m2)]患者中,有9例患者(23.08%)上升至eGFR≥90 mL/(min·1.73 m2)。 結論替比夫定治療乙型肝炎肝硬化失代償期患者在有效抑制病毒及改善肝臟儲備功能方面療效肯定,隨著治療時間的延長治療效果更加明顯,但有部分患者出現耐藥變異;替比夫定有改善腎臟功能的作用,對于基線腎功能受損的患者,其腎臟功能可得到一定程度的恢復。
替比夫定;乙型肝炎;肝硬化;療效;腎臟功能
乙型肝炎肝硬化是HBV長期持續復制、肝炎反復活動、發展的結果,一旦進入肝功能失代償期,患者預后極差。對乙型肝炎肝硬化患者,目前尚無標準、特效的治療方案,但對HBV進行長期抑制可延緩疾病進展,延長患者生命[1]。慢性乙型肝炎患者是肝硬化、肝癌、肝衰竭的高危人群。每年約有100萬人死于乙型肝炎相關的肝硬化、肝癌、肝衰竭。替比夫定有較好的抗HBV作用,且在CHB抗病毒過程中可改善腎功能[2-4]。本研究觀察了替比夫定治療失代償期乙型肝炎肝硬化的療效及對腎功能的影響,為優化治療提供依據。
資料和方法
一、研究對象
選擇2012年4月至2015年11月在上海市松江區中心醫院感染科就診的失代償期乙型肝炎肝硬化患者,將規律服用替比夫定(北京諾華制藥有限公司,600 mg/d)抗病毒治療且具有完整臨床資料的72例患者納入本研究。其中男性42例,女性30例,年齡42~66歲;Child-Pugh積分均為8~15分;其中12例患者有不同程度的腹水;HBV DNA水平(5.72±0.52)×103拷貝/mL。均符合2010年《慢性乙型肝炎防治指南》中失代償期肝硬化的診斷標準[1]。排除合并肝癌和或其他惡性腫瘤患者,合并其他病毒性肝炎患者,排除酒精、自身免疫性肝病等引起的肝臟損害者,存在嚴重心、腦、腎、神經系統疾病者,孕期或脯乳期婦女,曾接受過干擾素、核苷(酸)類藥物或其他免疫調節藥物者。所有患者均被告知需長期服用抗病毒藥物可能出現的耐藥、藥物不良反應等問題,本研究方案獲醫院倫理委員會批準,患者均簽署知情同意書。
二、實驗室檢測
監測治療前基線、治療24周、治療48周所有患者丙氨酸氨基轉移酶(ALT)、血清總膽紅素(TBil) 、白蛋白(Alb)水平及凝血酶原時間(PT),以Child-Pugh分級評價肝功能。腎功能采用羅氏Cobase501全自動生化分析儀檢測,CR值正常范圍是0.50~1.50 mg/dL。估算腎小球濾過率(estimated glomerular filtration rate, eGFR)采用簡化的美國腎臟病公式膳食改善(modification of diet in renal disease, MDRD)研究組開發的公式計算:186×血清肌酐-1.154×年齡-0.203×性別(男=1.000,女性=0.742)[5],其中eGFR單位為mL/(min·1.73 m2),腎功能輕度受損定義為eGFR 60~90 mL/(min·1.73 m2)。HBV DNA采用羅氏實時熒光定量聚合酶鏈反應檢測(檢測下限為500拷貝/mL)。HBV DNA基因型耐藥檢測采用反向線性探針雜交技術(INNO LiPA HBV DR v2試劑盒,比利時Innogenetics公司)。
三、統計學處理
應用SPSS 17.0進行數據統計分析,計量資料采用均數±標準差表示,治療前后的比較采用配對t檢驗。計數資料以頻數和百分數表示,采用χ2檢驗,P<0.05為差異有統計學意義。
結 果
一、比較替比夫定治療前后肝功能、凝血功能的變化
應用替比夫定治療24周和48周時,血清ALT、TBil、Alb水平及PT均較治療前明顯好轉,ALT復常率逐漸升高,結果見表1。
二、替比夫定治療前后Child-Pugh積分和病毒學指標的變化
應用替比夫定治療24周肝功能Child-Pugh積分較前好轉,但差異無統計學意義(P>0.05),隨著治療時間延長至48周時,Child-Pugh積分明顯改善(P<0.05);治療24周時無腹水消失的病例,治療48周時有3例患者腹水消失,較治療前差異無統計學意義(P>0.05)。替比夫定治療24周、48周時 HBV DNA陰轉率分別為75.00%和87.50%,且HBV DNA定量及陰轉率都較治療前有明顯改善(P<0.05);治療24周時發現有2例患者出現替比夫定耐藥,加用阿德福韋酯聯合治療后,患者病毒學指標均達到陰轉,隨訪至48周又有3例患者發生病毒耐藥,目前正在接受聯合阿德福韋酯治療,結果見表2。
三、替比夫定治療前后eGFR、CR值的變化
72例替比夫定治療24周與基線相比eGFR、CR值變化不明顯(P>0.05),39例腎功能輕度受損患者中僅有1例患者eGFR恢復正常;治療48周時eGFR、CR值較治療前明顯改善,差異有統計學意義(P<0.05),39例腎功能輕度受損者中有9例(23.08%)eGFR、6例(15.38%)CR值恢復正常,但腎功能輕度受損患者的eGFR、CR復常率較治療前無明顯的差異(P>0.05),結果見表3。

表1 72例患者替比夫定治療前后肝功能、凝血功能的變化(±s)
注:與治療前相比,*P<0.05
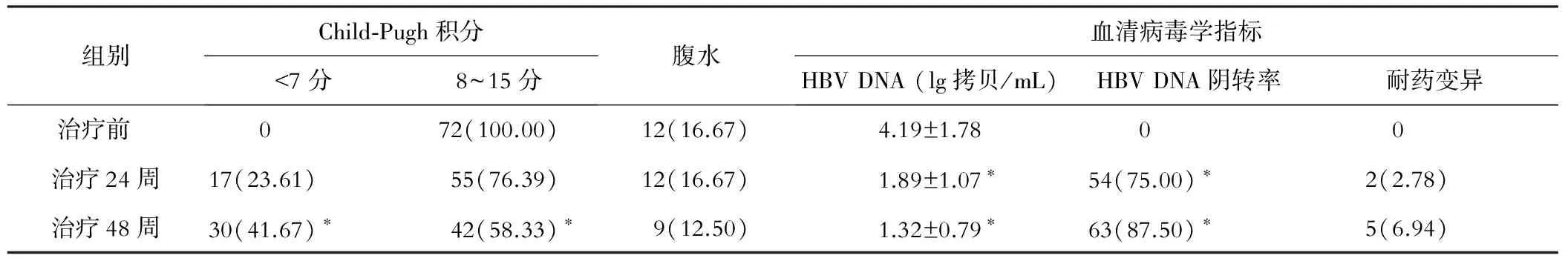
表2 替比夫定治療前后Child-Pugh積分、腹水和病毒學指標的變化[例,率(%)]
注:與治療前相比,*P<0.05
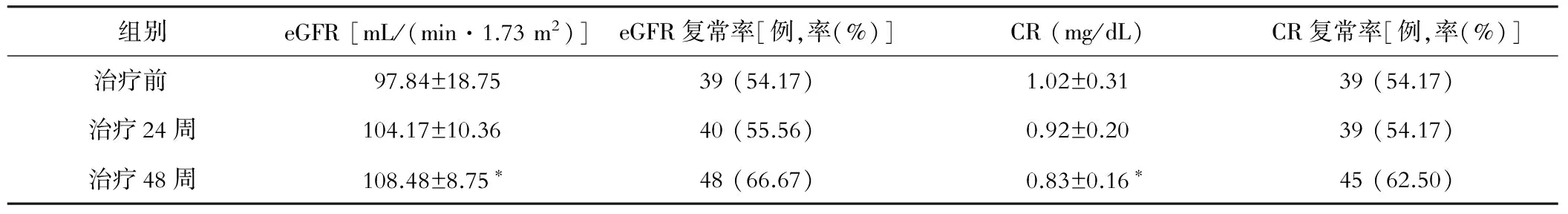
表3 替比夫定治療前后eGFR、CR值比較及輕度腎功能受損患者eGFR、CR復常率變化
注:與治療前相比,*P<0.05
討 論
對于HBV活躍的乙型肝炎肝硬化患者及早應用抗病毒治療對于延緩病情進展、預防并發癥、減少肝癌的發生非常重要[6],治療上應考慮使用能抑制病毒復制且安全性高的藥物。替比夫定為天然胸腺嘧啶脫氧核苷的自然L型對應體,是人工合成的胸腺嘧啶脫氧核苷類抗HBV DNA聚合酶藥物,在細胞激酶的作用下被磷酸化為有活性的代謝產物-腺苷,與天然底物胸腺嘧啶的5’腺苷競爭,從而抑制HBV DNA多聚酶的活性,可高度特異性地抑制HBV復制,避免正常細胞損害,這種高水平的特異性識別,使替比夫定在短期內抑制病毒復制且有良好的安全性[7-8]。本研究結果表明,應用替比夫定治療失代償期肝硬化患者24周時血清ALT、TBil水平、HBV DNA陰轉率較前明顯改善,但有2例患者出現了耐藥變異。隨訪至48周時,血清Alb水平、PT及Child-Pugh積分也較前有好轉,有5例患者出現了替比夫定的耐藥變異。本研究結果顯示,隨著治療時間的延長,替比夫定抗病毒治療后的病毒性應答、血清學應答、生化學應答等指標進一步改善。提示應用替比夫定可以通過抑制HBV復制,可以明顯達到改善失代償期慢乙型肝炎肝硬化患者生化指標和肝功能儲備的效果,隨著治療時間的延長,其治療效果更加明顯。乙型肝炎肝硬化患者抗病毒治療多主張終生服藥,因此應注意長期用藥的耐藥發生,本研究中在治療24周有耐藥病例的出現,但經聯合阿德福韋酯的治療,患者的病毒性指標可以達到HBV DNA的陰轉,隨訪至48周時,又有3例患者出現病毒耐藥,目前也采取了聯合阿德福韋酯的挽救治療,因此,隨著治療時間的延長,部分病例可以出現耐替比夫定藥物的病毒變異,但在應用抗病毒藥物治療乙型肝炎肝硬化出現耐藥的情況下可以考慮采用挽救措施以達到治療效果。
慢性HBV感染后可引起免疫復合物介導的腎小球疾病,如膜性腎病和膜毛細血管性腎小球腎炎,失代償期慢乙型肝炎肝硬化患者和慢性腎病存在密切聯系且常伴有腎功能的損害[9]。部分患者存在基線腎功能異常,伴有肝纖維化或肝硬化患者有20%~30%經eGFR評估有腎臟功能異常[10-11]。對于存在腎功能受損的高危因素的乙型肝炎肝硬化失代償患者,在抗病毒治療時,腎臟的安全性是十分重要的。隨著eGFR在評估腎小球濾過率中的廣泛應用,發現其臨床應用價值較CR大,可發現早期、輕度的腎功能下降,是評估個體的腎功能更為精確的指標[12]。本研究中有48例患者應用替比夫定治療48周后eGFR較基線水平明顯升高且肌酐水平下降,較治療前有明顯的差異,26例基線腎功能受損的患者中有6例患者eGFR復常,有4例患者CR復常。本研究結果提示,替比夫定治療能改善乙型肝炎肝硬化患者的腎臟功能,對于基線腎功能受損的乙型肝炎肝硬化失代償患者,使用L-DT抗病毒治療,其腎功能可得到一定程度的改善。慢性乙型肝炎、乙型肝炎肝纖維化及乙型肝炎肝硬化基線腎功能受損的患者,口服替比夫定抗病毒治療后可明顯改善患者的eGFR,提高腎功能[4,13-15]。研究表明[16],乙型肝炎肝硬化患者腹水產生和腎臟功能存在一定的關聯性,本研究12例腹水患者經替比夫定治療48周后有3例患者腹水消失,這將對提高肝硬化失代償患者的生存質量有很大幫助。以往的研究認為[17],由于乙型肝炎肝硬化失代償患者出現腎功能損傷的原因有腎前性損傷、急性腎小管壞死和肝腎綜合征,加之肝硬化失代償患者對腎素-血管緊張素-醛固酮系統激素滅活障礙,進一步影響了腎臟功能甚至腹水的產生,這些功能的恢復是需要一定時間的。這也可能是經治患者在24周時腎功能沒有明顯變化,而到48周才有eGFR明顯改善且有3例患者出現腹水治愈的原因之一。
總之,對于失代償期乙型肝炎肝硬化患者經替比夫定治療可以有效的抑制患者體內的HBV復制,改善肝功能,延緩病情進展,隨著治療時間的延長治療效果更加明顯;L-DT有改善腎臟功能的作用,對于基線腎功能受損患者可能有保護作用。然而本研究入選病例較少,隨訪時間短,缺乏長期療效評價,尚需擴大樣本量、延長觀察時間進一步驗證結論;對于替比夫定長期治療可改善腎功能的機制需進一步研究。
[1]中華醫學會肝病學分會 中華醫學會感染病學分會. 慢性乙型肝炎防治指南 (2010 年版). 肝臟,2011,16:2-16.
[2]Hou J,Yin YK,Xu D,et al. Telbivudine versus lamivudine in Chinese patients with chronic hepatitis B:Results at 1 year of a randomized, double-blind trial. Hepatology,2008,47:447-454.
[3]Lai CL,Gane E,Liaw YF,et al. Telbivudine versus lamivudine in patients with chronic hepatitis B. N Engl J Med,2007,357:2576-2588.
[4]Gane EJ,Deray G,Liaw YF,et al. Telbivudine improves renal function in patients with chronic hepatitis B. Gastroenterology,2014,146:138-146.
[5]Levey AS,Stevens LA,Schmid CH,et al. A new equation to estimate glomerular filtration rate. Ann Intern Med,2009,150:604-612.
[6]Cholongitas E,Papatheodoridis GV,Goulis J,et al. The impact of newer nucleos(t)ide analogues on patients with hepatitis B decompensated cirrhosis. Ann Gastroenterol,2015,28:109-117.
[7]Amarapurkar DN. Telbivudine:A new treatment for chronic hepatitis B. World J Gastroenterol,2007,13:6150-6155.
[8]Zhao S,Tang L,Fan X,et al. Comparison of the efficacy of lamivudine and telbivudine in the treatment of chronic hepatitis B: a systematic review. Virol J,2010,7: 211.
[9]Appel G. Viral infections and the kidney: HIV,hepatitis B,and hepatitis C. Cleve Clin J Med, 2007,74:353-360.
[10]Kim YJ, Cho HC, Sinn DH, et al. Frequency and risk factors of renal impairment during long-term adefovir dipivoxil treatment in chronic hepatitis B patients. J Gastroenterol Hepatol, 2012,27:306-312.
[11]左璐,孫鳳霞,王憲波,等. 298 例乙型肝炎肝硬化患者合并腎功能不全情況分析. 中華肝臟病雜志,2014,22:504-508.
[12]Levey AS,Coresh J,Balk E,et al. National kidney foundation practice guidelines for chronic kidney disease:evaluation, classification, and stratification. Ann Intern Med,2003,139:137-147.
[13]Liaw YF,Gane E,Leung N,et al. 2-year GLOBE trial results:telbivudine Is superior to lamivudine in patients with chronic hepatitis B. Gastroenterology,2009,136:486-495.
[14]Chan HL,Chen YC,Gane EJ,et al. Randomized clinical trial:efficacy and safety of telbivudine and lamivudine in treatment-na?ve patients with HBV-related decompensated cirrhosis. J Viral Hepat,2012,19:732-743.
[15]李小溪,鐘春秀,楊淑玲,等. 阿德福韋酯和替比夫定單藥治療慢性乙型肝炎對腎臟功能影響的比較. 南方醫科大學學報,2012, 32:826-829.
[16]Hung CH,Hu TH,Lu SN,et al. Tenofovir versus entecavir in treatment of chronic hepatitis B virus with severe acute exacerbation. Antimicrob Agents Chemother,2015,59:3168-3173.
[17]Russ KB,Stevens TM,Singal AK. Acute kidney injury in patients with cirrhosis. J Clin Transl Hepatol,2015,28:195-204.
(本文編輯:錢燕)
Efficacy of telbivudine in chronic hepatitis B patients with decompensated liver crirrhosis and its influence on renal function
GAODe-yong,WANGYing-ying,WANGYan-yan,XUGuo-rong,WUJian-qing,XIALi-ping,LIULiang-ming.
DepartmyntofInfectiousDiseases,SongjiangHospitalAffiliatedtoShanghaiFirstPeople’sHospital,ShanghaiJiaotongUniversity,Shanghai201600,ChinaCorrespondingauthor:GAODe-yong,Email:gaodeyong1970@163.com
ObjectiveTo investigate the efficacy of telbivudine (LDT) in patients with hepatitis B virus (HBV)-related decompensated liver cirrhosis and evaluate its influence on renal function. MethodsIn the retrospective analysis, 72 patients with HBV-related decompensated liver cirrhosis in our hospital from April 2012 to October 2015 received LDT (600 mg/d) antiviral therapy. The levels of alanine aminotransferase (ALT), total bilirubin (TBil), albumin (Alb), prothrombin time (PT), ascites, Child-Pugh integral, HBV DNA load, HBV DNA undetectable rate and resistance mutation were evaluated at baseline, week 24 and 48. Serum creatinine (CR) and estimated of glomerular filtration rate (eGFR) were also monitored. Comparisons among baseline, week 24 and 48 were carried out by chi-square test and t-test. ResultsAt week 24, mean levels of ALT, TBil, HBV DNA load and HBV DNA undetectable rate were 46.12 U/L, 44.31 mol/L, 1.89 lg copies/mL and 75.00%, respectively. All results were significantly improved, as compared with those at baseline (P<0.05). Meanwhile, resistance mutations occurred in 2 cases, and ascites regression had not been reported. At week 48, levels of Alb and PT were 34.16 g/L and 15.09 sec, and Child-Pugh integral was significantly decreased as compared to that at baseline (P<0.05). In addition, resistance mutations occurred in 5 cases, and ascites regression was found in 3 cases. Compared with those at baseline, CR level reduced to 0.83 mg/dL and eGFR level raised to 108.48 mL/(min·1.73 m2) after 48-week treatment (P<0.05). Furthermore, 9 (23.08%) patients with mild renal impairment improved with eGFR≥90 mL/(min·1.73 m2). ConclusionLDT is a crucial strategy for inhibiting virus replication and improving liver function in chronic hepatitis B patients with decompensated liver cirrhosis. Although prolonging treatment can enhance therapeutic efficacy, it also increases resistance mutations risk. In terms of patients with mild renal impairment, LDT might be an appropriate option for its improvement in renal function.
Telbivudine;Chronic hepatitis B;Liver cirrhosis;Efficacy;Renal function
上海市松江區計劃和生育委員會重點項目(2012-III-06)
201600上海交通大學附屬第一人民醫院松江分院感染科
高得勇,Email:gaodeyong1970@163.com
2016-03-11)