伴馬尾神經沉降征陽性腰椎管狹窄癥患者的手術療效觀察
許 鵬 史建剛 葉曉健 史國棟 許國華 侯 洋 袁 文 賈連順
上海長征醫院脊柱外科,上海200003
伴馬尾神經沉降征陽性腰椎管狹窄癥患者的手術療效觀察
許 鵬 史建剛 葉曉健 史國棟 許國華 侯 洋 袁 文 賈連順
上海長征醫院脊柱外科,上海200003
目的分析馬尾神經沉降征(SS)在腰椎管狹窄癥中的表現特咖,以及行改良腰椎后路椎體間融合術(PLIF)治療的臨床療效。方法回顧分析2013年1月~2O14年6月上海長征醫院脊柱外科收治的LSS患者126例的臨床資料,依據仰臥位MRI橫斷面馬尾神經是否沉降分為SS陽性組和SS陰性組。采用日本骨科學會(JOA)評分標準(29分法),比較兩組患者的術前、術后3個月和末次隨訪的療效。結果SS陽性患者109例,SS陰性患者17例,SS陽性發生率為86.5%。SS陽性組JOA評分術前、術后3個月及末次隨訪分別為(10.2±3.4)、(22.3± 3.1)、(23.1±2.3)分,術后JOA評分均較術前升高(P<0.05);SS陰性組JOA評分術前、術后3個月及末次隨訪分別為(11.1±4.4)、(21.4±5.4)、(23.6±3.1)分,術后JOA評分均較術前升高(P<0.05);但是,兩組患者術前及術后JOA評分差異無統計學意義(P>0.05)。結論SS陽性廣泛存在于腰椎管狹窄患者中,并不影響患者術后療效,SS陽性仍無法作為手術效果的預判指標,改良PLIF手術對SS陽性患者效果確切。
腰椎后路椎體間融合術;腰椎管狹窄;馬尾神經;磁共振成像
腰椎管狹窄癥指腰椎管容量減少,硬膜囊和/或神經根受壓而出現功能障礙,發生率<為30%,60歲以上發病率更高[1]。腰椎管狹窄癥是一種常見的老年腰椎退變性疾患,常表現為間歇性跛行,由于缺乏明確的臨床體征和影像學標準,目前,臨床醫生只能通過綜合多種方法來診斷并判斷是否需要手術[2,3]。腰后路椎板切除減壓伴或不伴椎間植骨融合術是治療腰椎管狹窄癥的標準術式[4-5]。2010年,Barz等[6]提出馬尾神經沉降征(sedimentation sign,SS)可以直觀判斷椎管狹窄。但是,SS提出后對臨床的指導意義尚需進一步明確,為此,本研究回顧分析了126例手術治療多節段腰椎管狹窄癥患者,現總結報道如下:
1 料與方法
1.1 一般資料
回顧分析2013年1月~2O14年6月在上海長征醫院脊柱外科收治的2個節段以上腰椎管狹窄癥患者126例的臨床資料,其中男51例,女75例;年齡47~74歲,平均(63.15±6.29)歲;病程4~32個月,平均(10.51±6.05)個月;手術節為2~6個,平均(3.03±1.02)個;臨床表現:典型間歇性跛行98例,腰痛104例,單側下肢酸脹不適或疼痛67例,雙側下肢不適32例,伴有不同程度下肢感覺障礙102例,肌力減弱22例;所有患者均行改良PLIF術。
納入標準:①間歇性跛行或伴腰痛和下肢疼痛、麻木;②核磁共振(magnetic resonance imaging,MRI)檢查確診中央椎管或神經根管狹窄;③經正規保守治療3個月及以上無明顯療效。排除標準:①蛛網膜炎、下肢血管病變患者;②單節段腰椎間盤突出繼發椎管狹窄患者;③合并有腰椎手術史、外傷、強直性脊柱炎、病理性骨折、嚴重的骨質疏松等的患者。
1.2 方法
1.2.1 MR檢查及SS判定采用PHILIPS 1.5T磁共振成像儀,行腰椎矢狀面及橫斷面掃描,層厚4.0 mm,層距1.0 mm。由兩名經驗豐富的骨科醫生分別閱片收集數據,協商一致后進行結果判定并分組。
Barz等[6]將馬尾神經束在仰臥位腰椎MRI橫斷面上的形態分為兩類(上下二分法):正常情況下馬尾神經束懸浮于腦脊液中,仰臥位時神經束由于重力作用沉降到椎管背側,從而在MRI圖像上表現為除了下節段神經根外,馬尾神經束集中于硬膜囊背側部分,即SS征陰性;SS陽性即仰臥位時神經束仍懸浮于硬膜囊內。見圖1。
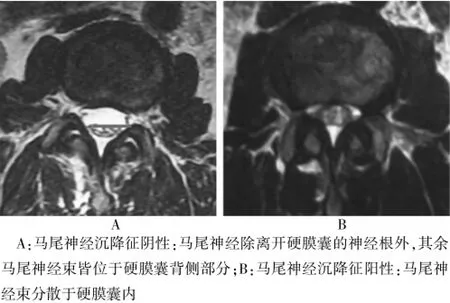
圖1 腰椎MRI平掃T2加權象橫斷面
1.2.2 手術方法改良后路椎體間融合內固定術(modified-PLIF):患者俯臥位,采取標準后正中入路切口,分離椎旁肌,暴露相鄰上下椎體的關節突關節。在病變間隙上下椎體常規置入椎弓根螺釘進行固定。棘突咬骨鉗切除棘突,骨鑿切除下關節突,槍鉗咬除部分上關節突、黃韌帶,暴露硬膜囊和出口及行走神經根,神經拉鉤向一側牽開硬膜囊和神經根,顯露椎間盤,去除椎間盤和軟骨終板,置入合適大小的椎間融合器。探查出口根及行走神經根管是否狹窄。對側及上、下節段做相同處理。安裝連接桿,將置入融合器間隙椎弓根螺釘加壓固定。止血、縫合切口。改良方法較標準PLIF下關節突去除略多,更利于減壓出口神經根,并在行椎間融合時減少對神經根和硬膜囊的牽拉,降低損傷神經根的概率。見圖2。
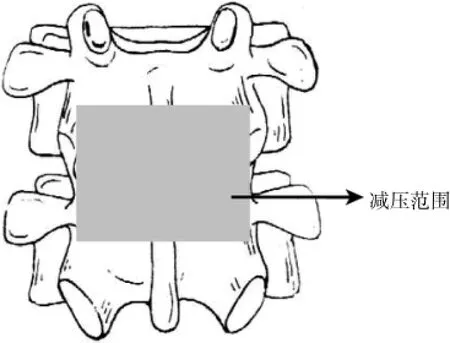
圖2 改良PLIF減壓范圍示意圖
術后24 h內給予抗生素預防感染,如合并基礎疾病或感染高危因素患者,延長抗生素使用時間。術后第2天后拔除引流管,床上開始雙下肢抬高和挺腹鍛煉,2~3周后腰圍保護下可下床進行活動,腰圍需要佩戴3個月。
1.2.3 療效評價根據日本骨科學會(JOA)評分標準(29分法)對患者的術前、術后3個月和末次隨訪的療效進行比較。并對SS陽性組和SS陰性組療效進行對比。JOA評分標準主要包括主觀癥狀(下腰背痛、腿痛及步態)、臨床體征(直腿抬高試驗、感覺障礙及運動障礙)、日常活動受限度和膀胱功能等。
1.3 統計學方法
應用SPSS 13.0對數據進行分析,正態分布的計量資料以均數±標準差(x±s)表示,兩組間比較采用t檢驗;計數資料以率表示,采用X2檢驗。以P<0.05為差異有統計學意義。
2 果
126例患者SS陽性者109例,SS陰性者17例,SS陽性發生率為86.5%。SS陽性組術后JOA評分均較術前升高(P<0.05);SS陰性組術后JOA評分均較術前升高(P<0.05);但是,兩組患者術前及術后JOA評分比較,差異均無統計學意義(P>0.05)。見表1。典型病例影像學資料見圖3。

表1 兩組JOA評分比較(分,x±s)
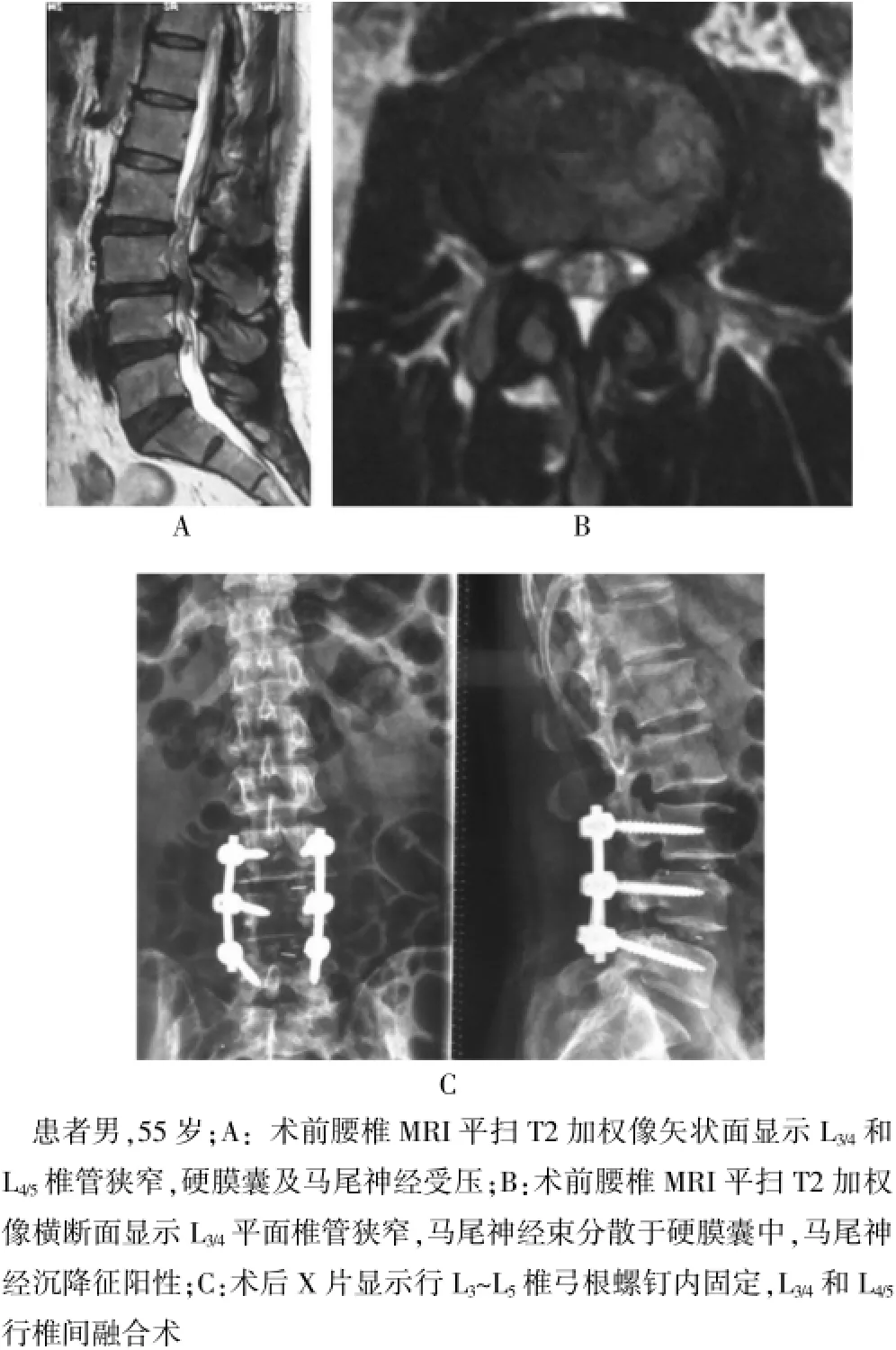
圖3 腰椎管狹窄癥行改良后路椎體間融合內固定術術前、術后影像學資料
3 論
3.1 腰椎管狹窄癥的影像學診斷
腰椎管狹窄癥主要以長期慢性腰痛、間歇性跛行等為主要癥狀的特咖[7]。因為缺乏典型的癥狀、體征,所以,臨床中往往根據臨床表現、電生理學檢查和影像學表現進行診斷[8]。然而,對于手術指征與責任節段存在較多的爭議[9-10]。腰椎MRI橫斷面椎管面積(cross-sectional area,CSA)被認為是主要測量指標[11],但是,臨床癥狀、評分系統與椎管CSA關聯度不佳[12],特別是部分老年患者椎管狹窄程度較重,但是,臨床癥狀不重。因此,部分學者研究應用站立位或增強、軸向負重、直腿抬高狀態下的MRI或CT可以提高診斷率[13-14],但是,尚未獲得廣泛認可。所以,本研究的納入標準中,既包括影像學表現,也包括臨床表現。
3.2 SS的提出與定義
2010年由Barz等[6]首先提出SS。由于行仰臥位MRI檢查時,漂浮在硬膜囊內的馬尾神經隨重力作用沉降到背側,除去下節段神經根外,即SS陰性;SS陽性即仰臥位時神經束仍懸浮于硬膜囊內。考慮L5/S1節段S1和S2神經根位于硬膜囊腹側,不存在馬尾神經束的沉降,故排除L5/S1節段。Barz等[6]的報道中根據馬尾神經束在腹側與背側的分布進行定義,即“二分法”,而不是以關節突連線來分類;考慮最狹窄節段馬尾神經束被擠壓在硬膜囊內影響馬尾神經沉降征的判斷,故其選擇病變狹窄最嚴重節段的上或下一個節段至少一個層面存在馬尾神經束沉降現象即可診斷馬尾神經沉降征陽性,并配以橫斷面MRI平掃圖片為例,但是,配圖未指明所取橫斷面的具體層面,因此易產生誤解。由于椎體中央水平與椎間隙水平馬尾神經束在硬膜囊內的分布可能有差別,進一步可能影響馬尾神經沉降征陽性率的判定,因此,Barz等[15]進一步明確為L1/2~L4/5節段中最狹窄節段中上、下椎體中央水平,避免了易引起的誤解。針對SS的具體界定應進一步加強,避免因認定標準與方法不一而導致的陽性率差別巨大,產生更多誤解。
3.3 SS在腰椎管狹窄癥中的應用價值
Barz等[6]報道SS在有癥狀腰椎管狹窄癥患者中陽性率為94%,而在腰痛組的陽性率為0%,而且不受腰椎節段的影響,SS診斷腰椎管狹窄癥可信度高。但是,其進一步研究顯示SS并不能作為手術治療效果的預判因素,但是SS陽性患者保守治療效果不佳[15]。Rachel[16]報道病例SS陽性率為66%(76/115),且多發生在L2/3或L3/4節段,多表現為中央椎管狹窄,陽性組患者手術治療效果明顯改善。Tomkins-Lane等[17]認為SS陽性具有較高的組內和組間信度,但是,其并不能幫助鑒別腰椎管狹窄癥與下腰痛、血管性間歇性跛行等疾病[18]。
3.4 改良PLIF手術
19世紀早期Hibbs脊柱植骨融合術出現以后,人們進行了不懈的創新改進。20世紀中《,Cloward[19]首先報道了脊柱椎間融合術,之后,椎間融合器進行了多次更新,使腰椎后路椎體間融合術(PLIF)成為應用最為廣泛的融合技術之一[20]。由于標準PLIF手術要求保留部分下關節突,而中國人退變性腰椎疾病常伴有嚴重的側隱窩狹窄和神經根袖處的壓迫,一味保留下關節突易造成減壓不徹底,而且,為椎間融合需過度牽拉相應節段神經根和硬膜囊,若牽拉力量過大容易造成神經根損傷或術后下肢酸脹,而且,因L3以上節段神經根和硬膜囊的活動度小,牽拉范圍有限[21,22]。因此,本研究在保證充分椎間融合的基礎上,較標準PLIF下關節突去除略多,更利于減壓出口神經根,并在行椎間融合時減少對神經根和硬膜囊的牽拉,降低損傷神經根的概率。
綜上所述,SS作為診斷腰椎管狹窄癥的補充方法已經引起大家的充分關注,但是,人們如不充分了解其操作方法與標準可能會導致錯誤,對臨床產生誤導。同時,SS對腰椎管狹窄癥治療效果的指導意義仍需觀察研究。
[1]Kalichman L,Cole R,Kim DH,et al.Spinal stenosis prevalence and association with symptoms:the Framingham Study[J].Spine J,2009,9(7):545-50.
[2]Kim HJ,Lee JI,Kang KT,et al.Influence of pain sensitivity on surgical outcomes after lumbar spine surgery in patients with lumbar spinal stenosis[J].Spine(Phila Pa 1976),2015,40(3):193-200.
[3]Tomkins-Lane C,Melloh M,Lurie J,et al.Consensus on the clinical diagnosis of lumbar spinal stenosis:results of an international delphi study[J].Spine(Phila Pa 1976),2016.[Epub ahead of print]
[4]Stromqvist BH,Berg S,Gerdhem P,et al.X-stop versus decompressive surgery for lumbar neurogenic intermittent claudication:randomized controlled trial with 2-year follow-up[J].Spine(Phila Pa1976),2013,38(17):1436-1442.
[5]de Graaf I,Prak A,Bierma-Zeinstra S,et al.Diagnosis of lumbar spinal stenosis:a systematic review of the accuracy of diagnostic tests[J].Spine(Phila Pa 1976),2006,31(10):1168-1176.
[6]Barz T,Melloh M,Staub LP,et al.Nerve root sedimentation sign:evaluation of a new radiological sign in lumbar spinal stenosis[J].Spine(Phila Pa 1976),2010,35(8):892-897.
[7]Chen J,Wang J,Wang B,et al.Post-surgical functional recovery,lumbar lordosis,and range of motion associated with MR-detectable redundant nerve roots in lumbar spinal stenosis[J].Clin NeurolNeurosurg,2016,140:79-84.
[8]Udeh B L,Costandi S,Dalton JE,et al.The 2-year costeffectiveness of 3 options to treat lumbar spinal stenosis patients[J].Pain Pract,2015,15(2):107-116.
[9]Burgstaller JM,Schuffler PJ,Buhmann JM,et al.Is there an association between pain and magnetic resonance Imaging parameters in patients with lumbar spinal stenosis?[J].Spine(Phila Pa 1976),2016.[Epub ahead ofprint]
[10]Mekhail N,Costandi S,Abraham B,et al.Functional and patient-reported outcomes in symptomatic lumbar spinal stenosis following percutaneous decompression[J].Pain Pract,2012,12(6):417-425.
[11]Lurie JD,Tosteson AN,Tosteson T D,et al.Reliability of readings ofmagnetic resonance imaging features of lumbar spinal stenosis[J].Spine(Phila Pa 1976),2008,33(14):1605-1610.
[12]SirvanciM,Bhatia M,Ganiyusufoglu KA,et al.Degenerative lumbar spinal stenosis:correlation with Oswestry Disability Index and MR imaging[J].Eur Spine J,2008,17(5):679-85.
[13]Alyas F,Connell D,and Saifuddin A.Upright positional MRIof the lumbar spine[J].Clin Radiol,2008,63(9):1035-1048.
[14]Madsen R,Jensen TS,Pope M,et al.The effect of body position and axial load on spinal canal morphology:an MRI study of central spinal stenosis[J].Spine(Phila Pa 1976),2008,33(1):61-67.
[15]Barz T,Staub LP,Melloh M,et al.Clinical validity of the nerve root sedimentation sign in patients with suspected lumbar spinal stenosis[J].Spine J,2014,14(4):667-674.
[16]Moses R A,ZhaoW,Staub L P,et al.Is the sedimentation sign associated with spinal stenosis surgical treatment effect in sport?[J].Spine(Phila Pa 1976),2015,40(3):129-136.
[17]Tomkins-Lane CC,Quint DJ,Gabriel S,et al.Nerve root sedimentation sign for the diagnosis of lumbar spinal stenosis:reliability,sensitivity,and specificity[J].Spine(Phila Pa 1976),2013,38(24):E1554-E1560.
[18]Zhang L,Chen R,Liu B,et al.The nerve root sedimentation sign for differential diagnosis of lumbar spinal stenosis:a retrospective,consecutive cohort study[J].Eur Spine J,2016.[Epub ahead of print]
[19]Cloward RB.The treatment of ruptured lumbar intervertebral discs by vertebral body fusion.I.Indications,operative technique,after care[J].JNeurosurg,1953,10(2):154-68.
[20]Hentenaar B,Spoor AB,Malefijt JW,et al.Clinical and radiological outcome ofminimally invasive posterior lumbar interbody fusion in primary versus revision surgery[J]. JOrthop Surg Res,2016,11(1):2.
[21]Nakashima H,Kawakami N,Tsuji T,et al.Adjacent segment disease after posterior lumbar interbody fusion:based on caseswith aminimum of10 yearsof follow-up[J]. Spine(Phila Pa 1976),2015,40(14):E831-E841.
[22]Liu J,Deng H,Long X,et al.A comparative study of perioperative complications between transforaminal versus posterior lumbar interbody fusion in degenerative lumbar spondylolisthesis[J].European Spine Journal,2015,25(5):1575-1580.
Operation effect observation of lumbar spinal stenosis w ith positive sedimentation sign of cauda equina nerve
XU Peng SHIJiangang YE Xiaojian SHIGuodong XUGuohua HOU Yang YUANWen JIA Lianshun Departmentof Spinal Surgery,Shanghai Changzheng Hospital,Shanghai 200003,China
Objective To analyze the characters of cauda equina nerve root sedimentation sign(SS)in patients with lumbar spinal stenosis and the effect of posterior lumbar interbody fusion(PLIF).M ethods The clinical data of 126 patients with LSS underwentmodified PLIF surgery in Shanghai Changzheng Hospital from January 2013 to June 2014 were retrospective analyzed.According to the supine MR examination,the cases were divided into positive SS group and negative SSgroup.Japanese Orthopaedic Association(JOA-29)score system was respectively used to evaluate the treatment effect before operation,3months after operation and last follow-up.Results There were 109 caseswith positive SS and 17 cases with negative SS.The incidence of positive SSwas 86.5%.The JOA scores in SS positive group were respectively(10.2±3.4),(22.3±3.1),(23.1±2.3)scores before operation,3 months after operation and last followup,the JOA scores increased after operation(P<0.05).The JOA scores in SS positive group were respectively(11.1± 4.4),(21.4±5.4),(23.6±3.1)scores before operation,3monthsafter operation and last follow up,The JOA scores also increased after operation(P<0.05).However,therewas no difference of JOA scores between two groups before and after operation(P>0.05).Conclusion SS is commonly found in the lumbar spinal stenosis patients,and it does not influent the postoperative outcome.However,SS is not still considered as the predict factor of postoperative effect.Themodified PLIF surgery is a valid treatmentmethod for SSpositive patients.
Posterior lumbar interbody fusion;Lumbar spinal stenosis;Cauda equina;Magnetic resonance imaging
R687.3
A
1673-7210(2016)05(c)-0096-04
2016-02-25本文編輯:蘇暢)
聚合物分子工程國家實驗室(復旦大學)開放研究課題基金(K2012-10)。
許鵬(1982.4-),男,博士;研究方向:脊柱外科疾病的基礎與臨床,骨科相關材料的基礎。
史建剛(1968.7-),男,博士,主任醫師;研究方向:脊柱外科疾病的基礎與臨床。

