水貂犬瘟熱病毒RT-PCR檢測方法建立及應用
于紅鴿 (山東省即墨市畜牧獸醫局266100)
水貂犬瘟熱病毒RT-PCR檢測方法建立及應用
于紅鴿 (山東省即墨市畜牧獸醫局266100)
水貂犬瘟熱病毒 (Canine distemper virus,CDV)屬于副黏病毒科 (Paramyxoviridae)麻疹病毒屬 (Morbillivirus)。形狀多種,病毒直徑大小多在150~300nm[1]。本實驗通過RTPCR技術檢測了水貂病料中犬瘟熱病毒的感染情況,建立具有快速、靈敏的RT-PCR檢測方法。
1 材料與方法
1.1 材料
1.1.1 參考毒株
犬瘟熱CDV-3弱毒株。
1.1.2 試劑
DNAzol Regent、TRIzol LS?Reagent、RNA提取試劑盒;rTaqDNA ploymerase、 dNTPs、 AMV Reverse Transcriptase、Rnase-Inhibitor、 DNA Marker(DL2000); Agarose 瓊脂糖;異丙醇、無水乙醇、DEPC水、氯仿、瓊脂粉等。
1.1.3 儀器設備
超凈工作臺、臺式高速冷凍離心機、PCR擴增儀 (Alpha Unit Black Assembly PCR、PTC-200)、42℃可調恒溫水浴鍋、高速離心機、微波爐、電子天平、DYY-Ⅲ-7型、DYY-Ⅲ-8B核酸電泳儀、紫外凝膠成像系統[2]。
1.1.4 檢測的組織病料來源及病料采集方法
某新建貂場飼養水貂1600只,其中44日齡斷奶幼貂1100只,2016年4月23日突然發病176只,死亡114只。
無菌操作剪取1.0~2.0g病料,加少量滅菌PBS(含青霉素、鏈霉素),注意邊研磨邊加液氮,防止RNA被降解。用PBS按1∶4稀釋成懸液,-20℃反復凍融3次,4℃10000r/min離心10min,取上清,-70℃保存。
1.2 方法步驟
1.2.1 引物設計與合成
根據GenBank中CDV-3N蛋白基因序列,用Primer軟件設計了特異性引物,擴增引物:CDV-3-P1(5′TAGGTTAGGGCTGTGGCCTT3′); CDV-3-P2 (5′CCGCACCTTCGGATATACTG3′)。
1.2.2 CDV的RNA提取
1.5ml離心管中加入 250μl組織液;加 TRIzol LSR Reagent750μl,顛倒 6~8 次,4℃靜止 5min; 加 200μl氯仿充分震蕩,在4℃冰箱,靜止10min;4℃離心12000轉15min;取上清液500μl,轉入新EP管,加等量的異丙醇,顛倒6~8次 (-70℃冰箱中靜置45min),充分沉淀核酸;4℃離心12000轉15min,棄上清液;加入75%冷乙醇 (DEPC配置)1000μl,離心5min,棄上清液,干燥核酸;加20μlDEPC水溶解-20℃保存,備用。
1.2.3 CDV RNA的反轉錄
CDV反轉錄反應 (RT-PCR)總體積為 20μl:5×Buffer4μl,M-MLV(反轉錄酶)0.5μl,RNase inhibitor 0.5μl,RT 引物 1μl,2.5mM dNTP2.5μl,DEPC 滅菌水 8.5μl,病毒RNA模板3μl,混勻42℃水浴1h,70℃5min滅活反轉錄酶。得到cDNA模板,-20℃保存備用。
1.2.4 CDV PCR的反應條件的優化及體系的建立
最適模板量確定:分別以2、3、4、5、6、7和8μl反轉錄的cDNA為模板,對擴增產物進行瓊脂糖凝膠電泳觀察,保持其他試劑濃度及反應條件不變,確立最佳模板濃度。最適引物濃度確定:在PCR反應體系中分別加入上、下游引物(20μmol/μl) 0.1、 0.3、 0.5、 0.7、 1.0μl,通過瓊脂糖凝膠電泳進行對擴增產物觀察,確立最佳引物濃度。最佳退火溫度確定:分別以47、49、51、53、55和 57℃退火溫度進行PCR反應,通過瓊脂糖凝膠電泳進行對擴增產物的觀察,確立最佳退火溫度。CDV最佳反應體系:總體積25μl,10×Buffer2.5μl,dNTP Mixture(2.5mmol/L)2μl,P1+P2 0.5μl+0.5μl,Taq0.5μl,滅菌雙蒸水 17μl,DNA 模板 2μl。 最佳擴增條件:95℃預變性 5min,94℃變性 30s,51℃退火 40s,72℃延伸2min,共30個循環,72℃終延伸10min。
在PCR儀中進行擴增:95℃預變性5min;94℃變性30s,51℃退火40s,72℃延伸2min,循環數30次;72℃終延伸10min。對PCR產物進行瓊脂糖凝膠電泳:用TAE緩沖液配制1%瓊脂糖凝膠,瓊脂糖加熱溶化后加入溴化乙錠 (EB,10mg/ml)至終濃度0.5μg/μl,混勻,制成電泳凝膠板待用。取3μl擴增產物加3μl6×Loading Buffer(上樣緩沖液)混勻,加入上樣孔,同時以標準DNA分子量 (DL-2000 Marker)為對照,100V電泳30min,紫外凝膠成像系統觀察分析結果。
1.3 CDV PCR檢測方法的特異性、敏感性、重復性試驗
1.3.1 RT-PCR特異性試驗
分別取犬瘟熱病毒 (CDV)、犬冠狀病毒 (CCV)反轉錄產物及犬細小病毒 (CPV)抽提的DNA,用已建立的方法進行擴增,驗證本方法的特異性。
1.3.2 RT-PCR敏感性試驗
從疫苗中抽提CDV-3的RNA,用DEPC水將RNA依次進行10-1~10-7倍稀釋,分別進行RT-PCR檢測,確定其敏感性。
1.3.3 RT-PCR重復性性試驗
用已建立的RT-PCR檢測方法對用免疫膠體金試紙跟RT-PCR同檢測為水貂犬瘟熱病毒為陽性的病料進行重復檢測3次,驗證本方法的重復性和穩定性。
1.4 RT-PCR的臨床應用
從儲存水貂病料中隨機取2份病料,分別用膠體金和RT-PCR方法檢測。
2 結果
2.1 RT-PCR檢測方法反應條件的確定
以CDV-3株為模板,利用設計的特異性引物進行RTPCR反應。顯示擴增得到與預期目的條帶大小相符的特異性片段。經過不同條件,優化PCR反應體系,確定采用2μl的模板量,上、下游引物各0.5μl,退火溫度為51℃進行擴增。以優化的PCR反應的最佳條件進行PCR擴增并進行凝膠電泳,在287bp處得到清晰可見的目的條帶。
2.2 CDV PCR檢測方法的特異性、敏感性、重復性試驗結果
2.2.1 特異性試驗結果
RT-PCR能從提取的核酸中擴增出287bp特異條帶,其他泳道的病毒:犬細小病毒 (CPV)、犬冠狀病毒 (CCV)擴增結果為陰性,說明本引物特異性好 (見圖1)。

圖1 RT-PCR特異性實驗結果
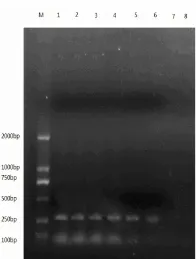
圖2 RT-PCR敏感性實驗結果

圖3 RT-PCR重復性實驗結果
2.2.2 敏感性試驗結果
對不同濃度CDV-3RNA進行RT-PCR擴增,顯示該RT-PCR方法最低能檢出約稀釋濃度10~5倍的病毒RNA(見圖 2)。
2.2.3 重復性試驗結果
3次重復操作RT-PCR方法檢測結果一致,表明方法穩定可靠 (見圖3)。
2.3 臨床收集樣品檢測結果
本試驗RT-PCR檢測方法比免疫膠體金法敏感度高,結果準。
[1]高娃,楊敬,陳振文,等.犬瘟熱病毒分子生物學研究進展[J].中國比較醫學雜志,2004,14(4):241-244.
[2]殷震,劉景華.動物病毒學[M].第2版.北京科學出版社,1997,16(7):329-330.
于紅鴿 (1989.9-),女,山東省即墨市人,大學本科,助理獸醫師,主要從事動物疾病防控、動物疾病診斷工作。

