氯化苯丙胺鹽法全自動化檢測微量總蛋白存在重大的方法學缺陷
莊小青,羅士來,楊 露,夏前鳳,薛 夢
(1.泗陽仁慈醫院檢驗科,江蘇宿遷 223700;2.泗陽縣中醫院檢驗科,江蘇宿遷 223700)
?
·經驗交流·
氯化苯丙胺鹽法全自動化檢測微量總蛋白存在重大的方法學缺陷
莊小青1,羅士來2,楊 露1,夏前鳳2,薛 夢2
(1.泗陽仁慈醫院檢驗科,江蘇宿遷 223700;2.泗陽縣中醫院檢驗科,江蘇宿遷 223700)
目的 探討氯化苯丙胺鹽法全自動化檢測腦脊液或尿液中微量總蛋白發生嚴重差錯的原因。方法 將定值總蛋白采用連續遞減稀釋法獲得35例標本(總蛋白質量濃度0~30 g/L),然后在貝克曼DXC800生化分析儀上采用氯化苯丙胺鹽法檢測。結果 (1)當總蛋白質量濃度為0~3 g/L時檢測值呈線性增加,與理論值一致。(2)當總蛋白質量濃度為3~9 g/L時檢測值遞減,在0.5~2.5 g/L之間。當總蛋白質量濃度大于9 g/L時檢測值趨于0.5 g/L左右。結論 該法不能滿足全自動化檢測的單區間要求,即檢測值存在二元性,故不宜單獨采用全自動生化分析儀檢測。
生物化學/儀器和設備; 自動化; 血蛋白質類; 氯化苯丙胺鹽
氯化苯丙胺鹽與腦脊液或尿液中微量總蛋白結合產生穩定的濁度,通過濁度變化確定微量蛋白質的質量濃度。據文獻報道,該方法穩定性好、靈敏度高、線性范圍寬、抗干擾能力強[1]。2014年7月至2015年5月作者使用該法試劑盒在全自動生化分析儀上檢測微量總蛋白共計120例,其中結果出現嚴重偏差5例,與臨床診斷不符。經實驗研究表明,該法存在重大方法學缺陷,即對高質量濃度標本無反應飽和點,無法進行糾正與監測,導致檢測值存在二元性,易誤診病理性高值,現報道如下。
1 材料與方法
1.1 材料 美國貝克曼定值血清(總蛋白質量濃度30 g/L)。
1.2 儀器與試劑 美國貝克曼全自動生化分析儀 Dxc 800及其配套試劑、校準品;氯化苯丙胺鹽法腦脊液及尿蛋白檢測試劑盒(檢測線性0~3 g/L),配套標準品及質控品(國產)。
1.3 方法 確認按照試劑盒說明書設置檢測參數并定標,連續檢測質控品20個工作日,確認試劑穩定、測量狀態在控;確認檢測人員已熟練掌握儀器與試劑盒使用方法。采用生理鹽水將貝克曼定值血清按約1 g/L質量濃度遞減連續稀釋獲得30份標本,再將第30號標本(總蛋白質量濃度為0.9 g/L)按倍比稀釋法獲取5份標本,見表1。將35份標本編號后按1~35號和35~1號次序測量2次,取均值。
1.4 數據處理 應用Excel2003軟件進行數據分析、計算、繪圖與制表等。
2 結 果
總蛋白質量濃度大于3 g/L時檢測值不是趨于飽和而是下降,造成檢測值二元性,不能滿足全自動化檢測的單區間要求。35份標本檢測結果見表2。
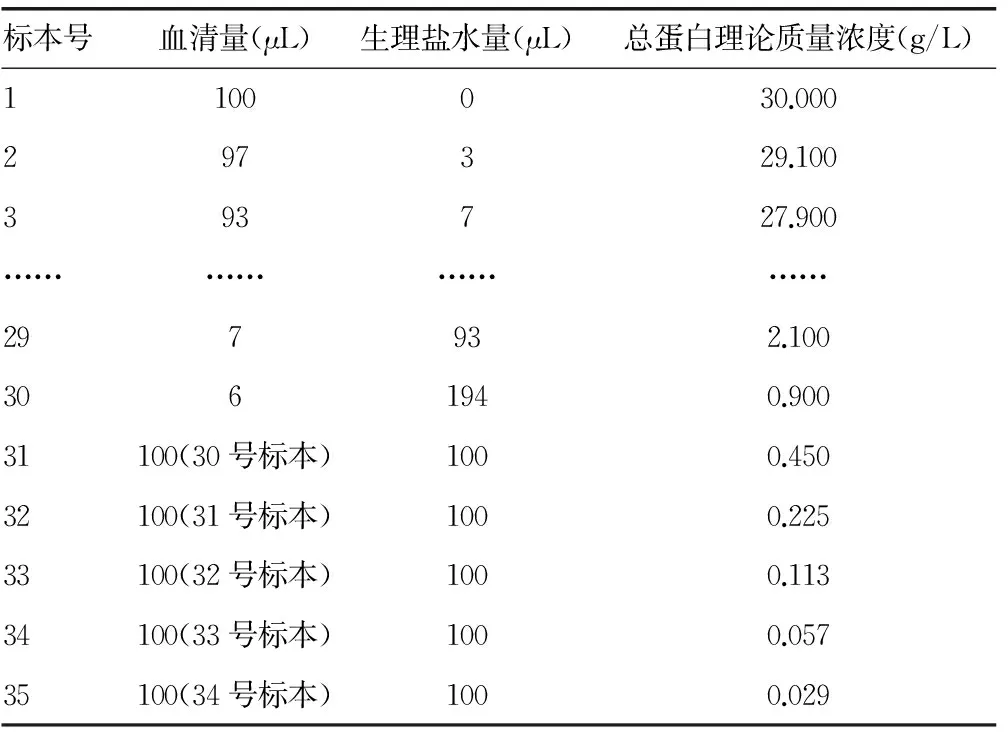
表1 定值血清稀釋后質量濃度(g/L)

表2 35份標本檢測結果
3 討 論
在微量總蛋白檢測方法中磺基水楊酸比色法需要自配試劑、操作繁瑣、易產生凝塊造成誤差且標準液不統一、精密度較低。染料結合法和鄰苯三酚紅鉬絡合法對清蛋白的靈敏度高于球蛋白,且染料易污染比色杯。干化學法測定線性寬、速度快,但成本很高。據文獻報道氯化苯丙胺鹽法是較理想的方法[2-8]。
作者在使用該法時發現會出現嚴重誤差并據此進行深入探討。對35份標本的檢測結果與理論值繪制成散點圖,見圖1。當總蛋白質量濃度為0.029~3 g/L時檢測結果與理論值相關性好,其散點圖呈直線型(Ⅰ區);3~6.9 g/L時圖形呈快速下降趨勢(Ⅱ區);8.1~30 g/L時其散點圖呈低吸光度平緩趨勢(Ⅲ區)。很直觀地表明采用該法檢測高質量濃度標本時其檢測值不成飽和狀態,反而快速、無規律下降(是形成大小不一的凝塊所致),造成所有結果均存在二元性。即使采用定性方法確定送檢標本為病理性,需進行稀釋測定,但也絕對不知如何稀釋才能確保稀釋標本待測質量濃度在該法檢測線性范圍內,否則檢測結果仍為二元性,說明該法存在重大方法學缺陷。
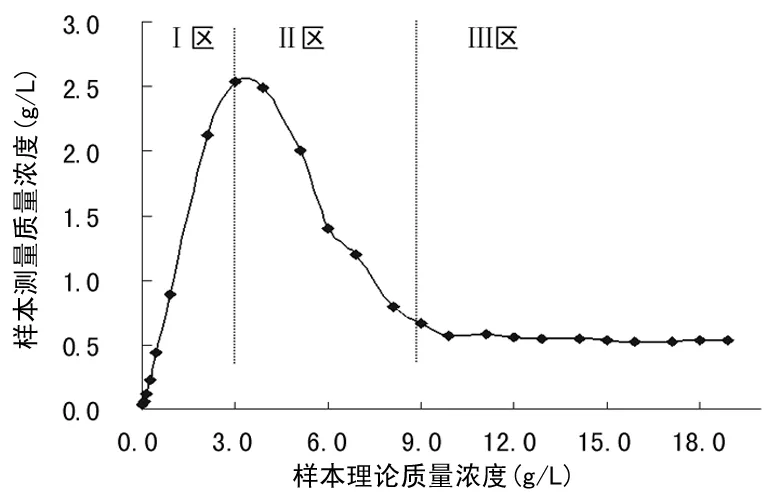
圖1 35份標本檢測值與理論值配對散點圖
通過對35份標本檢測過程進行連續監測,根據圖1的3個不同區域選擇代表性標本繪制檢測反應曲線圖,見圖2。曲線1、2、3總蛋白質量濃度在該法檢測范圍內并逐漸增加,由圖2可見,隨著總蛋白質量濃度增加,測量吸光度亦逐漸增加,對每一個標本而言,在整個反應過程中吸光度是穩定逐漸增加的。曲線4、5、6總蛋白質量濃度大于該法檢測范圍并逐漸增加,但其最大吸光度、測量吸光度、反應速度及反應過程均無固定規律并與曲線1、2、3重疊交叉,說明該法方法學缺陷是無法在全自動生化分析儀上設置參數進行監測與糾正[9-11]。
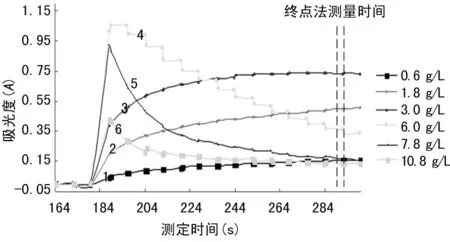
圖2 典型檢測反應曲線圖
綜上所述,采用全自動生化分析儀應用氯化苯丙胺鹽法檢測微量總蛋白會因方法學存在缺陷造成所有測量結果均在其檢測線性范圍之內,需人工對檢測值甄別避免高值誤診,故不宜單獨采用全自動生化分析儀檢測。
[1]唐曉霞.氯化苯丙胺鹽比濁法檢測腦脊液蛋白質方法學評價[J].檢驗醫學與臨床,2013,10(12):1553-1554.
[2]葉應嫵,王毓三,申子瑜.全國臨床檢驗操作規程[M].3版.南京:東南大學出版社,2006:342.
[3]張文英,趙毓祥,沈廣虎.腦脊液蛋白檢測方法學評價[J].國際檢驗醫學雜志,2010,31(11):1334-1335.
[4]陳新寬.伊紅Y染料結合法測定腦脊液蛋白在全自動生化分析儀上的應用[J].檢驗醫學與臨床,2012,9(3):335-336.
[5]胡志斌.兩種腦脊液及尿蛋白定量方法的比較[J].檢驗醫學與臨床,2012,9(10):1251-1252.
[6]殷舟,陳屹一,蔣朱秀,等.腦脊液微量總蛋白檢測體系最低檢出限的非參數評估方案[J].醫學研究雜志,2013,42(7):70-73.
[7]胡盈瑩,胡望平,周長邵,等.尿液與腦脊液總蛋白測定方法研究[J].醫學研究雜志,2007,36(3):56-57.
[8]黃小燕,李宇雄,戴小波.芐索氯銨比濁法測定腦脊液蛋白質的方法學評價[J].檢驗醫學與臨床,2008,5(15):902-903.
[9]徐國賓,蔣琳.臨床生物化學常規定量方法的分析性能評價[J].中華檢驗醫學雜志,2007,30(6):718-720.
[10]羅梅,賀巖,張曉宇.全自動生化分析儀參數設置與應用[J].國際檢驗醫學雜志,2012,33(2):222-223.
[11]肖玉鵬,吳衛平.自動生化分析儀定量測定腦脊液總蛋白[J].檢驗醫學與臨床,2007,4(2):116-117.
10.3969/j.issn.1673-4130.2016.02.063
B
1673-4130(2016)02-0275-03
2015-07-09)

