基于Au納米顆粒/還原氧化石墨烯C-反應蛋白免疫傳感器的研制
張 茜,夏介仁,李德蕾,張坤蕾,白茹燕,胡 蓉,楊云慧
(云南師范大學 化學化工學院,云南 昆明 650500)
基于Au納米顆粒/還原氧化石墨烯C-反應蛋白免疫傳感器的研制
張 茜,夏介仁,李德蕾,張坤蕾,白茹燕,胡 蓉*,楊云慧*
(云南師范大學 化學化工學院,云南 昆明 650500)
采用還原氧化石墨烯-金納米顆粒(RGO-Au NPs)作為免疫傳感器的固定基質,將C-反應蛋白(CRP)抗體固定在玻碳電極表面,用蒽醌二羧酸作為標記物,制成夾心型的CRP免疫傳感器。在最優實驗條件下,通過示差脈沖伏安法對CRP的含量進行檢測。該傳感器在0.25~100 ng/mL范圍內具有良好的線性關系,檢出限為0.08 ng/mL,線性系數為0.997。該傳感器為C-反應蛋白的檢測提供了一種新的手段。
夾心型免疫傳感器;C-反應蛋白(CRP);還原氧化石墨烯;電化學
進入新世紀以來,心血管疾病嚴重危害人類的身體健康。我國心血管疾病的發病率和死亡率逐年增加。近10年來,研究表明C-反應蛋白(C-reactive protein)直接參與各種炎癥和動脈粥樣硬化等心血管疾病的發病機理。該蛋白已成為心血管疾病很重要的預示因子和危險因子[1],與心血管疾病具有很好的相關性[2]。
CRP是由肝細胞合成的一種急性蛋白,當受到炎癥的刺激或細菌感染時,其值會在受刺激4~6 h后開始升高,每隔8 h升高1倍,一般36~50 h達到峰值。隨著炎癥的恢復,CRP值會不斷降低[3]。人體中正常的CRP具有一定的生理作用,可增強機體的免疫能力[4]。以往,由于檢測CRP的方法比較落后,易產生假陰性和假陽性結果,在很大程度上影響了它在臨床上的應用價值,故導致其臨床作用被弱化。近年來,隨著研究的進展,快速、靈敏、簡便、可靠的檢測CRP的方法已被建立,使得CRP在臨床上的應用價值得以提升,其應用領域也大大增加。
一般來說,人體內CRP的正常值小于2.0 mg/L,但當患有急性炎癥時其值會增大至1 000倍以上[5]。CRP水平值的高低可直接用來估測心血管疾病的嚴重程度。美國心臟協會和疾病控制預防中心提出3個級別的CRP濃度:小于1.0 mg/L為低危險;1.0~3.0 mg/L之間為一般危險;大于3.0 mg/L為極度危險[6]。目前,研究發現CRP在臨床上具有很大的應用價值:①CRP在血清中的水平可預測發熱性癌癥病人是細菌感染還是過濾性感染[7]。②C-反應蛋白在血清中的水平可作為心肌梗塞、中風和動脈粥樣硬化的重要預測指示因子[8-9]。③如果CRP在血清中的值升高,患癌癥的風險會增大,C-反應蛋白與非小細胞肺癌具有很好的相關性[10]。
2011年,侯建國等[11]將多壁碳納米管(MCNTs)-硫堇(Thi)-Nafion復合物固定于絲網印刷電極(SPCE)表面作為基底電極,再利用磁性Au@Fe3O4標記C-反應蛋白酶抗體(HRP-anti CRP),并將其吸附到基底電極表面,研發了可再生使用的信號放大的磁性納米修飾CRP電流型免疫傳感器,該傳感器的線性范圍為0.1~110 ng/mL,具有靈敏度高、結果穩定性好、可再生使用等特點。2013年,Bryan等[6]利用金電極制備了一種無標記型電化學生物傳感器用于檢測血液中的CRP,其線性范圍為0.5~50 nmol/L。楊云慧等[12]利用Pd/共價有機骨架材料(COF-LZUll)多孔復合材料將CRP抗體(anti-CRP)固定在玻碳電極表面,構建了一種非標記型C-反應蛋白免疫傳感器。
碳納米材料是一種地球上較普遍而特殊的材料,具有獨特的物理化學性質[13]。1991年,Iijima發現了碳納米管,其直徑在0.7~60 nm之間[14]。隨后,各種碳材料相繼被發現并被應用于不同的領域。石墨烯作為一種碳二維材料,其碳原子的雜化方式為sp2[15],在力學、熱學和電學方面均具有優良的性能,被稱為一種理想的增強體[16]。目前,其制備方法主要有Boride法、Staudemnaier法和Hummer法等[17-18]。2004年,Geim和Novoselov成功地從石墨中分離出石墨烯,證明它可以單獨存在[19]。近年來,石墨烯被廣泛應用于電化學方面的研究[20-22],Ramesh等[23]將石墨烯的氧化物懸浮液負載到玻碳電極(GCE)和金電極的表面,分別形成氧化石墨烯修飾的電極,并用于研究一些典型的氧化還原電對的特性。李燾等[24]將納米石墨烯修飾到電極上,并采用電化學發光法測定了鹽酸氯丙嗪。
本文將氧化石墨烯通過電沉積的方法沉積到玻碳電極上變成還原氧化石墨烯,并負載Au納米顆粒,用蒽醌二羧酸作為標記物,制成夾心型的免疫傳感器,從而實現了CRP的定量檢測。利用還原氧化石墨烯修飾電極,增加了電極的表面積,進一步增加了導電性。本文構建的基于還原氧化石墨烯(RGO)的傳感器具有準確度高、特異性強、靈敏度高、檢測速度快等優點。
1 實驗部分
1.1 試劑與儀器
氯金酸(HAuCl4·4H2O,昆明鉑銳材料有限公司);碳酸鈉、硝酸鈉(天津市大茂化學試劑廠);濃硫酸(云南楊林工業開發區汕滇藥業有限公司);高錳酸鉀、N-羥基琥珀酰亞胺(NHS)、1-乙基-(3-二甲基氨基丙基)碳二亞胺鹽酸鹽(EDC)(麥克林試劑網);尿素(Amresco公司);石墨粉、無水乙醇(天津市風船化學試劑科技有限公司);C-反應蛋白抗體(anti-CRP)、C-反應蛋白(CRP)(上海領潮生物科技有限公司);30%過氧化氫(西隴化工股份有限公司);牛血清蛋白(BSA)、磷酸緩沖溶液(PBS,pH 7.40)(美國Sigma公司);蒽醌二羧酸(QC,梯希愛(上海)化成工業發展有限公司);冰醋酸(成都化學試劑廠);實驗所用試劑均為分析純,所用水為二次蒸餾水。
示差脈沖伏安法(DPV)、電化學交流阻抗(EIS)均用CHI 660D電化學工作站(上海辰華儀器公司)測量;以飽和甘汞電極(SCE)為參比電極,玻碳電極(GCE)為工作電極,鉑電極為輔助電極;JEM2100透射電鏡(日本電子株式會社);TGL16離心機(長沙湘智離心機儀器有限公司);CS501超級恒溫器(重慶實驗設備廠);ST2200HP超聲波清洗器(上海科導超聲儀器有限公司);DZF-6020型真空干燥箱(上海博迅實業有限公司)。
1.2 實驗方法
1.2.1 氧化石墨烯的制備 在圓底燒瓶中分別加入1.5 g NaNO3和30 mL濃硫酸,在磁力攪拌器上攪拌直至完全溶解,隨后加入2 g石墨粉并攪拌均勻,在冰水浴攪拌的條件下緩慢加入9 g KMnO4,在該條件下攪拌2 h后,在室溫下攪拌5 d,然后緩慢加入200 mL 5%的H2SO4,在室溫下攪拌2 h,緩慢加入100 mL 3% 的H2O2,溶液變成亮黃色后在室溫下攪拌2 h,反應完成后將溶液離心并棄去上清液,再用3%的H2SO4和0.5%的H2O2混合溶液洗滌離心3次,最后用水反復洗滌直至溶液呈中性,方可合成氧化石墨烯。
1.2.2 蒽醌二羧酸標記的CRP抗體的制備 將2.0 mg NHS和1.3 mg EDC分散于1 mL H2O中混勻,之后加入1 mL 1 mg/mL QC充分混勻,在振蕩儀上攪拌一夜,離心,分散在PBS中,隨后逐滴加入10 μL 1 mg/mL的CRP抗體,振蕩20 h,在10 000 r/min的條件下離心5 min,棄去上清液后分散于1 mL PBS中,之后加入25 μL 10%的BSA,振蕩30 min,封閉非特異性位點,離心,最后分散于1 mL PBS中備用。
1.3 免疫傳感器的制備
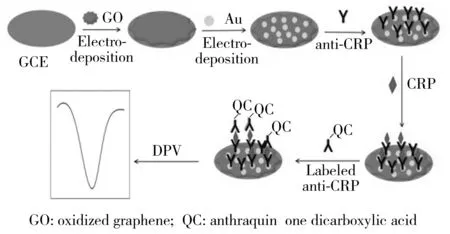
圖1 免疫傳感器的制備流程Fig.1 Stepwise of fabricating immunosensor
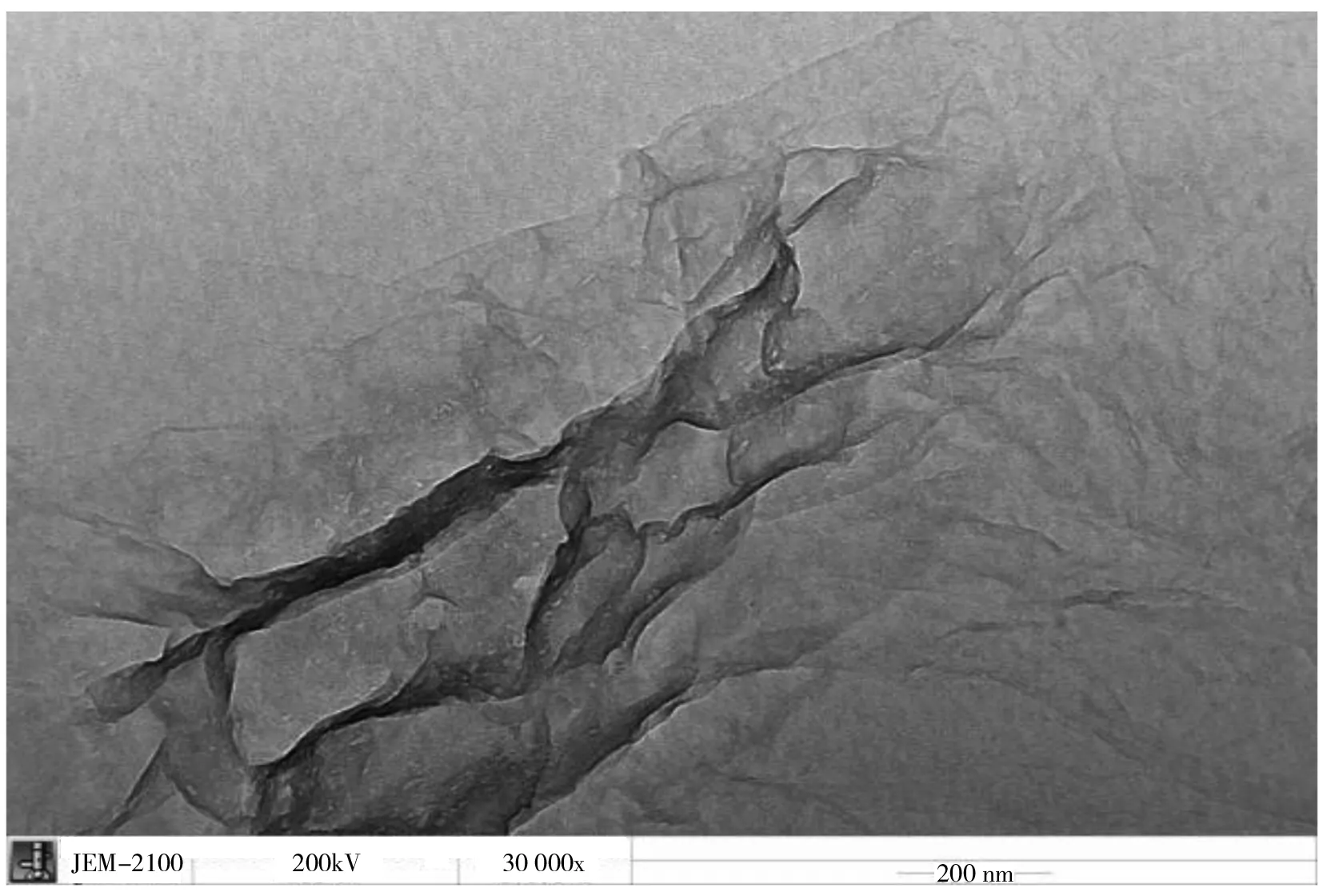
圖2 氧化石墨烯的透射電鏡圖Fig.2 TEM image of GO
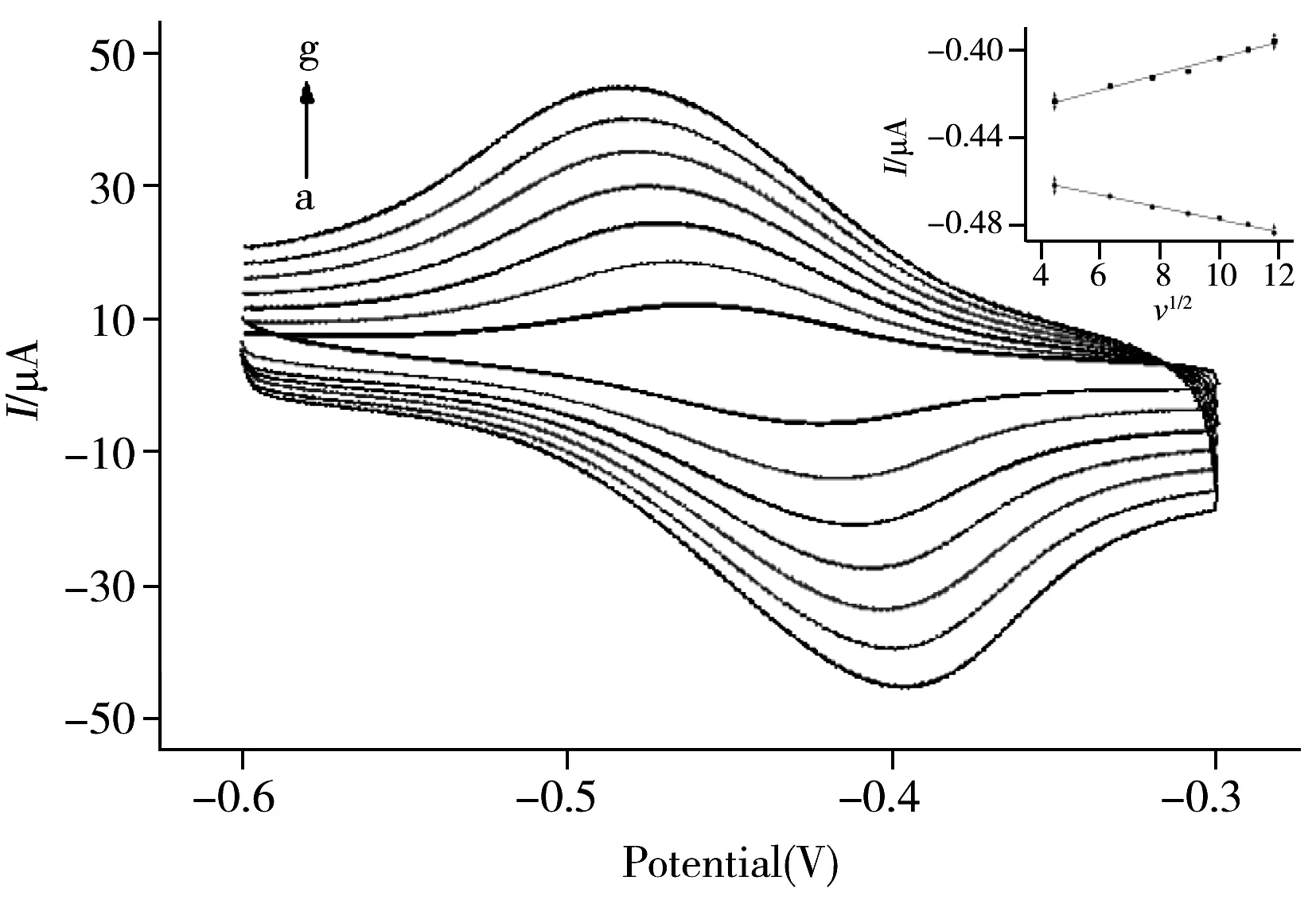
圖3 掃描速度對傳感器響應電流的影響Fig.3 Effect of scan rates on response current of immunosensor scan rate(a-g):20,40,60,80,100,120,140 mV/s; inset:the plot of peak current vs.v1/2
用金相砂紙將玻碳電極(Φ=3 mm)打磨干凈,將電極表面在不同粒徑大小的Al2O3粉末上拋光,再將電極分別用硝酸水溶液(1∶1)、無水乙醇、水各超聲洗滌5 min,自然風干后,將電極放在氧化石墨烯溶液中通過電沉積的方法沉積,在-1.4~1.2 V范圍內采用循環伏安法沉積,電極上得到RGO;取出電極用PBS緩沖液清洗干凈,放入HAuCl4溶液中用同樣的方法,在-0.8~2.0 V范圍內采用循環伏安法沉積上Au納米顆粒。電沉積完成后用PBS溶液沖洗干凈,自然風干,在電極表面滴加CRP抗體10.0 μL,置于冰箱中在4 ℃條件下過夜。將已修飾好CRP抗體的玻碳電極用PBS緩沖液沖洗3次,自然晾干,在電極上滴加10 μL 1%的BSA溶液,將電極放在恒溫箱中(溫度為37 ℃)封閉1 h。封閉好的電極用PBS溶液沖洗3次,自然晾干后,用于CRP的測定。CRP 免疫傳感器的制備流程如圖1所示。
1.4 檢測方法
在該免疫傳感器上滴加不同濃度的CRP抗原,將電極放在恒溫箱中(溫度為37 ℃)培育,培育完之后取出并用PBS沖洗干凈,自然晾干。然后滴加10.0 μL蒽醌二羧酸標記的CRP抗體,置于上述恒溫箱中培育。之后取出并用PBS沖洗干凈,自然晾干。該傳感器作為工作電極,與鉑電極、甘汞電極組成三電極系統,置于pH值為6.5的醋酸緩沖溶液中,通過示差脈沖伏安法(DPV)進行測定,得到DPV曲線,根據傳感器響應電流值與CRP濃度成正比的關系,實現對CRP的定量測定。每次測定完后用4 mol/L尿素洗脫30 min,用PBS緩沖液洗干凈,重復上述實驗過程。
2 結果與討論
2.1 氧化石墨烯的微觀形貌
對合成的氧化石墨烯材料進行透射電鏡(TEM)表征,如圖2所示,可以看出該材料是一種層狀結構,片層中存在褶皺,說明氧化石墨烯的層數很少。表面非常光滑,呈透明的薄片狀。
2.2 氧化還原峰電流與掃描速度的關系

圖4 不同修飾電極界面的交流阻抗行為Fig.4 EIS curves of different modified electrodea:bare GCE;b:RGO/GCE;c:Au/RGO/GCE;d:anti-CRP/BSA/anti-CRP /Au/RGO /GCE;e:CRP/anti-CRP/BSA/anti-CRP/Au/RGO/GCE;f:labeled anti-CRP/CRP/BSA/anti-CRP/Au/RGO/GCE
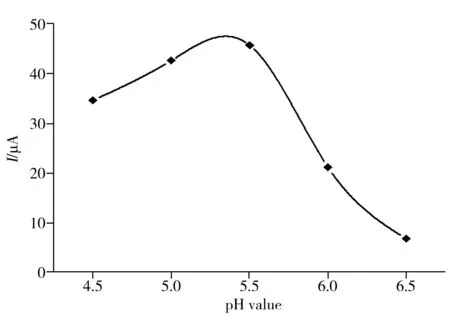
圖5 pH值對免疫傳感器響應電流的影響Fig.5 Effect of pH value on response of CRP immunosensor
為考察QC-labeled anti-CRP/CRP/anti-CRP/RGO/GCE免疫傳感器的電化學行為,實驗考察了掃描速度對氧化還原峰電流的影響,當掃描速度在20~140 mV/s 范圍內變化時,傳感器在HAc-NaAc緩沖溶液(pH 5.5)中的循環伏安曲線如圖3所示。可以看出,氧化峰和還原峰電流隨著掃描速度的增大而增大,且氧化還原峰電流與掃描速度的平方根成正比,說明電流受擴散控制。
2.3 不同修飾電極界面的交流阻抗行為
圖4為不同修飾電極界面在5 mmol/L[Fe(CN)6]3-/4-溶液中的交流阻抗行為。圖中曲線a為裸玻碳電極(GCE)的阻抗曲線,可以看出該電極對電子傳遞幾乎無阻礙作用,只受擴散控制;曲線b為修飾了RGO電極的交流阻抗圖,其電阻值增大,說明RGO成功修飾在電極上;曲線c為Au/RGO修飾電極的交流阻抗圖,電阻值減小,說明金納米顆粒的導電性良好;曲線d為anti-CRP/Au/RGO修飾電極的交流阻抗圖,與曲線c相比其電阻值明顯增大(Rct=1 100 Ω),說明抗體已固定在電極表面,從而阻礙了[Fe(CN)6]3-/4-電子的傳遞作用;曲線e為anti-CRP/Au/RGO修飾的電極在培育了20 ng/mL 的CRP抗原后的交流阻抗曲線,其阻抗明顯增大(Rct=1 800 Ω),說明抗原和抗體間發生了特異性結合,導致阻抗增大,進一步阻礙了[Fe(CN)6]3-/4-電子的傳遞;曲線f為QC labeled anti-CRP/CRP/anti-CRP/RGO/GCE免疫傳感器的阻抗曲線,加了標記的抗體后,標記抗體與抗原進一步特異性結合,使得阻抗值進一步增大(Rct=3 500 Ω),說明電極修飾膜對電子傳遞的阻礙作用增強。
2.4 實驗條件的優化
2.4.1 緩沖溶液pH值對傳感器響應電流的影響 緩沖溶液的pH值會影響蒽醌二羧酸的氧化還原峰電流,從而進一步影響免疫傳感器的靈敏度,本實驗考察了不同pH值的HAc-NaAc緩沖溶液對標記抗體材料中QC的氧化峰電流響應的影響。如圖5所示,當pH值從4.5增至5.5時,氧化峰電流隨之增加,繼續增加pH值時,QC的氧化峰電流反而減小,當pH值為5.5時,免疫傳感器的電流響應值最大。因此實驗選擇pH值為5.5的HAc-NaAc緩沖溶液作為最佳測試底液。
2.4.2 固定抗體濃度對傳感器響應電流的影響 為了考察固定抗體濃度對該免疫傳感器響應電流的影響,本實驗在電極表面固定不同濃度的抗體(5,10,20,30,40,50 μg/mL )制備傳感器并測其電流響應值,結果顯示,響應電流隨著固定抗體濃度的增加而增大,并在固定抗體濃度為20 μg/mL時達到最大值,之后響應電流隨著固定抗體濃度的增加反而減小。因此,本實驗選擇最佳固定抗體濃度20 μg/mL。
2.4.3 抗原培育時間對傳感器響應電流的影響 固定20 μg/mL抗體和20 μg/mL 抗原,改變抗原培育時間,通過測定響應電流值的大小,考察了抗原培育時間對傳感器響應電流的影響。結果顯示,隨著培育時間的延長,響應電流逐漸增大,45 min時達到最大值,之后電流值隨培育時間的增長反而下降。因此選擇最佳的抗原培育時間為45 min。
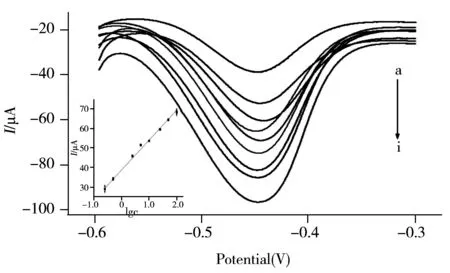
圖6 免疫傳感器對不同濃度CRP的響應曲線Fig.6 DPV response curves of immunosensor incubated with different concentration of CRP CRP concentration(a-h):0.25,0.5,2.5,5.0,10.0,25.0,50.0,100 ng/mL;inset:calibration curve for the CRP immunosensor
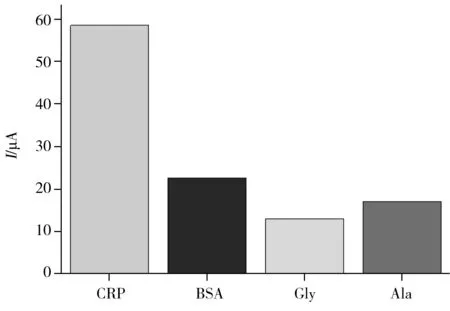
圖7 CRP電化學免疫傳感器的選擇性Fig.7 Selectivity of the CRP electrochemical immunosensor
2.4.4 標記抗體的培育時間對傳感器響應電流的影響 固定20 μg/mL抗體和20 μg/mL抗原,同時保持抗體抗原結合時間不變,改變標記抗體培育時間,測定響應電流值,考察了標記抗體的培育時間對免疫傳感器響應信號的影響。結果顯示,隨著標記抗體培育時間的延長,響應電流先增大后略有減小,在45 min時電流出現峰值。所以實驗選擇45 min為標記抗體的最佳培育時間。
2.5 傳感器的校正曲線
為了獲得該傳感器對不同濃度CRP的響應工作曲線,在最佳實驗條件下,分別培育不同濃度CRP的傳感器,并對其響應電流值進行測定,結果如圖6所示。該傳感器在0.25~100 ng/mL范圍內具有良好的線性響應,其線性方程為I(μA)=15.37lgc+38.69,相關系數為0.997;靈敏度較高,根據3σ規則,其檢出限為0.083 ng/mL。
2.6 免疫傳感器的選擇性
為考察該免疫傳感器的選擇性,本實驗選擇200 ng/mL的甘氨酸(Gly)、1%牛血清蛋白(BSA)和200 ng/mL丙氨酸(Ala)作為干擾物質測定其響應電流值,通過與20 ng/mL CRP的響應電流值作對比來考察傳感器的抗干擾能力。從圖7可看出,相同的實驗條件下甘氨酸、丙氨酸和BSA的響應電流均遠小于CRP的響應電流。說明甘氨酸、丙氨酸和BSA對CRP檢測的干擾較小,進一步說明該傳感器對CRP具有較高的選擇性。
2.7 回收率的測定
為了考察該傳感器可否用于真實樣品中CRP的檢測,采用標準加入法將3種不同濃度的CRP抗原分別加至稀釋的血清樣品中,測定其回收率。由表1可看出,3種加標濃度的回收率在(100±10)%以內,平均回收率為101.5%,且3次測定值的相對標準偏差(RSD)在5%以內,說明該傳感器用于真實樣品中CRP的測定具有一定的可行性。

表1 真實血樣中CRP回收率的測定Table 1 Recoveries of CRP in real human serum
2.8 穩定性的檢測
在相隔12 d后,用該傳感器在相同實驗條件下對CRP進行檢測,響應電流值下降了6.4%;相隔25 d后在相同的實驗條件下檢測CRP,響應電流值下降了7.7%。說明該傳感器的穩定性較好,在真實樣品中CRP含量的檢測方面具有較好的應用價值。
2.9 與其他CRP檢測方法的對比
將本方法與其它檢測CRP的方法進行對比(如表2),本文所制的傳感器具有較高的靈敏度和較低的檢出限。
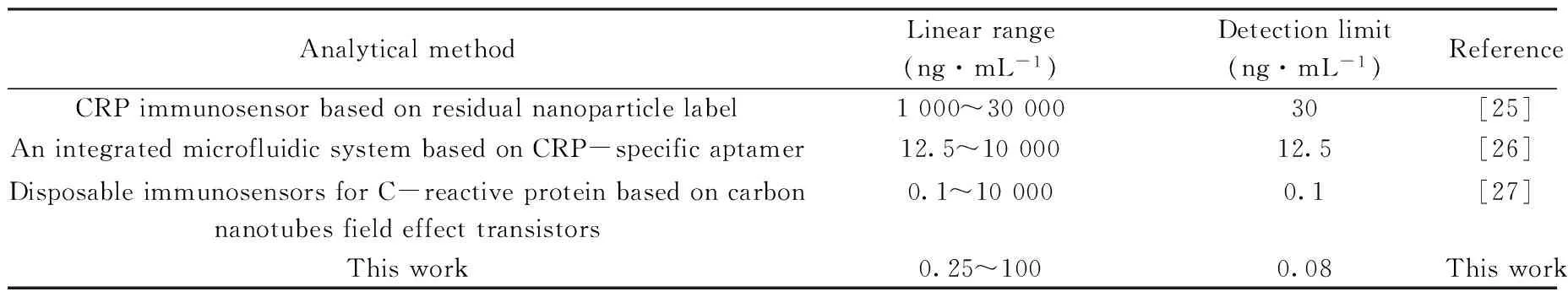
表2 幾種檢測CRP方法的對比Table 2 The comparison of several detection methods of CRP
3 結 論
本文以AuNPs/RGO作為C-反應蛋白抗體的固定基質,采用蒽醌二羧酸標記C-反應蛋白抗體,制成夾心型的免疫傳感器,實現了對CRP的定量檢測。利用還原氧化石墨烯修飾電極,增加了電極的表面積,進一步增強了導電性。該傳感器具有選擇性好、靈敏度高、線性范圍寬、檢出限低等優點,在測定血清樣品中的CRP方面具有較好的應用價值。
[1] Bai S L,Li J J.Chin.J.Caroiol.(白書玲,李建軍.中華心血管病雜志),2004,32(8):765-768.
[2] Yoshida Y,Iwasa H,Kumagai S,Yoshida H,Suzuki T.Arch.Gerontol.Geriatr.,2010,51(2):164-168.
[3] Arinzon Z,Peisakh A,Schrire S,Berner Y.Arch.Gerontol.Geriatr.,2011,53(3):364-369.
[4] Xie L L,Wang X.Prog.Physiol.Sci.(謝良麒,王憲.生理科學進展),2004,35(2):113-118.
[5] Huang C J,Lin H I,Shiesh S C,Lee G B.Biosens.Bioelectron.,2010,25(7):1761-1766.
[6] Bryan T,Luo X,Bueno P R,Davis J J.Biosens.Bioelectron.,2013,39(1):94-98.
[7] Sklavou R,Karavanaki K,Critselis E,Kossiva L,Giannaki M,Tsolia M,Papadakisa V,Papargyria S,Vlachoua A,Karantonisa F,Polychronopouloua S,Gourgiotis D.Clin.Biochem.,2012,45(15):1178-1182.
[8] Zhao Y P,Wang H R,Liu S J,Zhao X H,Chen Y C,Yang Y C,Wang W,Wu Y M,Chen A Q,Tang J M,Yao Y S,Li Y,Chen J F,Shen C,Yang S.Gene,2013,512(1):41-46.
[9] Gupta R K,Periyakaruppan A,Meyyappan M,Koehne J E.Biosens.Bioelectron.,2014,59:112-119.
[10] Aref H,Refaat S.Egypt.J.ChestDiseasesTuberculosis,2014,63(3):717-722.
[11] Hou J G,Cao Y T,Zhou H K,Meng L H,Hu F T,Gan N.Chin.J.Sens.Actuators(侯建國,曹玉廷,周漢坤,孟令花,胡富陶,干寧.傳感技術學報),2011,24(10):1371-1378.
[12] Liu T Z,Xia J R,Li Y,Chen W K,Zhang S,Liu Y,Zheng L,Yang Y H.Chem.J.Chin.Univ.(劉婷知,夏介仁,李瑤,陳文凱,張帥,劉儀,鄭麗,楊云慧.高等學校化學學報),2015,36(10):1880-1887.
[13] Li W Z,Liang C H,Xin Q.Chin.J.Catal.(李文震,梁長海,辛勤.催化學報),2004,25(10):839-843.
[14] Liu Z,Chen X H,Song H H.NewCarbonMater.(劉治,陳曉紅,宋懷河.新型炭材料),2002,17(2):73-76.[15] Lü Q,Yan H X,Liu C.Eng.PlasticsAppl.(呂青,顏紅俠,劉超.工程塑料應用),2016,44(2):140-144.
[16] Hu K,Kulkarni D D,Cho I,Tsukruk V V.Prog.Polym.Sci.,2014,39(11):1934-1972.
[17] Wei H M,Tian Z H.J.Yangtze.Univ.:Nat.Sci.Ed.(魏紅敏,田志宏.長江大學學報:自然科學版),2015,12(5):58-62.
[18] Xiao S J,Yu S W,Tan X Y.Chem.World(肖淑娟,于守武,譚小耀.化學世界),2015,56(6):378-382.
[19] Zhou C,Chen S H,Lou J Z.Mater.Rev.(周超,陳思浩,樓建中.材料導報),2014,28(1):15-20.
[20] Zhuang Q F,Wang Y,Ni Y N.ChemJ.Chin.Univ.(莊欠粉,王勇,倪永年.高等學校化學學報),2015,36(9):1674-1680.
[21] Feng Y J,Wei Y P,Zhao X H,Fu X W,Huang L L,Yang H,Yang Y H.Chem.Res.Appl.(馮亞娟,魏玉萍,趙曉慧,符雪文,黃亮亮,楊華,楊云慧.化學研究與應用),2011,23(4):444-450.
[22] Li H M,Zhang H Y,Lai X W,Liang L,Liu K P,Gou X J.J.Instrum.Anal.(李惠茗,張惠怡,賴祥文,梁立,劉坤平,茍小軍.分析測試學報),2016,35(3):292-298.
[23] Ramesh P,Bhagyalakshmi S,Sampath S.J.ColloidInterfaceSci.,2004,274(1):95-102.
[24] Li T,Tan X C,Hu Q,Wu J W,Fang X X,Liu S G,Yu H C,Huang Z Y.J.Instrum.Anal.(李燾,譚學才,胡琪,吳佳雯,方曉雪,劉紹剛,余會成,黃在銀.分析測試學報),2014,33(2):212-216.
[25] Huttunen R J,N?reoja T,Mariani L,H?rm? H.Biosens.Bioelectron.,2016,83:54-59.
[26] Lee W B,Chen Y H,Lin H I,Shiesh S C,Lee G B.Sens.ActuatorsB,2011,157(2):710-721.
[27] Justino C I,Freitas A C,Amaral J P,Rocha-Santos T A,Cardoso S,Duarte A C.Talanta,2013,108:165-170.
Development of a C-Reactive Protein Immunosensor Based on Au Nanoparticles/Reduced Graphene Oxide
ZHANG Xi,XIA Jie-ren,LI De-lei,ZHANG Kun-lei,BAI Ru-yan,HU Rong*,YANG Yun-hui*
(College of Chemistry and Chemical Engineering,Yunnan Normal University,Kunming 650500,China)
In this paper,Au nanoparticles(Au NPs)/reduced graphene oxide(RGO) was used as the matrix of immunosensor to immobilize c-reactive protein(CRP) antibody on the surface of glassy carbon electrode.A sandwich immunosensor was constructed using quinone dicarboxylic acid as tag.Under the optimal experiment conditions,the concentration of CRP was detected by differential pulse voltammetry.The linear range is 0.25-100 ng/mL with a detection limit of 0.08 ng/mL and a correlation coefficient of 0.997.This immunosensor provides a new simple means for the determination of c-reactive protein.
sandwich immunosensor;c-reactive protein(CRP);reduced graphene oxide;electrochemistry
10.3969/j.issn.1004-4957.2017.03.009
2016-09-12;
2016-11-10
國家自然科學基金項目(21465026,21165023)
O657.1;O629.73
A
1004-4957(2017)03-0349-06
*通訊作者:楊云慧,博士,教授,研究方向:電分析化學與生物傳感器,Tel:0871-65941086,E-mail:yyhui2002@aliyun.com 胡 蓉,博士,講師,研究方向:生物傳感器,Tel:0871-65941086,E-mail:hudierong_168@163.com

