正極材料LiFePO4液相法合成中反應液循環研究
馬君君,祖雪敏,王興堯
(天津大學理學院,天津 300072)
LiFePO4由于其具有礦藏豐富、價格便宜、無毒、環境友好、較高的比容量(理論比容量170 mAh/g)和較高的工作電壓(3.4 V,以金屬鋰為負極)、充放電壓平緩、循環壽命長、安全性能好等優點,LiFePO4材料有望成為下一代鋰離子電池的主導正極材料[1-2]。目前LiFePO4材料常見的合成方法有高溫固相法、共沉淀法、溶膠凝膠法、液相法、水熱法等[3-9]。目前制備LiFePO4材料最常用、最成熟的方法是高溫固相法,此方法雖合成設備和工藝簡單,制備條件易控制,適合工業生產,但是反應需要很高的溫度,原料不易混合均勻,制備的產物顆粒較大,能源消耗大。水熱法可以在較低的溫度下反應,制備出單一物相,晶粒小,不過此方法僅限于少量粉體制備,若大規模生產,耐高溫耐高壓的反應釜設計很困難,造價也高。綜合考慮,利用液相方法可以實現低溫條件下合成材料,也很好控制合成中的樣品顆粒尺寸,制得的LiFePO4具有活性大、粒度小、分布均勻等優點,且液相法的工藝比較簡單,比較適合大批量生產。由于LiFePO4對合成過程中環境氣氛的要求較高,因而利用液相方法制LiFePO4的研究并不多見。如果用液相法制備LiFePO4,反應中需要大量水和乙醇,這2種液體使用后,直接排放會污染環境且浪費資源。液相法合成LiFePO4要實現工業化生產,不僅要考慮產品質量問題,還要考慮生產成本和環境污染問題。因此本課題探究了反應液循環使用對液相法合成的正極材料LiFePO4的影響,期望解決液相合成中資源浪費問題。
1 實驗方法
1.1 試劑與儀器
無水醋酸鋰(分析純);無水乙醇(分析純);乙炔黑(電池級):天津江天化工技術有限公司;N-甲基吡咯烷酮(分析純):天津市大茂化學試劑;聚偏氟乙烯(PVDF,電池級):美國蘇威。熱恒溫水浴鍋(HHS-112,江蘇常熟醫療器械廠);手套箱[Lab2000,伊特克斯惰性氣體系統(北京)有限公司]。
1.2 材料的制備
1.2.1磷酸鐵FePO4·xH2O制備
按n(Fe)∶n(P)=1∶1稱取FeSO4·7H2O和NH4H2PO4,將其分別溶于去離子水中配制成1 mol/L的溶液。在攪拌條件下將NH4H2PO4溶液加入到FeSO4溶液中,然后加入H2O2[n(Fe)∶n(H2O2)=1∶1.1]溶液立即有乳白色沉淀生成。再用NH3·H2O(1∶1)調pH=2.5,制備前驅體FePO4·xH2O。按照此方法制備前驅體FePO4·xH2O,第1次分離出的產品FePO4·xH2O記作#A,濾液不做任何處理,直接再次用于配制1 mol/L的品FePO4·xH2O記作#B,如此反復循環,直至分離出第5次產品FePO4·xH2O,分別記作#C、#D、#E。
1.2.2磷酸鐵鋰LiFePO4制備
按n(Fe)∶n(Li)=1.0∶1.2稱取前驅體磷酸鐵FePO4·xH2O和無水CH3COOLi置于圓底燒瓶中,加入適量的無水乙醇溶液,攪拌混合均勻后放入60 ℃水浴中,再加入還原劑n(FePO4·xH2O)∶n[還原劑(自制)]=1.0∶0.6,持續攪拌反應5 h后,靜置2 h后抽濾。60 ℃烘干后,將制備出的LiFePO4放入管式爐中,在氬氣保護下,600 ℃煅燒2 h。按照溶劑乙醇1次使用和2次使用,所得樣品LiFePO4編號為#1和#2。
1.3 材料表征
材料表征方法和所用儀器如下:X射線衍射(X-ray diffraction,XRD),日本理學Rigaku D/max2500v/pc;采用日本日立公司S4800型掃描電子顯微鏡,加速電壓:0.5~30.0 kV,最小步進:0.1 kV。
1.4 模擬電池的制備以及電化學性能測試
按質量比8∶1∶1用JJ500型電子分析天平稱取活性物質LiFePO4、導電劑乙炔黑、黏結劑聚偏氟乙烯(PVDF),加入溶劑N-甲基吡咯烷酮(NMP)后,超聲攪拌混合均勻,得到糊狀的正極漿。用刮刀流延法將其涂覆在正極集流體鋁箔上。常壓80 ℃烘干后沖切成直徑為14 mm的小圓片,再放入真空干燥箱內120 ℃干燥12 h,稱質量。
采用CR2032型扣式電池,負極為金屬鋰片,電解液為1 mol·L-1的LiPF6/EC+DEC+EMC(體積比為1∶1∶1)溶液,隔膜為聚丙稀膜(Celgard2400),電池的整個裝配過程是在充滿氬氣的手套箱中進行。采用武漢CT-2001ALand測試系統進行恒流充放電測試,充放電電壓范圍為2.5~4.2 V。
2 結果與討論
2.1 反應液循環對FePO4·xH2O的影響
2.1.1前驅體FePO4·xH2O的XRD圖
圖1所示為反應液循環使用不同次數所制備FePO4·xH2O經過650 ℃氬氣氛圍下煅燒2 h后的XRD圖。
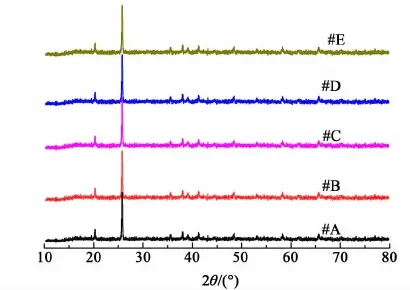
圖1 FePO4·xH2O的XRD圖Fig.1 XRD patterns of FePO4·xH2O
從圖1中可以看出:每一個樣品的主要衍射峰峰形尖銳且強度高,峰位相同,與純相FePO4(JCPDS29-715)譜圖一致,無雜質相存在,說明制備出的FePO4·xH2O樣品結晶好,純度較高,反應液5次循環使用對制備FePO4·xH2O的結構無影響。
2.1.2FePO4·xH2O的SEM圖
圖2為制備FePO4·xH2O的SEM圖。

圖2 制備FePO4·xH2O的SEM圖Fig.2 SEM images of FePO4·xH2O
由圖2可知:循環制備出FePO4·xH2O樣品形貌規則,均為球形,表面光滑,顆粒粒徑較均勻,均有少量二次粒子的形成,第5個樣品與第1個樣品相比,形貌沒有太大差別。
2.2 反應液循環對合成的LiFePO4樣品的影響
2.2.1結構分析
圖3為合成的LiFePO4的XRD圖。
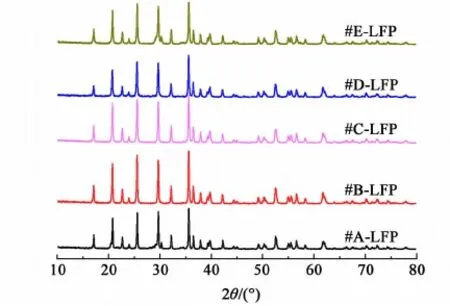
圖3 合成的LiFePO4的XRD圖Fig.3 XRD patterns of LiFePO4 synthesized
由圖3可知:這5個樣品的衍射峰半峰寬都很小,峰形尖銳,與標準卡片JCPDS No.40-1499對比,樣品均屬單一晶相的橄欖石型LiFePO4,均未發現有其他雜質(Li3PO4等[8])存在。說明合成產物LiFePO4均為純相,反應液循環對其橄欖石型結構無影響。
2.2.2形貌分析
圖4為合成的LiFePO4的SEM圖。

圖4 合成的LiFePO4的SEM圖Fig.4 SEM images of LiFePO4 synthesized
由圖4可知:樣品均為球形或類球形,顆粒大小均勻。與圖2比較可以發現:用前驅體FePO4·xH2O制備的LiFePO4保持了前驅體的形貌,只是顆粒的粒徑略有變化。說明反應液循環對制備的LiFePO4樣品形貌幾乎無影響。
2.2.3能譜分析
圖5和表1分別是反應液循環5次使用后制備的LiFePO4能譜分析圖和組分表。
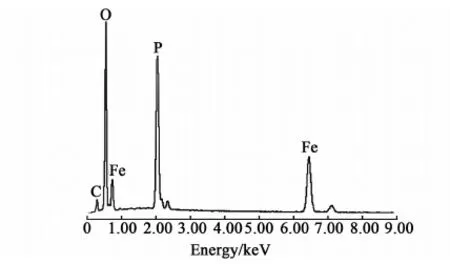
圖5 LiFePO4樣品的能譜圖Fig.5 EDS spectra of LiFePO4 samples

元素COPFe總量LiFePO4940335621803524100
可以看出合成的材料LiFePO4樣品中只含有C、O、P和Fe(考慮到能譜分析法并不能檢測出Li元素的含量),無其他元素的雜質。其中C元素來源于LiFePO4樣品掃描所用的導電材料。
2.3 乙醇循環對樣品LiFePO4的影響
2.3.1乙醇循環制得LiFePO4樣品的XRD
圖6為合成的LiFePO4的XRD圖。
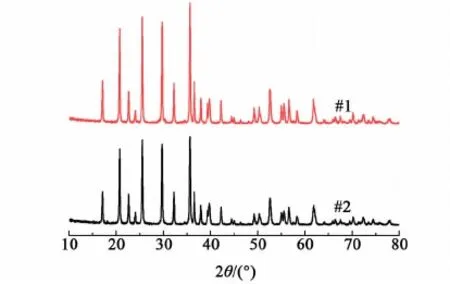
圖6 合成的LiFePO4的XRD圖Fig.6 XRD patterns of LiFePO4 synthesized
由圖6可知:#1、#2這2個樣品主要衍射峰形尖銳,強度高,與標準卡片(JCPDS No.40-1499)對比,樣品均屬橄欖石型LiFePO4,且2個樣品均未發現有其他雜質存在。說明合成LiFePO4樣品結晶度好,純度高。另外在合成的過程中,乙醇第1次和第2次循環使用對合成LiFePO4樣品結構幾乎無影響。
2.3.2LiFePO4的SEM圖
圖7給出了合成的LiFePO4的SEM圖。
由圖7圖可知:2個LiFePO4樣品均是類球形,顆粒均勻,分散性好,且2樣品形貌無明顯差別,說明乙醇的循環使用對LiFePO4樣品形貌無影響,這可能因為LiFePO4樣品的形貌主要取決于前驅體FePO4·xH2O的形貌。
2.4 電化學性能測試
2.4.1反應液循環合成LiFePO4的電化學性能
圖8給出反應液循環合成的LiFePO4的電化學性能。
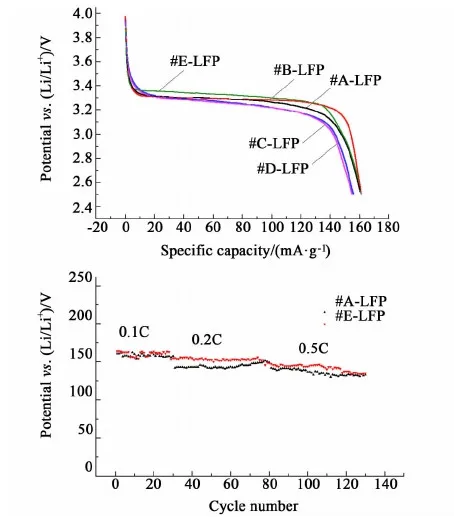
圖8 反應液循環合成的LiFePO4的電化學性能Fig.8 Electrochemical properties of LiFePO4 samples synthesized with reaction liquid circulation
由圖8可知:反應液循環使用制備的FePO4·xH2O為前驅體合成的5個LiFePO4樣品電化學性能。從圖8可以看出,樣品以0.1 C倍率進行恒流放電,各個樣品放電曲線都有非常平緩的電壓平臺,放電電壓平臺在3.35 V左右,對應于LiFePO4正極材料放電中鋰離子的嵌入與脫出,也就是LiFePO4和FePO4兩相間的轉化。反應如下:
LiFePO4→FePO4+Li++e-(1)
第1次到第5次樣品的首次放電比容量分別為161.1、161.2、156、155和160.3 mAh·g-1,第5次和第1次的首次放電比容量基本相等,而第3次和第4次稍有下降。
第1次和第5次反應液循環下合成的LiFePO4在不同倍率下的循環性能圖,第1次循環時合成的LiFePO4在0.1 C、0.2 C和0.5 C倍率下首次放電比容量依次為161.1、144.6和142.1 mAh·g-1。其中0.1 C倍率下循環30圈后,容量保持率為97.76%。第5次循環時合成的LiFePO4在0.1 C,0.2 C,0.5 C倍率下首次放電比容量依次為160.3、153.8和146 mAh·g-1。0.1 C倍率下循環30圈后,容量保持率為96.69%。上述電化學性能表明,5次反應液循環下制備的LiFePO4正極材料具有較高的充放比容量及優良的循環性能。
2.4.2乙醇循環合成的LiFePO4電化學性能
圖9為乙醇循環合成的LiFePO4的電化學性能。
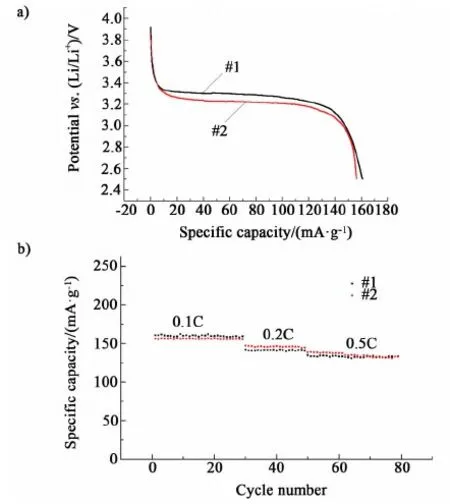
圖9 乙醇循環合成的LiFePO4的電化學性能Fig.9 Electrochemical properties of synthesized LiFePO4 samples synthesized with ethanol circulation
由圖9可知:乙醇循環合成的LiFePO4樣品的電化學性能,0.1 C倍率下的首次放電曲線都有平緩的電壓平臺,放電電壓平臺在3.35 V左右。#1樣品首次放電比容量為160.8 mAh·g-1,#2樣品首次放電比容量為156.3 mAh·g-1,兩者首次放電比容量差別不大。
乙醇循環合成的LiFePO4在不同倍率下的循環性能圖,#1樣品0.1 C,0.2 C,0.5 C倍率下首次放電比容量依次為160.8、142.1和134.9 mAh·g-1。其中0.1 C倍率下循環30后容量保持率為99.20%。#2樣品0.1 C、0.2 C和0.5 C倍率下首次放電比容量依次為156.3、147.1和138.5 mAh·g-1。其中0.1 C倍率下循環30圈后容量保持率為99.49%。上述電化學性能表明,2次乙醇循環下制備的LiFePO4正極材料具有良好的電化學性能。
3 結論
研究了磷酸鐵鋰液相法制備中反應液循環。反應液不經過任何處理循環使用5次制備FePO4·xH2O,經表征表明反應液5次循環使用對前驅體FePO4·xH2O結構、形貌及電化學性能影響不大。第5次時制備出的LiFePO4樣品和第1次制備出的LiFePO4樣品相比,首次放電比容量差別不大,分別為160.3和161.1 mAh·g-1。
乙醇經過蒸餾處理后可以循環使用,對制備的LiFePO4樣品結構及形貌影響不大。首次使用和循環使用制備的LiFePO4樣品首次放電比容量分別為160.8和156.3 mAh·g-1。反應液循環使用的研究成果有望促進鋰離子電池正極材料LiFePO4液相法大規模生產。
參考文獻:
[1]Padhi A K, Naanjundaswamy K S, Masquelier C,etal. Phospho-Olivines as positive-electrode materials for rechargeable lithium batteries[J]. Journal of the Electrochemical Society, 1997, 144: 1 188-1 194
[2]Yang J, Kang X, Hu L,etal. Synthesis and electrochemical performance of Li2FeSiO4/C/carbon nanosphere composite cathode materials for lithium ion batteries[J]. Journal of Alloys and Compounds, 2013, 572: 158-162
[3]Gim J, Song J, Nguyen D,etal. A two-step solid state synthesis of LiFePO4/C cathode with varying carbon Contents for Li-ion batteries[J]. Ceramics International, 2014, 40:1 561-1 567
[4]Zhang Y, Feng H, Wu X,etal. One-Step microwave synthesis and characterization of carbon-modified nanocrystalline LiFePO4[J]. Electrochimica Acta, 2009, 54: 3 206-3 210
[5]Devaraju M K, Honma I. Hydrothermal and solvothermal process towards development of LiMPO4(M=Fe, Mn) nanomaterials for lithium-ion batteries[J]. Advanced Energy Material, 2012, 2: 284-297
[6]Ogihara T, Kodera T, Myoujin K,etal. Preparation and electrochemical properties of cathode materials for lithium ion battery by aerosol process [J]. Materials Science and Engineering B, 2009, 161: 109-114
[7]Miao C, Bai P, Jiang Q,etal. A novel synthesis and characterization of LiFePO4and LiFePO4/C as a cathode material for lithium-ion battery[J]. Journal of Power Sources, 2014, 246: 232-238
[8]Aimable A, Aymes D, Bernard F,etal. Characteristics of LiFePO4obtained through a one step continuous hydrothermal synthesis process working in supercritical water[J]. Solid State Ionics, 2009, 180: 861-866
[9]Arnold G, Garche J, Hemmer R,etal. Fine-Particle lithium iron phosphate LiFePO4, synthesized by a new low-cost aqueous precipitation technique[J]. Journal of Power Sources, 2003, 119(6): 247-251
[10]Xu G, Zhong K, Zhang J,etal. First-Principles investigation of the electronic and Li-ion diffusion properties of LiFePO4by sulfur surface modification [J]. Journal of Applied Physics, 2014, 116: 63 703-63 708
[11]Qiao Y, Pan L, Jia P,etal. Effect of magnetic treatment on microstructure and cycle performance of LiFePO4/C cathode material[J]. Materials Letters, 2014, 137:432-434
[12]Zhong S, Wu L, Zheng J,etal. Preparation of high tap-density 9LiFePO4·Li3V2(PO4)3/C composite cathode material by spray drying and post-calcining method[J]. Powder Technology, 2012, 219:45-48
[13]Xu G, Li F, Tao Z,etal. Monodispersed LiFePO4@C core-shell nanostructures for a high power Li-ion battery cathode[J]. Journal of Power Sources, 2014, 246: 696-702
[14]Zhong K, Cui Y, Xia X,etal. Study on the stability of the LiFePO4Li-ion battery via an electrochemical method[J]. Journal of Power Sources, 2014, 250: 296-305
[15]Wang Q, Deng S, Wang H,etal. Hydrothermal synthesis of hierarchical LiFePO4microspheres for lithium ion battery[J]. Journal of Alloys and Compounds, 2013, 553: 69-74

