抗人PD-L1單克隆抗體的制備及其應用①
馮沛然 黃建芳 王敏珍 廖偉聰 郝代玲 向軍儉
(暨南大學抗體工程研究中心,廣東省分子免疫與抗體工程重點實驗室,廣州510632)
抗人PD-L1單克隆抗體的制備及其應用①
馮沛然 黃建芳 王敏珍②廖偉聰 郝代玲 向軍儉
(暨南大學抗體工程研究中心,廣東省分子免疫與抗體工程重點實驗室,廣州510632)
目的:獲得能應用于臨床診斷以及阻斷PD-L1與PD-1結合的抗人PD-L1單克隆抗體。方法:采用重組表達的人PD-L1蛋白免疫BALB/c小鼠,通過雜交瘤細胞融合技術獲得穩定分泌抗人PD-L1單抗的陽性細胞株,ELISA方法鑒定抗體的特異性、親和力、亞型等方面特性;免疫印跡、間接免疫熒光方法對腫瘤細胞進行檢測;腫瘤殺傷實驗驗證抗體阻斷活性。結果:共獲得2株抗人PD-L1單抗,抗體效價分別為1∶2.56×106和1∶3×105,親和力分別為1.5×109L/mol和2.5×108L/mol,均與PD-L2蛋白無交叉反應。免疫印跡、間接免疫熒光證實抗體有診斷作用。殺傷實驗顯示抗體有阻斷作用。結論:共獲得兩株穩定分泌高效價、高特異性的抗人PD-L1單抗的雜交瘤細胞株,能作為診斷抗體應用于腫瘤表型檢測和預后有效性的評估。抗體的阻斷功能可應用于聯合CIK細胞免疫治療。
PD-L1;單克隆抗體;流式細胞術;CIK細胞;腫瘤診斷
程序性細胞死亡配體(Programmed cell death ligand-1,PD-L1)也稱B7-H1、CD274,主要表達于活化的T細胞、B 細胞、巨噬細胞、樹突狀細胞表面。PD-L1與表達于活化T細胞表面的PD-1結合后可向T細胞傳遞抑制信號,抑制T細胞的功能。在腫瘤抗機體免疫中,腫瘤組織異常高表達PD-L1,通過與PD-1結合抑制CTL對其的殺傷,PD-1/PD-L1通路與免疫細胞的抗腫瘤免疫應答息息相關。Francisco等[1]發現Treg細胞表面高表達PD-1分子,其通過PD-1/PD-L1執行其免疫調節作用。當PD-1與APC細胞上的PD-L1結合后可抑制CD8+T細胞的活化,促進CD4+T細胞的活化,從而對免疫系統進行負調節。Dong等[2]制備出抗人B7-H1的單克隆抗體,通過流式免疫熒光標記方法檢測B7-H1主要高表達于腫瘤細胞而非正常組織,并通過體內和體外實驗均發現腫瘤相關的B7-H1的表達能增加CTL細胞的凋亡,而阻斷PD-1/PD-L1通路恢復CTL對腫瘤細胞的殺傷能力。Castella等[3]在多發性骨髓瘤患者(MM)骨髓中的Vγ9Vδ2-T細胞中發現其PD-1異常高表達,首次報道PD-1在腫瘤區域中Vγ9Vδ2-T細胞中的表達,并發現MM患者BM中Vγ9Vδ2-T細胞經過PD-1治療后增長率提高了2倍,細胞毒性提高了5倍。Khan等[4]還發現高表達PD-L1的B細胞能抑制B細胞的體液免疫功能。早在2002年已經報道了PD-L1能協助腫瘤進行免疫逃逸,接下來的報道逐漸證明阻斷PD-1/PD-L1通路能增強T細胞的抗腫瘤免疫應答能力[5-7]。臨床的研究表明PD-L1的表達與疾病進行以及預后效果息息相關。因此,運用抗PD-1或抗PD-L1的單克隆抗體將PD-1/PD-L1信號通路阻斷成為一種新的免疫治療手段[8]。免疫檢查點抑制療法在臨床上如火如荼地進行著,最熱門的PD-1/PD-L1抗體免疫治療占據免疫檢查點治療20%的比例。2016年5月18日,羅氏PD-L1藥物Atezolizumab獲得FDA批準,用于膀胱癌適用癥,成為第一個上市的PD-L1藥物;2017年3月23日,FDA批準默克/輝瑞旗下的Avelumab上市,成為第二個上市的PD-L1藥物。目前還在臨床試驗的還有BMS-936559、MEDI4736、MPDL3280A等抗體,PD-L1抗體藥物的發展前景十分廣闊。
本研究旨在通過雜交瘤細胞融合技術篩選出能分泌高特異性、高親和力的抗人PD-L1單克隆抗體細胞株,結合流式細胞術驗證抗體與腫瘤細胞表面的結合能力,用腫瘤殺傷實驗驗證抗體的阻斷功能,為后續檢測抗體以及抗體藥物的研發奠定基礎。
1 材料與方法
1.1材料
1.1.1主要試劑 人PD-L1重組蛋白(novop-rotein,Catalog# C315);抗人PD-L1標準抗體(R&D,Catalog# MAB1561);Freund完全佐劑、Freund不完全佐劑、BCA protein assay kit購自Pierce公司,PRMI1640 培養基、胎牛血清、HAT、HT均為Gibco公司產品;SBA Clonotyping System-HRP(Southern-Biotech,5300-05);質粒提取試劑盒、膠回收試劑盒均購自Magen公司;APC-PD-L1、Alexa Flour 647 Goat anti-mouse IgG購自Biolegend;CytoTox 96? Non-Radioactive Cytotoxicity Assay試劑盒(Promega,Catalog# G1780);酶標二抗(KPL,Catalog #074-1806)。
1.1.2實驗材料 無特定病原體(Specific pathogen free,SPF)級BALB/c純系雌性小鼠,鼠齡6~8周,購自南方醫科大學動物中心。Sp2/0小鼠骨髓瘤細胞、Caov3、H1299、OV2008、C13、A549、A549/DDP、MCF-7等腫瘤細胞株為暨南大學抗體工程中心實驗室傳代保存;正常人血清采集于健康志愿者。
1.2實驗方法
1.2.1PD-L1 mAb的制備 采用購買的人PD-L1重組蛋白為免疫原,取6周齡的BALB/c雌鼠,皮下多點免疫方法,免疫劑量為50 μg/只。采用常規細胞融合及篩選方法[9],最終篩選出4株陽性細胞株,采用小鼠體內誘生法制備腹水型抗體;Protein G親和層析柱進行純化后備用。
1.2.2PD-L1 mAb Ig類及亞類的鑒定 采用SBA Clonotyping System-HRP試劑盒對篩選的抗體Ig類及亞類進行測定,所有操作嚴格依照試劑盒說明書操作。
1.2.3PD-L1 mAb抗體親和常數的測定 非競爭酶免疫實驗測定其親和常數(Affinity constant),Ka值。參考Raghava等[10]的方法,按照公式Ka=(n-1)/2(n[Ab′]t-[Ab]t)計算親和常數Ka值。
1.2.4PD-L1 mAb抗體特異性的鑒定 將人PD-L2蛋白稀釋為1 μg/ml,每孔100 μl加入酶標板中,4℃孵育過夜。用含0.05%吐溫的PBST洗滌3次,每次3 min,再用5%的脫脂奶粉于37℃封閉1 h,PBST洗滌3次,每次3 min。將純化后抗體從1∶1 000開始進行倍比稀釋。每孔加入100 μl,37℃孵育1 h。PBST洗滌3 次,每次3 min,再加入8 000倍稀釋的HRP標記的羊抗鼠酶標二抗100 μl,37℃孵育40 min。PBST 洗滌5次,加入TMB單組分顯色液,室溫避光反應10 min后加入50 μl濃硫酸終止液終止反應,酶標儀讀取OD450值,進行結果分析。
1.2.5PD-L1抗體在Western blot檢測上的應用 裂解腫瘤細胞,提取總蛋白[11],經SDS-PAGE電泳后將蛋白轉到PVDF膜上,5%脫脂奶粉封閉膜后加入稀釋的PD-L1純化抗體(1∶2 000),4℃反應過夜后取出膜PBST洗滌3次,加入HRP酶標二抗(1∶8 000)室溫反應1 h,洗滌5次,加入化學發光液反應,在凝膠成像儀成像。
1.2.6PD-L1抗體在流式檢測腫瘤細胞PD-L1表型上的應用 離心收集細胞,用PBS洗滌,用制備的抗體(10 μg/ml)與腫瘤細胞室溫孵育15 min,預冷PBS洗滌1次后加入Alexa Flour 647 Goat anti-mouse IgG室溫避光反應15 min,預冷PBS洗滌1次后用300 μl PBS重懸細胞,上流式細胞儀檢測[12]。
1.2.7PD-L1單抗阻斷功能驗證 CIK(Cytokine-induced killer)是體外培養獲得的一群以CD3+CD56+細胞為主要效應細胞的異質細胞群[13],其既具有T淋巴細胞強大的抗腫瘤活性,又具有NK細胞(自然殺傷細胞)的非MHC(主要組織相容性抗原)限制性腫瘤殺傷能力,是目前臨床上廣泛使用的過繼性免疫治療細胞。然而,CIK在腫瘤殺傷過程中,受到PD-1/PD-L1信號的限制,在高表達PD-L1的腫瘤殺傷中效果不佳,因此,阻斷PD-1/PD-L1通路是增強CIK免疫治療的有力措施。
從外周血中分離PBMC細胞,第0天加入1 000 U/ml IFN-γ 37℃,5%CO2培養;24 h后加入50 ng/ml 的CD3單克隆抗體和300 U/ml的重組人IL-2,刺激CIK細胞的生長和增殖[14];每3 d半量換液或擴瓶一次,并補加重組人IL-2 300 U/ml;在培養的第14天,收獲CIK細胞。用anti-TCR抗體刺激CIK細胞,每隔6 h收集細胞檢測其PD-1表達情況。另外,用CIK細胞與腫瘤細胞A549/DDP以40∶1、20∶1、10∶1、5∶1比例混合,并加入PD-L1抗體10 μg/ml,37℃ 5%CO2培養4~6 h,用CytoTox96? Non-Radioactive Cytotoxicity Assay試劑盒檢測各組釋放LDH的量,通過公式:%Cytotoxicity=(LDHexperimental-LDHeffector cells-LDHspontaneous)/(LDHmaximal-LDHspontaneous)×100%,計算CIK細胞的腫瘤殺傷率[15]。
1.3統計學分析 采用Graph Pad Prism 5.0軟件進行作圖,并分析不同數據間統計學差異。運用SPSS軟件對不同組數據之間進行統計學分析。
2 結果
2.1抗人PD-L1蛋白單克隆抗體的制備 用購買的重組人PD-L1蛋白免疫BALB/c小鼠3次,按常規方法進行細胞融合,通過3次陽性克隆,獲得4株穩定分泌抗人PD-L1單抗的雜交瘤細胞株,分別命名為Ab1、Ab2、Ab3、Ab4。制備大量的腹水型抗體后,通過親和純化,用還原性SDS-PAGE分析。結果顯示,抗體重鏈和輕鏈條帶Mr分別在50 bp和25 bp 左右(圖1),無明顯雜帶,抗體純化效果較好,可用于后續實驗。
2.2抗人PD-L1抗體Ig 亞型、腹水效價及特異性鑒定 用SBA小鼠mAb分型試劑盒測定純化的4種單克隆抗體Ig類及其亞類。結果顯示Ab3為IgG2b,其余3株抗體均為IgG1。采用間接ELISA對4株抗體效價進行測定,結果顯示其腹水效價在1∶2.56×106~1∶4×104之間,親和力在1.5×109~1.0×107之間,且與結構及功能相似的PD-L2蛋白無明顯交叉反應,說明特異性較好(表1)。
2.3PD-L1抗體在Western blot檢測腫瘤細胞PD-L1蛋白表達量上的應用 用Ab2抗體對腫瘤細胞裂解液中PD-L1蛋白進行反應,結果見圖2。結果顯示Ab2抗體能在蛋白水平上與腫瘤細胞中PD-L1蛋白結合, 無明顯雜帶,說明抗體特異性良好,能應用于Western blot方法檢測腫瘤細胞PD-L1蛋白的表達量。
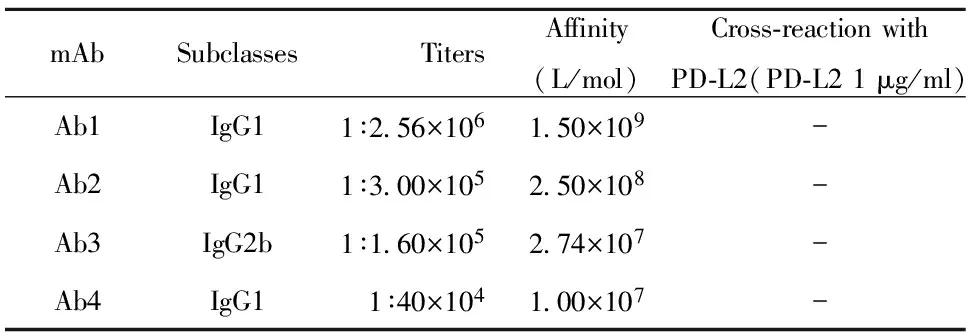
表1 抗體特異鑒定
Note:“-”Indicating that the OD450 value is less than twice the negative value,proved no cross-reaction with the PD-L2 protein.
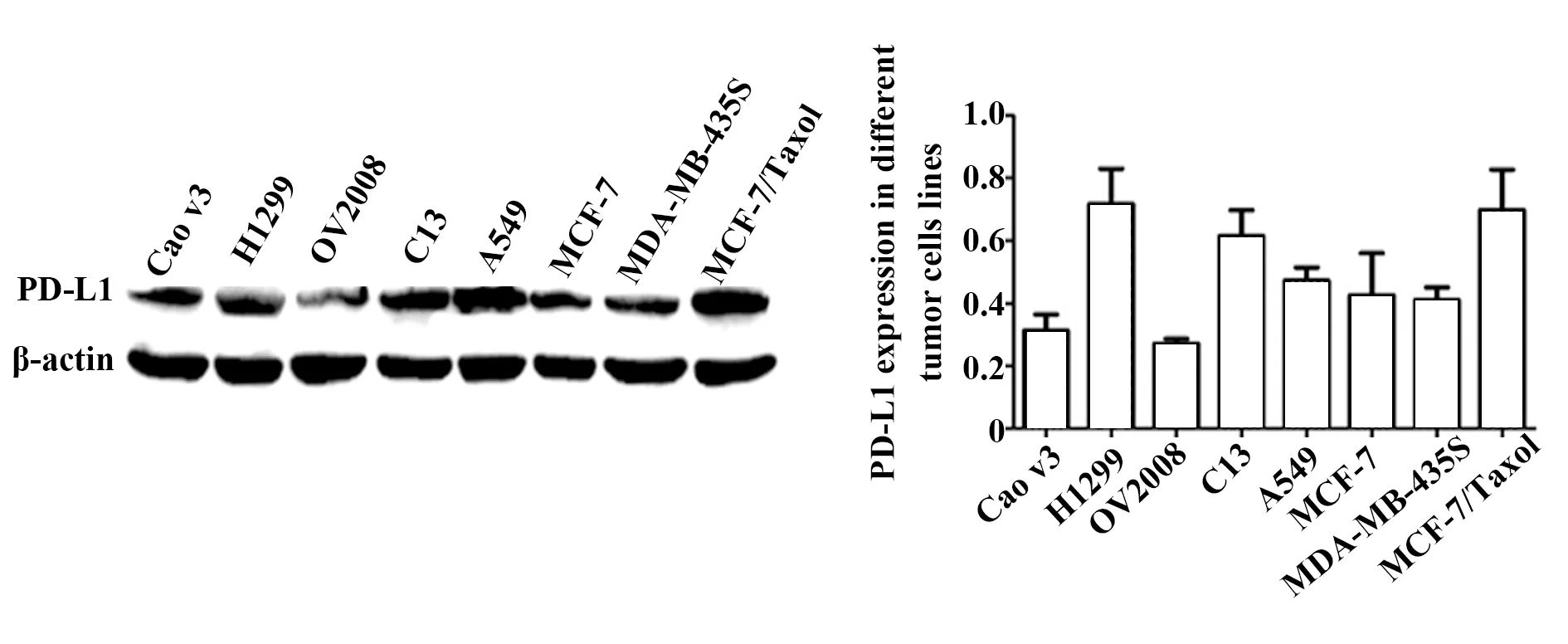
圖2 PD-L1單抗應用于免疫印跡分析不同腫瘤細胞PD-L1蛋白的表達Fig.2 Expression of PD-L1 in different kinds of tumor cell lines were analyzed by Western blot used PD-L1 mAb
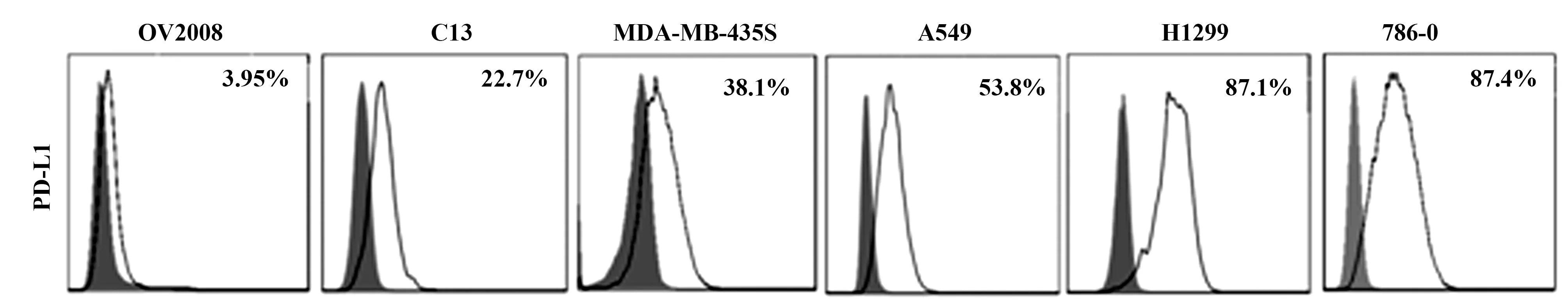
圖3 流式細胞術分析不同腫瘤細胞系中PD-L1蛋白的表達Fig.3 Expression of PD-L1 in different kinds of tumor cell lines were analyzed by FACS

圖4 PD-L1抗體在CIK細胞殺傷腫瘤中的作用Fig.4 Function of PD-L1 antibody in CIK cell killing tumorNote:A.Differential expression of two main phenotypic subsets of CIK cells over in vitro culture are shown for identification of CIK cells,CD3/CD56/CD8;B.PD-1 expression after CIK cell activation;C.PD-L1 blocking antibodies efficiently increases tumor-killing activity of CIK cells.*.P<0.05;**.P<0.01;***.P<0.001.
2.4PD-L1抗體在流式檢測腫瘤細胞PD-L1表型上的應用 用制備的Ab1作為一抗,Alexa Flour 647 Goat anti-mouse IgG作為熒光二抗,采用流式細胞儀檢測腫瘤細胞膜表面PD-L1蛋白表達情況,結果見圖3。結果顯示制備的Ab1抗體能特異性標記腫瘤細胞膜PD-L1蛋白,說明Ab1能與PD-L1天然蛋白特異性結合,能很好的應用于流式檢測抗體。
2.5抗體具有促進CIK細胞對腫瘤細胞的殺傷作用 因CIK有CTL(殺傷性T細胞)的特性,因此具有CD3+CD8+表型;另一方面它還具有NK細胞的非MHC限制性殺傷特性,因此具有CD56+表型。培養14 d后的CIK細胞中CD3+CD8+細胞比例高達77.7%,CD3+CD56+細胞比例高達43.3%(見圖4A),證明CIK細胞培養成功,可用于后續實驗。
用anti-TCR抗體激活CIK細胞后發現其PD-1分子表達量顯著增高(見圖4B),證明PD-1分子在CIK細胞激活后表達升高,從而通過PD-1/PD-L1通路負調控CIK細胞的活性和功能。用培養14 d的成熟CIK細胞對腫瘤細胞系A549/DDP進行殺傷,并加入PD-L1抗體和Control IgG,檢測靶細胞的死亡率。結果顯示與對照組相比,加入Ab1和Ab2抗體組均能促進CIK細胞對腫瘤細胞的殺傷(見圖4C),表明這兩株抗體可能具有阻斷PD-1/PD-L1通路活性,進而在細胞免疫治療中發揮促進腫瘤殺傷的作用。
3 討論
近來越來越多的研究表明,PD-1以及PD-L1的表達與癌癥患者的臨床病征以及預后密切相關[16],因此PD-L1抗體無論在檢測診斷中或者藥物治療中都有著廣闊的應用前景。本研究通過免疫PD-L1重組蛋白,經過細胞融合、克隆化篩選、抗體大量制備、純化等技術獲得了4株特異性識別人PD-L1蛋白的單克隆細胞株,其中Ab1和Ab2具有較高的滴度和親和力,Ab1腹水型抗體效價更是高達1∶2.56×106,明顯優于國內報道制備的抗人PD-L1單抗[17];在流式檢測中,Ab1抗體的工作濃度為3 μg/106cells,略低于國外生產的流式檢測抗體(2.5 μg/106cells);后續實驗將改進檢測方法以提高檢測靈敏度。所獲得的Ab2抗體在Western blot 檢測腫瘤細胞表面PD-L1表達量中抗體工作濃度為 2 μg/ml,檢測條帶單一清晰,說明其特異性強,可適用于Western blot檢測;制備的Ab1、Ab2抗體能促進CIK細胞對A549/DDP細胞系的殺傷作用,證實該抗體具有一定的阻斷PD-1/PD-L1通路的作用,可作為阻斷抗體應用于臨床研究。
隨著PD-1/PD-L1抗體治療的廣泛應用,PD-L1在腫瘤及正常組織上的檢測成為評估該治療方法有效性的重要指標。而國外的檢測抗體價格普遍偏高,因此制備成本較低的高效價、高特異性PD-L1抗體具有極大的意義,而本研究制備的抗體能滿足基本的檢測需要。但是由于制備的PD-L1抗體是鼠源抗體,在腫瘤治療中將有很大的限制,后續研究將進行人源化改造以及親和力成熟,為進一步PD-L1抗體藥物的研發奠定基礎。
[1] Francisco LM,Sage PT,Sharpe AH.The PD-1 pathway in tolerance and autoimmunity[J].Immunol Rev,2010,236(1):219-242.
[2] Dong H,Strome SE,Salomao DR,etal.Tumor-associated B7-H1 promotes T-cell apoptosis:a potential mechanism of immune evasion[J].Nat Med,2002,8(8):793-800.
[3] Castella B,Foglietta M,Sciancalepore P,etal.Anergic bone marrow Vγ9Vδ2 T cells as early and long-lasting markers of PD-1-targetable microenvironment-induced immune suppression in human myeloma[J].Oncoimmunology,2015,4(11):e1047580.
[4] Khan AR,Hams E,Floudas A,etal.PD-L1hi B cells are critical regulators of humoral immunity[J].Nat Commun,2015,6:5997.
[5] Hamanishi J,Mandai M,Iwasaki M,etal.Programmed cell death 1 ligand 1 and tumor-infiltrating CD8+T lymphocytes are prognostic factors of human ovarian cancer[J].Proc Natl Acad Sci,2007,104(9):3360-3365.
[6] Thompson RH,Kuntz SM,Leibovich BC,etal.Tumor B7-H1 is associated with poor prognosis in renal cell carcinoma patients with long-term follow-up[J].Cancer Res,2006,66(7):3381-3385.
[7] Thompson RH,Gillett MD,Cheville JC,etal.Costimulatory molecule B7-H1 in primary and metastatic clear cell renal cell carcinoma[J].Cancer,2005,104(10):2084-2091.
[8] Ohaegbulam KC,Assal A,Lazar-Molnar E,etal.Human cancer immunotherapy with antibodies to the PD-1 and PD-L1 pathway[J].Trends Mol Med,2015,21(1):24-33.
[9] 劉詩琴,黃建芳,向軍儉,等.人 N 端腦鈉肽前體 (NT-ProBNP) 單抗制備及雙抗體夾心 ELISA 檢測方法的建立[J].免疫學雜志,2016,32(5):441-445.
[10] Raghava GPS,Agrewala JN.Method for determining the affinity of monoclonal antibody using non-competitive ELISA:a computer program[J].J Immunoassay Immunochem,1994,15(2):115-128.
[11] 周 瑩,陳永井,張學光,等.鼠抗人 PD-L1 功能性單克隆抗體的研制及其生物學特性的鑒定[J].細胞與分子免疫學雜志,2011,27(11):1208-1211.
[12] Sun J,Xu K,Wu C,etal.PD-L1 expression analysis in gastric carcinoma tissue and blocking of tumor‐associated PD-L1 signaling by two functional monoclonal antibodies[J].Tissue Antigens,2007,69(1):19-27.
[13] Jiang J,Wu C,Lu B.Cytokine-induced killer cells promote antitumor immunity[J].J Transl Med,2013,11(1):83.
[14] Dai C,Lin F,Geng R,etal.Implication of combined PD-L1/PD-1 blockade with cytokine-induced killer cells as a synergistic immunotherapy for gastrointestinal cancer[J].Oncotarget,2016,7(9):10332.
[15] Zhu B,Ju S,Shu Y.CD137 enhances cytotoxicity of CD3+CD56+cells and their capacities to induce CD4+Th1 responses[J].Biomed Pharmacother,2009,63(7):509-516.
[16] 唐宛豫,張國偉,王慧娟,等.PD-1/PD-L1 抑制劑在晚期非小細胞肺癌中的臨床進展與治療策略[J].中國免疫學雜志,2016,32(10):1558-1561.
[17] 陳 嬌,戴麗娜,張 平,等.鼠抗人 PD-L1 單克隆抗體的制備及鑒定[J].四川大學學報:醫學版,2011,42(1):5-9.
[收稿2017-03-13 修回2017-04-09]
(編輯 倪 鵬)
Preparationandapplicationofanti-humanPD-L1monoclonalantibodies
FENGPei-Ran,HUANGJian-Fang,WANGMin-Zhen,LIAOWei-Cong,HAODai-Ling,XIANGJun-Jian.AntibodyEngineeringResearchCenter,JinanUniversity,GuangdongProvinceKeyLaboratoryofMolecularImmunologyandAntibodyEngineering,Guangzhou510632,China
Objective:To obtain a high specificity and high affinity anti-human PD-L1 monoclonal antibody which can be used for clinical diagnosis and block PD-L1 and PD-1 binding.Methods:BALB/c mice were immunized with recombinant PD-L1 protein.The positive cell clones stably secreting anti-human PD-L1 monoclonal antibody were obtained by classical hybridoma cell fusion technique.The specificity,affinity,subtype and other characteristics of the antibody were identified by ELISA.Immunofluorescence and indirect immunofluorescence were used to detect the tumor cells.Antibody blocking activity was confirmed by tumor killing test.Results:Two cell strains stably secreting monoclonal antibodies against human PD-L1 were screened out.Ab1 and Ab2 had high titer and affinity.The antibody titers were 1∶2.56×106and 1∶3×105,and the affinity was 1.5×109L/mol and 2.5×108L/mol respectively.There was no cross reaction between these two antibodies and PD-L2.Immunoblotting,indirect immunofluorescence confirmed that the antibody can be used to the diagnosis.Experiment showed that PD-L1 antibodies can increases tumor-killing activity of CIK cells.Conclusion:Two hybridoma cell lines capable of stably secreting highly specific and high affinity anti-human PD-L1 monoclonal antibody are obtained.They can specifically bind to PD-L1 molecules on tumor cells and can be used to the diagnosis of tumor phenotype and prognosis.Antibody blocking function can be applied to combined CIK cell immunotherapy.
PD-L1;Monoclonal antibody;Flow cytometry;Cytokine-induced killer cells;Tumor diagnosis
10.3969/j.issn.1000-484X.2017.06.015
①本文為廣東省人才引進創新團隊項目《重大疾病的臨床診斷試劑研發》(2013S028)。
②暨南大學轉化醫學轉化研究院國際免疫學中心,廣州510632。
馮沛然(1992年-),女,在讀碩士,主要從事抗體制備及應用方面研究。
及指導教師:向軍儉(1952年-),男,博士,教授,博士生導師,主要從事工程抗體及其應用研究,E-mail:txjj@jnu.edu.cn。
R392.1
A
1000-484X(2017)06-0879-05

