開環(huán)法聚丁二酸丁二醇酯酯化過程動力學研究
李錚
上海華誼集團技術研究院上海煤基多聯(lián)產工程技術研究中心(上海 200241)
科研開發(fā)
開環(huán)法聚丁二酸丁二醇酯酯化過程動力學研究
李錚
上海華誼集團技術研究院上海煤基多聯(lián)產工程技術研究中心(上海 200241)
以丁二酸酐與丁二醇為原料,采用開環(huán)法合成了可完全生物降解的聚丁二酸丁二醇酯(PBS)樹脂。根據(jù)實驗及相關文獻數(shù)據(jù)建立了開環(huán)法制備PBS的酯化動力學模型,并得到了相關的模型參數(shù),為今后工業(yè)連續(xù)化生產奠定基礎。
生物降解塑料 PBS 開環(huán)聚合 反應動力學
中國分類號 TQ323.4+3
高分子材料的應用極大地方便了人們的生活,但部分產品回收困難且無法降解,導致使用后的廢棄物越來越多,造成了日益嚴重的環(huán)境問題[1-2]。因此,近年來開發(fā)合成新型完全生物降解高分子材料引起了越來越多科研人員的重視,其中,一種以脂肪族二元酸、二元醇為主要原料縮聚而成的新型脂肪族聚酯——聚丁二酸丁二醇酯(PBS)因其優(yōu)異的綜合性能而受到了廣泛的研究與應用[3-5]。與傳統(tǒng)的生物降解聚酯材料相比,PBS樹脂的力學性能優(yōu)異,且熔點相對較高,改性后的使用溫度可超過100℃[6-7],在餐具、包裝、一次性醫(yī)療用品及農用薄膜等領域有著廣泛的應用,符合環(huán)境保護與可持續(xù)發(fā)展戰(zhàn)略的要求。
上海華誼集團技術研究院自主開發(fā)了通過順酐加氫制備丁二酸酐(SA)的技術,且該技術所用加氫催化劑的活性較高。國內順酐產能過剩,價格低廉且來源廣泛,因此加氫制備的丁二酸酐原料成本較低,甚至低于通過直接酯化法所得丁二酸原料的成本,使得開環(huán)法制備PBS成為極具競爭力的工藝路線(具體見圖1),同時,該路線具有很好的社會意義和經濟效益。
目前關于開環(huán)法制備PBS的研究報道,主要集中在其合成配方、工藝以及產品熱性能、力學性能研究等方面,而其反應動力學和模型化方面的研究則較少。因此,本文主要對開環(huán)法PBS酯化過程的反應動力學及其模型化進行了研究,并得到相關的模型參數(shù),為今后工業(yè)連續(xù)化生產奠定基礎。
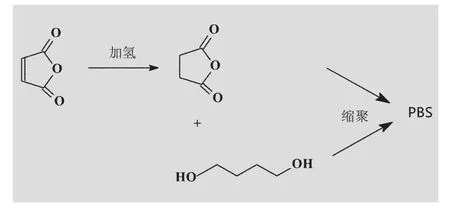
圖1 開環(huán)法PBS的合成工藝路線
1 實驗部分
1.1 主要原料
丁二酸酐:工業(yè)級,純度≥99%,帝斯曼(中國)有限公司;1,4-丁二醇(BDO):分析純(≥99%),國藥集團化學試劑有限公司。
1.2 主要儀器與設備
ReactIRTM4000型在線反應紅外分析系統(tǒng),瑞士梅特勒-托利多公司。
1.3 合成方法
采用20 L聚酯間歇反應成套裝置進行PBS聚合反應研究。向反應釜中加入一定比例的BDO和SA及適量的催化劑。首先進行氣體置換,保證反應在氮氣氛圍中和常壓下進行,使反應溫度逐步上升,在140~200℃進行酯化反應,反應時間為1.0~2.0 h。當反應餾出液不再增加時,停止酯化反應。縮聚反應在同一反應釜中進行,使體系的壓力緩慢降低到-90 kPa(表壓)左右,反應30~50 min;然后將反應溫度逐漸升高至240℃,體系的絕對壓力緩慢降低到150 Pa(絕壓)左右,反應時間為1.5~2.5 h。
2 結果與討論
2.1 開環(huán)法制備PBS聚合反應
2.1.1 開環(huán)法PBS聚合反應過程
開環(huán)法制備PBS聚合反應過程中,主要存在SA開環(huán)、酯化、縮聚(酯交換)等類型的反應。
(1)SA開環(huán)反應
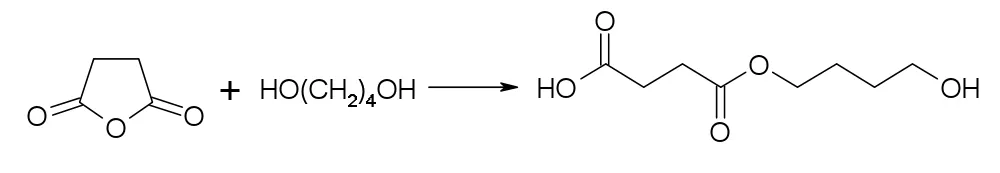
(2)酯化反應

(3)縮聚(酯交換)反應
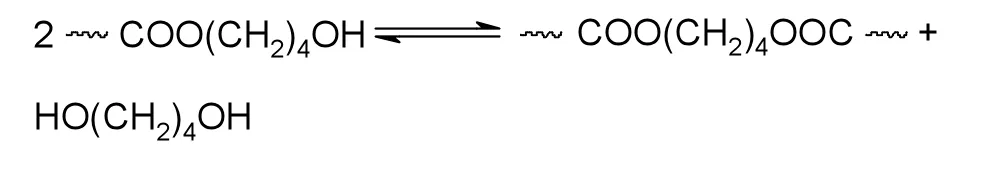
(4)四氫呋喃(THF)副反應

在PBS聚合反應過程中,不可避免地會發(fā)生BDO環(huán)化生成THF和端羥丁基分解生成THF的副反應,從而影響PBS產品的收率。
2.1.2 開環(huán)反應
采用ReactIRTM4000型在線紅外分析儀跟蹤了體系中SA開環(huán)反應過程(1),并初步研究了SA開環(huán)的反應速率。由在線紅外測試結果(見圖2)可知,SA特征峰在1787 cm-1處,開環(huán)產物特征峰在1730 cm-1處;隨著反應溫度升高,原料SA溶解,隨后發(fā)生開環(huán)反應,原料急劇消耗,同時開環(huán)產物迅速生成。根據(jù)產物生成曲線可知,SA開環(huán)反應在10 min內基本趨于平衡。由于SA開環(huán)反應迅速,在酯化反應初期已完全生成開環(huán)產物,因此可以認為酯化階段的初始反應物由SA開環(huán)產物和剩余BDO組成。
2.2 酯化反應動力學模型及其參數(shù)

圖2 丁二酸酐開環(huán)反應在線紅外測試結果
通過上述實驗及分析可知,開環(huán)法制備PBS聚合過程中,SA開環(huán)反應速率快,而酯化過程為慢反應,因此只需定量研究酯化反應動力學過程,即SA開環(huán)產物和剩余BDO的反應動力學。
2.2.1 酯化過程模型建立
酯化過程的反應機理如下:在酯化階段,主要反應是酯化反應(1)和(2);同時伴隨著單羥基丁二醇之間發(fā)生的縮聚反應(3)、副反應BDO環(huán)化生成THF(4)和端羥丁基分解生成THF的反應(5)。其中反應(1)~(3)為可逆反應。
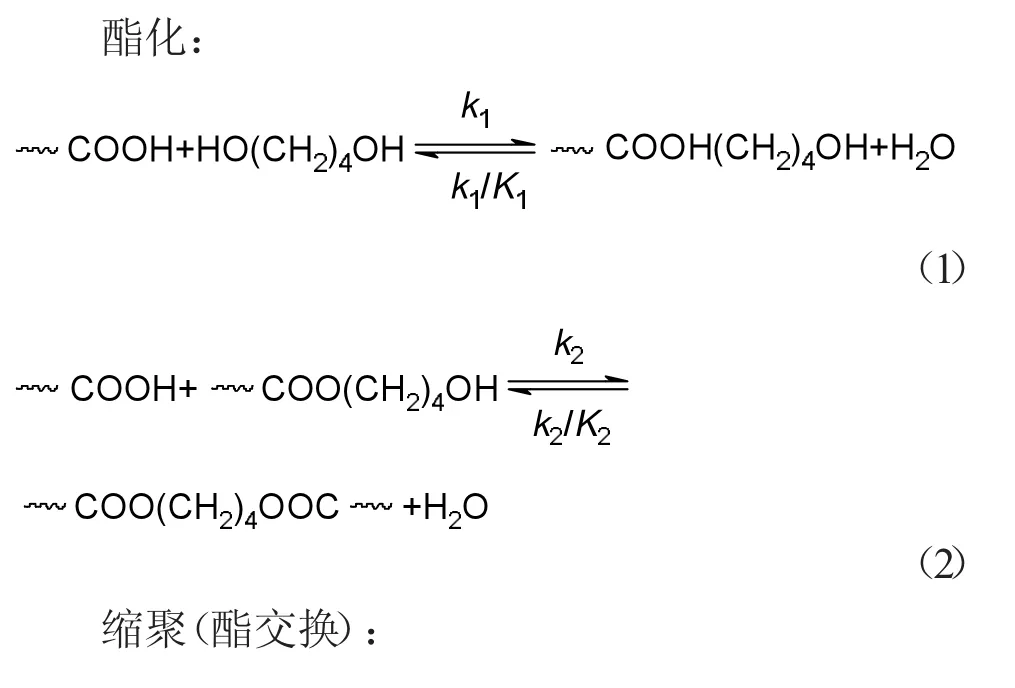

為了簡化處理,分別用G表示BDO單體,tG表示端羥丁基官能團,bG表示丁基酯鍵,w表示生成的水。
通過反應過程中官能團的變化,建立模型方程,并擬合得到相關的動力學常數(shù)。根據(jù)相關文獻的研究結果[8-10],建立酯化動力學模型,相關的模型參數(shù)也可參考上述文獻。
為了得到酯化過程相應的數(shù)學模型,作出如下假設:
(1)SA開環(huán)反應速率快假定:根據(jù)上述分析,SA開環(huán)反應速率極快,可以假定反應體系中一旦SA溶解完全就全部反應。
(2)等活性假設:SA分子中的羧基以及低聚物分子鏈上的羧基參加酯化反應時的活性相同;單羥丁酯基的反應活性相同,且與分子鏈長度無關,但其反應活性為BDO單體中羥基反應活性的一半,即kl=2k2。
(3)動力學二級反應假設:酯化反應符合外加酸催化劑的二級動力學。
(4)BDO全回流假設:反應器的分餾柱能有效地分離氣相中的BDO,使之回流到反應釜內。除反應消耗外,其余BDO均存在于體系的液相之中。
(5)不可逆假設:由于酯化反應在高溫下進行,且足夠大流量的氮氣能及時把產生的小分子帶出體系,認為酯化反應(1)和(2)不可逆,即不考慮平衡常數(shù)K3。
根據(jù)反應速率方程的定義和上述假設,建立模型方程:


其中,ni(i=COOH,G,tG,bG,CO O)表示體系中各物質的物質的量,V為反應體系的體積。(R1,R2忽略了由于體系中水的存在而造成的逆反應。)
根據(jù)模型假設和各反應之間的關系,可以推導出反應體系中各官能團變化的微分方程,各官能團的量均以物質的量表示。聚合過程中,由于低分子產物的脫除,反應體積一直處于變化中,需對體積變化作簡化處理。

酯化反應過程中,反應體系密度(ρ)變化不大,保持在1.12 g/cm3左右,體積變化主要是由體系中小分子的移除引起的,因此可以通過小分子的移除量近似估算反應體系的體積變化,其中mA,0和mB,0為SA和BDO的初始質量,md為小分子餾出液的質量(即水和THF的質量之和)。

2.2.2 酯化反應模型參數(shù)的擬合
在醇酸投料比為1.3,金屬催化劑濃度為1.5 mmol/mol酸酐的條件下進行不同溫度(170~200℃)下的酯化動力學實驗。根據(jù)上述非線性微分方程組,采用最小二乘法對酯化動力學實驗結果進行擬合,不同溫度下酯化反應各基元的反應速率常數(shù)如表1所示。
可以采用阿倫尼烏斯方程對各速率常數(shù)進行進一步擬合,從而求得各基元反應的活化能。所得各基元反應的活化能(E)及指前因子(A)見表2。
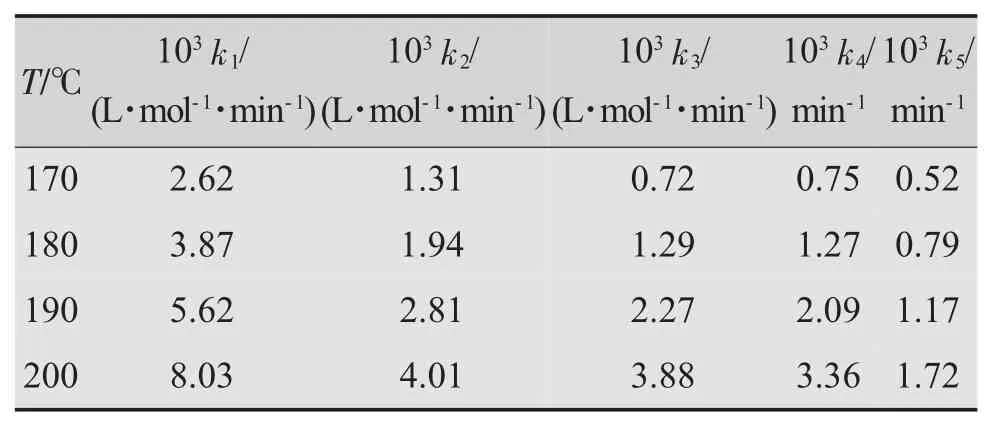
表1 不同溫度下各基元反應速率常數(shù)


表2 各基元反應的活化能E及指前因子A
2.2.3 模型預估結果
對酯化反應模型的非線性微分方程組進行模擬,可以得出不同溫度下酯化反應的程度及THF的生成量。以pCOOH表示反應的酸酐/酸單元剩余的比例,將其作為酯化反應程度的定量指標。由圖3可以看出,由于SA開環(huán)反應已迅速完成,因此在酯化反應開始時,反應程度已達0.5。隨著反應溫度的升高,酯化反應速率加快,在200℃時酯化時間為100 min,酯化反應程度可達0.94,之后隨時間延長酯化程度增加緩慢,因此可以選擇200℃、100 min作為最優(yōu)酯化條件。

圖3 不同溫度下的酯化反應程度
nTHF為生成THF的物質的量,nG,0為初始投入的BDO的物質的量,二者比值反映了THF生成量的多少。由圖4可知,在200℃、100 min的酯化條件下,nTHF/nG,0的值為0.1,表明此時約有10%的BDO生成了THF。模擬結果顯示,隨著反應溫度的升高,THF的生成量迅速增加,趨勢與實際情況一致。

圖4 不同溫度下生成的THF與丁二醇投料之比
3 結論
根據(jù)實驗及相關文獻數(shù)據(jù)建立了開環(huán)法制備PBS的動力學模型,并根據(jù)模型對酯化反應進行了模擬,得到了最優(yōu)酯化反應條件。
(1)由在線紅外測試結果可知,SA開環(huán)速率快,因此在建立酯化反應模型時,可以不考慮其反應速率,認為酯化反應剛開始時,SA開環(huán)反應已結束。
(2)根據(jù)實驗建立了開環(huán)法制備PBS酯化階段的動力學模型,由酯化反應、酯交換反應、THF副反應等基元反應組成,并擬合得到了各基元反應的反應速率及活化能。
(3)依據(jù)所建立的動力學模型及參數(shù),對不同溫度下酯化程度及THF的生成量進行了模擬,模擬結果表明200℃、100 min為最優(yōu)酯化反應條件。
[1]OKADA M.Chemical syntheses of biodegradable polymers [J].Progress in Polymer Science,2002,27(1):87-133.
[2]KIMMN,Lee A R,Yoon S J,et al.Biodegradation of poly (3-hydroxybutyrate),Sky-Green?and Mater-Bi?by fungi isolated from soils[J].European Polymer Journal,2000,36 (8):1677-1685.
[3]王國利,徐軍,郭寶華.可生物降解聚丁二酸丁二醇酯及其共聚物的合成及改性研究進展[J].高分子通報,2011 (4):99-109.
[4]MONTAUDO G,RIZZARELLI P.Synthesis and enzymatic degradation ofaliphatic copolyesters[J].Polymer Degradation and Stability,2000,70(2):305-314.
[5]孫杰,譚惠民,羅運軍,等.(丁二酸丁二酯/丁二酸己二酯)共聚物的合成及性能[J].工程塑料應用,2004,32(4):14-16.
[6]高明,王秀芬,郭銳,等.PBS基生物降解材料的研究進展[J].高分子通報,2004(5):51-55.
[7]LEE S M,CHO D W,PARK W H,et al.Novel silk/poly (butylenes succinate)biocomposites:the effect of short fiber content on their mechanical and thermal properties[J].Composites Science and Technology,2005,65(3-4):647-657.
[8]BIKIARIS D N,ACHILIAS D S.Synthesis of poly(alkylene succinate)biodegradable polyesters I.Mathematical modelling of the esterification reaction[J].Polymer,2006,47 (13),4851-4860.
[9]BIKIARIS D,ACHILIAS D S.Synthesis of poly(alkylene succinate)biodegradable polyesters,Part II:Mathematical modelling of the polycondensation reaction[J].Polymer, 2008,49(17),3677-3685.
[10]胡麗霞.脂肪-芳香族共聚酯合成過程的反應動力學研究[D].杭州:浙江大學,2010.
Reaction Kinetics Research in Esterification of Poly(butylene succinate)by Ring-opening Polymerization
Li Zheng
The biodegradable poly(butylene succinate)(PBS)was synthesized by ring-opening polymerization with 1,4-butanediol and succinic anhydride as raw materials.Based on the in-situ infrared spectroscopy test and some literature,the esterification kinetics model of PBS synthesized by ring-opening polymerization was established,and the basic parameters were obtained,hoping to lay a foundation for the industrialized continuous production in the future.
Biodegradable polymer;PBS;Ring-opening polymerization;Reaction kinetics
2017年5月
李錚女1983年生碩士工程師研究方向為高分子材料聚合

