蒙古冰草苗期抗旱相關microRNA的差異表達分析及靶基因預測
馬艷紅,張旭婷,于肖夏,劉旭婷,高 慧,于 卓
(內蒙古農業大學農學院,內蒙古呼和浩特 010019)
蒙古冰草苗期抗旱相關microRNA的差異表達分析及靶基因預測
馬艷紅,張旭婷,于肖夏,劉旭婷,高 慧,于 卓
(內蒙古農業大學農學院,內蒙古呼和浩特 010019)
為明確蒙古冰草抗旱相關microRNA(miRNA)的表達特征及其靶基因,利用實時熒光定量PCR技術,對前期測序篩選到的4個miRNA(amo-miR21、amo-miR44、amo-miR62、amo-miR82)在干旱脅迫下的苗期差異表達情況進行了定量驗證,用Target Finder軟件和psRNATarget數據庫在線預測其靶基因,并用MegAlign軟件對預測的靶基因進行了同源性比對分析。結果表明,干旱脅迫下,蒙古冰草中amo-miR21、amo-miR82和amo-miR62的表達量呈上調趨勢,而amo-miR44的表達呈下調趨勢,與前期測序結果相符;4個miRNA共預測出32個靶基因,其中,amo-miR44在玉米、水稻和小麥數據庫中未發現同源的靶基因,在擬南芥、大麥、蒺藜苜蓿中發現的靶基因相似性較低;而amo-miR21、amo-miR82和amo-miR62的靶基因均與小麥中預測的靶基因存在較高同源性(68.6%~95.6%),推測這3個靶基因是參與干旱逆境脅迫響應的基因。
蒙古冰草;干旱脅迫;microRNA;熒光定量RT-PCR;靶基因預測
Abstract:In order to know the expression characteristics and target gene of drought-responsive microRNA(miRNA) inAgropyronmongolicumKeng,the temporal expression of four miRNA(amo-miR21,amo-miR44,amo-miR62 and amo-miR82) under drought stress treatment at seedling stage were monitored by fluorescent quantitative real-time polymerase chain reaction,of which miRNA have been selected based on the previous researches of small RNA-seq. Their target genes were predicted by Target Finder software and psRNATarget database,and the homology were analyzed with MegAlign. The results showed that amo-miR21,amo-miR82 and amo-miR62 were significantly up-regulated in leaves,while amo-miR44 was down-regulated under drought stress,and the expression of the four miRNA were consistent with sequencing data. Thirty-two target genes of the four miRNAs ofA.mongolicumwere predicted by Target Finder software and homologously searched in psRNATarget database. The homologous target genes of amo-miR44 are not found in corn,rice or wheat database,and the similarity index of target gene sequence pairs fromA.mongolicumandArabidopsisthaliana,Hordeumvulgare,Medicagotruncatulais low. The three target genes of amo-miR21,amo-miR82,and amo-miR62 are homologous with the target genes fromTriticumaestivum(68.6%-95.6%),which can be speculated as drought-responsive genes.
Keywords:AgropyronmongolicumKeng; Drought stress; microRNA; Fluorescent quantitative RT-PCR; Target gene prediction
蒙古冰草(AgropyronmongolicumKeng)為小麥族冰草屬(Agropyron)二倍體多年生牧草,是耿以禮教授于1938年發現的新種,模式標本產地為內蒙古烏蘭察布盟的百靈廟地區[1-2],在內蒙古集中分布在渾善達克沙地和嘎亥額勒蘇沙地,為典型的寒旱生植物,其根系發達、具沙套、返青早、分蘗多、抗旱性極強,是麥類作物抗旱性改良的優良基因資源[3-5]。
MicroRNA(miRNA)是植物體內普遍存在的長度約21~25 nt的內源單鏈小分子非編碼RNA,其與靶mRNA序列的互補程度決定其對靶mRNA的剪切或翻譯的阻遏,主要在轉錄后水平進行調控,是mRNA表達的關鍵調控因子之一[6-7]。miRNA數據庫miRBase(miRBase V21.0)共收錄了223個物種的35 828個成熟的miRNA,涵蓋了73個植物種的849個miRNA。大量研究表明,miRNA在植物的生育、細胞分化、抗非生物脅迫等過程中發揮重要作用[6,8]。目前,針對miRNA響應干旱脅迫并參與調控的研究已在擬南芥(Arabidopsisthaliana)、水稻(Oryzasativa)、煙草(NicotianatabacumL.)、大豆(GlycinemaxL.)、玉米(Zeamays)、小麥(Triticumaestivum)、楊樹(PopulustrichocarpaL.)、二穗短柄草(Brachypodiumdistachyon)、大麥(Hordeumvulgare)、蒺藜苜蓿(Medicagotruncatula)、桃(Prunuspersica)、擬二粒小麥(Triticumdicoccoides)、沙冬青(Ammopiptanthusmongolicus)等植物中有相關報道,研究發現,與抗旱相關的miRNA有miR156、miR159、miR167、miR168、miR171、miR172、miR319、miR393、miR394a、miR395、miR396、miR397、miR161、miR168、miR169等[9-14]。但至今尚未見有關于蒙古冰草抗旱相關miRNA的研究報道。
本試驗在前期對蒙古冰草Solexa高通量測序及生物信息學分析的基礎上,利用熒光定量RT-PCR技術對選出與抗旱性顯著相關的4個新預測的保守miRNA(amo-miR21、amo-miR44、amo-miR62和amo-miR82)進行定量分析,并對其靶基因進行預測,以期為闡明蒙古冰草抗旱相關miRNA調控機制及其靶基因的功能研究奠定基礎。
1 材料與方法
1.1 供試材料及干旱處理
供試材料為野生蒙古冰草,其種子采集于內蒙古烏蘭察布百靈廟鎮。
挑選籽粒飽滿的蒙古冰草種子,種植于裝有花卉土與蛭石混合(1∶1)的花盆(直徑20 cm,深30 cm)中,每盆播種50粒種子,共24盆,置人工氣候室內培養,室內晝夜溫度25±5 ℃,光強30 000 lx,光照時間14 h,定量澆水,濕度65%。待幼苗長至15 cm時,分成對照和處理兩組,處理組進行斷水干旱脅迫,脅迫天數為3、6、9、12、15、18、21 d(21 d干旱處理后,葉片較干枯,復水后僅有少數植株成活,為水分脅迫的臨界點),3次重復,每個處理同期取15株幼苗葉片等量混合,立即于液氮中速凍,-80 ℃冰箱中保存。
1.2 miRNA表達的熒光定量RT-PCR檢測
1.2.1 總RNA提取及miRNA反轉錄
取凍存的樣本經液氮研磨后,利用Trizol法提取各處理及對照的總RNA。取2 μL RNA原液稀釋至10 μL,用1%的瓊脂糖凝膠電泳20 min后,檢測其完整性和純度。各處理及對照樣品總RNA采用TianGen公司生產的miRcute miRNA cDNA 第一鏈合成試劑盒(KR211)反轉錄成cDNA。反轉錄反應體系包括2 μL的2×逆轉錄緩沖液、2 μL RNA模板、1.2 μL逆轉錄引物、0.2 μL MMLV逆轉錄酶(200 U·μL-1),加DEPC水至總體積20 μL。反應條件:26 ℃ 30 min,42 ℃ 30 min,85 ℃ 10 min。反轉錄產物于-20 ℃冰箱保存備用。
1.2.2 熒光定量RT-PCR

用Excel 2007軟件進行數據表格整理及柱形圖繪制,用SAS 9.0軟件進行方差及差異顯著性分析。

表1 熒光定量RT-PCR所用引物序列Table 1 Primer sequences used for RT-PCR
1.3 靶基因預測及生物信息學分析
利用Target Finder[18]軟件對蒙古冰草4個新預測miRNA進行靶基因預測,并用BLAST軟件[19]將預測得到的靶基因序列與nr[20]、Swiss-Prot[21]數據庫比對,獲得靶基因序列的注釋信息。同時,在植物microRNA靶基因數據庫psRNATarget[22](http://plantgrn.noble.org/psRNATarget/)中,基于模式植物擬南芥(Arabidopsisthaliana)、煙草(NicotianatabacumL.)及禾本科植物小麥(Triticumaestivum)、水稻(Oryzasativa)、玉米(Zeamays)、大麥(Hordeumvulgare)、二穗短柄草(Brachypodiumdistachyon)、豆科牧草蒺藜苜蓿(Medicagotruncatula)的基因組數據預測靶基因(Scoring Schema為Schema V2,2017 release),成熟的miRNA與其靶基因之間的錯配堿基不超過3個。
用軟件DNAstar中MegAlign[23]對蒙古冰草4個miRNA預測得到的靶基因進行多序列比對及相似度分析。
2 結果與分析
2.1 蒙古冰草總RNA的質量
利用Trizol法提取7個干旱處理及對照樣品的總RNA后,采用1%的瓊脂糖凝膠電泳檢測,結果(圖1)顯示,28S rRNA、18S rRNA條帶清晰穩定,RNA無降解,未出現DNA污染。OD260/280值在1.8~2.1之間。說明RNA含量和質量均符合PCR擴增要求。

CK:對照;1~7:干旱處理3、6、9、12、15、18、21 d。
CK:Control; 1-7:Drought stress treatment for 3,6,9,12,15,18,and 21 d.
圖1蒙古冰草干旱處理后總RNA的瓊脂糖凝膠電泳檢測結果
Fig.1TotalRNAofA.mongolicumunderdroughtstressdetectedbyagarosegel
2.2 與抗旱性相關的4個新預測miRNA的真實性
根據4個新預測的miRNA(amo-miR21、amo-miR44、amo-miR62和amo-miR82)前體序列設計莖環狀特異引物,以 U6作為內參基因,進行RT-PCR擴增,結果(圖2)顯示,這4個miRNA均能在7個干旱處理及對照樣品中檢測到,是一條片段大小約為100 bp的清晰條帶,與預期片段大小一致,表明這4個miRNA是真實存在的。
2.3 與抗旱性相關的4個新預測miRNA的表達分析
以 U6為內參基因,將蒙古冰草未經干旱脅迫的miRNA表達量作為對照,設其為1,然后分別計算出各干旱處理中的miRNA相對表達量(圖3)。由圖1可知,蒙古冰草中amo-miR21、amo-miR62和amo-miR82的表達量隨著干旱脅迫時間的延長均呈上升趨勢,在干旱脅迫21 d時,其表達量分別較對照增加2.39、2.60和2.46倍;另外,干旱處理15、18和21 d時,這3個miRNA的表達量差異不顯著,表明干旱15 d時蒙古冰草的miRNA表達為極限表達。amo-miR44的表達量呈下降趨勢,干旱處理條件下的表達量極顯著低于對照,干旱處理21 d時的表達量較對照降低69.9%。
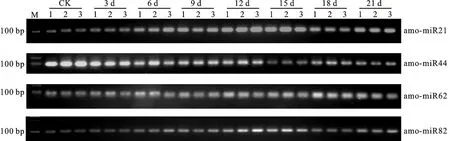
M:核酸分子量標準DL2000;CK:對照;1~3:3次重復。
M:DNA marker DL2000;CK:Control;1-3:Three replicates.
圖2干旱處理后蒙古冰草中與抗旱性相關的4個新預測miRNA的電泳檢測結果
Fig.2Electrophoretogramforthefournoveldrought-responsivemiRNAofA.mongolicumunderdroughtstress

圖注上不同字母表示處理間差異在0.01水平上顯著。
Different letters above the columns mean significant difference among different treatments at 0.01 level.
圖3干旱脅迫下蒙古冰草中miRNA的相對表達量
Fig.3RelativeexpressionlevelofmiRNAinA.mongolicumunderdroughtstress
2.4 與抗旱性相關的4個新預測miRNA的靶基因
利用Target Finder軟件預測分析發現,amo-miR21、amo-miR44和amo-miR82各有1個靶基因,其分別編碼光合系統II中的蛋白、PPR家族蛋白和泛素-蛋白酶體系統中的蛋白,amo-miR62有2個靶基因,編碼過氧化物還原酶和在線粒體中發揮作用的PPR蛋白家族。
在植物microRNA靶基因預測數據庫psRNATarget中,與模式植物擬南芥(A.thaliana)、煙草(N.tabacum)及禾本科作物大麥(H.vulgare)、小麥(T.aestivum)、水稻(O.sativa)、玉米(Z.mays)、二穗短柄草(B.distachyon)和豆科牧草蒺藜苜蓿(M.truncatula)數據進行比對,這4個miRNA共有27個靶基因(表2),且每個miRNA預測調控的靶基因數目不同。amo-miR62靶基因數最多,為9個,amo-miR21、amo-miR44和amo-miR82的靶基因數均為6個。盡管其中一部分靶基因沒有描述,但部分靶基因功能多種多樣,如光系統II反應中心M蛋白、α/β超家族蛋白水解酶、葡萄糖胺N-酰基轉移酶、抗壞血酸過氧化物酶、轉座子基因、假想蛋白等,一些參與干旱逆境脅迫響應過程(http://plantgrn.noble.org/psRNATarget/)。
2.5 預測的miRNA靶基因同源性
對Target Finder預測的靶基因與psRNATarget在線預測的靶基因進行序列比對分析發現,amo-miR21的靶基因與玉米Z.mays-GRMZM2G030695-T01的相似性指數為70.9%,與玉米Z.mays-GRMZM2- G055151-T01的相似性指數為84.2%,與小麥T.aestivum-CA679344的相似性指數高達95.6%,該基因注釋為光系統II反應中心M蛋白;amo-miR44的靶基因與擬南芥A.thaliana-AT4G06540.1的相似性指數為41.4%,與苜蓿M.truncatula-Medtr7g047630.1的相似性指數最高,也僅為46.2%,與大麥H.vulgare-TC256962的相似性指數為29.6%,均較低;amo-miR62靶基因2與玉米Z.mays-GRMZM2 G085845_T01的相似度為31.7%,與小麥T.aestivum-CA610180的相似性指數為48.2%,與短穗二柄草B.distachyon-Bradi2g52000.1的相似性指數為28.9%,與水稻O.sativa-LOC_Os02g28530.1的相似性指數為28.6%,與小麥T.aestivum-CA610180的相似性指數為40.2%,均較低;而amo-miR62的靶基因1和小麥中預測到的靶基因T.aestivum-TC459743的相似性指數高達91.3%,該基因注釋為抗壞血酸過氧化物酶;amo-miR82的靶基因與小麥T.aestivum-TC461760的相似性指數高達68.6%,相似度較高,該基因注釋為醛氧化酶-2。這表明蒙古冰草amo-miR21和amo-miR82的靶基因及amo-miR62的靶基因1與小麥中預測到的靶基因存在同源性。

表2 Target Finder和psRNATarget預測的靶基因Table 2 Target genes predicted by Target Finder and psRNATarget
3 討 論
蒙古冰草是干草原和荒漠草原上抗旱性強的叢生禾草,亦是麥類作物遺傳改良的寶貴野生近緣種,挖掘野生蒙古冰草的抗旱基因資源對于拓寬麥類作物的遺傳基礎具有重要意義。干旱是農作物生長發育最為嚴重的逆境脅迫之一,近年來大量研究報道表明,miRNA在干旱脅迫中起到重要調控作用,抗旱相關miRNA同作物遺傳改良中的新功能基因一樣重要,急需研究利用。RT-PCR是目前miRNA定量表達分析最常用且快速有效的方法之一[16]。本試驗選取前期蒙古冰草高通量測序獲得的4個抗旱相關的miRNA,利用熒光定量RT-PCR檢測其在不同干旱脅迫進程中的表達情況,結果發現,amo-miR21、amo-miR82和amo-miR62表達量在干旱脅迫15、18、21 d間差異不顯著,表明干旱15 d時蒙古冰草的miRNA表達為極限表達。隨著對蒙古冰草幼苗干旱脅迫處理天數的增加,amo-miR21、amo-miR82和amo-miR62的表達量呈上升趨勢,而amo-miR44的表達量呈下降趨勢,與前期的miRNA測序結果是一致的。根據MiRDeep軟件的保守性分析發現,amo-miR21、amo-miR44、amo-miR62和amo-miR82的不同物種的相似miRNA分別為bdi-miR5180b[9]、ath-miR854a[24]、zma-miR164g-3p[25]和bdi-miR5066[26](相似性分別為42.0%、30.7%、26.13%和43.5%),其中,bdi-miR5180b和bdi-miR5066未見有試驗驗證,zma-miR164g-3p和ath-miR854a響應生物逆境脅迫。本試驗中4個miRNAs在干旱脅迫響應中的功能有待進一步驗證。
miRNA的重要研究價值體現在其能夠調控靶基因的表達,預測和鑒定miRNA靶標基因是分析miRNA功能的前提。因植物體內miRNAs與其調控的靶基因序列近乎完全匹配,用生物信息學預測靶基因的方法更方便。利用已開發的Target Finder、PatScan、psRNATarget等軟件,通過同源性搜索和在線軟件預測植物miRNA靶標基因的方法得到了廣泛應用[27],如:Zhang等[28]利用在線預測軟件miRU(http://bioinofo3. noble. Org/ miRU. htm)對60個植物的miRNA靶基因預測得到了較好的結果,Kohli等[29]利用二代測序技術獲得了鷹嘴豆的122個保守miRNA和59個新miRNA,用psRNA-Target(http://plantgrn.noble.org /psRNATarget/)預測到358個靶基因。本試驗用Target Finder和psRNA-Target分別成功地預測到5個和27個靶基因,同源性比對發現蒙古冰草amo-miR21的靶基因、amo-miR62的靶基因1和amo-miR82的靶基因與小麥的靶基因(T.aestivum-CA679344、T.aestivum-TC459743、T.aestivum-TC461760)存在較高的同源性(68.6%~95.6%),靶基因功能依次注釋為光合系統II、過氧化物還原酶II、泛素-蛋白酶體系統中的蛋白,它們與干旱逆境脅迫響應有關,這為下一步蒙古冰草抗旱相關miRNA及其靶基因的功能驗證奠定了基礎。
[1] 云錦鳳,李瑞芬,米福貴.冰草的遠緣雜交及雜種分析[J].草地學報,1997,5(4):221.
YUN J F,LI R F,MI F G.Analysis on distant hybridization and hybrid of wheatgrass [J].ActaAcrestiaSinca,1997,5(4):221.
[2] 解新明.蒙古冰草(AgropyronmongolicumKeng)的遺傳多樣性研究[D].呼和浩特:內蒙古農業大學,2001:21.
XIE X M.Studies on the genetic diversity of mongolian wheatgrass(AgropyronmongolicumKeng) [D].Hohhot:Inner Mongolia Agricultural University,2001:21.
[3] 馬艷紅,于肖夏,于 卓,等.四倍體雜交冰草新品系的細胞學鑒定及SSR分析[J].麥類作物學報,2014,34(2):188.
MA Y H,YU X X,YU Z,etal.Cytological identification and SSR analysis of new strains of tetraploidy hybrid wheatgrass [J].JournalofTriticeaeCrops,2014,34(2):188.
[4] 于肖夏,姜志艷,于 卓,等.四倍體雜交冰草新品種-蒙雜冰草1號的選育[J].草業科學,2015,32(5):739.
YU X X,JIANG Z Y,YU Z,etal.The new variety breeding of tetraploid hybrid wheat grass-Mengza No.1 [J].PrataculturalScience,2015,32(5):739.
[5]HAN H M,LIU W H,LU Y Q,etal.Isolation and application of P genome-specific DNA sequences ofAgropyronGaertn.inTriticeae[J].Planta,2017,245:425.
[6]ALI N,SHAH F,MUHAMMAD A,etal.miRNAs:Major modulators for crop growth and development under abiotic stresses [J].BiotechnologyLetters,2017,39(5):1.
[7]AMANDEEP K,OM P G,NAND L M,etal.Comparative temporal expression analysis of microRNAs and their target genes in contrasting wheat genotypes during osmotic stress [J].AppliedBiochemistryandBiotechnology,2017,181:615.
[8]CANDAR C B,ARICAN E,ZHANG B H.Small RNA and degradome deep sequencing reveals drought and tissue-specific microRNAs and their important roles in drought-sensitive and drought tolerant tomato genotypes [J].PlantBiotechnologyJournal,2016,14:1727.
[9]GAO F,WANG N,LI H Y,etal.Identification of drought responsive microRNAs and their targets inAmmopiptanthusmongolicusby using high throughput sequencing [J].ScientificReports,2016,6:34601.
[10]BAEV V,MILEV I,NAYDENOV M,etal.Implementation of adenovogenome-wide computational approach for updatingBrachypodiummiRNAs [J].Genomics,2011,97:284.
[11]HACKENBERG M,GUSTAFSON P,LANGRIDGE P,etal.Differential expression of microRNAs and other small RNAs in barley between water and drought conditions [J].PlantBiotechnolJournal,2015,13:10.
[12]CHEN Q S,LI M,ZHANG Z C,etal.Integrated mRNA and microRNA analysis identifies genes and small miRNA molecules associated with transcriptional and post-transcriptional-level responses to both drought stress and re-watering treatment in tobacco [J].BMCGenomics,2017,18:12.
[13]ZHANG J W,LONG Y,XUE M D,etal.Identification of microRNAs in response to drought in common wild rice(OryzarufipogonGriff.) shoots and roots [J].PLoSOne,2017,12(1):12.
[14]XIE F,WANG Q,SUN R,etal.Deep sequencing reveals important roles of microRNAs in response to drought and salinity stress in cotton [J].JournalofExperimentalBotany,2015,66:800.
[15]CHEN C F,RIDZON D A,BROOMER A J,etal.Real-time quantification of microRNAs by stem-loop RT-PCR [J].NucleicAcidsResearch,2005,33(20):179.
[16]VARKONYI G E,WU R M,WOOD M,etal.Protocol:a highly sensitive RT-PCR method for detection and quantification of microRNAs [J].PlantMethods,2007,3:12.
[17] 張惟材,朱 力,王玉飛.實時熒光定量PCR[M].北京:化學工業出版社,2013:14-15.
ZHANG W C,ZHU L,WANG Y F.Real-time Quantitative PCR [M].Beijing:Chemical Industry Press,2013:14-15.
[18]FAHLGREN N,HOWELL M D,KASSCHAU K D,etal.High-throughput sequencing ofArabidopsismicroRNAs:Evidence for frequent birth and death of MIRNA genes [J].PLoSOne,2007,2:e219.
[19]ALTSCHUL S F,MADDEN T L,SCHFFER A A,etal.Gapped BLAST and PSI BLAST:A new generation of protein database search programs [J].NucleicAcidsResearch,1997,25(17):3389.
[20]DENG Y Y,LI J Q,WU S F,etal.Integrated nr database in protein annotation system and its localization [J].ComputerEngineering,2006,32(5):71.
[21]APWEILER R,BAIROCH A,WU C H,etal.UniProt:The universal protein knowledgebase [J].NucleicAcidsResearch,2004,32:115.
[22]DAI X B,ZHUANG Z H,ZHAO P X.psRNATarget:A plant small RNA target analysis server(2017 update)[DB/OL].http://plantgrn.noble.org/ psRNATarget/home.
[23]STEWART C,KON T,ROJAS M,etal.Mixed infection ofSidajamaicensisin Jamaica reveals the presence of three recombinant begomovirus DNA A components [J].ArchivesofVirology,2014,15(9):2509.
[24]MARIO A V,JUAN C P,JEAN P V C.A family of microRNAs present in plants and animals [J].ThePlantCell,2006,18(12):3355.
[25]ZHANG L,CHIA J M,KUMARI S,etal.A genome-wide characterization of microRNA genes in maize [J].PLoSGenetics,2009,5:e1000716.
[26]SCHREIBER A W,SHI B J,HUANG C Y,etal.Discovery of barley miRNAs through deep sequencing of short reads [J].BMCGenomics,2011,12:129.
[27] 劉卓琦,萬福生,羅達亞.miRNA靶基因的篩選方法及其相關網絡資源[J].中國生物化學與分子生物學報,2015,31(2):122.
LIU Z Q,WAN F S,LUO D Y.Methods and their online resources for miRNA targets screening [J].ChineseJournalofBiochemistryandMolecularBiology,2015,31(2):122.
[28]ZHANG B H,PAN X P,WANG Q L,etal.Identification and characterization of new plant microRNAs using EST analysis [J].CellResearch,2005,15(5):336.
[29]KOHLI D,JOSHI G,DEOKAR A A,etal.Identification and characterization of wilt and salt stress-responsive microRNAs in chickpea through high-throughput sequencing [J].PLoSOne,2014,9(10):e108851.
DifferentialExpressionAnalysisofDrought-ResponsiveMicroRNAandPredictionofTheirTargetGenesinAgropyronmongolicumatSeedlingStage
MAYanhong,ZHANGXuting,YUXiaoxia,LIUXuting,GAOHui,YUZhuo
(Agronomy College,Inner Mongolia Agricultural University,Hohhot,Inner Mongolia 010019,China)
時間:2017-09-13
網絡出版地址:http://kns.cnki.net/kcms/detail/61.1359.S.20170913.1138.010.html
S512.9;S330
A
1009-1041(2017)09-1168-07
2017-01-28
2017-07-18
國家自然科學基金項目(31360573)
E-mail:mayanhong80@126.com
于 卓(E-mail:yuzhuo58@sina.com)

