例析中考化學溶液配制的考查方式
張峰

配制一定溶質質量分數的溶液一直是中考的熱點,主要考查實驗步驟、儀器的選擇及數據的分析,明確導致所配溶液的質量分數偏大或偏小的原因,常見題型為選擇題和實驗題。
一、考查對所需儀器的選擇
例1實驗室用氯化鈉固體配制質量分數為6%的氯化鈉溶液,不需要用到的儀器是()。
A.燒杯B.量筒C.集氣瓶D.托盤天平
解析實驗室用氯化鈉固體配制質量分數6%的氯化鈉溶液,燒杯用于完成溶解操作,量筒用于準確量取水,托盤天平用于稱取固體氯化鈉,不需要使用集氣瓶。
答案:C
點評實驗室用固體配制一定質量分數的溶液需要的儀器主要有:托盤天平、燒杯、玻璃棒、藥匙、量筒、膠頭滴管等。
二、考查實驗操作
例2在“配制一定溶質質量分數的氯化鈉溶液”實驗中,圖1所示操作正確的是()。
圖1
A.甲圖表示稱取7.5g氯化鈉
B.乙圖表示量取42.5mL水
C.丙圖表示溶解氯化鈉
D.丁圖表示向試劑瓶中轉移溶液
解析托盤天平的使用要遵循“左物右碼”的原則,圖中所示操作砝碼與藥品位置放反了,A錯誤;量取42.5mL水,應該選用量筒,而不能用燒杯,B錯誤;溶解時,在燒杯中進行,并用玻璃棒進行攪拌,C正確;向試劑瓶中轉移溶液時,瓶塞要倒放,瓶口要緊挨,D錯誤。
答案:C
點評實驗室用固體配制一定質量分數的溶液操作步驟一般為:①計算(溶質的質量、溶劑的質量),②稱量(用托盤天平稱量所需溶質的質量、用量筒和膠頭滴管量取所需溶劑的體積),③溶解(將溶劑倒入裝有溶質的燒杯中,并用玻璃棒攪拌),④裝瓶(將溶液裝入貼有試劑名稱和溶質質量分數標簽的試劑瓶中,塞好瓶塞,放到指定地點)。
三、考查相關計算
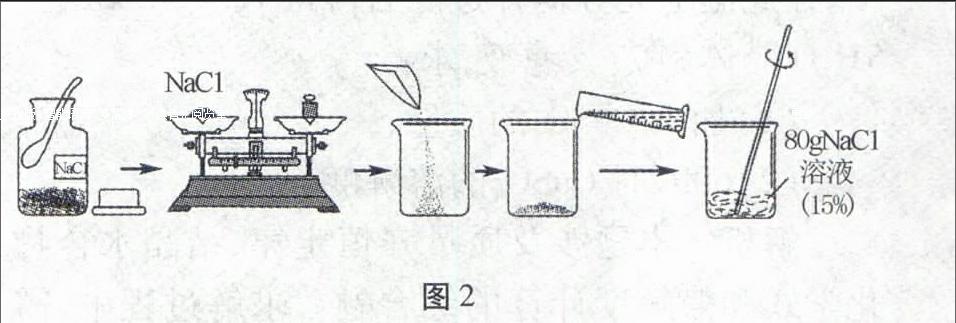
例3圖2所示是實驗室配制一定溶質質量分數的氯化鈉溶液的流程。
圖2
請根據示意圖回答:
(1)托盤天平左盤中固體氯化鈉的質量為g,量筒中水的體積為mL;
(2)上述溶液取10g加水40g進行稀釋,所得氯化鈉溶液的溶質質量分數是。
解析(1)溶質質量=溶液質量×溶質的質量分數,配制15%的氯化鈉溶液80g,需氯化鈉的質量=80g×15%=12g;溶劑質量=溶液質量-溶質質量,則所需蒸餾水的質量=80g-12g=68g(合68mL);(2)溶液稀釋前后溶質的質量不變,上述溶液取10g加水40g進行稀釋,所得氯化鈉溶液的溶質質量分數是10 g×15%10 g+40 g×100%=3%。
答案:(1)1268(2)3%
點評實驗室配制一定質量分數的溶液過程中的主要計算公式有:①溶質質量=溶液質量×溶質的質量分數,②溶劑質量=溶液質量-溶質質量,③濃溶液質量×濃溶液溶質的質量分數=稀溶液質量×稀溶液溶質的質量分數。
四、考查對實驗結果的分析
例4在配制一定溶質質量分數的蔗糖溶液時,導致溶液中蔗糖的質量分數偏大的可能原因有()。
A.用量筒量取水時俯視讀數
B.用來配制溶液的燒杯剛用少量蒸餾水潤洗過
C.用托盤天平稱取蔗糖時,將蔗糖放在右盤,且稱量時使用了游碼
D.用了含少量雜質的蔗糖配制溶液
解析用量筒量取水時,俯視讀數,讀數比實際液體體積大,會造成實際量取的水的體積偏小,則使溶質質量分數偏大,A正確;用來配制溶液的燒杯剛剛用少量蒸餾水潤洗過,會造成實際量取的水的體積偏大,則使溶質質量分數偏小,B錯誤;用托盤天平稱取蔗糖時,將蔗糖放在右盤,且稱量時使用了游碼,會造成實際所取的溶質的質量偏小,則使溶質質量分數偏小,C錯誤;用了含少量雜質的蔗糖配制溶液,會導致溶質的質量小于配制所需要的溶質質量,引起質量分數偏小,D錯誤。
答案:A
點評解答溶液配制過程中的誤差分析時,要從溶質質量分數的概念入手,即分析在實驗操作中溶質的質量和溶劑的質量是否發生改變,由此判斷溶質質量分數是否發生變化。
(收稿日期:2017-01-10)endprint

