殼聚糖磷酸酯糖用澄清劑的制備及結構表征
宋小榮,任勤,范松林,張佳欣,梁欣泉
(廣西大學輕工與食品工程學院,南寧 530004)
殼聚糖磷酸酯糖用澄清劑的制備及結構表征
宋小榮,任勤,范松林,張佳欣,梁欣泉*
(廣西大學輕工與食品工程學院,南寧 530004)
殼聚糖具有較好的吸附性、成膜性、成纖性、吸濕性及生物相溶性等,對殼聚糖進行磷酸化改性,制備殼聚糖磷酸酯(PCTS),改善水溶性,并將其應用于甘蔗混合汁澄清,以清汁色值和純度差為考核指標,采用單因素和正交試驗探索殼聚糖磷酸酯制備的最佳工藝條件,利用掃描電鏡(SEM)、傅立葉紅外變換光譜儀(FT-IR)對其進行結構表征。實驗表明:微波合成殼聚糖磷酸酯制備的最佳工藝條件為微波功率260 W,微波時間9 min,m(CH2O)∶m(殼聚糖)為1∶1,m(H3PO4)∶m(殼聚糖)為3.2∶1,處理混合汁后清汁純度提高2.97%,色值為756.52 IU。與傳統亞硫酸法澄清效果對比發現,PCTS澄清效果得到的清汁色值與純度差均有所提高,認為PCTS能夠代替SO2用于蔗汁無硫澄清生產。
殼聚糖磷酸酯;蔗汁;色值;純度差
白砂糖是國家戰略物資,制糖業作為廣西的支柱性產業,其廣西白砂糖產量約占全國總產量的60%以上。全國約90%以上的甘蔗糖廠采用亞硫酸法澄清工藝[1],但此法存在諸多問題,如白砂糖中殘留的部分SO2,不能滿足醫藥和高端食品的需求;隨著儲存時間的延長,白砂糖出現發黃、潮解現象等。因此,研究探索新的澄清劑及工藝對提高白砂糖質量,提高我國白砂糖國際競爭力至關重要。近年來,已有不少專利介紹了新型的澄清技術,包括磷酸上浮工藝、煙道氣二氧化碳、復合酶制劑澄清劑等[2-4],相關文獻也描述了多種澄清劑應用于制糖行業,均取得一定效果。目前,無硫澄清工藝極具吸引力,已成為我國制糖行業的研究熱點,具有廣闊的研究前景。
殼聚糖化學穩定性良好,吸濕性較強,遇水易分解;無毒無害,具有優良的生物相溶性,可被溶菌酶等溶解[5],可生物降解,其代謝產物無毒,且能被生物體完全吸收,但其溶解性能大大限制了其應用范圍。殼聚糖分子中含有氨基、羥基,活性較高,可利用化學方法在這些基團上引入其他化學鍵,即通過改性,改善殼聚糖衍生物物理化學性質,提高水溶性和機械強度,使其在溶液中的構象發生改變,表現出利于吸附絮凝的構象,并伴隨著吸附選擇性的提高,吸附量增大,絮凝效果較好,進而擴大應用范圍。
本文將殼聚糖進行磷酸化改性得到的殼聚糖磷酸酯(PCTS)屬于水溶性殼聚糖,與殼聚糖相比,其溶解性能有所改善,且吸附性能、可降解性能均得到提高。該研究以其對甘蔗混合汁澄清后的清汁色值、純度差為指標,通過條件優化,制備出適用于混合汁澄清的澄清劑殼聚糖磷酸酯。同時采用掃描電鏡(SEM)、傅立葉紅外變換光譜儀(FT-IR)對其進行結構表征及性能分析[6]。
1 材料與方法
1.1 材料、試劑與儀器
1.1.1 材料與試劑
甘蔗混合汁(采樣于廣西某糖廠);殼聚糖(工業級,實驗室測定脫乙酰度78%,上海西寶生物科技有限公司);乙酸(AR)、甲醛(AR)、磷酸(AR)、乙醇(AR)、鹽酸(AR)、NaOH(AR)。
1.1.2 主要儀器
101-2S型數顯式電熱恒溫干燥箱 上海滬越實驗儀器有限公司;WD900ATL23-2電腦型燒烤微波爐廣東Ganlanz公司;501A型超級恒溫器 上海實驗儀器廠有限公司;PHSJ-4A型酸度計 上海雷磁儀器廠;HJ-J多功能攪拌器 常州國華電器有限公司;日立S-3400N型掃描電鏡 日本日立電子有限公司;FT-IR傅立葉紅外光譜儀 美國Perkin Elmer公司;噴霧干燥器(產地);精密天平 上海梅特勒-托利多儀器有限公司。
1.2 殼聚糖磷酸酯的主要制備過程
殼聚糖磷酸酯主要采用微波反應[7],主要過程為:將適量殼聚糖溶于1%乙酸溶液,按比例添加濃度為40%的甲醛溶液、50%的磷酸溶液,待溶液混合均勻后,放入微波反應器中,設置微波功率、微波時間,反應結束后,將反應液冷卻至室溫,加入乙醇溶液,充分攪拌后,轉入離心瓶中,5000 r/min離心10 min,棄去上清液,將沉淀用蒸餾水溶解后再次加入乙醇溶液,待沉淀充分析出后,將含有析出物的混合液使用噴霧干燥法干燥,收集噴出物即得到產物殼聚糖磷酸酯,其主要工藝流程見圖1。

圖1 殼聚糖磷酸酯制備過程Fig.1 The preparation process of chitosan phosphate
1.3 殼聚糖磷酸酯的制備工藝實驗
1.3.1 制備工藝單因素試驗
通過單因素試驗考察甲醛、磷酸添加比例、微波功率、微波時間對制備的殼聚糖磷酸酯澄清效果的影響,將所制備出的產物對甘蔗混合汁進行澄清處理,并以澄清后的清汁色值(ΔIU)和純度差(ΔG.P.)為評定指標,以此來評定殼聚糖磷酸酯的最佳制備工藝條件。
1.3.2 制備工藝條件的優化
在單因素試驗的基礎上,采用L9(34)四因素三水平進行正交試驗[8,9],并以殼聚糖磷酸酯對甘蔗混合汁澄清的清汁色值和純度差為評價指標,優化殼聚糖磷酸酯的制備工藝條件,因素水平表見表1。
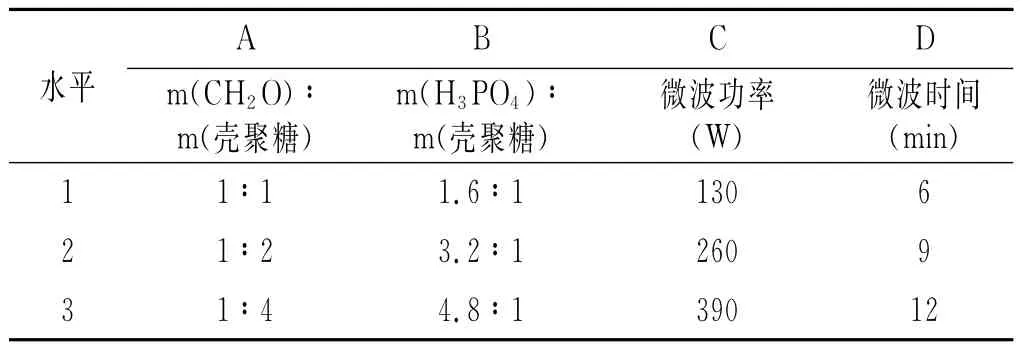
表1 四因素三水平正交試驗設計表Table 1 Design table of four-factor three-level orthogonal test
1.3.3 殼聚糖磷酸酯對甘蔗混合汁的澄清實驗
將1.2制備得到的產物溶于蒸餾水配制成適當濃度的溶液,采用圖2的步驟處理混合汁,此過程主要考察甲醛、磷酸添加比例、微波功率、微波時間對制備的殼聚糖磷酸酯澄清效果的影響,主要考核指標為純度差、清汁色值。
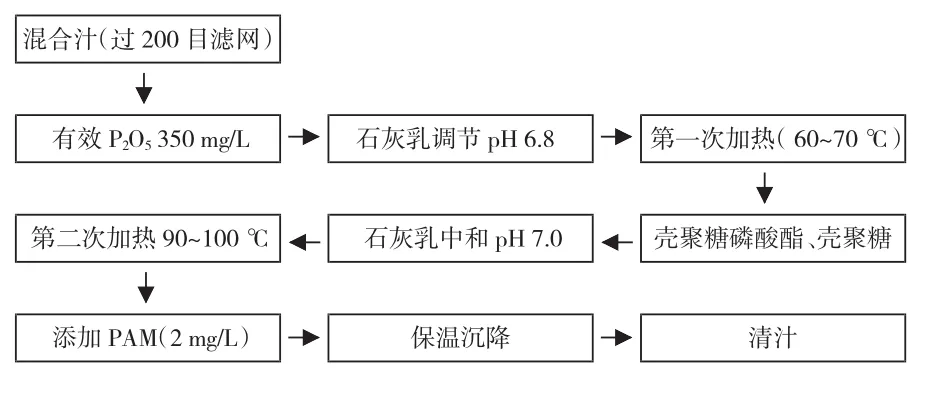
圖2 殼聚糖磷酸酯澄清甘蔗混合汁工藝流程圖Fig.2 The process flow diagram of chitosan phosphate clarifying sugarcane mixed juice
1.3.4 純度、色值的測定與計算
甘蔗混合汁與清汁的純度差、色值的測定與計算參照文獻[10]。
純度差的計算:
ΔG.P.=清汁的重力純度-混合汁的重力純度。
1.4 電鏡掃描(SEM)分析
選取最佳工藝制備的殼聚糖磷酸酯糖用澄清劑,用掃描電子顯微鏡對其進行表面掃描,觀察殼聚糖磷酸酯表面形貌情況,對原殼聚糖樣品進行掃描電鏡分析,以做對比分析。
1.5 傅里葉紅外光譜分析
將殼聚糖磷酸酯和殼聚糖進行壓片處理后,進行FT-IR掃描,分析其基團結構,得出制備的殼聚糖磷酸酯的基本結構。
2 結果與討論
2.1 單因素試驗結果
2.1.1 甲醛添加比例對澄清效果的影響
固定磷酸與殼聚糖m(H3PO4)∶m(殼聚糖)的添加比例為3.2∶1,微波功率130 W,微波時間9 min,考察甲醛與殼聚糖m(CH2O)∶m(殼聚糖)的添加比例為1∶1,3∶1,5∶1,7∶1,9∶1時,分別探究對試驗產生的影響,試驗結果見圖3。
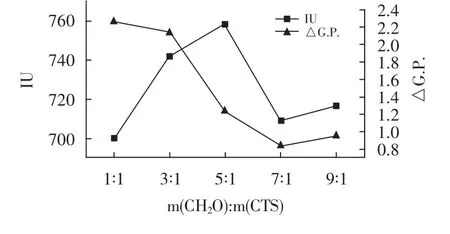
圖3 甲醛添加比例對澄清效果的影響Fig.3 Effect of formaldehyde additive ratio on clarification effect
由圖3可知,在不同甲醛配比下制備的殼聚糖磷酸酯澄清混合汁時,當甲醛量增加時,清汁純度逐步降低,色值先增加后減小,當m(CH2O)∶m(殼聚糖)為1∶1時,制備的殼聚糖磷酸酯處理混合汁,色值最低為700 IU,純度差最高為2.27%,澄清效果最佳,故選取最佳甲醛添加量為m(CH2O)∶m(殼聚糖)為1∶1。
2.1.2 磷酸添加量對澄清效果的影響
固定甲醛與殼聚糖m(CH2O)∶m(殼聚糖)的添加比例為1∶1,微波功率130 W,微波時間9 min,考察磷酸與殼聚糖m(CH2O)∶m(殼聚糖)的添加比例分別為1∶1,3∶1,5∶1,7∶1,9∶1時,探究5個磷酸比例各自對實驗產生的影響,試驗結果見圖4。

圖4 磷酸添加比例對澄清效果的影響Fig.4 Effect of phosphoric acid additive ratio on clarification effect
由圖4可知,在不同磷酸配比下制備的殼聚糖磷酸酯處理甘蔗混合汁時,清汁純度隨著磷酸量的增加呈現先增加后減小的趨勢,而清汁色值隨著磷酸量的增加逐步增大,而在m(H3PO4)∶m(殼聚糖)為3.2∶1時,清汁純度最高,純度差為2.46%,色值較低為839.29 IU,綜合考慮,選取磷酸與殼聚糖添加量:m(H3PO4)∶m(殼聚糖)為3.2∶1。
2.1.3 微波功率對澄清效果的影響
固定甲醛與殼聚糖m(CH2O)∶m(殼聚糖)的添加比例為1∶1,磷酸與殼聚糖m(H3PO4)∶m(殼聚糖)的添加比例為3.2∶1,微波時間9 min,考察微波功率為130,260,390,420,650 W時,對試驗產生的影響,實驗結果見圖5。
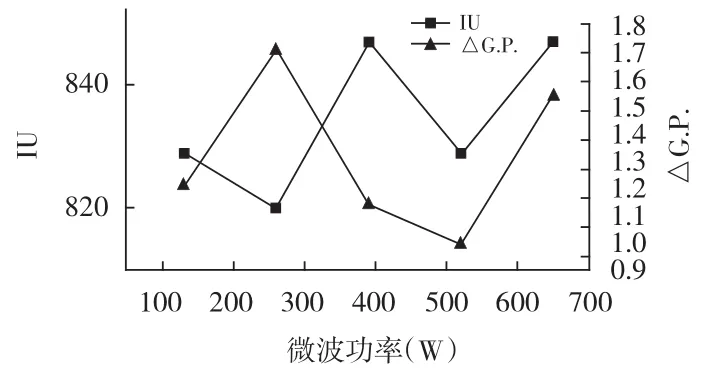
圖5 微波功率對澄清效果的影響Fig.5 Effect of microwave power on clarification effect
由圖5可知,當控制微波功率制備的殼聚糖磷酸酯處理甘蔗混合汁時,澄清效果有所不同,無明顯規律,在微波功率為260 W時,清汁色值最低為819.82 IU,純度最高,純度差為1.7%,故最佳微波功率為260 W。
2.1.4 微波時間對澄清效果的影響
固定甲醛與殼聚糖m(CH2O)∶m(殼聚糖)添加比例為1∶1,磷酸與殼聚糖m(H3PO4)∶m(殼聚糖)添加比例為3.2∶1,微波功率為260 W,考察微波時間為6,9,12,15,18 min時,對試驗產生的影響,實驗結果見圖6。
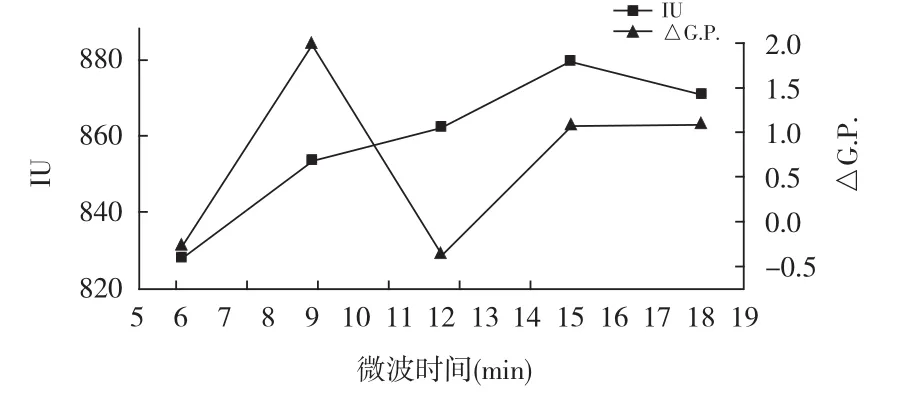
圖6 微波時間對澄清效果的影響Fig.6 Effect of microwave time on clarification effect
由圖6可知,控制微波時間制備的殼聚糖磷酸酯處理甘蔗混合汁效果存在顯著差異,隨著微波時間的延長,清汁色值逐步增加,清汁純度無明顯規律,當微波時間為9 min時,清汁純度最高,純度差為1.98%,而色值為827.59 IU,與6 min時相比,增加幅度不大,綜合考慮,選取微波時間為9 min。
2.2 殼聚糖磷酸酯制備工藝條件的優化結果

表2 正交試驗結果Table 2 The results of orthogonal test
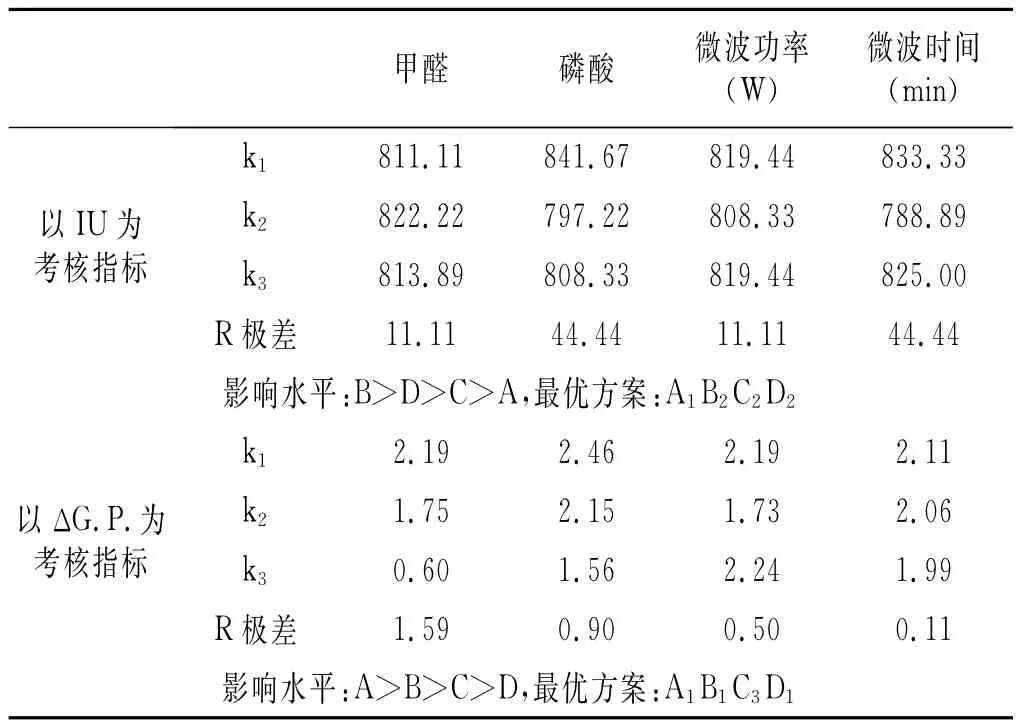
表3 正交結果極差分析Table 3 The range analysis of orthogonal results
由表2和表3可知,以清汁色值為考核指標,得到最優試驗方案:m(CH2O)∶m(殼聚糖)為1∶1,m(H3PO4)∶m(殼聚糖)為3.2∶1,微波功率260 W,微波時間9 min;以純度差為考核指標,得到最優試驗方案:m(CH2O)∶m(殼聚糖)為1∶1,m(H3PO4)∶m(殼聚糖)為1.6∶1,微波功率390 W,微波時間6 min。考慮到殼聚糖與磷酸的充分反應,將磷酸添加量定為m(H3PO4)∶m(殼聚糖)為1.6∶1,而考慮到反應耗能,將微波功率定為260 W,微波時間定為9 min。
將最佳制備條件下制備的殼聚糖磷酸酯用于混合汁的澄清,通過3次平行實驗,得到最終實驗結果,清汁純度提高2.97%,清汁色值為756.52 IU。
2.3 殼聚糖和殼聚糖磷酸酯的電鏡掃描(SEM)表征分析
殼聚糖和殼聚糖磷酸酯放大倍數(8000倍)的電鏡掃描SEM圖見圖7。

圖7 殼聚糖和殼聚糖磷酸酯的電鏡掃描(SEM)圖(×8000)Fig.7 SEM photograph of chitosan and chitosan phosphate(×8000)
由圖7可知,殼聚糖改性后微觀形態發生了較大變化。未改性的殼聚糖為無規則形態,表面粗糙,有較多褶皺,呈現凹凸狀。改性后的殼聚糖磷酸酯呈較規則的圓球狀,相同放大倍數下,可以看到單個殼聚糖磷酸酯顆粒體積變小,且大小不一,表面有褶皺凸起。規則的圓球狀可能與干燥方法有關,本實驗干燥方法采用的是噴霧干燥法,顆粒體積變小可能是微波反應使殼聚糖大分子結構發生斷裂,顆粒表面凸起說明殼聚糖分子中引入了磷酸基團。
2.4 殼聚糖磷酸酯FT-IR圖譜分析[11]
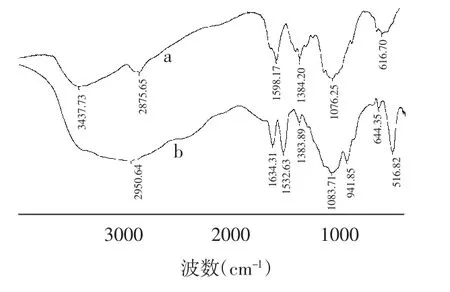
圖8 殼聚糖(a)與殼聚糖磷酸酯(b)FT-IR曲線比較圖Fig.8 Curve comparison diagram of chitosan(a)and chitosan phosphate(b)on FT-IR
由圖8可知,在4000~500 cm-1范圍內,殼聚糖磷酸酯的吸收峰與殼聚糖大致類似,同時也存在較多差異。
3437 cm-1處是形成氫鍵締合的-OH伸縮振動吸收峰與-NH2的伸縮振動吸收峰重疊的多重吸收峰[12]。
在2875 cm-1處為C-H的伸縮振動吸收峰[13];
1654 cm-1是酰胺彎曲振動吸收峰,根據這2個峰的大小可以判定殼聚糖的脫乙酰化程度。因本實驗所用殼聚糖脫乙酰度為78%,故1654 cm-1處的吸收峰相對較小;
1598 cm-1是氨基(-NH2)伸縮振動峰;
殼聚糖紅外光譜中1384 cm-1是-CH2-的彎曲振動特征峰;
殼聚糖紅外光譜中1076 cm-1是醇羥基特征峰;
殼聚糖紅外光譜中616cm-1譜帶處于指紋區,無法判斷其結構;
殼聚糖磷酸酯的紅外圖譜與殼聚糖相比,變動較大:3437 cm-1,2875 cm-1處的C-H的伸縮振動吸收發生位移,出現了2950 cm-1新的吸收峰,說明在殼聚糖的羥基、氨基上發生了反應。1598 cm-1處的強氨基吸收峰消失,1634 cm-1處的振動峰明顯增強,在1532 cm-1處出現了新的強吸收峰[14]。同時,1076 cm-1處的醇羥基特征峰消失,在941 cm-1,1083 cm-1處出現2個明顯強吸收峰,這可能是因為-OH上的氫原子被P所取代,變成了P-O鍵的特殊伸縮振動和彎曲振動吸收峰,說明殼聚糖磷酸化反應中磷酸基團成功地引入了殼聚糖分子中。
3 結論
對殼聚糖進行磷酸化改性,制備殼聚糖磷酸酯(PCTS),以清汁色值和純度差為考核指標,通過單因素實驗及正交實驗優化制備工藝,最終確立殼聚糖磷酸酯糖用澄清劑最佳制備工藝:m(CH2O)∶m(殼聚糖)為1∶1,m(H3PO4)∶m(殼聚糖)為3.2∶1,微波功率為260 W,微波時間為9 min,處理混合汁后清汁純度提高2.97%,色值為756.52 IU。與亞法澄清生產工藝相比,認為殼聚糖磷酸酯可以取代SO2作為糖用澄清劑。
通過SEM和FT-IR分析,確定改性后的殼聚糖發生了磷酸化反應,反應產物為殼聚糖磷酸酯。改性后的殼聚糖磷酸酯改善了水溶性,將其應用于甘蔗混合汁的澄清,清汁的純度差、色值等得到明顯改善,澄清效果明顯優于傳統亞硫酸法。本研究為探索無硫工藝新澄清劑提供理論和實踐依據[15]。
[1]梁欣泉,何惠歡,謝志榮,等.季銨化殼聚糖糖用澄清劑的制備及結構表征[J].廣西大學學報(自然科學版),2014(3):544-551.
[2]鐘偉,岑躍,王銳.磷酸上浮工藝技術的應用[J].廣西輕工業,2001(1):48-51.
[3]凌國士,郭光海,余華,等.國內亞硫酸法蔗糖生產除雜澄清工藝中的酶制劑應用研究進展[J].輕工科技,2016(12):23-27.
[4]董毅宏,黃世釗,何華柱,等.糖廠鍋爐煙道氣二氧化碳的富集及其在亞硫酸法制糖澄清工藝的應用[J].廣西大學學報(自然科學版),2009(5):631-634.
[5]馬如,黃明智.殼聚糖的溶菌酶降解[J].北京化工大學學報(自然科學版),2002,29(6):40-43.
[6]Amaral I F,Granja P L,Barbosa M A.Chemical modification of chitosan by phosphorylation:an XPS,FT-IR and SEM study[J].Journal of Biomaterials Science Polymer Edition,2005,16(12):1575-1593.
[7]謝志榮.糖用改性殼聚糖澄清劑的制備及其應用工藝研究[D].南寧:廣西大學,2011.
[8]李利華.正交試驗法優化超聲輔助提取大蒜多糖工藝[J].中國調味品,2014,39(7):70-73.
[9]王勇,賴偉勇,魏娜,等.單因素和正交試驗法優選檸檬草油超臨界CO2萃取條件[J].海南醫學院學報,2012(3):305,307,309.
[10]李墉,鄭長庚.甘蔗制糖化學管理分析方法[M].廣州:中國輕工總會甘蔗糖業質量監督檢測中心,1995:27-53.
[11]Vineet Bhardwaj,Vikesh Shukla,Narendra Goyal,et al.Formulation and evaluation of different concentration chitosan based periodontal film of ofloxacin[J].Journal of Pharmacy Research,2010,2(3):528-532.
[12]許海峰,周建,波曾.N-亞甲基磷酸殼聚糖有機錫酯的合成、表征及殺螺活性研究[J].精細化工中間體,2011(4):24-28.
[13]趙國駿,姜涌明,孫龍生,等.不同來源殼聚糖的基本特性及紅外光譜研究[J].功能高分子學報,1998(3):403-407.
[14]Varma H K,Yokogawa Y,Espinosa F F,et al.Porous calcium phosphate coating over phosphorylated chitosan film by a biomimetic method[J].Biomaterials,1999,20(9):879-884.
[15]何惠歡,謝志榮,劉繼棟,等.羧甲基殼聚糖糖用澄清劑的制備及結構表征[J].食品工業科技,2015(6):117-121.
Preparation and Structural Characterization of Chitosan Phosphate as Sugarcane Juice Clarifying Agent
SONG Xiao-rong,REN Qin,FAN Song-lin,ZHANG Jia-xin,LIANG Xin-quan*
(College of Light Industry and Food Engineering,Guangxi University,Nanning 530004,China)
Chitosan has good properties of adsorption,film-forming,fiber-forming,hygroscopicity and biocompatibility.Chitosan is phosphorylated to prepare chitosan phosphate(PCTS).PCTS can improve the water solubility,and it is applied for the clarification of sugarcane mixed juice.With the analysis of orthogonal test,the optimum conditions for the preparation of PCTS are explored by color value and purity difference.The structure is characterized by scanning electron microscope(SEM)and fourier transform infrared spectrum(FT-IR).The results show that under the treatment of microwave power of 260 W,treatment time of 9 min,m(CH2O)∶m(chitosan)of 1∶1 and m(H3PO4)∶m(chitosan)of 3.2∶1,the clarification effect of PCTS is better.The purity difference of clear juice is increased by 2.97%,and the color value is 756.52 IU.Compared with the traditional sulfuric acid method,the clarification effect of PCTS is higher than the traditional sulfuric acid method.The results indicate that PCTS could replace SO2in sugarcane juice clarification to explore the sulfur-free clarification process.
chitosan phosphate;sugarcane juice;color value;puritydifference
TS246.4
A
10.3969/j.issn.1000-9973.2017.10.006
1000-9973(2017)10-0023-06
2017-05-15 *通訊作者
糖蜜酒精精餾過程節能技術開發及應用示范(AE120094);廣西區特色本科專業建設項目——食品科學與工程(制糖工程)
宋小榮(1994-),女,重慶人,碩士,研究方向:糖品過程強化理論與技術;梁欣泉(1966-),男,廣西南寧人,教授,博士,研究方向:糖品過程強化理論與技術。

