生物鐘的秘密——2017年諾貝爾生理學(xué)或醫(yī)學(xué)獎(jiǎng)簡(jiǎn)介
李禹正 張 婷 王曉民,3*
(1.首都醫(yī)科大學(xué)長(zhǎng)學(xué)制臨床醫(yī)學(xué)專業(yè), 北京 100069;2.首都醫(yī)科大學(xué)基礎(chǔ)醫(yī)學(xué)院神經(jīng)生物學(xué)系, 北京 100069;3 北京腦重大疾病研究院, 北京 100069)
·諾貝爾獎(jiǎng)·
生物鐘的秘密——2017年諾貝爾生理學(xué)或醫(yī)學(xué)獎(jiǎng)簡(jiǎn)介
李禹正1張 婷2王曉民2,3*
(1.首都醫(yī)科大學(xué)長(zhǎng)學(xué)制臨床醫(yī)學(xué)專業(yè), 北京 100069;2.首都醫(yī)科大學(xué)基礎(chǔ)醫(yī)學(xué)院神經(jīng)生物學(xué)系, 北京 100069;3 北京腦重大疾病研究院, 北京 100069)
北京時(shí)間2017年10月2日,瑞典卡羅琳斯卡醫(yī)學(xué)院在斯德哥爾摩宣布,將2017年諾貝爾生理學(xué)或醫(yī)學(xué)獎(jiǎng)授予美國(guó)科學(xué)家Jeffrey C. Hall,Michael Rosbash以及Michael W. Young,以表彰他們?cè)凇吧锕?jié)律的分子機(jī)制”方面的發(fā)現(xiàn)。
2017諾貝爾生理學(xué)或醫(yī)學(xué)獎(jiǎng);生物鐘;晝夜節(jié)律
地球上的所有生命都需要適應(yīng)地球的自轉(zhuǎn)。所有的生命體,包括人類,都有一個(gè)體內(nèi)的“時(shí)鐘”,使我們能夠適應(yīng)晝夜變換,調(diào)節(jié)生命活動(dòng)。但這個(gè)生物鐘到底是如何工作的?Jeffrey C. Hall、Michael Rosbash和 Michael W. Young三人對(duì)生物鐘的分子機(jī)制進(jìn)行了研究。他們的研究成果揭示了植物、動(dòng)物以及人類如何保持自身的生物節(jié)律,適應(yīng)環(huán)境變化。
1971年,Seymour Benzer和Ronald Konopka在果蠅體內(nèi)發(fā)現(xiàn)了一種與生物鐘調(diào)節(jié)相關(guān)的基因——period。十年后,Jeffrey C. Hall、Michael Rosbash和 Michael W. Young成功克隆出period基因。但在當(dāng)時(shí),period調(diào)節(jié)生物鐘的具體機(jī)制仍是一個(gè)謎題。經(jīng)過3位諾貝爾獎(jiǎng)得主的不懈努力,隨著與period相互作用的其他基因的發(fā)現(xiàn),科學(xué)家們提出了轉(zhuǎn)錄翻譯負(fù)反饋回路(transcription-translation feedback loop, TTFL)的概念,即period以及另一個(gè)生物鐘基因-timeless的轉(zhuǎn)錄會(huì)被它們自身翻譯出的蛋白-PER和TIM所抑制。該機(jī)制和隨后發(fā)現(xiàn)的一些更加復(fù)雜的分子機(jī)制共同調(diào)節(jié)著生物鐘的生理功能。
我們體內(nèi)的生物鐘在一天之中的不同時(shí)段對(duì)我們的生理功能進(jìn)行著精準(zhǔn)的調(diào)節(jié),例如行為、激素水平、睡眠情況、體溫以及新陳代謝等。當(dāng)我們所處的外部環(huán)境與我們體內(nèi)的生物鐘不匹配時(shí),我們的身體就會(huì)馬上反應(yīng)出不適,比如乘飛機(jī)穿越數(shù)個(gè)時(shí)區(qū)所導(dǎo)致的“時(shí)差”。此外,有跡象表明,當(dāng)我們的生活方式與生物鐘開始出現(xiàn)偏差時(shí),我們患上各種疾病的風(fēng)險(xiǎn)也會(huì)隨之增加。Jeffrey C. Hall、Michael Rosbash和 Michael W. Young三位科學(xué)家的發(fā)現(xiàn)闡釋了生物節(jié)律的重要生理機(jī)制,為人類健康及疾病研究提供了重要的依據(jù)。
1 獲獎(jiǎng)?wù)吆?jiǎn)介
1.1JeffreyC.Hall
Jeffrey C. Hall(圖1),1945年3月3日生于美國(guó)紐約布魯克林,遺傳學(xué)家。 1971 年獲得西雅圖華盛頓大學(xué)遺傳學(xué)博士學(xué)位,1974年成為Brandeis大學(xué)教員。1984年他和Michael Rosbash的研究小組克隆了果蠅的period基因,這個(gè)基因能夠調(diào)節(jié)果蠅的生物鐘。他們還揭示出該基因所編碼的mRNA和蛋白質(zhì)含量隨晝夜節(jié)律而變化。Hall于2001年入選人文與科學(xué)院院士,2003年入選美國(guó)國(guó)家科學(xué)院院士并獲美國(guó)遺傳學(xué)會(huì)勛章。因?yàn)樵趐eriod基因研究方面的杰出貢獻(xiàn),他于 2009年獲格魯伯神經(jīng)科學(xué)獎(jiǎng),2011年獲路易莎·格羅斯·霍維茨獎(jiǎng),2012年獲蓋爾德納國(guó)際獎(jiǎng),2013年獲得邵逸夫生命科學(xué)及醫(yī)學(xué)獎(jiǎng)。

圖1 Jeffrey C. Hall
1.2MichaelRosbash
Michael Rosbash(圖2),1944年3月7日生于美國(guó)密蘇里州堪薩斯,遺傳學(xué)家。Rosbash是Brandeis大學(xué)教授和Howard Hughes醫(yī)學(xué)研究所的研究員。1984年他和Jeffrey C. Hall的研究小組克隆了果蠅的period基因,1990年提出了生物鐘的轉(zhuǎn)錄翻譯負(fù)反饋回路的概念。他們?cè)诠夡w內(nèi)發(fā)現(xiàn)了period基因、cycle基因和clock基因等。2003 年入選美國(guó)國(guó)家科學(xué)院院士。2013年獲得邵逸夫生命科學(xué)及醫(yī)學(xué)獎(jiǎng)。

圖2 Michael Rosbash
1.3MichaelW.Young
Michael W. Young(圖3),1949年生于美國(guó)佛羅里達(dá)州邁阿密,遺傳學(xué)家、美國(guó)國(guó)家科學(xué)院院士。1975年獲得Texas大學(xué)Austin分校博士學(xué)位,1978年起任Rockefeller大學(xué)教員,后成為該校副校長(zhǎng)。2013 年獲得邵逸夫生命科學(xué)及醫(yī)學(xué)獎(jiǎng)。1984年他的團(tuán)隊(duì)克隆出果蠅的period基因。Young之后的研究還揭示了更多生物鐘相關(guān)基因以及它們的作用機(jī)制。

圖3 Michael W. Young
2 主要科學(xué)貢獻(xiàn)[1]
雖不能草率地說是全部生物,但的確大多數(shù)的生物都可以預(yù)測(cè)并適應(yīng)日常環(huán)境的變化。早在18世紀(jì),法國(guó)天文學(xué)家 Jean-Jacques d’Ortous de Mairan以含羞草屬植物為研究對(duì)象,發(fā)現(xiàn)不管陽光是否存在,葉子都會(huì)維持它們正常的晝夜節(jié)律(圖4)。這個(gè)實(shí)驗(yàn)也被認(rèn)為是生物具有內(nèi)源生物節(jié)律的最早證據(jù)。
隨后,陸續(xù)有其他研究人員發(fā)現(xiàn),不僅植物有這種“內(nèi)部時(shí)鐘”,其他動(dòng)物包括人類都存在這一現(xiàn)象,而這個(gè)“時(shí)鐘”其實(shí)有助于我們?yōu)槿粘;顒?dòng)做好準(zhǔn)備。這種規(guī)律性的適應(yīng)就被稱為“晝夜節(jié)律”(circadian rhythm),源自拉丁文詞匯“circa”(意為“環(huán)繞”)以及dies(意為“一天”)。生物鐘的背后又有著怎樣的生物機(jī)制呢?對(duì)其分子機(jī)制的研究吸引著一代又一代優(yōu)秀的科學(xué)家。

圖4 含羞草的生物鐘現(xiàn)象
含羞草葉子會(huì)在太陽光下張開,夜晚則會(huì)閉合。Jean-Jacques d’Ortous de Mairan通過實(shí)驗(yàn)證實(shí),在持續(xù)黑暗條件下,含羞草葉片的開合現(xiàn)象依然保持著與晝夜周期同樣的節(jié)律性。這表明含羞草屬植物有一個(gè)自主的“鐘表”可以保持一定的生物節(jié)律。
1)period基因的發(fā)現(xiàn)與克隆
20世紀(jì)70年代,Seymour Benzer博士和他的學(xué)生Ronald Konopka證明了某種未知的基因突變擾亂了果蠅的晝夜節(jié)律,他們命名這個(gè)基因?yàn)閜eriod[2],他們利用經(jīng)典的化學(xué)致突變作用誘導(dǎo)基因突變,進(jìn)而觀察果蠅的表型,試圖找出晝夜節(jié)律發(fā)生改變的突變種。經(jīng)過不懈努力,他們分離出3種品系的果蠅:無節(jié)律型、短節(jié)律型(19 h)和長(zhǎng)節(jié)律型(28 h)。他們進(jìn)一步的基因圖譜研究和雜交試驗(yàn)使他們確定了這3個(gè)突變種均為同一基因的不同突變,后來該基因被命名為period基因。20世紀(jì)80年代,Rockefeller大學(xué)的Young和Brandeis大學(xué)的Hall與Rosbash同時(shí)在進(jìn)行著果蠅period基因的克隆。1984年Young和Rosbash兩個(gè)團(tuán)隊(duì)幾乎同時(shí)拿到period基因附近的基因組DNA[3-4]。該段基因可產(chǎn)生4.5kb和0.9kb兩種長(zhǎng)度的mRNA。他們隨后發(fā)現(xiàn)4.5kb mRNA水平具有晝夜變化,其對(duì)應(yīng)基因?yàn)閜eriod基因[5-6]。克隆出基因固然是巨大的成功,但這僅僅意味著研究生物節(jié)律這項(xiàng)工作才剛剛開始。正如同我們?cè)缫淹瓿扇祟惢蚪M測(cè)序,而實(shí)現(xiàn)從基因水平來研究疑難雜癥的發(fā)病機(jī)制并徹底攻克他們,仍有很長(zhǎng)的一段路要走。基因只是工具,真正核心的部分是分子機(jī)制,仍有待闡明。
2)period基因負(fù)反饋調(diào)節(jié)環(huán)路的發(fā)現(xiàn)
一些研究者相繼提出幾個(gè)模型都未能完美地解釋period基因調(diào)節(jié)生物鐘的分子機(jī)制。在成功合成PER蛋白的抗體后,研究者們終于逐漸揭開了PER蛋白作用機(jī)制的神秘面紗。1988年,Rosbash小組發(fā)現(xiàn)period基因編碼的蛋白質(zhì)PER在夜間積累,白天則被降解。即PER蛋白的水平在24 h周期內(nèi)循環(huán)震蕩,而這一循環(huán)周期恰恰與晝夜節(jié)律同步[7]。1990年,Rosbash小組的博士后Paul Hardin通過檢測(cè)果蠅腦內(nèi)的mRNA發(fā)現(xiàn)period基因的mRNA也呈現(xiàn)晝夜變化[8]。有趣的是,periodmRNA水平的峰值出現(xiàn)的時(shí)間要比PER蛋白水平的峰值出現(xiàn)時(shí)間早幾個(gè)小時(shí)[8]。Period的無意義突變使periodmRNA水平的震蕩無法產(chǎn)生,而PER蛋白可以挽救周期性mRNA水平[8]。他們隨即提出了一個(gè)簡(jiǎn)單模型解釋這一現(xiàn)象:period基因轉(zhuǎn)錄、翻譯產(chǎn)生PER蛋白質(zhì)的過程存在著負(fù)反饋調(diào)節(jié),即PER表達(dá)過程中產(chǎn)生的mRNA和蛋白質(zhì)會(huì)影響PER基因自身的轉(zhuǎn)錄過程,這樣就可以形成一個(gè)連續(xù)的循環(huán)周期。換句話說,PER 蛋白進(jìn)入細(xì)胞核結(jié)合到period基因上與之發(fā)揮相互作用進(jìn)而抑制period基因的進(jìn)一步轉(zhuǎn)錄表達(dá),即PER 蛋白可以抑制基因合成自己,這樣就可以形成一個(gè)持續(xù)循環(huán)。這個(gè)模型以一種簡(jiǎn)單并且在生物體中普遍存在的機(jī)制近乎完美地解釋了PER蛋白的晝夜波動(dòng)。但只有在PER蛋白有能力從細(xì)胞質(zhì)進(jìn)入細(xì)胞核這一大前提的存在下,PER才能抑制period基因。Hall和Rosbash的研究能夠證明PER蛋白在夜間會(huì)在細(xì)胞核中積累,但未能成功解釋其進(jìn)入細(xì)胞核的分子機(jī)制。
1994 年,Michael W. Young發(fā)現(xiàn)了第2個(gè)晝夜節(jié)律基因:timeless[9]。timeless可以編碼 TIM蛋白,同樣為正常節(jié)律所需。Young通過實(shí)驗(yàn)完美地解釋了PER進(jìn)入細(xì)胞核的分子機(jī)制[10],他發(fā)現(xiàn) TIM蛋白含量同樣具有晝夜波動(dòng)性,TIM會(huì)結(jié)合到 PER 上,該復(fù)合物可以進(jìn)入細(xì)胞核,從而抑制period基因的活性。這些發(fā)現(xiàn)使我們進(jìn)一步證實(shí)了period負(fù)反饋調(diào)節(jié)環(huán)路的存在及其在生物鐘對(duì)機(jī)體作用過程中所扮演的重要角色。隨著clock基因和cycle基因的發(fā)現(xiàn),period和timeless基因的激活機(jī)制得到了解釋[11]。這兩個(gè)基因產(chǎn)生的蛋白質(zhì)CLK和CYC相互結(jié)合作為轉(zhuǎn)錄因子共同作用于period和timeless基因,激活基因表達(dá)PER和TIM蛋白。隨后有研究表明,TIM和PER蛋白可以抑制CLK的活性。至此,period基因表達(dá)的負(fù)反饋調(diào)節(jié)環(huán)路得到了圓滿的闡釋(圖5A)。
這3位諾貝爾獎(jiǎng)得主的研究闡述了生物鐘的基本理論基礎(chǔ)。在隨后的幾年里,其他一些分子也被發(fā)現(xiàn),進(jìn)一步解釋了生物鐘的機(jī)制和穩(wěn)定性。Young發(fā)現(xiàn)的另外一個(gè)生物鐘基因——doubletime[12],它編碼的DBT 蛋白是一種蛋白激酶,可以通過調(diào)節(jié)PER蛋白的降解進(jìn)而延遲 PER蛋白的積累,解釋了為什么PER蛋白的震蕩的周期會(huì)穩(wěn)定在 24 h左右。20世紀(jì)90年代末,Hall實(shí)驗(yàn)室發(fā)現(xiàn)chryptochrome(cry) 基因通過對(duì)光的調(diào)節(jié)參與果蠅生物鐘的控制[13-15]。光可以激活該基因的產(chǎn)物CRY蛋白并通過促進(jìn)CRY蛋白與TIM蛋白的結(jié)合調(diào)節(jié)TIM蛋白在蛋白酶體中的降解過程。在日照充足的白天,TIM被降解,導(dǎo)致PER易發(fā)生由DBT介導(dǎo)的磷酸化進(jìn)而也發(fā)生降解(圖5B)。
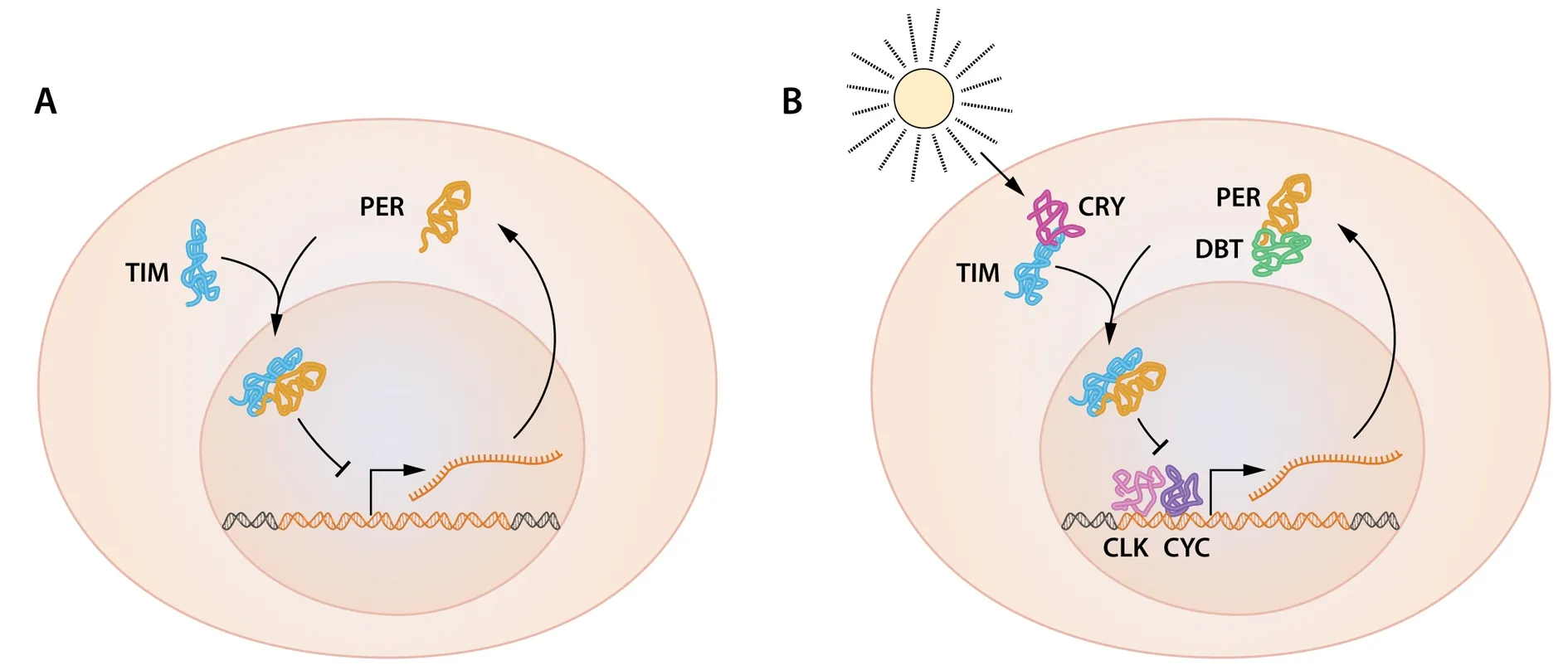
圖5 period基因負(fù)反饋調(diào)節(jié)環(huán)路[1]
A:period基因表達(dá)的mRNA和PER蛋白含量都會(huì)發(fā)生震蕩。PER蛋白在細(xì)胞核內(nèi)通過負(fù)反饋調(diào)節(jié)環(huán)路抑制period基因的表達(dá)。B:許多生物鐘蛋白都可以調(diào)節(jié)period基因的表達(dá)。由timeless基因編碼的TIM蛋白含量也存在一個(gè)震蕩周期并且會(huì)與period基因發(fā)揮作用,TIM蛋白與PER蛋白結(jié)合相互作用對(duì)PER蛋白能否進(jìn)入細(xì)胞核通過負(fù)反饋環(huán)路調(diào)節(jié)period基因的表達(dá)至關(guān)重要。由doubletime基因編碼的DBT蛋白是一種可以磷酸化PER蛋白的蛋白激酶,PER蛋白的磷酸化可導(dǎo)致其降解失活。由DBT蛋白調(diào)節(jié)的PER蛋白的降解最終導(dǎo)致了period表達(dá)的mRNA和PER蛋白聚集的時(shí)間差。由clock基因編碼的CLK和由cycle基因編碼的CYK是兩個(gè)可以激活period表達(dá)的轉(zhuǎn)錄因子。
3)科學(xué)意義
生物鐘涉及人體生理活動(dòng)的方方面面。我們已知的所有多細(xì)胞生物,包括人類,都使用一個(gè)相似的機(jī)制來調(diào)節(jié)生理節(jié)律,例如,生物鐘可以調(diào)節(jié)睡眠模式、進(jìn)食行為、激素釋放、血壓和體溫等(圖6)。生物鐘能調(diào)節(jié)我們大部分的基因,并最終使我們的生理活動(dòng)得以適應(yīng)一天中的不同時(shí)段。不僅如此,生物鐘基因在外周組織中也發(fā)揮重要作用。動(dòng)物模型中敲除生物鐘基因會(huì)導(dǎo)致如皮質(zhì)醇和胰島素等釋放異常[16];生物鐘基因通過影響糖異生、胰島素敏感性以及全身血糖水平來調(diào)節(jié)機(jī)體代謝[17];生物鐘異常導(dǎo)致睡眠障礙會(huì)引起抑郁、認(rèn)知和記憶障礙等神經(jīng)系統(tǒng)疾病[18];如果內(nèi)源性生物鐘異常導(dǎo)致生活方式與生物鐘長(zhǎng)期錯(cuò)位會(huì)增加癌癥、神經(jīng)退變性疾病、代謝性疾病以及炎性反應(yīng)的發(fā)病風(fēng)險(xiǎn)[19]。人們正在努力尋找調(diào)節(jié)生物鐘的手段以改善人類健康。

圖6 生物鐘參與人體生理節(jié)律方方面面的調(diào)節(jié)[1]
生物鐘可以調(diào)節(jié)睡眠模式、進(jìn)食行為、激素釋放、血壓和體溫。我們體內(nèi)大部分基因的表達(dá)都由生物鐘進(jìn)行調(diào)控。
動(dòng)植物的變化只是生物鐘的外在表現(xiàn),而其核心則是復(fù)雜的分子機(jī)制。我們可以很容易地通過鐘表得知時(shí)間,但想要了解其內(nèi)部構(gòu)造,時(shí)針分針的運(yùn)動(dòng)機(jī)制卻是需要一番研究。對(duì)生物鐘的分子機(jī)制研究就好比研究鐘表復(fù)雜的機(jī)芯。就目前來看,對(duì)生物晝夜節(jié)律的研究仍有很長(zhǎng)的路要走。
[1] Scientific Background :Discoveries of Molecular Mechanisms Controlling the Circadian Rhythm[EB/OL] .(2017-10-02)[2017-10-11]https://www.nobelprize.org/nobel_prizes/medicine/laureates/2017/advanced.html
[2] Smith R F, Konopka R J. Effects of dosage alterations at the per locus on the period of the circadian clock of Drosophila[J]. Mol Gen Genet, 1982, 185(1): 30-36.
[3] Zehring W A, Wheeler D A, Reddy P, et al. P-element transformation with period locus DNA restores rhythmicity to mutant, arrhythmic Drosophila melanogaster[J]. Cell, 1984, 39(2): 369-376.
[4] Bargiello T A, Jackson F R, Young M W. Restoration of circadian behavioural rhythms by gene transfer in Drosophila[J]. Nature, 1984, 312(5996): 752-754.
[5] Bargiello T A, Young M W. Molecular Genetics of a Biological Clock in Drosophila[J]. Proc Natl Acad Sci U S A, 1984, 81(7): 2142-2146.
[6] Lorenz L J, Hall J C, Rosbash M. Expression of a Drosophila mRNA is under circadian clock control during pupation[J]. Development, 1989, 107(4): 869-880.
[7] Siwicki K K, Eastman C, Petersen G, et al. Antibodies to the period gene product of drosophila reveal diverse tissue distribution and rhythmic changes in the visual system[J]. Neuron, 1988, 1(2): 141-150.
[8] Hardin P E, Hall J C, Rosbash M. Feedback of the Drosophila period gene product on circadian cycling of its messenger RNA levels[J]. Nature, 1990, 343(6258): 536.
[9] Saez L, Young M W, Baylies M K, et al. Per—no link to gap junctions[J]. Nature, 1992, 360(6404): 542.
[10] Vosshall L B, Price J L, Sehgal A, et al. Block in nuclear localization of period protein by a second clock mutation, timeless[J]. Science, 1994, 263(5153): 1606-1609.
[11] Vitaterna M H, King D P, Chang A M, et al. Mutagenesis and mapping of a mouse gene, Clock, essential for circadian behavior[J]. Science, 1994, 264(5159): 719.
[12] Price J L, Blau J, Rothenfluh A, et al. double-time is a novel Drosophila clock gene that regulates PERIOD protein accumulation[J]. Cell, 1998, 94(1): 83.
[13] Plautz J D, Straume M, Stanewsky R,et al. Quantitative analysis of Drosophila period gene transcription in living animals[J]. J Biol Rhythms, 1997,12(3):204-217.
[14] Stanewsky R, Jamison C F, Plautz J D, et al. Multiple circadian-regulated elements contribute to cycling period gene expression in Drosophila[J]. EMBO J, 1997, 16(16): 5006.
[15] Brandes C, Plautz J D, Stanewsky R, et al. Novel features of drosophila period Transcription revealed by real-time luciferase reporting[J]. Neuron, 1996, 16(4): 687-692.
[16] Son G H, Chung S, Choe H K, et al. Adrenal peripheral clock controls the autonomous circadian rhythm of glucocorticoid by causing rhythmic steroid production[J]. Proc Natl Acad Sci U S A, 2008, 105(52): 20970.
[17] Panda S. Circadian physiology of metabolism[J]. Science, 2016, 354(6315): 1008.
[18] Gerstner J R, Yin J C. Circadian rhythms and memory formation[J]. Na Rev Neurosci, 2010, 11(8): 577-588.
[19] Patke A, Murphy P J, Onat O E, et al. Mutation of the human circadian clock gene CRY1 in familial delayed sleep phase disorder[J]. Cell, 2017, 169(2): 203.
Discoveriesofmolecularmechanismscontrollingthecircadianrhythm—the2017NobelPrizeinPhysiologyorMedicine
Li Yuzheng1, Zhang Ting2, Wang Xiaomin2,3*
(1.ClinicalMedicalSciences,CapitalMedicalUniversity,Beijing100069,China;2.DepartmentofNeurobiology,BasicMedicalSciences,CapitalMedicalUniversity,Beijing100069,China;3BeijingInstituteforBrainDisorders,Beijing100069,China)
In October 2, 2017, the Nobel Assembly at Karolinska Institute has decided to award the 2017 Nobel Prize in Physiology or Medicine jointly to Jeffrey C. Hall, Michael Rosbash and Michael W. Young for their discoveries of molecular mechanisms controlling the circadian rhythm.
the 2017 Nobel Prize in Physiology or Medicine;biological clock;circadian rhythm
*Corresponding authors, E-mail:xmwang@ccmu.edu.cn
時(shí)間: 2017-10-14 16∶19
http://kns.cnki.net/kcms/detail/11.3662.R.20171014.1619.038.html
10.3969/j.issn.1006-7795.2017.05.026]
2017-10-11)
編輯 陳瑞芳

