近紅外光熱轉換納米晶研究進展
李欣遠,紀穆為,王虹智,涂國鵬,萬曉冬,劉佳佳,劉 佳,徐 萌,張加濤
(北京理工大學 材料學院 結構可控先進功能材料與綠色應用北京市重點實驗室,北京 100081)
近紅外光熱轉換納米晶研究進展
李欣遠,紀穆為,王虹智,涂國鵬,萬曉冬,劉佳佳,劉 佳,徐 萌*,張加濤*
(北京理工大學 材料學院 結構可控先進功能材料與綠色應用北京市重點實驗室,北京 100081)
近紅外光熱轉換納米晶材料因其在近紅外區(普遍位于780~1 400 nm)的高效光熱轉換性能,已廣泛應用于光熱殺死癌細胞、腫瘤治療、海水淡化等領域。因其多樣的液相制備方法和形貌控制、納米結構復合、逐漸提高的光熱轉換效率以及表面易于藥物修飾等優點,該材料在光熱成像診斷、光熱治療等領域引起了學術界的廣泛關注。本文綜述了近紅外光熱轉換納米晶的研究進展,主要包括貴金屬納米晶、銅硫族半導體納米晶、碳相關納米晶以及這些納米晶材料構成的復合結構,同時介紹了具有較高光熱轉換效率的表面等離子體共振(SPR)材料的研究進展,尤其是雙模態SPR性質的耦合在光熱轉換領域的應用前景。基于其性能協同耦合的特性,雙模態表面等離子體共振耦合的復合納米晶將是近幾年光熱轉換納米晶發展的重要方向。
納米晶;近紅外光熱轉換;光熱治療;表面等離子體共振
1 引 言
近年來,光熱材料用于生物醫療方向的研究是納米學術界的重點課題,而光熱治療腫瘤細胞更是吸引了生物醫學界的廣泛興趣。在疾病診斷及治療等領域,具有光熱轉換性能的納米材料在光熱治療[2-3]、光熱成像診斷[6-12]、藥物速遞[7,13]、生物靶向治療[8]等領域發揮著重要的作用。
針對應用于生物光熱治療的光熱轉換納米材料,還需要具備以下特點:(1)其光譜吸收峰最好位于近紅外光范圍(Near Infrared Region,NIR),從而增加光的透皮傳播深度、減少生物體本身對光的吸收。(2)具有良好的生物相容性及較低的細胞毒性。(3)易于進行表面修飾,使其易與其他靶向分子官能團結合以實現靶向治療。(4)在生物體內環境中具有良好的分散性與親和性[2-3]。
現階段,被廣泛研究的光熱轉換納米材料主要包括貴金屬納米晶(Nanocrystals NCs)[2-3,10,14-27],銅基硫族半導體納米晶(Cu2-xS(Se))[6,9,28-32],貴金屬/Cu2-xS(Se)異質納米晶[32-35]以及碳基納米晶材料[37-48],其光熱轉換原理與光熱轉換材料結構密切相關。本文綜述了近幾年國內外主要的近紅外光熱轉換納米晶材料以及其光熱治療方面的研究進展,在討論光熱轉換的機理、光熱轉換效率的計算基礎上,論述近紅外光熱轉換納米晶的制備、結構復合,尤其是結構復合產生的雙模態表面等離子體共振耦合效應新原理以及其在光熱性能方面的提高。
2 光熱轉換
2.1光熱轉換的機理及光熱轉換效率的計算

圖1 納米粒子在光照情況下的示意圖[3] Fig.1 Schematic diagram of nanoparticle when irradiated by a light beam[3]
光熱轉換主要是因為材料在吸收電磁輻射后產生晶格振動或電子振蕩而引起材料溫度升高,對于不同的光熱轉換材料,其光熱轉換的原理也不盡相同。比如貴金屬納米晶(如Pt NCs等)由于吸收外來輻射后,表面電子振蕩增強[49-50],在沒有形成光電效應的情況下主要以熱能形式釋放增加的能量從而形成光熱轉換;而具有LSPR的半導體納米晶(如Cu2-xS NCs等)材料,主要是通過表面等離子體共振效應增強光吸收和光熱轉換;碳材料(如碳納米管,石墨烯以及碳基復合材料)基于其特殊的結構在近紅外光區有很強的吸收和光熱轉換效率[3]。由此可見,材料的光熱轉換性能主要與材料吸收外來輻射和產生聲子的強弱有關,通常采用光熱轉化效率(η)進行表征。
通常情況下,將納米晶分散于水或其它溶劑中形成溶膠后光照,監測溶膠溫度隨光照時間的變化。相應的光熱轉換效率使用Roper等建立的熱傳遞模型進行計算[48]:
友好的歡迎和支持總是能讓我們倍感溫暖。在皮蘭,當地政府批準我們駕駛那些跑車進入原本禁止游客車輛進入的中心廣場,我們在那里瞬間成為了所有人關注的焦點。起初,我還自作多情地以為那里的游客是為我們這些“有錢人”而來,但過了一段時間我才意識到,他們真正感興趣的只是那幾輛跑車而已。在那里,我們聽到最多的話就是:“不好意思,稍微靠邊一點好嗎,順便幫我和這輛車拍張合影吧?”
式中,Tmax和Tsurr分別為溶膠最高溫度和環境溫度。I和A分別為激光光強能量密度和納米晶在λ波長處的吸收值,h、S和Qdis分別為熱傳導系數,輻射面積和體系熱量流失。
其中,hS可以通過以下公式進行計算:
式中,mi和Cp,i分別表示納米溶膠的質量和熱容。在實際計算中由于納米晶的濃度很小,納米溶膠一般近似于純水處理。t表示光照之后,溶膠冷卻至室溫所需時間。
2.2近紅外光熱轉換納米晶材料
常見的光熱轉換納米材料包括Au、Ag、Pt和Pd等貴金屬納米晶,Cu2-xS、Cu2-xTe等半導體納米材料,以及碳基納米材料等。
貴金屬納米晶由于其在Vis-NIR光區的吸收主要取決于其形貌與尺寸,且具有連續可調性,在光熱轉換治療、藥物釋放等方面具有重要的意義。比如Lin課題組利用Au納米顆粒在532 nm和565 nm激光的作用實現了對腫瘤細胞的有效殺傷,并發現其對目標淋巴細胞具有光熱解作用[14]。Halas等人制備了在硅顆粒表面形成金納米殼層,在近650到950 nm有很好的吸收[15]。El-Sayed等人成功合成了Au納米棒(Nanorods,NRs),并通過調節Au納米棒的長徑比實現了其吸收光譜在可見光-近紅外光區連續可調[10]。Xia等人制備的貴金屬納米籠,通過控制貴金屬的置換反應程度,也實現了光譜吸收峰從500到900 nm的可調光吸收[16]。這些納米晶的制備和形貌調控為貴金屬納米晶在光熱材料的應用奠定了良好的基礎。如El-Sayed等將具有紅外吸收的Au納米棒應用于光熱療殺死癌細胞實驗中取得了良好的效果。
Cu2-xS等銅基硫族半導體(Cu2-xX,X=S,Se,Te)納米晶等由于其組分非化學計量比導致的Cu空穴在光電場作用下的共振引起LSPR效應,在近紅外光區具有較強的吸收和較高的光熱轉換效率,可作為光熱療試劑。Hu等人制備了納米花狀Cu2-xS納米晶,實現了在980 nm的激發光下25.7%的光熱轉換效率[28]。Wang等人成功合成的Cu7S4納米晶,在808 nm激光照射下,光熱轉換效率達到52.92%,在光熱成像以及光學指紋偵測領域具有良好的應用價值[6]。
通過在Cu2-xS納米晶與貴金屬形成異質納米結構是增強體系光吸收和光熱轉換效率的有效手段。Jiang等在惰性氣體保護下制備合成了Au-Cu9S5二元等離子體異質納米晶,實現了Au和Cu9S5的LSPR耦合增強效果[33]。
Au與Cu2-xS納米晶具有兩種不同模式的LSPR效應,其二元協同耦合效果的最大化,是提高其光熱轉換效率的有效途徑。最近,Zhang課題組使用陽離子交換引發的全新非外延生長制備方法[61-62],成功合成了具有高結晶性且形貌與尺寸精確可控的Au@Cu2-xS核殼納米晶[34]。通過研究其在光熱轉換和抑制宮頸癌細胞生長的應用發現,核殼結構有效地實現了Au和半導體殼層兩種不同模式LSPR效應二元協同耦合作用的最大化,并有效提高了其光熱轉化效率和在光熱療中的應用潛力。通過此種方法制備具有晶面最大程度直接接觸的金屬@半導體核殼結構納米晶,可以實現金屬核和半導體殼層的功能最大程度耦合,實現不同模態的SPR性能的耦合及光熱性能的提高。最近,Zhang等人實現了三元半導體納米晶與貴金屬Au耦合的核殼納米晶,即Au@Ag3AuTe2核殼納米晶的精準制備。通過Au與Ag3AuTe2在納米尺度的最大程度耦合,實現了對可見光、近紅外光的連續吸收及高效光熱轉換性能[52]。因為yolk-shell納米復合結構還能提供微反應腔,Zhang課題組最近通過連續可控的陰離子交換和陽離子交換反應原理,普適性制備了一系列Au/半導體yolk-shell納米晶結構,為后續的納米光熱療及光熱催化合成新應用奠定了堅實的材料基礎[36]。
3 光熱轉換納米晶材料的可控制備及性能開發研究進展
近年來,光熱轉換材料的概念吸引了科學界的廣泛關注,其潛在應用非常廣泛,例如針對腫瘤細胞的光熱治療等。光熱轉換材料,作為光熱轉換過程的重要部分,對于光熱轉換效率起到非常重要的作用。盡管關于光熱轉換材料的研究近年來一直是熱點課題,目前階段的光熱轉換材料仍面臨著很多挑戰,比如光熱轉換效率有待提高,無毒性,持久性有待進一步研究等等。本部分將對近幾年的近紅外光熱轉換納米晶的可控制備、結構復合及性能耦合進行綜述,并綜述其在光熱療方面的應用前景,以及作為光熱催化劑的前景展望。
3.1貴金屬納米晶

圖2 不同形貌的金納米晶及對應光譜吸收圖。 (a,c)Au納米棒(長徑比為5.2)的低分辨透射電子顯微鏡圖片,以及不同長徑比的Au納米棒的消光光譜圖[10]; (b,d)Au納米籠的掃描電子顯微鏡圖,以及置換反應程度的吸收光譜圖[16] Fig.2 LRTEM images of Au with various types of nanostructures and their plasmonic absorbance respectively. (a,c)LRTEM image of Au nanorods with aspect ratio 5.2 and the extinction of Au NRs with different aspect ratio[10]; (b,d)LRTEM image of Au nanocages and their plasmonic absorbance[16]
貴金屬(如Au、Ag、Pt、Pd等)納米晶,作為傳統的光熱轉換材料吸引了全世界科研工作者的廣泛興趣,其中Au納米晶的合成方法最成熟且光熱應用研究最為廣泛。本部分以Au納米晶為例,介紹貴金屬納米晶的光熱轉換特點。Au納米晶的光熱特性主要來源于其局域表面等離子體共振效應,很多課題組已經證實Au納米晶是一種通用的穩定的癌癥診斷和光熱療材料。相比于其他材料,Au納米晶具有以下優點:(1)通過調節其形貌、尺寸與結構,Au納米晶在可見-近紅外光區具有連續可調的吸收,尤其,Au納米球的光譜吸收峰位于520 nm左右,而對于Au納米棒,隨著其長徑比的增加,表面等離子體共振吸收逐漸紅移,其吸收峰在600~1 300 nm內連續可調;(2)Au納米晶的合成方法研究較為成熟,易于進行表面修飾,為后續的應用提供了前提條件;(3)Au納米晶是一種化學惰性材料,具有較好的生物相容性,在生物體內疾病治療方面具有很好的應用前景。
2003年,Lin課題組利用Au納米顆粒在532 nm和565 nm激光的作用實現了對腫瘤細胞的有效殺傷,并發現其對目標淋巴細胞具有光熱解作用[14]。此外,在實驗中脈沖激光的成本較高,且由于脈沖時間較短使得熱量散失較快,致使光熱轉換效率較低。然而,限制Au納米顆粒光熱應用的最主要因素在于其吸收峰主要集中于可見光范圍(520 nm左右),而此波長下的可見光被生物體組織的吸收很嚴重,光的透過性較差,難以實現有效的體內腫瘤等疾病治療。Kim等人通過調節反應環境的pH值,實現了Au納米顆粒的可控聚集,使其表面等離子體共振吸收峰從524 nm到650 nm的紅移[18]。2005年,West和Drezek等人制備了以硅納米球為核,Au為殼層的異質納米結構,并通過調節Au納米殼層的厚度,實現了其在650 nm到950 nm近紅外區的高效吸收和光譜可調,為光熱治療和光熱成像提供了基礎[15,19]。Au納米棒,由于其特殊的結構特點,短軸和長軸具有兩種表面等離子體共振模式,短軸模式的共振范圍在520 nm左右(類似Au球),長軸模式的共振范圍則與Au納米棒的長徑比有關,隨長徑比的增加而增大,因而具有從可見光區到近紅外光區的連續可調光吸收效應(600 nm到1 300 nm),被認為具有更廣泛的光熱轉換應用潛力[10]。目前,制備Au納米棒的主要方法為種子生長法,這種方法目前十分成熟,具有產率高,步驟簡單,以及形貌易于調控等特點。2001年,Jana等人首次通過種子生長法合成了Au納米棒溶膠,將檸檬酸鈉體系中合成的小尺寸Au顆粒放入具有CTAB,抗壞血酸,銀離子和氯金酸的生長液中,從而制得了Au納米棒溶膠[26]。2003年,El-Sayed等人對Jana等人的方法進行改進,通過引入CTAB包附的Au種子,生長液中加入BDAC并調節Ag離子的加入量,實現了產率的提高和長徑比的可調,并于2006年,證實了Au納米棒可用于體內分子成像以及光熱治療[20,27]。Van Maltzahn等人制備了聚乙二醇(PEG)包附Au納米棒,實現了在功率為2 W/cm2的810 nm激光照射下,在5 min內將體系溫度由室溫提高到70 ℃,實現了Au納米棒的體內光熱治療應用[21]。2010年,Wang等人同樣利用種子生長法合成的Au納米棒,探究入射激光波長、光熱轉換納米晶濃度、以及表面殼層等因素對于光熱轉換效率的影響,并實現了Au納米棒溶膠在810 nm的激光照射10 min后使體系溫度從室溫提高到75 ℃,且轉換效率高達95%[22]。除Au納米棒外,Xia等人通過貴金屬間的置換反應,制備了Au納米籠,根據置換反應的程度的不同實現了其光譜吸收峰從500 nm到900 nm的連續調節[16]。除上述材料外,Ray等人制備的Au納米花(nanopopcorn)[23],Vo-Dinh 等人制備的Au納米星(nanostars)[24],de la Fuente等人制備的Au納米三棱柱(nanoprisms)結構[25],均在NIR光區具有良好的光熱轉換效果,為貴金屬納米顆粒在光熱轉換及光熱治療領域的應用提供了多元發展方向。
3.2Cu2-xX(X=S,Se,Te)半導體納米晶
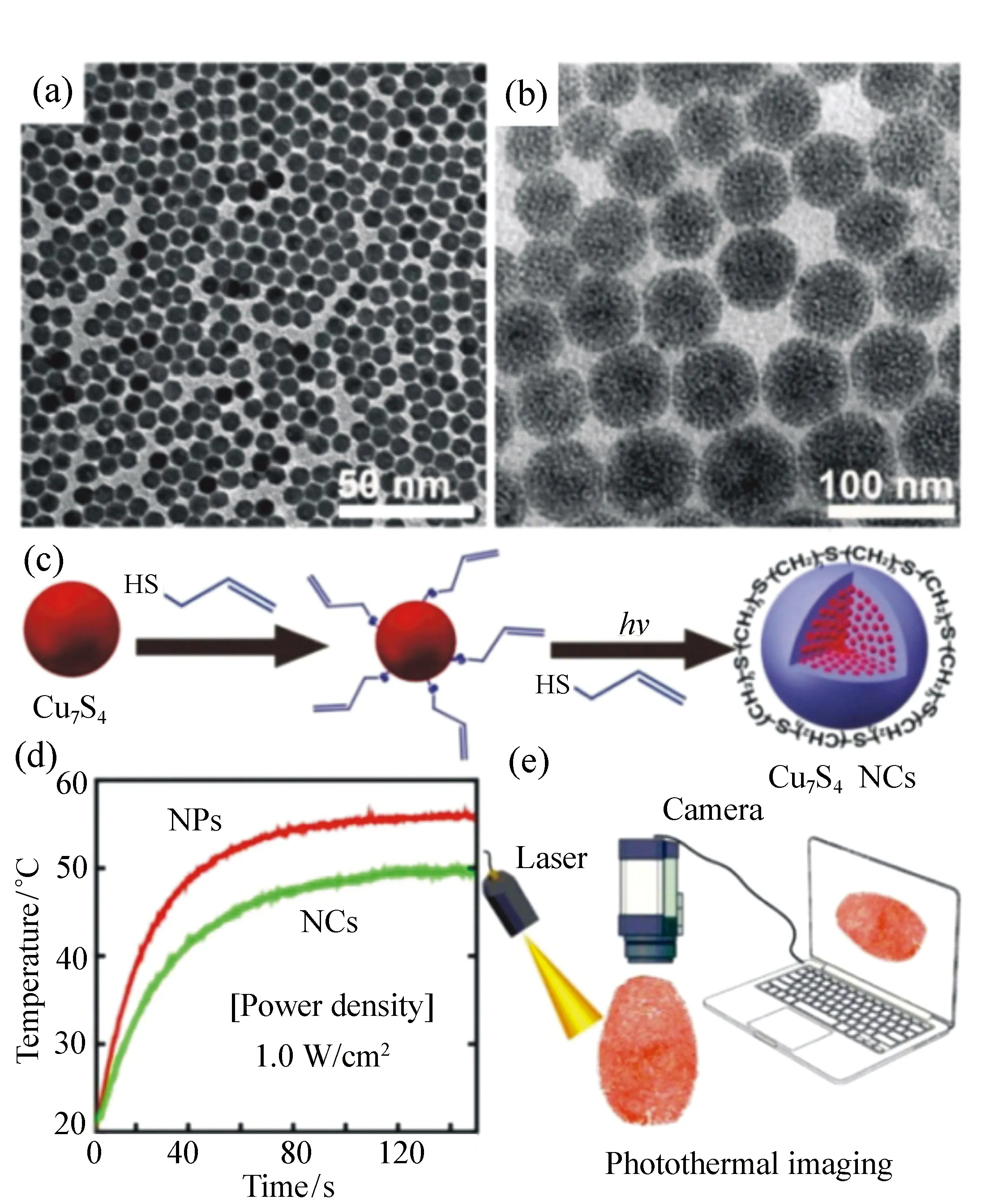
圖3 (a)疏水性Cu7S4納米顆粒的低分辨透射電子顯微鏡圖; (b)親水性的Cu7S4納米晶的低分辨透射顯微鏡圖; (c)親水性Cu7S4納米晶形成機理; (d)兩種材料的在808 nm的激光照射下的光熱轉換圖譜; (e)光熱成像指紋檢測示意圖[6] Fig.3 (a)LRTEM image of hydrophobic Cu7S4 NPs. (b)LRTEM image of amphiphilic Cu7S4 NCs. (c)Fabrication strategy for Cu7S4 NCs. (d)PT activity of Cu7S4 NPs and NCs. (e)Schematic representation of photothermal imaging process[6]
貴金屬納米材料具有良好的光熱轉換效率,但昂貴的價格限制了其實際應用。相比之下,銅基硫族化合物,如CuS[9]、Cu2-xS[6,28,30]、Cu2-xTe[31]等因為非計量比引起的銅空位產生的在近紅外區的SPR性能,都具有光熱轉換能力,并且具有價格優勢,是理想的光熱轉換材料。多年來,制約銅的硫族化物應用于光熱轉換領域的重要因素在于其光熱轉換效率相對貴金屬材料較低。2010年,Li課題組成功合成了不含螯合劑的平均粒徑為11 nm的CuS納米晶,實現了對930 nm近紅外光的有效吸收,具有一定的體內腫瘤細胞光熱治療的應用前景[9]。2011年,Hu等人制備了平均粒徑1 um的花狀硫化銅納米晶,在980 nm的NIR光區有良好的光熱轉換效果[29]。同年,Hu等人通過熱分解和表面配體交換相結合的方法,成功合成了親水性的Cu9S5納米片,由于其中存在Cu+空位,使其具有LSPR效應[28]。該親水性的Cu9S5納米片,在40 ppm的濃度下,經功率為0.51 W/cm2的980 nm波長激光照射7 分鐘,體系溫度提高了15.1 ℃,該Cu9S5納米片在980 nm波長近紅外光下的光熱轉換效率為25.7%。2015年,Pellegrino等人通過液相法和配體交換法,成功合成了Cu2-xS納米晶,該納米晶的平均粒徑為6.5 nm,如圖3所示。并通過ESR光譜和DCF熒光免疫法證實,該Cu2-xS納米晶在具有良好的光熱治療效果的同時,還具有光動力治療效果[30]。通過在所合成的Cu2-xS納米晶表面包覆PEG分子,使其具有良好的生物相容性在不影響其光熱治療效果的同時,更容易與病灶部位結合,從而為其的進一步應用提供了可能。Wang等人也成功合成了Cu7S4納米晶(如圖3所示),并證實了其具有良好的光熱轉換性能(808 nm,1.0 W/cm2激光照射下,光熱轉換效率達到52.92%),在光熱成像以及光學指紋偵測領域具有良好的應用價值[6]。Kriegel等人以CdTe或CdSe為原料通過離子交換法制備了Cu2-xTe以及Cu2-xSe等納米晶,通過控制其形貌實現了可見光范圍到近紅外區(Cu2-xTe納米棒吸收峰位于1 103 nm)的吸收光譜可調[31]。然而,Cu2-xX(X=S,Se,Te)半導體納米晶雖然成本相對貴金屬材料較低,但其光熱轉換效率有待進一步提高,且實際應用中的光熱穩定性仍有提高空間。
3.3雙模態表面等離子體共振耦合的復合納米晶
多組分材料的整合是目前納米材料研究領域的重要課題,通過多組分的協同作用,納米晶的物理化學性質有顯著的提高[54-55]。核殼結構,作為二元協同材料,由于其良好的界面調控以及最大化的接觸面積,實現了在光學[56]、光催化[57-58]、太陽能電池[56]以及生物技術領域[8,16,20,60]的廣泛應用。貴金屬納米顆粒所具備的等離子體的共振效應已經被廣泛應用于光熱轉換,生物醫學和光電應用,然而一些非金屬納米材料通過摻雜引起的自由電子也能引發表面等離子效應。基于多組分協同的思想,將具有表面等離子體效應的非金屬和貴金屬材料的耦合,是目前納米光熱材料合成和發展中的重要方向之一,然而此類研究更是少之又少。表面等離子體共振耦合材料相比于貴金屬納米材料和半導體材料,其優勢在于相比貴金屬材料可以節約成本,而相比半導體材料可以顯著提高其光熱轉換效率,且共振耦合材料產生的效果要高于兩者的直接混合材料,從而有更廣闊的應用前景。
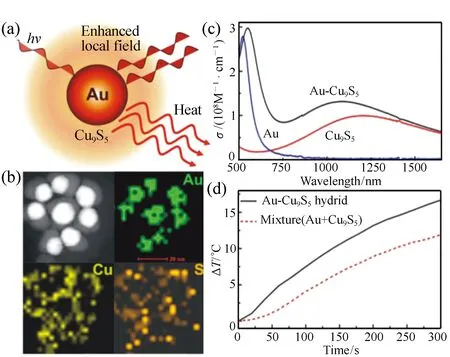
圖4 (a)Au-Cu9S5異質二聚體納米晶材料; (b)Au-Cu9S5元素分部圖; (c)Au顆粒,Cu9S5納米顆粒,Au-Cu9S5異質結構的UV-Vis吸收示意圖; (d)Au-Cu9S5異質結構和Au與Cu9S5混合機構的光熱準換效率對比圖[33] Fig.4 (a)Schematic representation of Au-Cu9S5 dual plasmonic hybrid NCs when irradiated by laser. (b)STEM image of Au-Cu9S5 NCs and their EDS element mapping images. (c)Molar extinction coefficient of Au-Cu9S5, Cu9S5 and Au colloidal respectively. (d)PT activity comparison of Au-Cu9S5 and physical mixture of Au and Cu9S5 at same concentration when irradiated by 808 nm, 0.7 W/cm2 laser[33]
2013年,Jiang等人利用有機體系合成的Au納米顆粒并通過外延法在惰性氣體保護下成功合成了Au-Cu9S5異質二聚體納米晶材料,如圖4所示[33]。同樣的條件下,由于Au-Cu9S5納米晶的LSPR協同耦合作用,相比于單獨的Cu9S5納米晶,等離子體效應提高50%(1 064 nm處的吸收峰值提高50%),且經計算,其光熱轉換效率提高了37%。同時,DDA的計算值表明Au和Cu9S5確實有局域場增強效果。另外,Au-Cu9S5用較好的光穩定性,以及較低的生物毒性,從而被認為是光熱治療腫瘤細胞的理想材料。
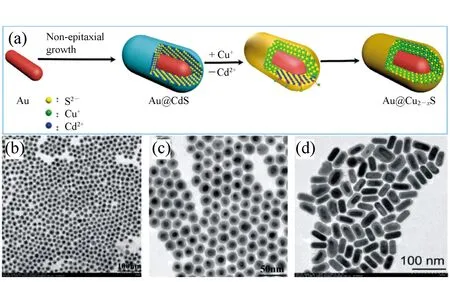
圖5 (a)Au納米顆粒到Au@Cu2-xS NCs合成示意圖; (b,c)Au@Cu2-xS納米晶的低分辨透射電子顯微鏡圖; (d)Au@Cu2-xS納米棒的低分辨投射電子顯微鏡圖[34] Fig.5 (a)Schematic of the synthesis method of Au@Cu2-xS NCs from Au NPs. (b,c)LRTEM of Au@Cu2-xS NCs. (d)LRTEM image of Au@Cu2-xS NRs[34]
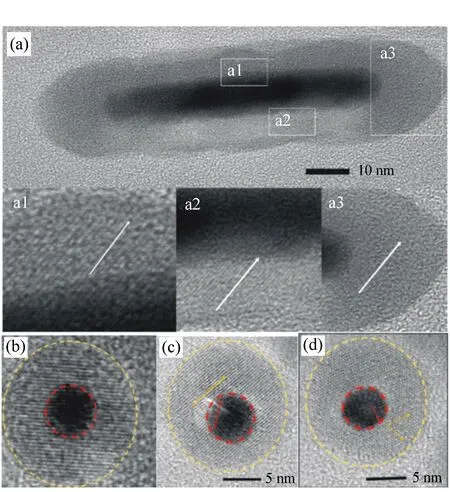
圖6 (a)Au@Cu2-xS納米棒高分辨透射電子顯微鏡圖; (b~d)Au@Cu2-xS納米顆粒高分辨透射電子顯微鏡圖[34] Fig.6 (a)HRTEM images of Au@Cu2-xS NRs. (b-d)LRTEM images of Au@Cu2-xS NPs [34]
Cu2-xS納米晶由于其材料組分的非化學計量比,導致材料內的Cu空穴在近紅外光作用下發生共振,引起LSPR效應,同時,通過調節Cu2-xS中亞銅離子的化學計量比,可以調節其LSPR吸收峰的位置[6,28,30]。基于之前的研究成果,Zhang課題組利用陽離子交換誘發的非外延生長方法成功合成了單分散性良好(如圖5(b)~5(d)),且具有高結晶性的Au@Cu2-xS核殼納米晶(如圖6),實現了在大晶格失配度下核殼納米晶形貌、尺寸及異質界面的精確調控并首次實現了不同產生機理的LSPR效應在三維方向上最大程度的協同耦合[34]。在合成方法上,基于之前的研究工作[61-62],通過將非外延生長法合成的Au@CdS單晶核殼納米晶顆粒與Cu(CH(CH(CH3CN)CN)CN)4PF6進行離子交換反應,成功得到形貌完整保持,殼層均勻完整,且結晶性良好的Au@Cu2-xS核殼納米晶,其合成示意圖及低分辨透射電鏡圖如圖5所示。同時,在保證結晶性的前提下,實現了不同尺寸和殼層厚度的球狀或棒狀Au@Cu2-xS納米晶的合成。其中通過調控Au@Cu2-xS納米棒的長徑比,利用實驗與理論模擬相結合的方法,證實了其在不同NIR光區(750~900 nm的第一NIR窗口區及1 000~1 400 nm的第二NIR窗口區)均具有高效的LSPR協同耦合效應及較高的光熱轉換效率(圖7(a)~7(c))。通過計算得出,Au@Cu2-xS核殼納米晶溶膠在808 nm激光下的光熱轉換效率為59.01%,在1 064 nm下的光熱轉換效率為43.25%。在具有較高光熱轉換效率的同時,在808 nm和1 064 nm的激光照射下,使用Au@Cu2-xS納米棒實現了對宮頸癌細胞的高效光熱殺傷(圖7(e))。實驗證明,利用Au@Cu2-xS納米棒在光照10 min后,宮頸癌細胞的存活率下降到僅為20%。Au@Cu2-xS納米棒比單獨的Au納米棒或Cu2-xS納米顆粒有更好的殺傷效果,從而證明了LSPR協同耦合效應在光熱轉換效應中所發揮的重要作用,并證明該材料在腫瘤光熱治療領域的應用潛力。
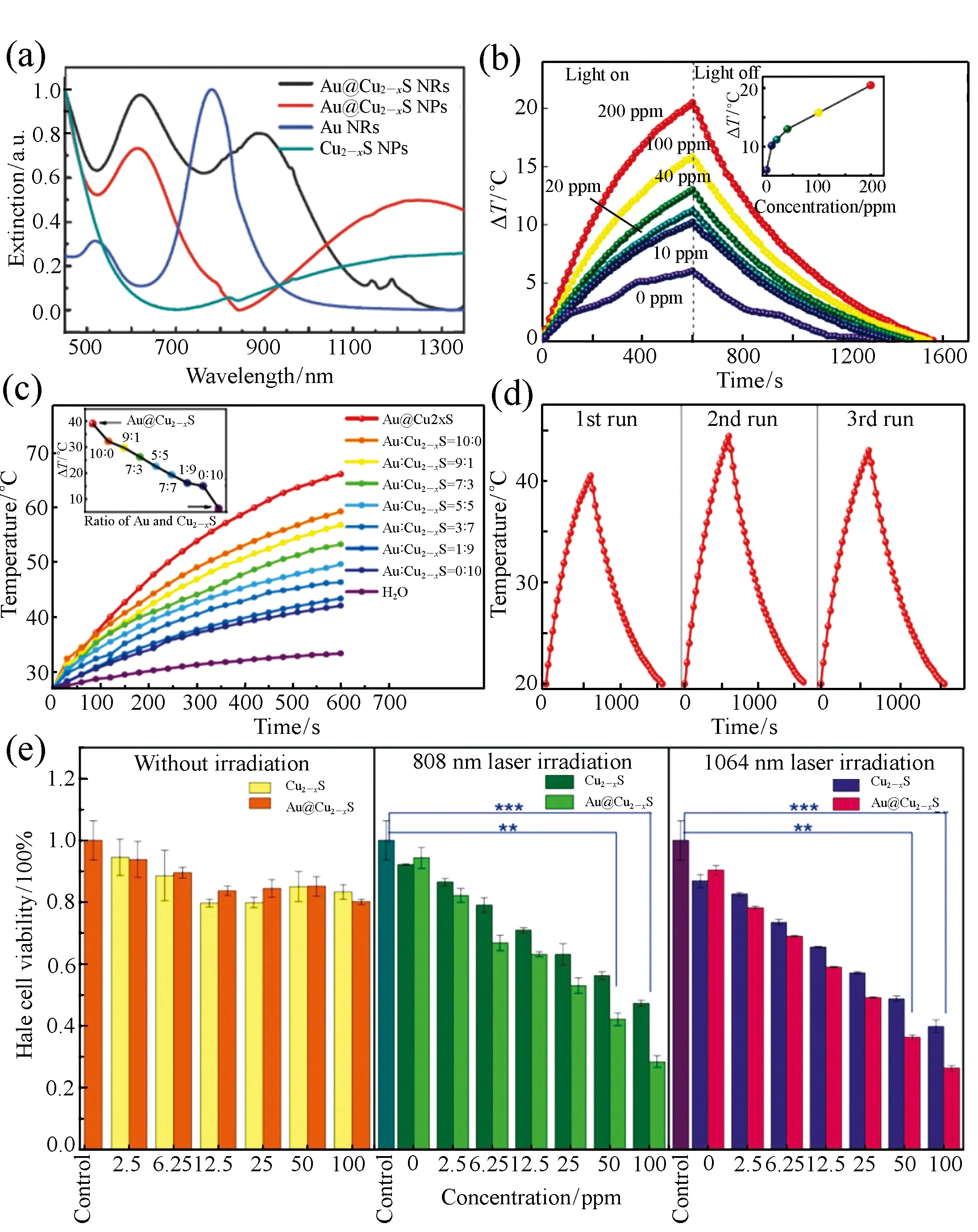
圖7 (a)Au@Cu2-xS納米棒,Au@Cu2-xS納米顆粒,Au納米棒以及Cu2-xS納米顆粒溶膠的UV-Vis-NIR光譜圖; (b)不同濃度的Au@Cu2-xS納米棒膠體在0.7 W/cm2 1 064 nm 的激光照射下的光熱轉換曲線; (c)Au@Cu2-xS與不同配比的Au,Cu2-xS的混合膠體的光熱轉換曲線對比; (d)Au@Cu2-xS納米棒膠體在0.7 W/cm2 1 064 nm激光照射下的光熱轉換循環測試; (e)Au@Cu2-xS納米棒和Cu2-xS納米晶在808nm和1 064nm激光照射下赫拉細胞存活率對比[34] Fig.7 (a)UV-Vis-NIR spectra of the as prepared Au@Cu2-xS nanorods, Au@Cu2-xS NPs, Au nanorods and Cu2-xS NPs colloidal respectively. (b)PT conversion curve of Au@Cu2-xS NRs by 0.7 W/cm2 1 064 nm laser. (c)PT activity of Au NRs, Cu2-xS nanoparticles and their physical mixtures for various ratios compared with Au@Cu2-xS nanorods. (d)PT cycling test of Au@Cu2-xS nanorods irradiated by 0.7 W/cm2 1 064 nm laser. (e)Hela cell viability of Au@Cu2-xS NRs under irradiation of 808 nm and 1 064 nm laser irradiation compared to Cu2-xS NPs[34]
Au納米顆粒或LSPR二元協同耦合效應納米顆粒在光熱應用方面具有良好的前景,然而這類材料的NIR光區吸收范圍普遍較窄,因此如何拓寬該類材料的吸收范圍是提高其光熱轉換率拓寬應用范圍的重要方面。基于之前對于納米材料合成和光熱轉換領域的研究,以及多元化納米晶的特殊性能優勢[63],Zhang等人實現了三元半導體納米晶與貴金屬Au耦合,且在NIR區具有連續吸收能力的Au@Ag3AuX2(X=Te,Se)核殼納米晶,在合成上實現了納米晶殼層從二元到三元的拓展,性能上為拓寬該類材料在NIR區的吸收提供了一種有效的方法[52]。合成方法上通過將Au@Ag核殼立方塊納米晶與Te的水合肼溶液進行水熱反應,生成結晶性良好且形貌、尺寸可控的Au@Ag3AuX2(X=Te,Se)納米晶(圖8(b)),其在700 nm到1 200 nm的NIR光區具有連續吸收。通過使用808 nm和1 064 nm的激光照射,測得Au@Ag3AuTe2(Au@Ag3AuSe2)納米晶的光熱轉換效率分別高達76.7%(50.7%)和49.6%(34.1%),(圖8(c),8(d))從而證明Au@Ag3AuX2(X=Te,Se)為良好的光熱轉換材料,且有較好的光熱轉換應用潛力。

圖8 (a)Au@Ag3AuTe2 納米晶效果圖; (b)Au@Ag3AuTe2 納米晶的低分辨透射電子顯微鏡和高分辨透射電子顯微鏡圖; (c,d)不同濃度下Au@Ag3AuTe2納米晶在808 nm和1 064 nm激光照射下的光熱轉換曲線[52] Fig.8 (a)Scheme of Au@Ag3AuTe2 NCs. (b)LRTEM and HRTEM images of Au@Ag3AuTe2 NCs. (c,d)PT conversion characterizations of Au@Ag3AuTe2 NCs colloid with various concentrations by 0.7 W/cm2 808 nm (c), 0.7 W/cm2 1 064 nm (d)[52]

圖9 (a)Au@MS(M=Cd, Sn) yolk-shell納米晶合成過程示意圖。(b,c)Au@CdS與Au@SnS yolk-shell納米晶分別的低分辨透射電子顯微鏡圖[36] Fig.9 (a)Synthesis scheme of Au@MS(M=Cd,Sn) yolk-shell NCs. (b,c)LRTEM images of Au@CdS and Au@SnS yolk-shell NCs, respectively[36]

圖10 (a)Cu2O@MS(M=Cd,Zn,Sn) yolk-shell納米晶合成過程示意圖; (b)Cu2O@CdS yolk-shell納米晶低分辨透射電子顯微鏡圖; (c)Cu2O@CdS yolk-shell納米晶 高分辨透射電子顯微鏡圖; (d)Cu2O@CdS yolk-shell納米晶STEM模式下的元素分布圖[36] Fig.10 (a)Synthesis scheme of Cu2O@MS (M=Cd,Zn,Sn) yolk-shell NCs. (b)LRTEM image of Cu2O@CdS yolk-shell NCs. (c)HRTEM image of Cu2O@CdS yolk-shell NCs. (d)Element mapping of Cu2O@CdS yolk-shell NCs[36]
相比于二元材料實現最大限度接觸的核殼結構,yolk-shell結構納米材料具有與之完全不同的界面環境,為藥物緩釋、靶向治療和光熱療的協同作用提供了材料學基礎[64]。光熱治療殺死癌細胞是光熱研究的重要應用方向之一,然而在實際臨床應用中,光熱轉換材料在到達指定部位光生熱的同時,需要化療藥物同時到達指定腫瘤部位,從而定向協同發揮作用,這對于藥物輸送來說仍具備很大挑戰。yolk-shell結構不同于核殼結構,其在結合兩種組分材料的同時,還留有可控空間的微反應腔,因此在光熱治療的同時,為藥物緩釋,靶向治療,藥物定向輸送等提供了良好的操作環境,可以實現藥物和光熱轉換材料同時到達指定治療部位。Zhang課題組最近通過連續可控的陰離子交換和陽離子交換反應原理,普適性制備了一系列Au/半導體yolk-shell納米晶結構,為后續的納米光熱療及光熱催化合成新應用奠定了堅實的材料基礎[36]。合成方法通過將Cu2O或Au@Cu2O納米晶經過陰離子交換反應引發的柯肯達爾效應,形成Cu2O@Cu2-xS或Au@Cu2-xS,再通過膦配體引發的離子交換反應,實現了普適性的Cu2O@MS和Au@MS(M=Cd,Zn,Sn) yolk-shell結構的合成(如圖9、圖10所示)。此方法合成的yolk-shell納米晶,具有很高的單分散性(如圖9(a)、9(b)所示),且具有較好的結晶性(如圖10(c)所示),這種普適性的合成方法,為具有光熱治療效果的同時具有藥物緩釋功能的研究提供了材料學基礎。Yang等人通過種子合成法合成了長徑比均一的Au納米棒,并通過外延法合成出Au@Cu2O納米棒,再進一步將之轉化為Au@Cu7S4yolk-shell納米晶[65-66],在915 nm的NIR光照射下其光熱轉化效率達到了68.6%[35]。并且進一步研究了腔體尺寸、殼層厚度對光熱轉換效率的影響,證實了在其實驗條件下,一定的耦合空間范圍內(157.2 nm的yolk-shell結構)有最佳的耦合共振效果。其對表面介孔性質的研究為其作為理想藥物緩釋材料提供了重要的事實依據。此外,除了核殼和yolk-shell結構外,Zhang和Liu等人制備的Au納米棒/介孔硅基材料(PMO)Janus結構納米晶,為藥物光熱協同治療提供了材料學基礎[67]。
3.4碳基納米晶
近年來,sp2碳材料吸引了廣泛的興趣。最典型的也是最受歡迎的碳材料包括零維富勒烯材料,一維碳納米管以及二維石墨烯,這幾類材料在藥物傳遞,生物成像探針等領域等應用收到了廣泛的研究。碳納米材料的特點在于其具有紫外到近紅外的較寬的光譜吸收,且具有可觀的光熱穩定性,另外其毒性和生物相容性基本取決于其表面的化學配體。2005年,Dai等人利用經DNA分子修飾的碳納米管材料,在808 nm,1.4 W/cm2的激光照射2 min后,實現了其針對腫瘤細胞的有效體外光熱殺傷效果[37]。2009年,Moon等人證實了經PEG修飾的單壁碳納米管通過瘤內注射的方法,在808 nm的近紅外光照下實現了對腫瘤細胞的高效光熱殺傷效果[38]。Burke和Ghosh課題組均利用合成多壁碳納米管,通過在其表面負載不同的基團,在生物體內實現了良好的腫瘤光熱治療效果[39-40]。Liu等人通過改變碳納米管的表面配體,改善了瘤內注射所涉及到的光熱轉化率較低和納米管體內殘留等問題。基于碳納米管在光熱領域的成功,由于石墨烯在近紅外區的高效光吸收及更好的生物相容性,被認為在光熱疾病治療領域有潛在的應用價值[41]。2010年,Liu等人首次研究了PEG包覆的石墨烯納米片(NGS-PEG)在體內注射治療腫瘤細胞的效果,其示意圖及光熱轉換圖譜如圖11所示,通過使用2 W/cm2的激光照射在20 mg/kg的劑量下實現了100%的腫瘤細胞殺傷效果,為后續的石墨烯光熱治療研究奠定了基礎[42]。在其后續的nRGO-PEG的研究工作中,實現了0.15 W/cm2光照5 min殺死全部腫瘤細胞的效果[43]。2009年,Kim等人將Au納米顆粒負載到碳納米管表面,實現了其在生物體內的成像和光熱治療效果,為碳基復合材料的研究奠定了基礎[44]。類似的,近年來很多研究組成功制備了貴金屬顆粒等物質在碳納米管和石墨烯上的負載,從而在光熱治療領域實現了不同程度的提高[45-46]。然而制約碳材料進一步應用于光熱治療領域的因素在于其光吸收系數有待提高,且制備過程相比其他材料較為復雜,如需應用于光熱治療則需要對其表面進行大量配體修飾以保證其生物相容性,其表面配體的穩定性還有很大的提高空間。最近的研究中,Zhu和Wang等人通過熱解ZIF-8納米立方塊,制備了石墨納米立方塊,在具有良好的的生物相容性和光熱穩定性的同時,實現了40.4%的光熱轉換效率[47]。

圖11 PEG包附的石墨烯納米片(NGS-PEG)。(a)Cy7修飾的NGS-PEG示意圖; (b)NGS-PEG的原子力顯微鏡圖; (c)NGS-PEG的UV-Vis-NIR吸收光譜圖'; (d)808 nm,2 W/cm2激光照射下NGS-PEG的光熱轉換圖譜[42] Fig.11 NGS coated with PEG. (a)schematic diagram of NGS-PEG labeled with Cy7. (b)AFM image of NGS-PEG. (c)UV-Vis-NIR absorbance of NGS-PEG solution. (d)PT activity of NGS-PEG under 808 nm 2 W/cm2 laser treatment[42]
4 結束語
光熱轉換效應在腫瘤治療、光熱催化等領域有廣泛的應用潛力,納米光熱轉換材料由于其較高的光熱轉換效率,吸引了學術界的廣泛關注。目前,納米光熱轉換材料的主要應用領域在于光熱成像,光熱治療以及藥物緩釋等生物醫學領域。貴金屬納米顆粒,空位半導體材料以及碳材料是受關注最早,最被廣泛研究的3種光熱轉換材料。貴金屬納米顆粒,以Au納米棒為主,通過控制其形貌,調節其光譜吸收峰位置,從而實現了近紅外區較高的光熱轉換效率,然而其昂貴的價格是制約其實際應用的重要因素。空位半導體材料,相比于貴金屬顆粒,價格較為便宜,但其光熱轉換效率及生物相容性有待進一步研究。碳材料,以碳納米管,石墨烯以及碳基復合材料為主,近年來吸引了學術界的廣泛興趣。其優勢在于材料成本低,且表面易于修飾,以實現生物靶向治療。然而其制備工藝比較復雜,且表面配體生物相容性和持久性有待研究。
雙模態表面等離子體共振耦合的復合納米晶,通過形成異質結構的兩種材料(以貴金屬顆粒和半導體材料形成異質結構居多),基于貴金屬和空位半導體材料的表面等離子體共振效應,實現了兩種材料的協同耦合效果。通過制備高結晶性及形貌可控的貴金屬/空位半導體核殼結構,實現了兩種不同模式LSPR效應二元協同耦合作用的最大化,從而在提高光熱轉化效率的同時降低了材料的成本,為光熱轉換材料的未來發展提供了重要手段。通過制備具有微反應腔的yolk-shell異質結構納米晶,為后續的光熱療及光熱催化新應用奠定了材料學基礎。
[1] CHEN X,CHEN Y,YAN M,etal.. Nanosecond photothermal effects in plasmonic nanostructures[J].ACSNano,2012,6(3):2550-2557.
[2] CHENG L,WANG C,FENG L,etal.. Functional nanomaterials for phototherapies of cancer[J].ChemicalReviews,2014,114(21):10869-10939.
[3] JAQUE D,MARTINEZ MAESTRO L,DEL ROSAL B,etal.. Nanoparticles for photothermal therapies[J].Nanoscale,2014,6(16):9494-9530.
[4] ZHU G,XU J,ZHAO W,etal.. Constructing black titania with unique nanocage structure for solar desalination[J].ACSAppliedMaterials&Interfaces,2016,8(46):31716-31721.
[5] WANG X,OU G,WANG N,etal.. Graphene-based recyclable photo-absorbers for high-efficiency seawater desalination[J].ACSAppliedMaterials&Interfaces,2016,8(14):9194-9199.
[6] CUI J,XU S,GUO C,etal.. Highly efficient photothermal semiconductor nanocomposites for photothermal imaging of latent fingerprints[J].AnalyticalChemistry,2015,87(22):11592-11598.
[7] CHEN G,ROY I,YANG C,etal.. Nanochemistry and nanomedicine for nanoparticle-based diagnostics and therapy[J].ChemicalReviews,2016,116(5):2826-2885.
[8] CHENG L,YANG K,LI Y,etal.. Facile preparation of multifunctional upconversion nanoprobes for multimodal imaging and dual-targeted photothermal therapy[J].AngewandteChemieInternationalEdition,2011,50(32):7385-7390.
[9] ZHOU M,ZHANG R,HUANG M,etal.. A chelator-free multifunctional [64Cu]CuS nanoparticle platform for simultaneous micro-PET/CT imaging and photothermal ablation therapy[J].J.AmericanChemicalSociety,2010,132(43):15351-15358.
[10] HUANG X,NERETINA S,EL-SAYED M A. Gold nanorods:from synthesis and properties to biological and biomedical applications[J].AdvancedMaterials,2009,21(48):4880-4910.
[11] MOU J,CHEN Y,MA M,etal.. Facile synthesis of liposome/Cu2-xS-based nanocomposite for multimodal imaging and photothermal therapy[J].ScienceChinaMaterials,2015,58(4):294-301.
[12] 王英帥,周穎,王珺楠,等.金納米棒核/二氧化硅殼納米復合結構的可控制備及細胞成像[J].中國光學,2013,6(5):743-749.
WANG Y SH,ZHOU Y,WANG J,etal.. Controlled synthesis and cell imaging of gold nanorod-silica core-shell nanoparticles[J].ChineseOptics,2013,6(5):743-749.(in Chinese)
[13] CHAI Z,HU X,LU W. Cell membrane-coated nanoparticles for tumor-targeted drug delivery[J].ScienceChinaMaterials,2017:1-7.
[14] PITSILLIDES C M,JOE E K,WEI X,etal.. Selective cell targeting with light-absorbing microparticles and nanoparticles[J].BiophysicalJournal,2003,84(6):4023-4032.
[15] LOO C,LOWERY A,HALAS N,etal.. Immunotargeted nanoshells for integrated cancer imaging and therapy[J].NanoLetters,2005,5(4):709-711.
[16] SKRABALAK S E,CHEN J,SUN Y,etal.. Gold nanocages:synthesis, properties, and applications[J].AccountsofChemicalResearch,2008,41(12):1587-1595.
[17] EL-SAYED I H,HUANG X,EL-SAYED M A. Selective laser photo-thermal therapy of epithelial carcinoma using anti-EGFR antibody conjugated gold nanoparticles[J].CancerLetters,2006,239(1):129-135.
[18] NAM J,WON N,JIN H,etal.. pH-induced aggregation of gold nanoparticles for photothermal cancer therapy[J].J.AmericanChemicalSociety,2009,131(38):13639-13645.
[19] GOBIN A M,LEE M H,HALAS N J,etal.. Near-infrared resonant nanoshells for combined optical imaging and photothermal cancer therapy[J].NanoLetters,2007,7(7):1929-1934.
[20] HUANG W,QIAN W,EL-SAYED M A. Gold nanoparticles propulsion from surface fueled by absorption of femtosecond laser pulse at their surface plasmon resonance[J].J.AmericanChemicalSociety,2006,128(41):13330-13331.
[21] VON MALTZAHN G,PARK J-H,AGRAWAL A,etal.. Computationally guided photothermal tumor therapy using long-circulating gold nanorod antennas[J].CancerResearch,2009,69(9):3892-3900.
[22] CHEN H,SHAO L,MING T,etal.. understanding the photothermal conversion efficiency of gold nanocrystals[J].Small,2010,6(20):2272-2280.
[23] LU W,SINGH A K,KHAN S A,etal.. Gold nano-popcorn-based targeted diagnosis, nanotherapy treatment, and in situ monitoring of photothermal therapy response of prostate cancer cells using surface-enhanced raman spectroscopy[J].J.AmericanChemicalSociety,2010,132(51):18103-18114.
[24] YUAN H,FALES A M,VO-DINH T. TAT peptide-functionalized gold nanostars:enhanced intracellular delivery and efficient NIR photothermal therapy using ultralow irradiance[J].J.AmericanChemicalSociety,2012,134(28):11358-11361.
[25] PELAZ B,GRAZU V,IBARRA A,etal.. Tailoring the synthesis and heating ability of gold nanoprisms for bioapplications[J].Langmuir,2012,28(24):8965-8970.
[26] JANA N R,GEARHEART L,MURPHY C J. Seed-mediated growth approach for shape-controlled synthesis of spheroidal and rod-like gold nanoparticles using a surfactant template[J].AdvancedMaterials,2001,13(18):1389-1393.
[27] NIKOOBAKHT B,EL-SAYED M A. Preparation and growth mechanism of gold nanorods(NRs) using seed-mediated growth method[J].ChemistryofMaterials,2003,15(10):1957-1962.
[28] TIAN Q,JIANG F,ZOU R,etal.. Hydrophilic Cu9S5nanocrystals: a photothermal agent with a 25.7% heat conversion efficiency for photothermal ablation of cancer cells in vivo[J].ACSNano,2011,5(12):9761-9771.
[29] TIAN Q,TANG M,SUN Y,etal.. Hydrophilic flower-like CuS superstructures as an efficient 980 nm laser-driven photothermal agent for ablation of cancer cells[J].AdvancedMaterials,2011,23(31):3542-3547.
[30] WANG S,RIEDINGER A,LI H,etal.. Plasmonic copper sulfide nanocrystals exhibiting near-infrared photothermal and photodynamic therapeutic effects[J].ACSNano,2015,9(2):1788-1800.
[31] KRIEGEL I,RODR GUEZ-FERN NDEZ J,WISNET A,etal.. Shedding light on vacancy-doped copper chalcogenides:shape-controlled synthesis, optical properties, and modeling of copper telluride nanocrystals with near-infrared plasmon resonances[J].ACSNano,2013,7(5):4367-4377.
[32] HUANG S,LIU J,HE Q,etal. Smart Cu1.75S nanocapsules with high and stable photothermal efficiency for nir photo-triggered drug release[J].NanoResearch,2015,8(12):4038-4047.
[33] DING X,LIOW C H,ZHANG M,etal.. Surface plasmon resonance enhanced light absorption and photothermal therapy in the second near-infrared window[J].JournaloftheAmericanChemicalSociety,2014,136(44):15684-15693.
[34] JI M,XU M,ZHANG W,etal.. Structurally well-defined Au@Cu2-xS core-shell nanocrystals for improved cancer treatment based on enhanced photothermal efficiency[J].AdvancedMaterials,2016,28(16):3094-3101.
[35] YU X,BI J,YANG G,etal.. Synergistic effect induced high photothermal performance of Au nanorod@Cu7S4Yolk-Shell nanooctahedron particles[J].TheJournalofPhysicalChemistryC,2016,120(43):24533-24541.
[36] JI M,LI X,WANG H,etal.. Versatile synthesis of yolk/shell hybrid nanocrystals via more kinds of ions exchange reactions:towards novel metal/semiconductor and semiconductor/semiconductor conformations[J].NanoResearch,2017,DOI:10.1007/s12274-017-1508-4.
[37] KAM N W S,O'CONNELL M,WISDOM J A,etal.. Carbon nanotubes as multifunctional biological transporters and near-infrared agents for selective cancer cell destruction[J].ProceedingsoftheNationalAcademyofSciences,2005,102(33):11600-11605.
[38] MOON H K,LEE S H,CHOI H C,etal.. In vivo near-infrared mediated tumor destruction by photothermal effect of carbon nanotubes[J].ACSNano,2009,3(11):3707-3713.
[39] BURKE A,DING X,SINGH R,etal.. Long-term survival following a single treatment of kidney tumors with multiwalled carbon nanotubes and near-infrared radiation[J].ProceedingsoftheNationalAcademyofSciences,2009,106(31):12897-12902.
[40] GHOSH S,DUTTA S,GOMES E,etal.. Increased heating efficiency and selective thermal ablation of malignant tissue with DNA-encased multiwalled carbon nanotubes[J].ACSNano,2009,3(9):2667-2673.
[41] LIU X,TAO H,YANG K,etal.. Optimization of surface chemistry on single-walled carbon nanotubes for in vivo photothermal ablation of tumors[J].Biomaterials,2011,32(1):144-151.
[42] YANG K,ZHANG S,ZHANG G,etal.. Graphene in mice:ultrahigh in vivo tumor uptake and efficient photothermal therapy[J].NanoLetters,2010,10(9):3318-3323.
[43] YANG K,WAN J,ZHANG S,etal.. The influence of surface chemistry and size of nanoscale graphene oxide on photothermal therapy of cancer using ultra-low laser power[J].Biomaterials,2012,33(7):2206-2214.
[44] KIM J.-W,GALANZHA E I,SHASHKOV E V,etal.. Golden carbon nanotubes as multimodal photoacoustic and photothermal high-contrast molecular agents[J].NatNano,2009,4(10):688-694.
[45] WANG C,LI J,AMATORE C,etal.. Gold nanoclusters and graphene nanocomposites for drug delivery and imaging of cancer cells[J].AngewandteChemieInternationalEdition,2011,50(49):11644-11648.
[46] MA X,TAO H,YANG K,etal.. A functionalized graphene oxide-iron oxide nanocomposite for magnetically targeted drug delivery, photothermal therapy, and magnetic resonance imaging[J].NanoResearch,2012,5(3):199-212.
[47] CHEN W,ZHANG X,AI F,etal.. Graphitic carbon nanocubes derived from ZIF-8 for photothermal therapy[J].InorganicChemistry,2016,55(12):5750-5752.
[48] SONG X,CHEN Q,LIU Z,etal.. Recent advances in the development of organic photothermal nano-agents[J].NanoResearch,2015,8(2):340-354.
[49] 蘇彥勛,柯沅鋒,蔡士良,等.層層自組裝金納米粒子表面等離子體引發光電流應用于等離子體增感太陽能電池[J].中國光學,2014,7(2):267-273.
SU Y X,KE Y F,CAI SH L,etal.. Layer self-assembly of gold nanoparticles surface plasmon triggered photoelectric current applied plasmon sensitized solar cell[J].ChineseOptics,2014,7(2):267-273.(in Chinese)
[50] 秦沛,任玉,劉麗煒,等.金屬納米顆粒等離激元共振增強非線性介質諧波的發展現狀[J].中國光學,2016,9(2):213-225.
QIN P,REN Y,LIU L W,etal.. Development of plasmon-resonance of metal nanoparticles enhanced harmonic generation in nonlinear medium[J].ChineseOptics,2016,9(2):213-225.(in Chinese)
[51] ROPER D K,AHN W,HOEPFNER M. Microscale heat transfer transduced by surface plasmon resonant gold nanoparticles[J].TheJournalofPhysicalChemistryC,2007,111(9):3636-3641.
[52] CHEN T,XU M,JI M,etal.. Aqueous phase synthesis of Au@Ag3AuX2(X=Se,Te) core/shell nanocrystals and their broad NIR photothermal conversion application[J].Cryst.Eng.Comm.,2016,18(29):5418-5422.
[53] KIM J,PARK J,KIM H,etal.. Transfection and intracellular trafficking properties of carbon dot-gold nanoparticle molecular assembly conjugated with PEI-pDNA[J].Biomaterials,2013,34(29):7168-7180.
[54] JIANG R,LI B,FANG C,etal.. Metal/Semiconductor hybrid nanostructures for plasmon-enhanced applications[J].AdvancedMaterials,2014,26(31):5274-5309.
[55] COZZOLI P D,PELLEGRINO T,MANNA L. Synthesis, properties and perspectives of hybrid nanocrystal structures[J].ChemicalSocietyReviews,2006,35(11):1195-1208.
[56] JANSSENS S,WILLIAMS G V M,CLARKE D. Systematic study of sensitized LaF3∶Eu3+nanoparticles[J].J.AppliedPhysics,2011,109(2):023506.
[57] ZHANG Q,LEE I,JOO J B,etal.. Core-Shell nanostructured catalysts[J].AccountsofChemicalResearch,2013,46(8):1816-1824.
[58] HU Y,LIU Y,LI Z,etal.. Highly asymmetric, interfaced dimers made of Au nanoparticles and bimetallic nanoshells:synthesis and photo-enhanced catalysis[J].AdvancedFunctionalMaterials,2014,24(19):2828-2836.
[59] SHEEHAN S W,NOH H,BRUDVIG G W,etal.. Plasmonic enhancement of dye-sensitized solar cells using Core-Shell-Shell nanostructures[J].TheJournalofPhysicalChemistryC,2013,117(2):927-934.
[60] HALAS N J,LAL S,CHANG W S,etal.. Plasmons in strongly coupled metallic nanostructures[J].ChemicalReviews,2011,111(6):3913-3961.
[61] GUI J,JI M,LIU J,etal.. Phosphine-initiated cation exchange for precisely tailoring composition and properties of semiconductor nanostructures:old concept, new applications[J].AngewandteChemieInternationalEdition,2015,54(12):3683-3687.
[62] ZHANG J,TANG Y,LEE K,etal.. Nonepitaxial growth of hybrid Core-Shell nanostructures with large lattice mismatches[J].Science,2010,327(5973):1634-1638.
[63] YU Z,XIONG S,JIANG J,etal.. Phase-controlled synthesis of Cu2ZnSnS4nanocrystals:the role of reactivity between Zn and S[J].J.AmericanChemicalSociety,2013,135(49):18377-18384.
[64] WANG X,FENG J,BAI C,etal.. Synthesis, properties, and applications of hollow micro-/nanostructures[J].ChemicalReview,2016,116:10983-11060.
[65] KONG L,CHEN W,MA D Y,etal.. Size control of Au@Cu2O octahedra for excellent photocatalytic performance[J].J.MaterialsChemistry,2012,22(2):719-724.
[66] KUO C H,CHU Y T,SONG Y F,etal.. Cu2O nanocrystal-templated growth of Cu2S nanocages with encapsulated Au nanoparticles and in-situ transmission X-ray microscopy study[J].AdvancedFunctionalMaterials,2011,21(4):792-797.
[67] HU H,LIU J,YU J,etal.. Synthesis of Janus Au@periodic mesoporous organosilica(PMO) nanostructures with precisely controllable morphology:a seed-shape defined growth mechanism[J].Nanoscale,2017,9:4826-4834.
Researchprogressofnear-infraredphotothermalconversionnanocrystals
LI Xin-yuan, JI Mu-wei, WANG Hong-zhi, TU Guo-peng, WAN Xiao-dong, LIU Jia-jia, LIU Jia, XU Meng*, ZHANG Jia-tao*
(BeijingKeyLaboratoryofConstruction-TailorableAdvancedFunctionalMaterialsandGreenApplication,SchoolofMaterialsScience&Engineering,BeijingInstituteofTechnology,Beijing100081,China)
Near-infrared photothermal(PT) conversion nanocrystals(NCs), due to their excellent PT conversion performance in near-infrared region(generally in range of 780-1 400 nm), has a wide application potential in the field of cancer cell killing, tumor therapy as well as desalination. These NCs attracted great attention on PT imaging and PT therapy, because of their diverse liquid phase synthesize methods, morphology-controll, nanostructure composite, increasing PT conversion efficiency and easy functionalization . This review aimed to summarize the research progress of near-infrared PT conversion NCs, including noble metal NCs, copper chalcogenide semiconductor NCs, carbon-related NCs, hybrid structure composed of nanocrystalline materials. In addition, the research progress of surface plasmon resonance(SPR) materials with high photothermal conversion efficiency is introduced, especially the application prospect of dual-mode SPR coupling in the field of photothermal conversion. Through the research on the literatures at home and abroad, it is known that the hybrid nanocrystals with dual mode surface plasmon resonance coupling will be an important direction for the development of photothermal conversion nanocrystals in recent years due to the characteristics of performance coordination and coupling.
nanocrystals;near-infrared photothermal conversion;photothermal therapy;surface plasmon resonance
TP394.1; TH691.9
A
10.3788/CO.20171005.0541

李欣遠 (1991—),男,黑龍江齊齊哈爾人,博士研究生,2014年于哈爾濱工業大學獲得學士學位,2015年于英國曼徹斯特大學獲得碩士學位,主要從事納米晶合成方面的研究。E-mail:137419214@qq.com

徐 萌(1986—),男,黑龍江哈爾濱人,講師,2009年于浙江大學獲得學士學位,2014年于中科院國家納米科學中心獲得博士學位,主要從事納米晶合成及生物應用方面的研究。E-mail:xumeng@bit.edu.cn

張加濤 (1975—),男,山東臨沂人,教授,博士生導師,2000年于山東建材學院獲得學士學位,2003年于在北京理工大學獲得碩士學位,2006年于清華大學獲得博士學位,主要從事多功能低維納米復合材料的形貌設計、合成、光電性能及其在光電信息、能源轉化與存儲、光催化應用方面的研究。E-mail:zhangjt@bit.edu.cn
2017-04-18;
2017-05-19
國家自然科學基金項目(No.21643003, No.51631001, No.91323301, No.51501010, No.51372025)
Supported by National Natural Science Foundation of China(No.21643003, No.51631001, No.91323301, No.51501010, No.51372025)
2095-1531(2017)05-0541-14
*Correspondingauthor,E-mail:zhangjt@bit.edu.cn;xumeng@bit.edu.cn

