偽狂犬病及其根除:美國經(jīng)歷的回顧—PRV控制方面的早期嘗試、疫苗及診斷方法
譯校│張淼潔 劉祥 張倩 楊文歡(中國動物疫病預防控制中心)
偽狂犬病及其根除:美國經(jīng)歷的回顧—PRV控制方面的早期嘗試、疫苗及診斷方法
譯校│張淼潔 劉祥 張倩 楊文歡(中國動物疫病預防控制中心)

一、PRV控制的早期嘗試
1.檢疫隔離。偽狂犬病毒(PRV)的暴發(fā)給美國愛荷華州、印第安納州和伊利諾伊州兩個相鄰的大型豬群造成了重大損失。這促使伊利諾伊州在1975年初成立特別工作組,并呼吁召開全國性的PRV研討會。PRV研討會于1975年春季在牲畜保護學會(現(xiàn)為美國國家畜牧業(yè)學會)年會之前召開,會議地點設在伊利諾伊州皮奧里亞市。與會人員報告,從伊利諾伊州牲畜屠宰加工廠采集的6200份血樣中,有139份血樣的PRV檢測結果呈陽性,陽性率為2%。這139份血樣來自43個豬群。共有150~200名豬肉生產(chǎn)商、獸醫(yī)和監(jiān)管官員參與了該次研討會。會上,豬肉生產(chǎn)商要求對發(fā)現(xiàn)的PRV感染豬群進行檢疫隔離。伊州州級獸醫(yī)Paul Doby博士提醒來自其他州的監(jiān)管官員,應注意隔離檢疫帶來的相關問題(尤其是缺乏解除檢疫的方法)。
伊利諾伊州豬肉生產(chǎn)商協(xié)會理事會于次日召開會議,呼吁開展PRV檢疫工作。Paul Doby博士宣布將啟動檢疫隔離項目。此外,伊利諾伊州的豬肉集團請求牲畜保護學會成立PRV常務委員會。這一請求于次日獲得牲畜保護學會理事會的批準。
2. 抗血清現(xiàn)場試驗。
(1)伊利諾伊州。為制定措施以減少PRV所造成的損失,伊利諾伊州農(nóng)業(yè)部門和對生豬行業(yè)感興趣的人士采取了若干項行動,其中有一項行動是由伊利諾伊大學獸醫(yī)學院提出的。該項行動基于這樣的設想:將從感染豬群采集的超免疫抗血清注射到出生時間不超過2天的仔豬體內(nèi),可防止仔豬感染PRV。伊利諾伊大學獸醫(yī)學院為相關項目制定了一套方案。若能籌集到資金,伊利諾伊州官員計劃探索建立PRV超免疫抗血清庫,提供可能的治療方法以減少PRV損失。
該項研究由伊利諾伊州豬肉生產(chǎn)商協(xié)會資助(25000美元)。協(xié)會與伊州卡里市的一家實驗室簽訂了一份收集和處理血清的合同。該項研究利用來自伊州比爾茲敦市某個感染豬群的12頭母豬生產(chǎn)血清。
這一抗血清項目最終生產(chǎn)出了50升PRV超免疫抗血清。項目人員根據(jù)伊利諾伊大學獸醫(yī)學院制定的方案開展現(xiàn)場試驗:同一窩豬有一半以皮下方式注射5毫升超免疫抗血清,另一半作為空白對照。伊利諾伊州農(nóng)業(yè)廳人員花費大量時間與生豬感染群的畜主共同開展抗血清試驗和隔離、分配、注射、收集數(shù)據(jù)、制表等工作。該項研究證實,注射超免疫抗血清使豬的死亡率降低近28%,但在經(jīng)濟上缺乏可行性。
(2)愛荷華州。抗血清在PRV暴發(fā)時仍能發(fā)揮作用,因此被視為抗擊PRV的一種手段。作為豬瘟抗血清來源的豬通常曾接觸過PRV(PRV以非臨床形式普遍存在于豬群中)。這一事實使得關于抗血清功效的現(xiàn)場報告更加合乎邏輯。
早期嘗試生產(chǎn)抗血清期間,伊利諾伊大學通過注射活病毒(3~4次)使母豬具備超免疫性,然后將母豬麻醉并抽血。通過簡單的凝血和離心操作獲得血清。若干家生產(chǎn)商為伊利諾伊大學開展的研究提供了少量資金。這些生產(chǎn)商的設施被作為試驗現(xiàn)場。PRV暴發(fā)期間,在新生豬免疫處理方面開展的早期嘗試并未取得顯著的成功。一位經(jīng)驗豐富的疫苗公司代表指出,一半的豬注射血清、另一半作為空白對照可能導致對照組出現(xiàn)病毒復制和排出現(xiàn)象,進而導致注射超免血清豬體內(nèi)的抗血清失去防護作用。這一意見獲得了項目人員的認可。不久之后,研究證實,如果同一窩的所有豬均注射抗血清(或者采取更好的做法——若干個相鄰豬窩的所有豬均注射抗血清),抗血清將發(fā)揮非常好的防護作用。
抗血清被證明是一種有效的預防性物質(zhì),但它最終并未投入使用。導致這一結果至少有兩個原因:商業(yè)公司追求開發(fā)和生產(chǎn)過程的經(jīng)濟性,一般將重點放在疫苗開發(fā)活動上;批準這種可能含有外來病毒的產(chǎn)品會引發(fā)廣泛的擔憂,且這種產(chǎn)品缺乏實用的消毒方法。
二、疫苗診斷方法及其許可
1.歷史。20世紀70年代初,獸醫(yī)學診斷專家利用當時可用的試驗手段,通過剖檢、鏡檢、病毒分離和組織熒光抗體試驗檢測活病毒。
隨著PRV的擴散,通過生物控制和診斷試驗檢測抗原和抗體(特別是以診斷、監(jiān)管和根除為目的快速測試大量血清標本)成為一項迫切的需求。血清病毒中和試驗是當時惟一可開展的血清學試驗。該項試驗從開始到結束,需要3天的時間。
血清學試驗的首次改良是利用96孔板將血清病毒中和試驗微型化。這次改良產(chǎn)生了一項金標準——微量滴定血清病毒中和試驗。該試驗被認為擁有良好的敏感性和特異性,且能夠利用倍比稀釋方法對抗體進行量化。但是,該試驗同樣需要消耗大量的時間和人力,特別是需要通過顯微鏡對多次反應進行觀察。限制了每天可測試的樣本數(shù)量。
下一項重大改良是愛德士實驗室有限公司(緬因州,韋斯特布魯克)于1986年獲得批準的篩選試驗——ELISA(HerdChek?Anti-PRV)。ELISA用于從大量血清標本中篩選PRV抗體,在推出之后不久就取代了血清病毒中和試驗。ELISA可大大縮短試驗時間,大幅提升實驗室的處理能力,因為它不需要對血清標本進行滴定,反應速度快,試驗結果通過機器讀取和解釋。
隨著PRV疫苗被開發(fā)并廣泛用于豬群,人們需要將接種PRV疫苗的豬與感染PRV的豬區(qū)分開。血清病毒中和試驗和ELISA都可以檢測PRV抗體,但無法區(qū)分疫苗抗體和野毒感染抗體。診斷專家和監(jiān)管官員最初嘗試根據(jù)血清病毒中和試驗的抗體滴度將接種疫苗的生豬與感染生豬區(qū)分開。這種嘗試所基于的假設是,相比接種疫苗,感染野毒能產(chǎn)生更強烈的體液反應。該方法將抗體滴度≤(1∶16)視為接種疫苗的結果,而不是感染的結果。但是,在任一生物系統(tǒng)中,不同豬(尤其是多次接種疫苗的豬)的抗體反應會呈現(xiàn)差異。這意味著,許多動物和畜群會被誤判為感染或未感染。該方法在臨床上多少能發(fā)揮一些作用,但不能作為監(jiān)管決策(例如關于生豬跨州運輸和其他監(jiān)管問題的決策)的依據(jù)。
隨著PRV在美國豬群中的持續(xù)擴散,生物控制成為首要的需求。諾登實驗室(內(nèi)布拉斯加州,林肯)于1977年批準了首個常規(guī)弱毒活疫苗和滅活PRV疫苗。總體而言,PRV弱毒活疫苗之所以得到廣泛的應用,是因為它的免疫反應和所產(chǎn)生的防護作用優(yōu)于滅活PRV疫苗。
PRV弱毒活疫苗和后續(xù)開發(fā)的二代基因缺失疫苗對于減少和防范PRV的臨床癥狀十分有效。接種PRV弱毒活疫苗的豬后續(xù)感染PRV野毒株時,病毒較少侵入組織,且妊娠母豬未將病毒傳播給胎豬。因此,該疫苗可防止流產(chǎn)。但是,接種PRV疫苗的豬感染PRV野毒株時至少排出成千的病毒,減少病毒的排出對于根除PRV至關重要。某些PRV弱毒活疫苗聚集在主要參與潛伏性感染的組織內(nèi)(三叉神經(jīng)節(jié)),進而阻斷PRV野毒株通過重復感染實現(xiàn)潛伏的過程。
2. 疫苗和診斷方法的開發(fā)。私營企業(yè)曾針對豬群開發(fā)若干種基因缺失PRV疫苗。這些疫苗獲得了動植物檢疫署獸用生物制品中心的許可。首個基因缺失疫苗(含一套相應的血清學鑒別診斷試驗)在“國家PRV根除項目”啟動的前一年,即1988年獲得許可。該疫苗毒株缺失糖蛋白基因gX(gG),由SyntroVet有限公司(堪薩斯州,雷那克薩)制造。該疫苗配套的ELISA血清學鑒別診斷試驗(HerdChek?Anti-PRV-gpX)由愛德士實驗室有限公司開發(fā)。多家生產(chǎn)商表示,這一名為“Marker Blue”的疫苗注射到北卡羅來納州生豬密集區(qū)域的豬群體內(nèi)后產(chǎn)生了高度的防護作用。一年之后,普強公司(密歇根州,卡拉馬祖)獲批了一種缺失gG基因的疫苗(Tolvid?)(配套相應的血清學鑒別診斷試驗)。這兩種疫苗都很有效,但診斷試驗的敏感性不夠理想。
表1列出了各類PRV疫苗、配套的鑒別診斷試驗及其制造商和所采用的PRV毒株。
1990年,SyntroVet和IDEXX再次開展合作,推出了一種基于缺失糖蛋白基因gI(gE)的病毒開發(fā)出的新疫苗(SyntroVet PRV/Marker Gold?),含配套的ELISA血清學鑒別診斷試驗(HerdChek?Anti-PRV-gl)。與首個基因缺失疫苗一樣,Marker Gold在實踐中表現(xiàn)出良好的功效。此外,血清學鑒別診斷試驗的敏感性和特異性有顯著提升。
另外兩家生物制品公司也開發(fā)了缺失gE基因的疫苗。諾登實驗室的PR-Vac?疫苗缺失天然gE基因。收購諾登實驗室的史克必成公司于1990年開發(fā)并推出了一種血清學鑒別診斷試驗——Clin- Ease-PRV?。勃林格殷格翰公司的PRV疫苗BioCeutic?與IDEXX開發(fā)的HerdChek?Anti-PRV-gI配套血清學鑒別診斷試驗一起獲得許可。
PR-Vac和PRV/Marker Gold?是根除項目期間應用最廣泛的PRV疫苗。同時,IDEXX開發(fā)的HerdChek?Anti-PRV-gI ELISA試驗方法成為確定生豬或豬群是否接種PRV疫苗、是否感染PRV的“標準”血清學鑒別試驗。Tolvid疫苗非常有效,但配套的gG血清學鑒別診斷試驗缺乏敏感性,對其使用造成了限制。此外,由于行業(yè)當時呈現(xiàn)明顯的gE基因缺失技術標準化的趨勢,缺失gG基因對Tolvid疫苗而言是一種缺點。在豬群中同時使用gG基因缺失疫苗和gE基因缺失疫苗會造成混淆,因為接種gG基因缺失疫苗的生豬會產(chǎn)生gE抗體,進而導致gE血清試驗期間接種疫苗的豬群被錯誤地認定為感染豬群。反過來,利用gG ELISA對接種gE基因缺失疫苗的種豬進行試驗時,也會產(chǎn)生錯誤的診斷結果。因此,PRV根除項目要想獲得成功,必須為所有PRV疫苗確立統(tǒng)一的基因缺失標準。如果行業(yè)未能就PRV疫苗缺失哪種基因達成共識,將無法開展血清檢測。對基因缺失疫苗進行標準化(至少刪除表達gE的基因)的協(xié)議于1993年實施。
為檢測PRV抗體,行業(yè)開發(fā)了其他若干種血清學試驗方法。微粒濃縮熒光免疫分析和自動化乳膠凝集試驗是兩種在高通量診斷實驗室得到廣泛應用的方法。與ELISA類似,這兩種試驗以自動化方式開展,僅耗時2個小時,具有良好的敏感性和特異性。某些實驗室持續(xù)將自動化乳膠凝集試驗用于篩選PRV抗體。生物制品制造商還開發(fā)了補體結合、免疫擴散、對流免疫電泳、間接免疫熒光等其他若干種血清學試驗方法,但都存在敏感性有限、耗時過長或難以實施的問題。
2005年11月3日,獸用生物制品中心批準了IDEXX基于gII(gB)糖蛋白開發(fā)的新型阻斷式ELISA-PRV篩選試驗方法。據(jù)報道,該試驗的敏感性和特異性高達99.5%,已經(jīng)取代了HerdChek Anti-PRV篩選試驗。
PRV根除項目的成功很大程度上要歸功于開發(fā)出高效PRV疫苗和配套血清學鑒別診斷試驗方法的科學家和診斷專家。如果沒有這些技術,這一項目根本不會存在。
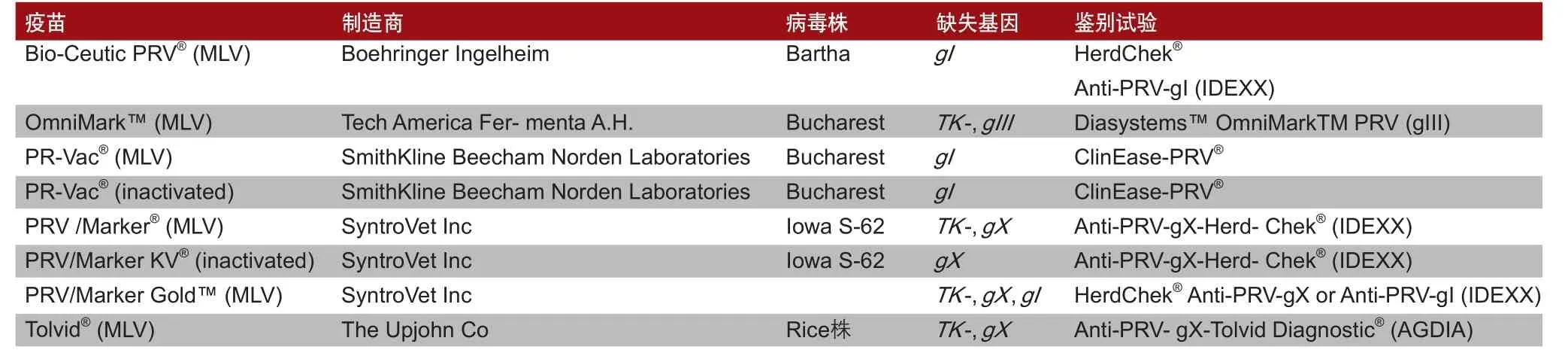
表1 PRV疫苗和伴隨診斷鑒別試驗
3.技術的實際應用。對于從事生豬藥物工作的獸醫(yī)而言,將鑒別試驗投入實際應用是一項高難度的教學和輔導活動。首先,獸醫(yī)們必須學習關于鑒別試驗為什么具備可行性的基礎理論。其次,他們必須讓生產(chǎn)商相信這一新的測試理念是有效的。以往的經(jīng)驗表明,當前使用的大多數(shù)疫苗可有效防止生豬的臨床疾病。
在疫苗的研究、開發(fā)和專利申請領域,科學家和動物衛(wèi)生企業(yè)之間存在激烈的競爭。這種競爭促使多種基因缺失疫苗被批準并投放市場。開發(fā)這些疫苗的企業(yè)必須與開展動物診斷試驗的企業(yè)合作,因為只有極少數(shù)的疫苗開發(fā)企業(yè)同時擁有生產(chǎn)經(jīng)批準的疫苗和開發(fā)配套診斷試驗所需的商業(yè)資產(chǎn)。
PRV根除活動初期,一些獸醫(yī)在同一豬群中使用超過一種PRV疫苗。此外,某些PRV疫苗既不具備特異性,也未開發(fā)配套的試驗方法。使用缺失不同基因的疫苗且未能充分保存記錄的畜主發(fā)現(xiàn),他們無法準確地解釋試驗結果,因而無法了解其豬群的狀況。
最初,生產(chǎn)商和獸醫(yī)期望試劑盒的敏感性和特異性達到100%。但是,實地條件下的經(jīng)歷表明,這一期望落空了。此外,不同系列的試劑盒的試驗結果之間存在一些差異,而非特異性反應要在測試數(shù)千個樣本之后才能觀測到。當時,診斷專家、執(zhí)業(yè)獸醫(yī)和監(jiān)管官員難以對造成試驗結果沖突的眾多原因進行分類。這些差異會造成一定的問題,少數(shù)生產(chǎn)商和獸醫(yī)最初以此為由拒絕全面采用這一新技術。
4.小步前進。率先理解這一技術并將其成功運用于豬群凈化方案的人士經(jīng)常受到批評。這些人通常擁有自己的豬群,并利用自己的豬群來證明相關疫苗及配套診斷試驗的效果。在學習過程中,很多人都有過“前進兩步、后退一步”的經(jīng)歷。生豬行業(yè)的領導者通過召開論壇,對該技術應用的成敗進行探討。存在競爭關系的科學家和動物衛(wèi)生公司的參與增加了這些討論活動的復雜性。他們每個人都在鼓吹自己的技術優(yōu)勢。論壇的參與者定期匯報田間案例,并對其進行討論。
關于成功案例的報告開始在生豬行業(yè)內(nèi)傳播,批評者甚至也開始注意到該技術在應用方面所取得的進展。隨著試驗技術的發(fā)展及各種試驗方法的敏感性和特異性的提高,評估豬群凈化方案的能力也有所提升。隨著實踐中應用數(shù)量的增加,這些產(chǎn)品開始證明哪些技術實現(xiàn)了疾病防控(疫苗)和實驗準確性(診斷方法)的最佳結合。這些“優(yōu)勝”的技術逐漸成為生豬行業(yè)的首選。
5.逐個完成。完成豬群凈化活動的例子有很多。將完成此類活動所需的各個步驟整理成名為“豬群凈化方案”的書面材料是一種普遍的做法。通過研究凈化感染豬群的實例,可以更好地理解這一過程。
(1)初步聯(lián)系。豬群的主治獸醫(yī)聯(lián)系疫苗公司的技術服務獸醫(yī)前往某個PRV凈化進度不如預期的豬群進行調(diào)查,并開展合作。
(2)現(xiàn)場訪問。技術服務獸醫(yī)和主治獸醫(yī)審核驗血結果和該豬群使用的PRV疫苗的品牌名稱。
(3)分析。技術服務獸醫(yī)和主治獸醫(yī)確認,該豬群過去4年使用了兩個品牌、缺失不同基因的PRV疫苗,其中一些年齡較大的生豬這兩種疫苗都使用過;該豬群過去2年只使用了一種疫苗;盡管使用了疫苗,該豬群仍存在感染PRV的情況。
(4)養(yǎng)殖場訪問。訪問養(yǎng)殖場期間,技術服務獸醫(yī)和主治獸醫(yī)對畜主當前的操作方法進行觀察。此外,他們還檢查了疫苗接種記錄和動物標識的完整性。
(5)初步行動計劃。豬群管理人員識別出所有年齡大于2周歲的生豬,并在下一窩豬斷奶之后將這些生豬出售,供宰殺。
(6)豬群重新接種疫苗。對整個豬群進行評估,確保所有生豬在過去90天均已接種疫苗。管理人員將沒有標識的生豬出售,供宰殺。
(7)檢測并挑選結果呈陰性的動物。對所有年齡小于2周歲、大于3個月的生豬進行檢測,以確定野毒感染的血清學狀況。如果某一豬只的測試結果呈陽性,該豬只將被盡快出售,供宰殺。血清反應呈陽性的豬只不會被用來交配。管理人員采取較為激進的措施清除曾注射兩種不同品牌的基因缺失疫苗、感染PRV以及年齡較大的豬只。
(8)隔離。技術服務獸醫(yī)和主治獸醫(yī)建議,將年齡較大的豬只與年齡較小的豬只隔離。
(9)選擇并使用同一品牌的疫苗。技術服務獸醫(yī)和主治獸醫(yī)提倡利用缺失同一種基因的疫苗產(chǎn)品繼續(xù)開展疫苗接種工作。此外,這些咨詢?nèi)藛T還建議,每90天對所有豬只開展一次疫苗接種工作,以盡量提高免疫性、盡量減少病毒的排出量。
(10)跟蹤計劃。在開展豬群凈化90天后對年齡較小的豬只進行統(tǒng)計抽樣,并在咨詢?nèi)藛T的建議下開展分析工作,旨在更好地評估病毒在年齡較小、易受影響、接種疫苗的豬只之間的傳播情況。這種分析還被用于向畜主證實凈化項目已取得的進展。
(11)評估。如統(tǒng)計樣本對野毒抗體的反應呈陰性,豬群凈化方案不作變更。如任一樣本的血清反應呈陽性,咨詢?nèi)藛T將對豬群凈化方案進行二次評估,明確方案的缺點并進行相應調(diào)整。
(12)區(qū)域評估。技術服務獸醫(yī)和主治獸醫(yī)對區(qū)域內(nèi)的豬群密度進行評估,以確定豬群接觸來自相鄰豬群的PRV的風險。地區(qū)監(jiān)管官員也參與決策過程,并為地區(qū)風險評估提供協(xié)助。
(13)完成。PRV通常在豬群凈化方案啟動兩年內(nèi)被清除。
每個豬群都面臨著一系列挑戰(zhàn)。某些時候,管理方法必須接受評估并進行多次變更。養(yǎng)殖場的雇員必須就如何實施各豬群凈化方案的各個步驟接受教育和輔導。畜主對成功實施豬群凈化方案的積極性存在差異。一位成功的獸醫(yī)能了解所有這些不斷變化的挑戰(zhàn)。
豬群有時會出現(xiàn)意想不到的問題。管理人員在評估和監(jiān)督過程中發(fā)現(xiàn)許多令人瞠目結舌的事件,例如心懷不滿的雇員將疫苗倒入糞池。分析發(fā)現(xiàn),養(yǎng)殖場的自來水中含有高濃度的氯,用這些自來水清洗注射器導致弱毒活疫苗失去活性。這些事件使人們關注到所有細節(jié)的重要性。
此外,試驗期間偶爾會發(fā)現(xiàn)某一豬群只有一頭豬的試驗結果呈陽性(又稱“個例”)。 有時對處死的豬只進行組織分析,發(fā)現(xiàn)其并未感染PRV。類似的意料之外的結果很少出現(xiàn),但提醒人們:不同豬只之間的生物差異性也需要納入考慮范疇。
6.基因缺失疫苗和診斷試劑盒的許可。PRV疫苗和診斷試劑盒在美國是依據(jù)《病毒-血清-毒素法案》(1913)(1985年修訂版)接受監(jiān)管的獸用生物產(chǎn)品。該法案規(guī)定,出售無效、受污染、危險或有害的獸用生物制品屬非法行為,在美國境內(nèi)或從美國運輸?shù)墨F用生物制品必須是在經(jīng)批準的設施內(nèi)按美國農(nóng)業(yè)部法規(guī)制備的產(chǎn)品。將這些產(chǎn)品投放美國市場之前,企業(yè)必須為其生產(chǎn)設施獲取“美國獸用生物制品公司許可證”,并為其生產(chǎn)的每一種產(chǎn)品獲取“美國獸用生物產(chǎn)品許可證”。
(1)疫苗的通用許可要求。某一經(jīng)批準的獸用生物制品公司如想為某個PRV弱毒活疫苗獲取獸用生物產(chǎn)品生產(chǎn)許可證,必須向動植物檢疫署獸用生物制品中心提交獸用生物產(chǎn)品許可證申請,并出示生產(chǎn)數(shù)據(jù)和支持性數(shù)據(jù)為產(chǎn)品申請?zhí)峁┲С帧Ia(chǎn)大綱是產(chǎn)品制造和試驗所依據(jù)的具體方案。
申請企業(yè)必須根據(jù)生產(chǎn)大綱提供數(shù)據(jù)證明產(chǎn)品的純度、安全性和功效。將主毒種作為疫苗生產(chǎn)所用的所有毒種的來源有助于保持生產(chǎn)活動的統(tǒng)一性。主毒種連續(xù)傳代的限定次數(shù)為5次。獸用生物制品中心的人員負責確保主毒種、主細胞庫、原代細胞、動物源性成分和最終產(chǎn)品根據(jù)標準試驗程序接受測試。產(chǎn)品的免疫原性必須通過具有統(tǒng)計有效性的動物疫苗接種和攻毒試驗(通常采用20頭接種疫苗的生豬和5頭對照組生豬)予以證明。疫苗接種必須在生產(chǎn)大綱規(guī)定的年齡最小的動物身上實施,并采用最低數(shù)量的抗原。產(chǎn)品應采用主毒種繁殖的最高代次的毒種生產(chǎn)。申請企業(yè)必須確定產(chǎn)品標簽顯示的各個成分的功效。具體的攻毒方法和作用確定保護力的標準隨免疫原的變化而變化。每一系列產(chǎn)品被許可之前,獸用生物制品中心的人員還會要求測定產(chǎn)品的效價。
安全測試結合了一系列研究工作。產(chǎn)品一般以10倍劑量在動物宿主體內(nèi)使用以接受評估。活疫苗產(chǎn)品必須進行特征化處理,以確定其是否有能力從宿主體內(nèi)排出,進而傳播至與宿主接觸的動物體內(nèi)。為了解遺傳穩(wěn)定性及實踐中疫苗注入動物體內(nèi)的預期結果,需開展直腸研究。

表2 獲得許可的基因改造PRV疫苗
一旦實驗室完成特征化研究,即可以獲得額外的安全數(shù)據(jù)為目的開展田間試驗。田間安全試驗的設計目的是檢測產(chǎn)品開發(fā)期間未觀察到的意外反應。相關試驗在動物宿主體內(nèi)開展,分布在各類場所,使用大量易感的動物。試驗動物應能代表擬使用相關產(chǎn)品的所有年齡階層和飼養(yǎng)方法。
獲得生產(chǎn)許可證的企業(yè)需在其經(jīng)批準的設施內(nèi)根據(jù)批準的生產(chǎn)大綱連續(xù)生產(chǎn)3個批次符合要求的產(chǎn)品,并將主毒種、主細胞庫和這些批次產(chǎn)品的標本發(fā)送給獸用生物制品中心的實驗室以接受許可前測試,以確認企業(yè)的試驗結果。
申請企業(yè)滿足所有要求(包括標簽、宣傳資料的審核和驗收方面的要求)之后,獸用生物制品中心發(fā)放“美國獸用生物產(chǎn)品許可證”。
(2)基因缺失疫苗的其他要求。獸用生物制品中心認為,重組體衍生的弱毒活疫苗與常規(guī)方法生成的疫苗之間沒有重大差異。因此,該中心認為現(xiàn)有法律法規(guī)適用于新型基因改造PRV疫苗,并要求這些疫苗滿足上文描述的適用于常規(guī)疫苗的純度、安全性和功效許可標準。但是,《國家環(huán)境政策法案》則要求,為這些基因改造活疫苗申請許可證的企業(yè)在疫苗被放行之前開展研究工作,評估這些疫苗對人類環(huán)境可能產(chǎn)生的所有影響。需開展的調(diào)查活動包括通過研究描述重組微生物的生物化學特性,評估其在體內(nèi)外的遺傳穩(wěn)定性,檢查其在宿主體內(nèi)的組織嗜性或毒性是否有任何變化,評估其從宿主體內(nèi)排出并擴散至靶宿主和非靶宿主的可能性,評估其在環(huán)境中持續(xù)生存的能力,檢查其與類似的微生物野毒株進行重組的可能性。在產(chǎn)品投入現(xiàn)場試驗或獲得許可證之前,獸用生物制品中心的人員利用來自這些研究活動的數(shù)據(jù),根據(jù)《國家環(huán)境政策法案》開展風險分析,為環(huán)境評估做準備。《國家環(huán)境政策法案》的程序還要求,該中心通過《聯(lián)邦公報》公示其擬開展的所有重組體微生物許可。
針對首類基因改造疫苗(缺失PRV基因組中的兩個基因),企業(yè)在獲準開展田間試驗之前必須滿足《國家環(huán)境政策法案》的要求。為確定該基因對人類環(huán)境的安全性,企業(yè)需通過開展研究工作證明:
①基因改造PRV活疫苗病毒無毒性,完全有能力引發(fā)使生豬免于感染PRV的免疫反應,但無法誘導產(chǎn)生gG抗體。因此,感染生豬與接種疫苗的生豬之間存在血清學差異。②接種疫苗的生豬或哨兵動物的鼻拭子無法證明這種由重組體DNA技術產(chǎn)生的疫苗病毒發(fā)生了傳播。③接種重組疫苗可減少野毒株的復制和排出現(xiàn)象。因此,這種疫苗可減少烈性病毒在環(huán)境中的傳播。④缺失TK基因是疫苗病毒的一個穩(wěn)定特性,這種缺失出現(xiàn)逆轉的可能性基本為零。⑤PRV野毒株在自然界分布廣泛,且不含致癌基因或致癌物質(zhì)。由于不含任何新的遺傳信息,病毒所產(chǎn)生的重組體不可能具有致癌性。⑥PRV野毒株對人類無致病性。缺失兩個基因是重組體衍生的疫苗與PRV野毒株存在的惟一區(qū)別。因此,重組體衍生的疫苗也被認為對人類無致病性。⑦生產(chǎn)該疫苗的企業(yè)制備并進行特征化處理的主毒種與親株的生物性質(zhì)相同。向獸用生物制品中心提交的數(shù)據(jù)確立了用于制備實驗疫苗的兩個病毒庫之間的相互關系。在此基礎上,獸用生物制品中心確定重組體衍生的活病毒疫苗的田間試驗不會對人類環(huán)境產(chǎn)生重大影響。
除評估整體安全性之外,現(xiàn)場研究還包括評估該疫苗對公豬的精子質(zhì)量、母豬和幼年母豬的生殖能力及在自然環(huán)境下飼養(yǎng)的架子豬的感染率和長勢的影響。現(xiàn)場研究結束且數(shù)據(jù)表明安全性符合要求之后,獸用生物制品中心在《聯(lián)邦公報》發(fā)布第二份公告,并在環(huán)境評估中考慮預示該產(chǎn)品將獲得許可證的田間試驗結果。重組體后續(xù)衍生的PRV疫苗(見表2)的許可工作重復這一過程。通過選擇天然突變的病毒開發(fā)出的疫苗以常規(guī)疫苗的身份獲得許可。
(3)診斷方法通用許可要求。診斷產(chǎn)品的許可在申請、證明材料和程序方面與上文針對常規(guī)疫苗描述的內(nèi)容一致,區(qū)別在于支持性數(shù)據(jù)必須涉及多項問題。診斷產(chǎn)品的數(shù)據(jù)必須證明產(chǎn)品的敏感性、特異性、耐用性、重復性、適用性及預測值。此類數(shù)據(jù)通過將新的診斷試驗方法與當前的“金標準”進行對比來獲得對高度特征化的參考標本(來自至少20只動物)進行測試,標本取自PRV測試結果呈陰性的動物(未被感染的動物)、PRV測試結果呈強陽性的動物、PRV測試結果呈弱陽性的動物、所產(chǎn)生的分析值在閾值周圍的標本,對密切相關的抗原(可能是交叉反應性抗原)有反應的動物或接種疫苗的動物及只對多抗原反應性檢測試劑盒中的某一個或某一組抗原有反應的動物。
(4)PRV診斷試驗的審批。隨著防止PRV擴散的生豬跨州流動法規(guī)的發(fā)布,經(jīng)批準的PRV診斷試驗被要求只在經(jīng)批準的實驗室內(nèi)開展。因此,獸用生物制品中心批準某項PRV診斷試驗方法并不會自動授權相關機構在生豬跨州流動的官方測試中采用該方法。除獲得許可證之外,PRV診斷試驗還需獲得動植物檢疫署國家獸醫(yī)服務實驗室人員的審批推薦,并獲得動植物檢疫署國家動物衛(wèi)生項目中心的批準,動植物檢疫署同時也是聯(lián)邦負責發(fā)布《州-聯(lián)邦-行業(yè)PRV根除項目標準》的機構。

表3 20世紀90年代中期獲得許可的PRV鑒別試驗方法
PRV診斷試驗批準程序的設計目的是為該試驗的潛在用戶提供體驗產(chǎn)品的機會,并使合作方能更可靠地確定疫苗產(chǎn)品能否按標簽上描述的內(nèi)容發(fā)揮作用,并在各類指定現(xiàn)場條件下和不同實驗室內(nèi)產(chǎn)生一致的、可再現(xiàn)的結果。為此,制造商負責開展田間試驗,并將結果上報給美國獸醫(yī)實驗室診斷專家協(xié)會、美國動物衛(wèi)生協(xié)會和國家獸醫(yī)服務實驗室。同時,制造商要向至少3個位于美國不同地區(qū)的實驗室提供試劑盒,比對金標準測試參考標本和實地標本。國家獸醫(yī)服務實驗室、美國獸醫(yī)實驗室診斷專家協(xié)會與國家動物衛(wèi)生項目中心、獸用生物制品中心共同審核這些實驗室提供的與產(chǎn)品在PRV根除項目中的潛在用途有關的數(shù)據(jù)。如符合前述設計目的,相關試驗方法將獲得審批推薦,國家動物衛(wèi)生項目中心將通過《聯(lián)邦公報》發(fā)布公告告知利益相關方:該方法被批準用于經(jīng)批準的PRV根除項目官方檢測實驗室。
PRV鑒別試驗的批準程序還要求試驗方法能將接種疫苗的生豬與感染野毒株的生豬區(qū)分開。此外,試驗方法應:僅用于接種相關官方批準的基因改造疫苗的豬群;用于對豬群(而非單頭生豬)進行診斷;在經(jīng)國家獸醫(yī)服務實驗室批準的實驗室實施。
首個PRV鑒別試驗方法于1988年8月1日獲得批準,并于1990年5月9日成為供PRV根除項目使用的“經(jīng)批準的PRV鑒別試驗方法”。截至20世紀90年代中期,已有5個PRV鑒別試劑盒獲得許可,其中2個PRV鑒別試劑盒獲得批準用于根除項目(見表3)。