與敵共生
楊醬醬
在人類與微生物的戰爭中,我們一直試圖將有害細菌斬盡殺絕。然而這種“鐵腕鎮壓”不僅造成了耐藥細菌的瘋狂反擊,還誤傷了人體內的有益菌群。隨著抗生素的研發越來越艱難,病菌的耐藥性越來越強,我們也許應該停止這種劍拔弩張的對立,和“敵人”握手言和。
人體內存在大約1萬種細菌,其中超過99%的細菌對人體無害。事實上,很多細菌能夠給人體提供營養,優化免疫系統,防止情感障礙。人類是依賴于這些細菌的。而對于少數有害的細菌,我們一向是除惡務盡,對付這些細菌最有效的武器就是抗生素。
然而,服用抗生素常常引發胃部不適,這是因為,當我們殺死少數致病菌時,也一并殺死了好的細菌。如今,隨著一代又一代醫生為流鼻涕這樣的小病開出抗生素,我們已經發現其導致的副作用遠遠超過了偶爾的肚子疼。
不加區別地清除細菌,可能導致過敏、肥胖、哮喘發病率的上升和其他問題。抗生素的這些不利影響,加上日益增長的抗生素耐藥性的威脅,促使一些研究人員轉變了對抗細菌的理念:是時候停止這場進行了近一個世紀、試圖將細菌全部清除的戰爭了。如果可以在不殺死它們的情況下清除致病菌,就可以有效降低細菌耐藥性,緩解藥物過度使用,并完好保留對人體有益的菌群。這可能意味著要啟用一些過去被遺忘的方法。如果說20世紀是由我們消滅致命病菌的能力所定義的,那么21世紀就是我們學會與細菌和平相處的時代。
19世紀末期,病菌被證明會導致疾病。自此,開始了人類與細菌近一個世紀的斗爭。我們用消毒液除去食物、水和房屋中的細菌,用疫苗激活免疫系統,利用青霉素等化學武器殺死細菌,因而死于感染性疾病的人數至少減少了90%。我們理所當然地享有長壽,免受瘟疫和感染的困擾,然而這在人類歷史上是絕無僅有的。
免受瘟疫和感染是需要付出代價的,可能導致免疫系統、代謝系統紊亂甚至精神問題。服用一劑抗生素就好像往地鐵里扔一顆臭氣彈,熏走罪犯嫌疑人的同時也趕走了普通人,而老鼠和蟑螂卻泰然自若。
活下來的細菌會對我們的武器——抗生素,產生抵抗力。在美國,每年約有2.3萬人死于耐藥菌感染。盡管如此,那些關于“超級細菌”即將到來的傳言還是有很多夸大的成分,因為這些耐藥細菌的主要“攻擊”對象是老年人或已經生病的人。但毋庸置疑的是,濫用抗生素會引起細菌耐藥性增強,而我們尋得新的替代藥品的速度又非常緩慢。

濫用抗生素不僅造成細菌耐藥,還會引發其他問題
抗毒力療法不僅為治療感染提供了更多可選擇的藥物,還能在確實需要使用抗生素的時候提高其療效。
如果能在不殺死細菌的情況下治療感染,那細菌就沒必要進化出耐藥性。這種治療方法叫做抗毒力療法,它不僅為治療感染提供了更多可選擇的藥物,還能在確實需要使用抗生素的時候提高其療效。專家認為,如果我們不是每一次感染都使用抗生素,那么細菌對抗生素產生耐藥性的速度就會變緩,我們就能在更長的時間內繼續使用抗生素。
那么我們該怎么做呢?答案是在細菌造成壞的影響前阻止它們。致病菌需要“占領”人體內的特定部位才會造成感染;如果它們不能“占領”這個位置,就無法形成感染。
運用抗毒力療法有望治療下尿路感染——一種在女性中特別常見的疾病。大部分尿路感染由大腸桿菌引起,它們將用自己毛發狀的菌毛黏附到細胞表面的糖類上。研究人員發現,如果給人類提供與細胞表面糖類物質結構相似的糖類作為誘餌,大腸桿菌會黏附在誘餌上而無法附著在細胞表面。這樣,這些細菌就會隨尿液排出體外。
一個針對患有頑固性尿路感染女性的小規模試驗顯示,在6個月內,使用單一糖類D-甘露糖的患者中僅有15%復發感染;使用抗生素的患者則有20%復發;而僅給予安慰劑的患者的復發率為61%。另一個試驗顯示,服用D-甘露糖溶液的患者,平均復發時間間隔超過6個月,而使用抗生素的患者僅間隔52天。
還有研究發現,當對進行過D-甘露糖治療的患者再次使用抗生素時,抗生素的療效增強了。因為在無抗生素的環境中,對抗生素敏感的常規菌株比耐藥菌株的適應性更強,這些常規菌株能競爭到更多資源,數量遠遠大于耐藥菌。這就意味著,當實在需要使用抗生素時,因為極大部分細菌都是容易被殺死的常規菌,抗生素就變得更有效。研究人員對細菌樣本進行檢測時發現,使用D-甘露糖后,細菌對抗生素的敏感性增加,而其產生的副作用很小。
更高級的阻斷劑也正在研發中。來自美國華盛頓大學的科學家研發出一種更有效的、能在人體內停留更久的合成甘露醇衍生物,只要使用很小的劑量就能產生良好的療效。老鼠實驗的結果顯示,一劑藥可阻斷大腸桿菌感染至少三天,并在6小時內開始清除已存在的感染。同時,由于這種藥物僅僅是阻斷大腸桿菌而不是殺死它們,細菌沒必要進化出耐藥性,在尿道里存在的有益菌也可以安全地保留下來。這項研究產生的潛在影響是巨大的:僅僅在美國,每年針對尿路感染開出的抗生素處方就多達2500萬份,并且,其中超過一半的患者會復發。藥物的開發者認為,阻斷劑將掀起一場免抗生素療法革命。
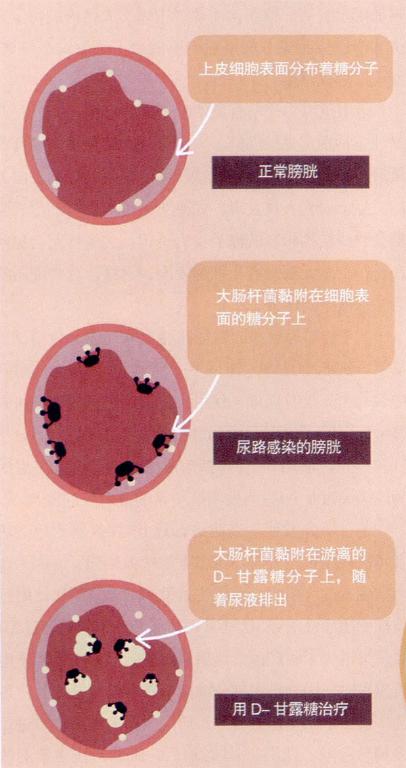
D-甘露糖治療尿路感染的原理
隨著耐藥性問題日益嚴重,被遺忘多時的抗毒素療法正在被重新審視。
如果不能阻止細菌繁殖,另一被遺忘多時的方法是抗毒素療法。這種方法通過中和細菌分泌的毒素,以阻止其破壞細胞和汲取營養。19世紀80年代,德國細菌學家埃米爾·馮·貝林和其日本同事北里柴三郎首次應用這一方法。他們將致死量的白喉毒素和破傷風毒素注入動物體內,提取出動物體產生的抗毒素,用以治療病人。這種方法最終將白喉和破傷風感染的死亡率降低了一半,并為貝林贏得了首屆諾貝爾生理學或醫學獎。但是,在抗生素出現之后,抗毒素療法幾乎被拋棄了。endprint
一位細菌學家說:“抗生素療法太過成功,以至于很多其他治療方法都被遺忘了,導致我們現在缺乏其他可供選擇的治療方法。”隨著耐藥性問題日益嚴重,抗毒素療法正在被重新審視。
在治療腹瀉上,抗毒素療法也具有很大潛力。在美國,每年有近3萬人死于艱難梭菌引起的腹瀉。這種細菌的感染通常發生在進行抗生素治療的住院期間。解決辦法通常是加大抗生素的使用量,但其中1/4的病人會再次感染。在最近的實驗中,如果同時給病人使用一種可中和艱難梭菌毒素的藥物,則幾乎可以將復發率降低一半。麻煩的是,這種治療方法并不一定能降低因感染造成死亡的風險。然而,也有學者認為,抗毒素療法的概念是正確的,并相信下一代抗毒素藥物將覆蓋更多的菌株并更加有效。
我們有理由對抗毒素療法抱有希望。已有實驗室針對金黃色葡萄球菌(其耐甲氧西林的菌株就是臭名昭著的MRSA)研制出了抗毒素,并證明其可以有效阻止老鼠的發病和死亡。目前,這種抗毒素正在試驗中,以測試它是否能幫助使用呼吸機的病人防治由金黃色葡萄球菌引發的肺炎。
感染所導致最致命的結果往往不是由感染本身造成的,而是因為過度刺激免疫系統引發的紊亂。
還有一種方法是從致病菌和免疫系統之間的關系入手,但這很棘手。在百萬年“貓鼠”游戲中,人和細菌共同進化。細菌隱藏自己,而人體免疫系統努力找到并消滅它們。于是細菌進化出新的躲藏方式。以金黃色葡萄球菌為例,它可以將自己藏進人體的蛋白質內。人體免疫系統會自動忽略自身組織,因此藏起來的金黃色葡萄球菌就無法被發現。
有一些研究試圖揭露這種偽裝,但對于這些善于隱藏的細菌,更有效的方法卻是反其道而行之——故意隱藏細菌。感染所導致最致命的結果往往不是由感染本身造成的,而是因為過度刺激免疫系統引發的紊亂,感染性休克是其中最嚴重的一種情況。在美國,每年因其導致的死亡人數超過死于癌癥的人數。
很多有害菌的細胞壁都具有一種叫作內毒素的微粒。盡管內毒素的名字聽起來很邪惡,它本身并不會對人體造成傷害。但是大量的內毒素分子可能會過分刺激人體免疫系統,引發劇烈的炎癥反應,嚴重時可導致感染性休克。研究表明,缺乏感知內毒素基因的小鼠,在受到感染時更不容易死亡(盡管它們在一開始更容易被感染)。實驗中,多重耐藥不動桿菌造成感染性休克導致小鼠死亡。但是,當對被感染的小鼠使用了可以阻止內毒素生成的實驗藥物后,其死亡率大幅度下降。由于細菌的其他標志物比起內毒素來說,激起的機體免疫反應更溫和,老鼠的免疫系統最終會打敗感染,且又不至于因免疫反應過于激烈而導致休克。該藥物的人體試驗將在幾年后開展。
細菌內毒素可能會引發過激的免疫反應,造成高燒、低血壓、凝血異常等癥狀,嚴重時可導致感染性休克
如果我們能操控病菌間的溝通過程,就能在不殺死病菌的情況下阻止感染。
另一個阻止細菌而不殺死它們的方法,是切斷它們之間的信息傳導。對很多種細菌而言,由和平的 “草食動物”轉變成侵略性的“捕食者”是一個共同的決定。這一過程是由所謂的群體感應基因啟動的。這種基因只有在有足夠的同類個體聚集在一起時才會發揮作用。如果能截獲這些基因發出的信號,細菌就不會發起攻擊。
專家表示,這種方法很具吸引力,因為它具有很寬的抗菌譜。一般來說,一種群體感應阻斷劑可以阻止很多種細菌產生完整的毒素。在老鼠的實驗中顯示這種方法是有效的。但這種方法也存在一個問題,如果阻斷劑效果太強,可能會起反作用。因為能抵抗群體感應干擾劑的細菌更易存活和造成危害。而這種藥物也許會無意地篩選出在沒有群體感應的情況下也可以持續分泌大量毒素的超級細菌。
最近一項研究發現,當一種細菌處于不利的生存環境下,群體內部會分泌某種信號分子進行“溝通”,集體進入休眠狀態。研究人員認為,如果我們能操控這種溝通過程,就能在不殺死細菌的情況下阻止感染,而這種方法基本不會產生耐藥性。
上述所有方法都不是萬全之策,但至少能提供給我們選擇的空間,有助于提高目前所用抗生素的療效,讓人類少受疾病的影響。這就是它們的實際價值所在。“我們必須在更廣泛的背景下重新考慮抗生素的使用,” 一位微生物學家說,“我們不想擾亂微生物和造成額外的損傷。”
如果不重新評估抗生素的使用,我們以后可能死于細菌性瘟疫或者其他小疾病。肥胖、脂肪肝、糖尿病、關節炎、炎癥性腸病、多發性硬化癥、哮喘,以及焦慮和抑郁等都被證實與濫用抗生素有關。如果我們喪失了對抗感染的能力,享受現代生活完全就是不可能的了。然而我們又依然需要維持微生物種群,這對于我們的健康和福祉來說至關重要。是時候學會與細菌和平共處了。
抗生素會對人體造成傷害嗎?
以前,人們會認為抗生素是最安全的藥物之一,因為它在殺死細菌或抑制細菌繁殖的同時不會損害人體細胞。醫生有時會在沒什么必要的情況下(如病毒感染)開出抗生素處方,理由是——“它們不會對人體造成傷害。”
然而現在,人們逐漸意識到,抗生素是會對人體造成傷害的,不僅僅是因為它會導致細菌耐藥性。因使用抗生素造成的腹瀉和過敏屢見不鮮。使用抗生素特別容易造成艱難梭菌增殖,引發嚴重腹瀉,而這種細菌每年僅僅在美國就會造成約3萬人死亡。
但微生物研究者認為,濫用抗生素的代價遠不止于此。舉個例子,丹麥的一項研究表明,那些在15年間使用抗生素達到5次以上的人,比使用抗生素僅1次或沒有使用抗生素的人得2型糖尿病的風險高很多。
抗生素還會影響人體內的健康菌群。最近的一些研究發現,肥胖、炎癥、免疫紊亂甚至抑郁,都與腸道菌群失衡有關。現已證明,抗生素的使用,特別是在兒童時期使用,是引起上述問題的風險因素。
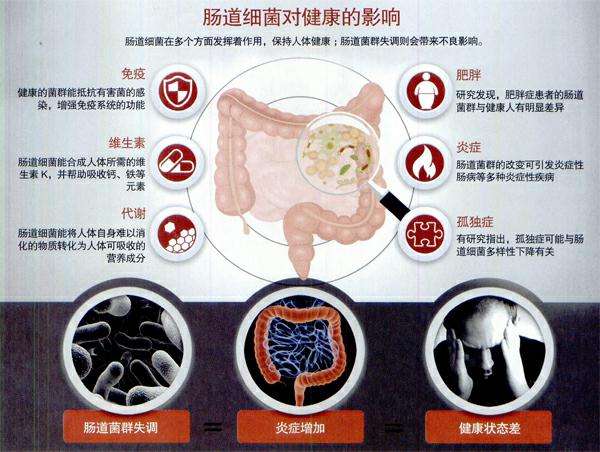
從某種意義上說,肥胖與抗生素之間的聯系不算是最新發現。從20世紀40年代開始,抗生素就被用于家禽家畜的育肥。而早在1955年就有研究發現,在人類中也有抗生素引發肥胖的現象。但其機制一直是未解之謎,而人們也沒有興趣追查下去。人們理所當然地認為,細菌是人類的敵人,抗生素能清除它們,所以抗生素就是好東西。
直到最近十年,才有科學家猜測,腸道菌群在人體免疫系統、神經系統等的發育中起到重要作用。而越來越多的研究顯示,患糖尿病、精神病、焦慮、抑郁、肥胖等疾病的風險高低與抗生素的使用相關,這一猜測也得到了證實。
關于人體內細菌的平衡,還有許多未知的領域,但是我們現在已經知道,不斷打亂菌群平衡是魯莽甚至危險的。這也推動了抗生素替代療法的需求,即使不是因為細菌耐藥性的威脅,為了保持健康,我們也要發掘新的療法。
基因編輯能否使致病菌變得無害?
另一個解除有害菌的“武器”而不殺死他們的方法是,破壞引起細菌攻擊的基因。但如今基因編輯技術的大步發展,為什么沒有更多的人來嘗試這一方法呢?
問題在于,細菌常常攜帶很多種致病基因,并形成各種各樣的組合。專家稱,僅針對單一的基因或致病因素可能是徒勞的,除非這個基因是所有致病因素的關鍵,否則細菌還是會造成感染。敲除某個非關鍵基因可能是無效甚至是有害的。
最基本的問題是,微生物擁有難以置信的多樣性。兩株來自同一腸道菌群的大腸桿菌可能僅有40%的基因相同。就基因相似度而言,人類和香蕉之間的親緣關系都比這些細菌之間的關系更親密。而相比之下,人類之間在遺傳學上有超過99.5%完全相同。若只針對細菌中的某個基因進行編輯,只能改變一小部分有害細菌,而它們又很快會被突變體和未經基因編輯的其他菌株所取代。endprint

