布魯氏菌IV型分泌蛋白及其參與免疫應答的研究進展
,,, , , ,,,
·綜述·
布魯氏菌IV型分泌蛋白及其參與免疫應答的研究進展
肖啟程1,田一男1,彭廣能1,李平2,魏斌1,涂蕊1,但佳明1,任志華1,鐘志軍1
布魯氏菌是一種胞內致病菌,主要寄生于宿主的滋養層細胞和巨噬細胞,能感染人、家畜和野生動物。動物感染后引起母畜的流產和公畜的睪丸炎等癥狀,而人感染后則引起關節疼痛、乏力、發熱及肝脾腫大等癥狀。布魯氏菌在與宿主的對抗中依賴免疫逃避機制,幫助布魯氏菌“偽裝”起來逃避宿主免疫系統的識別,進而在細胞內大量繁殖,引起機體的持續感染。由于該機制的存在,使得目前對布魯氏菌病的治療存在諸多困難。IV型分泌系統(T4SS)是布魯氏菌的一種關鍵毒力因子,其所分泌的效應蛋白幫助調節布魯氏菌在胞內的生存以及感染時的免疫應答。本文中,我們對布魯氏菌IV型分泌系統相關蛋白及其參與免疫應答的研究進行綜述,尤其對VirB操縱子所介導的IV型分泌系統產生的分泌效應蛋白與宿主免疫之間的關系進行詳細闡述。
布魯氏菌;分泌蛋白;免疫應答
布魯氏菌病是由布魯氏菌引起的一種自然疫源性、人獸共患傳染性疾病,臨床癥狀主要表現為波浪熱,可引發心包炎、腦膜炎,懷孕母畜出現流產,公畜出現睪丸炎等[1]。大多數病原菌會在先天免疫系統的監視下被阻止,與其他細菌感染相比較,動物感染布魯氏菌后,可通過免疫逃避機制躲避宿主的識別,從而引起更低的免疫反應[2]。研究表明體液免疫應答在免疫后期下降的情況下,疫苗的免疫保護力仍然保持恒定不變[3],表明細胞免疫是布魯氏菌免疫應答的主要方式。Mariana X Byndloss等[4]研究發現,流產布魯氏菌感染胚胎滋養層細胞時,IV型分泌系統(T4SS)的調理作用引起滋養層細胞發生非折疊蛋白應答,導致調節內質網反應的細胞死亡并釋放損傷相關分子模式,使吞噬細胞聚集在細胞周圍并釋放流產布魯氏菌。表明非折疊蛋白應答與布魯氏菌在宿主細胞內生存存在密切聯系。
布魯氏菌感染宿主細胞經歷以下階段: 1)布魯氏菌首先侵入宿主細胞中形成布氏小體; 2)晚期胞內體和溶酶體與布氏小體的融合受布魯氏菌的抑制,其中約10%的布氏小體未被降解得以存活; 3)未降解的布氏小體經轉運到達內質網并建立復制點進行復制; 4)布魯氏菌在內質網復制結束后,形成自體吞噬泡最終脫離宿主細胞進而到達其他細胞而持續感染傳播。研究表明,布魯氏菌在宿主細胞復制過程中,T4SS在晚期胞內體與溶菌酶的標記,識別內質網標記并作用于分泌途徑,識別自噬體的標記,抵御苛刻的胞內環境和調控免疫途徑的激活等一系列過程中發揮重要作用[2]。因此對T4SS進行研究對于理解布魯氏菌的感染有重要意義。
1 布魯氏菌IV型分泌系統與VirB操縱子
布魯氏菌的IV型分泌系統是II型染色體中的12個基因在細菌細胞膜上組成(VirB1-12)的多蛋白復合物,通過VirB操縱子編碼,參與布魯氏菌的胞內活動。一旦細菌的T4SS組裝完成,布魯氏菌就可以通過該系統分泌效應蛋白感染宿主細胞。布魯氏菌T4SS與其他細菌T4SS的組分相似,比如農桿菌和百日咳桿菌[5]。T4SS系統主要分為以下5部分:1)由VirB2組成的伸長區;2)由VirB7、VirB9和VirB10組成的中心區和外膜區;3)由VirB5和VirB10的片段組成連接區;4)由VirB3、VirB4、VirB6、VirB8和VirB10的N端組成的內膜區;5)由VirB4和VirB11組成的ATP酶能量區[2]。VirB作為布魯氏菌的毒力基因,它在宿主細胞的表達可影響布魯氏菌的胞內生存與復制[6]。VirB操縱子的12種基因所具有的功能不盡相同,目前關于12個VirB基因對布魯氏菌毒力的影響,主要集中在對牛種、羊種、豬種和綿羊附睪種布魯氏菌的研究(表1)。表1顯示了每個基因缺失后對牛種、羊種、豬種和綿羊附睪種布魯氏菌毒力的影響。VirB最初在豬種布魯氏菌中首次被發現,隨后在所有布魯氏菌種中都發現了高度保守的VirB基因序列,表明了該操縱子在布魯氏菌中有著重要的作用[7]。研究表明,牛種布魯氏菌VirB1突變體在人的宮頸癌細胞中不能復制,論證了VirB操縱子影響牛種布魯氏菌的胞內生存[8]。另一研究表明,牛種布魯氏菌VirB1突變株在小鼠巨噬細胞中生存能力也降低,進一步表明VirB1缺失后布魯氏菌的毒力受到抑制[9]。Andreas B. den Hartigh等[9]研究表明,牛種布魯氏菌VirB1突變株在巨噬細胞中的生存能力下降,而牛種布魯氏菌VirB2基因突變株在巨噬細胞和小鼠器官中的生存能力都下降,但VirB12對牛種布魯氏菌的毒力無影響。Yao-Hui Sun等[10]研究表明VirB12對牛種、羊種和豬種布魯氏菌的毒力同樣也無影響。Joicy C. Sa等[11]研究表明,綿羊附睪種布魯氏菌可以在脾臟中繁殖,而其VirB2突變株不能在巨噬細胞中生存和繁殖,證明了VirB2的缺失同樣使綿羊附睪種布魯氏菌的毒力減弱。R.-M. Delrue等[12]采樣免疫熒光法檢測羊種布魯氏菌16M菌株VirB2、VirB4和VirB9突變體在人宮頸癌細胞內的生存能力,結果表明,3種VirB突變體在人宮頸癌細胞的生存能力都明顯低于羊種布魯氏菌16M菌株。Nicolas Sprynski等[13]構建了豬種布魯氏菌VirB5突變株,巨噬細胞試驗表明,缺失VirB5降低了豬種布魯氏菌的毒力。David等[7]對VirB5和VirB9進行突變,巨噬細胞試驗顯示,豬種布魯氏菌VirB5和VirB9突變體的感染能力明顯下降,表明豬種布魯氏菌VirB5和VirB9突變株的毒力也受到影響。牛種布魯氏菌的VirB3~VirB11缺失突變株在小鼠巨噬細胞中的生存能力都有所下降,可能是由于VirB操縱子缺失所致,表明VirB操縱子對布魯氏菌的胞內生存具有重要作用。以上試驗都表明,T4SS可以調節布魯氏菌的胞內生存能力。同時有研究表明,T4SS參與引起細菌的炎癥反應和影響宿主感染時的免疫應答。試驗表明,在細菌中突變T4SS后,野生型菌株可以在宿主內引起比突變株更強的免疫應答反應,因此可推論T4SS對抑制宿主的免疫應答起重要作用[14-15]。在人的宮頸癌細胞和外周血單核細胞(THP1)培養布魯氏菌T4SS突變體試驗中,通過對布魯氏菌突變體在細胞內增殖能力的檢測,發現破壞T4SS能阻止布魯氏菌在細胞內的生存[12,16],從而論證了T4SS對布魯氏菌胞內存活的重要性。
不同細菌T4SS的組成較保守,但也存在一定的差異。布魯氏菌T4SS的結構沒有完全一致性,多數特征與農桿菌屬和幽門螺桿菌的T4SS結構相似。胞質和內膜是由VirB6和VirB8與ATP酶VirB4,VirB11和VirD4而組成。VirB7、VirB9和VirB10相互作用形成一個可跨越內膜和外膜的T4SS復合體核心。VirB2和VirB5能組成纖毛。VirB3可能與纖毛的形成有關。而農桿菌屬VirB1屬于一肽聚糖降解的轉糖激酶,可以調節周質的分泌系統[17]。研究報道,對幽門螺桿菌的Virb11同系物進行分析,結果表明該同系物是一種具有緊密、均勻對稱的動態蛋白質。而當組成virB11同系物的核苷酸結合時可以調節空間結構使T4SS進行組裝。雖然幽門螺桿菌和VirB10同系物都有中央鞘包裹,但是大多數T4SS的修飾物質是VirB5。農桿菌屬VirB5以那些短小、無結構的羧基端蛋白質為目標對纖毛進行修飾。VirB5出現在細菌表面,表明它可能與宿主蛋白發生反應[18]。
農桿菌屬和布魯氏菌T4SS間最重要的差異是后者VirB操縱子中存在一個額外的基因VirB12,可編碼一個外膜脂蛋白,同時布魯氏菌T4SS缺乏一個編碼VirD4耦合蛋白同系物的基因。VirD4耦合蛋白在T4SS發揮功能中扮演了重要的角色,即為轉運招募蛋白質底物。如農桿菌屬利用雙分子熒光互補技術和免疫熒光顯微技術證明了VirD4與VirE2效應子蛋白之間的兩極定位與相互作用[18]。
表1 VirB操縱子的12個基因及其在牛種、羊種、豬種及綿羊附睪種布魯氏菌中的作用
Tab.1 The 12 genes of VirB operon and their respective function in B. abortus, B. melitensis, B. suis and B. ovis
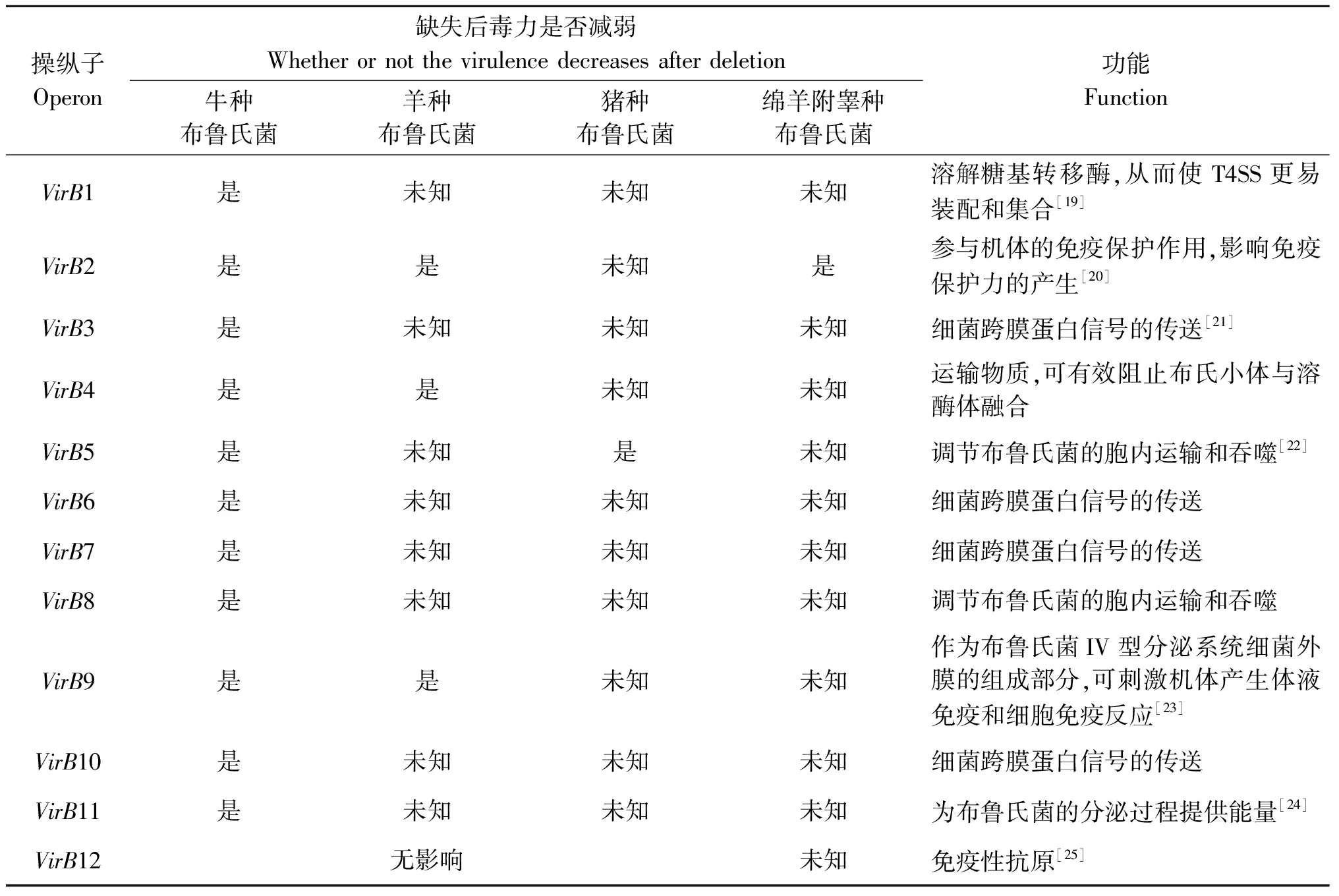
操縱子Operon缺失后毒力是否減弱Whetherornotthevirulencedecreasesafterdeletion牛種布魯氏菌羊種布魯氏菌豬種布魯氏菌綿羊附睪種布魯氏菌功能FunctionVirB1是未知未知未知溶解糖基轉移酶,從而使T4SS更易裝配和集合[19]VirB2是是未知是參與機體的免疫保護作用,影響免疫保護力的產生[20]VirB3是未知未知未知細菌跨膜蛋白信號的傳送[21]VirB4是是未知未知運輸物質,可有效阻止布氏小體與溶酶體融合VirB5是未知是未知調節布魯氏菌的胞內運輸和吞噬[22]VirB6是未知未知未知細菌跨膜蛋白信號的傳送VirB7是未知未知未知細菌跨膜蛋白信號的傳送VirB8是未知未知未知調節布魯氏菌的胞內運輸和吞噬VirB9是是未知未知作為布魯氏菌IV型分泌系統細菌外膜的組成部分,可刺激機體產生體液免疫和細胞免疫反應[23]VirB10是未知未知未知細菌跨膜蛋白信號的傳送VirB11是未知未知未知為布魯氏菌的分泌過程提供能量[24]VirB12無影響未知免疫性抗原[25]
2 目前已發現的效應蛋白
目前,我們對布魯氏菌T4SS的效應蛋白了解的還比較少,僅有部分效應蛋白的功能得到初步鑒定。表2中為目前在布魯氏菌T4SS中發現的15種效應蛋白。
2.1效應蛋白VceA和VceC 在T4SS分泌的效應蛋白質中,VirB調控的效應物A(VceA)和效應物C(VceC)是研究人員最早識別的兩個T4SS效應蛋白。通過半乳糖苷酶結合和β-半乳糖苷酶活性檢測顯示,在流產布魯氏菌VjbR突變體中,VceC和VirB的表達下調,表明它們受相同轉錄因子的調控[26]。VceC的C端含20種氨基酸,包含T4SS進行轉運識別的序列,主要參與VceC轉移到宿主細胞過程中;N端是由38種氨基酸形成的疏水跨膜區,主要與VceC的定位和干擾內質網的作用有關[26-27]。免疫共沉淀結果顯示,內質網的分子伴侶蛋白Bip/Grp78可以結合到VceC脯氨酸含量高的區域[27],此區域為VceC的特征域。與VceC的定位和對其有相互作用的宿主細胞進行識別相一致,VceC可激活非折疊蛋白應答,引起內質網進行蛋白質的折疊和修飾,同時還能在感染期間誘導脯氨酸的炎性反應。
2.2效應蛋白RicA RicA是IV型分泌系統分泌的重要蛋白之一,主要參與布魯氏菌的胞內運輸[28]。RicA不僅可以與小GTP結合蛋白Rab2相互作用,還與蛋白質的折疊有關[29]。此外,Xavier de Bolle等發現Rab2與布魯氏菌RicA蛋白相互作用可以調控布氏小體的成熟,從而間接影響牛種布魯氏菌和宿主細胞的活動。布魯氏菌RicA的抗原決定簇較多,主要存在于N端,且試驗結果表明該蛋白具有較強的免疫原性,因此宿主細胞會產生相應的免疫反應[26]。研究發現RicA的晶體結構和γ-碳酸酐酶類蛋白質的結構高度相似,這些蛋白質都含有鋅離子,但卻沒有碳酸酐酶的作用,說明RicA有一種尚未清楚的獨特功能[30]。RicA可以與機體內、外游離的鳥苷二磷酸(GDP)與結合GDP反應形成Rab2,但不能與結合GTP反應,說明RicA并不是一種激活GTP酶的蛋白質[30-31]。進一步的試驗表明,RicA不是Rab2的鳥嘌呤核苷酸的交換因子,因此它無法激活GTP酶。RicA缺失突變株在小鼠細胞和人宮頸癌細胞中毒力并未減弱,而且其細胞內化和胞內生存能力也沒有變化,但與野生型布魯氏菌相比,RicA突變株消耗了宿主細胞內大量的溶酶體相關膜蛋白LAMP1,表明RicA缺失突變株可以逃離晚期胞內體到達內質網并迅速建立復制點[31]。有研究表明,在牛種布魯氏菌感染過程中,布魯氏菌會將RicA蛋白轉運至巨噬細胞中,但RicA并不能在VirB缺失株感染細胞時進行轉運,而且經檢測在VirB缺失株的培養基中也發現了RicA。說明RicA是依賴于VirB的存在進行轉運,但其分泌卻不受VirB的影響[31]。
2.3效應蛋白BtpA和BtpB BtpA和BtpB是T4SS分泌的產生毒力的必要蛋白質,能抑制樹突細胞的成熟,但是它們在活化NF-kB時卻有著截然相反的作用,BtpA有抑制作用而BtpB則引起NF-kB的活化[32]。它們在哺乳動物中存在一個保守的TIR區域,負責在先天免疫識別過程中調節信號級聯放大效應[33]。這兩種蛋白通過CyaA試驗確認可以轉運到宿主細胞中,但TEM-1內酰胺酶的試驗中發現BtpB的轉運效率明顯低于其他效應蛋白質。為了調節宿主細胞Toll樣受體信號通路,細菌可以將BtpA轉運至細胞,而存在于細胞中的T4SS很可能是實現這種轉運最有效的機制之一。此外,BtpA和BtpB屬于同一類細菌蛋白質。它們都具有Toll受體結構域,Toll樣受體結構域存在于真核生物的Toll樣蛋白及其下游的Toll樣銜接蛋白,當這二者相互作用時會產生級聯信號引起核轉錄因子kB的核移位、促炎性細胞因子和I型干擾素的產生[34]。
2.4其他效應蛋白 BspC,BspE,BPE123, BPE005,BPE275和BPE043是另一部分由T4SS分泌的效應蛋白,具有高度的保守性,但目前對它們作用機制與功能的研究知之甚少。有研究表明,BspC和BspE存在于細胞核周圍,其中BspC存在于高爾基體,BspE則會形成囊泡[35]。BspC的N端有依賴于Sec的信號肽,在不影響蛋白質分泌的情況下能引起內質網的應激反應。BPE005,BPE275和BPE043發現于其他細菌,而BPE123只存在于幾種細菌中,包括桿菌狀巴爾通體,蒼白桿菌等[36]。BPE123是B型流產布魯氏菌通過VirB轉運的一種效應蛋白。María I. Marchesin等通過液相串聯質譜(LC/MS-MS)鑒別出了人的α-烯醇酶并用免疫共沉淀證明其可以與BPE123相互作用。α-烯醇酶的降解能阻礙牛種布魯氏菌在人宮頸癌細胞中的增殖,表明α-烯醇酶在布魯氏菌感染細胞的過程中起作用[37]。此外,BPE123和α-烯醇酶可以在布魯氏菌的胞內生存階段相互作用,且α-烯醇酶的活性很大程度上取決于BPE123的空間結構[37]。由此可推測,BPE123和宿主細胞α-烯醇酶相互作用有利于牛種布魯氏菌的胞內生存。布魯氏菌感染期間,BPE123存在于布氏小體的表面,它的N端含有25個氨基酸,可能是一種將其自身轉運至宿主細胞的信號肽。在幾種類型的細胞和小鼠模型中都發現BPE123缺失株和野生菌株的增殖能力并沒有明顯變化[36]。
表2 布魯氏菌T4SS分泌的15種效應蛋白
Tab.2 The 15 effectors secreted by Brucella through T4SS
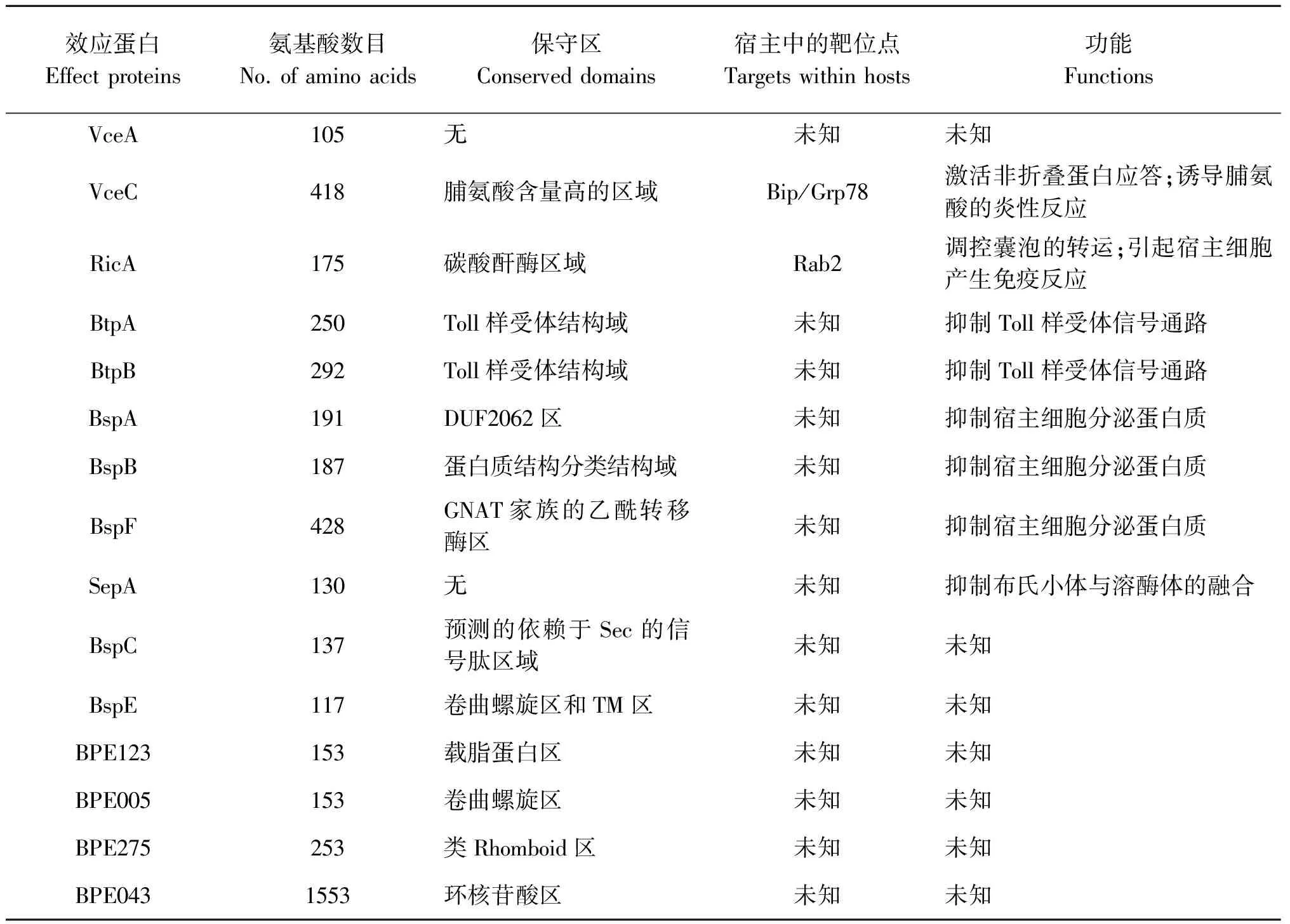
效應蛋白Effectproteins氨基酸數目No.ofaminoacids保守區Conserveddomains宿主中的靶位點Targetswithinhosts功能FunctionsVceA105無未知未知VceC418脯氨酸含量高的區域Bip/Grp78激活非折疊蛋白應答;誘導脯氨酸的炎性反應RicA175碳酸酐酶區域Rab2調控囊泡的轉運;引起宿主細胞產生免疫反應BtpA250Toll樣受體結構域未知抑制Toll樣受體信號通路BtpB292Toll樣受體結構域未知抑制Toll樣受體信號通路BspA191DUF2062區未知抑制宿主細胞分泌蛋白質BspB187蛋白質結構分類結構域未知抑制宿主細胞分泌蛋白質BspF428GNAT家族的乙酰轉移酶區未知抑制宿主細胞分泌蛋白質SepA130無未知抑制布氏小體與溶酶體的融合BspC137預測的依賴于Sec的信號肽區域未知未知BspE117卷曲螺旋區和TM區未知未知BPE123153載脂蛋白區未知未知BPE005153卷曲螺旋區未知未知BPE275253類Rhomboid區未知未知BPE0431553環核苷酸區未知未知
3 部分效應蛋白參與的免疫應答反應
VceC是布魯氏菌IV型分泌系統分泌的重要效應蛋白之一,可通過T4SS進入到宿主細胞內發揮作用。但是VceC在宿主細胞內參與免疫應答的機制尚未清楚。張沾等[9]通過對VceC功能的初步研究,發現VceC能夠使細胞分泌NO,NO再與O2-形成活性氮對蛋白進行修飾,造成免疫細胞的毒性反應。由此可推知,VceC可能引起了免疫細胞產生毒性反應,進而使宿主的免疫作用降低或喪失。
RicA的存在對布魯氏菌的增殖有阻礙作用,可參與布魯氏菌的胞內運輸過程,但其他作用還有待研究。韓玉霞等[28]通過免疫印跡試驗證明了RicA的免疫原性很強。這也就不難理解RicA的免疫原性增強,導致宿主產生大量的抗體或引起致敏T淋巴細胞介導的特異性免疫反應進而干擾布魯氏菌的胞內生存。
目前,很多細菌都存在含有TIR域的蛋白質,比如大腸桿菌中的TcpC,沙門氏菌中的TlpA,這些蛋白具有抑制toll樣受體信號通路的作用[38-44]。研究表明,Btp1含有TIR域,且可以干擾人先天性免疫相關蛋白TLR-2和TLR-4信號通路,從而抑制樹突狀細胞的成熟。當敲除Btp1后樹突狀細胞表面的MHCII和CD80的表達會升高,進而布魯氏菌的免疫逃避受到破壞[32,45],提示TIR域在布魯氏菌的免疫逃避中發揮了重要作用。
此外,孫志華等[46]構建了BPE123的原核表達載體,并檢測出BPE123具有免疫原性,表明BPE123可刺激機體產生抗體或進行細胞免疫。劉來珍等[47]構建了BMEI1069的原核表達載體,Western-blot檢測出其具有免疫原性,同時還發現IL-1、IL-10和TNF-α的含量在加入BMEI1069蛋白后均升高,而當細菌在感染期中存在較高水平的復制時會引起TNF-α的含量減少,表明BMEI1069可能在細菌感染后期行使功能。Zhan Y等[48]研究發現,布魯氏菌病的發生與小鼠體內的TNF-α被抑制有關,而BEMI1069引起了TNF-α含量升高會抑制布魯氏菌內吞小泡的形成,布魯氏菌受到溶菌酶和核內體的殺傷后會阻礙其感染宿主細胞,表明BEMI1069可以干擾布魯氏菌對宿主細胞的侵入。
4 展 望
目前,我們對布魯氏菌T4SS效應蛋白發揮的免疫作用了解得比較少,因此對布魯氏菌效應蛋白功能的鑒定有利于闡明T4SS的功能和作用機制。迄今為止,已鑒定的布魯氏菌T4SS分泌的效應蛋白有15種,其中大多數效應蛋白在布魯氏菌的致病機制尚不清楚。不同細菌T4SS分泌的效應蛋白雖然序列相似,但其結構、功能和作用機制、致病機理卻不盡相同。布魯氏菌是一種典型的胞內致病菌,研究布魯氏菌T4SS的作用機制和其效應蛋白有助于闡明胞內菌的致病機理。
和其他細菌相比,目前對布魯氏菌T4SS以及其效應蛋白的研究仍相對較少。根據目前的研究結果,未來以下研究可能是今后研究布魯氏菌IV型分泌系統以及相關分泌蛋白的重點方向: 1)對效應蛋白的生化特性研究,包括定位其在宿主細胞的靶標部位以及與靶部位間作用的生化機制。研究效應蛋白是否具有特征性的結構域以及是否具有相關酶的活性,如激酶或磷酸酶活性等; 2)效應蛋白的細胞生物學特性研究,包括他們對細菌在胞內持續生存、細胞膜之間的對接、與宿主間的相關信號通路以及對布魯氏菌內吞小泡轉運的調控等; 3)闡明效應蛋白對布魯氏菌在宿主體內毒力的影響,包括他們的必要性,在慢性感染中所扮演的角色,引起的炎癥反應及這些效應物是否能解釋布魯氏菌典型的胞內生存方式等。研究這些效應蛋白不僅有利于我們了解細菌的致病機理,而且對研究真核生物宿主細胞的免疫應答反應極為重要。由于缺乏適當的免疫應答反應,宿主細胞無法抑制布魯氏菌的感染[49-50]。因此,研究布魯氏菌的效應蛋白將有助于我們理解胞內細菌抑制宿主免疫系統信號通路的機制。認清這些機制才能幫助科研人員進一步改進布病的治療方法以及為今后疫苗研制提供理論依據。
[1] Liu QH .Type IV secretion system ofBrucella[J]. Chin J Zoonoses,2012,28(9):951-954.DOI:10.3969/j.issn.1002-2694.2012.09.019 (in Chinese)
劉倩宏.布魯氏菌的IV型分泌系統[J]. 中國人獸共患病學報,2012,28(9):951-954.
[2] Ke Y, Wang Y, Li W, et al. Type IV secretion system ofBrucellaspp. and its effectors[J]. Front Cellular Infect Microbiol, 2015, 5: 72. DOI: 10.3389/fcimb.2015.00072
[3] Zhu L, Feng Y, Zhang G, et al.Brucellasuisstrain 2 vaccine is safe and protective against heterologousBrucellaspp. infections[J]. Vaccine, 2016, 34(3): 395-400. DOI: 10.1016/j.vaccine.2015.09.116
[4] Byndloss MX, Rivera-Chávez F, Tsolis RM, et al. How bacterial pathogens use type III and type IV secretion systems to facilitate their transmission[J]. Curr Opin Microbiol, 2017, 35: 1-7. DOI: 10.1016/j.mib.2016.08.007
[5] Voth DE, Broederdorf LJ, Graham JG. Bacterial Type IV secretion systems: versatile virulence machines [J]. Future Microbiol, 2012, 7(2): 241-257. DOI:10.2217/fmb.11.150
[6] Cao XA, Qiu CQ, Qin TD. Progress in research of virulence gene ofBrucella[J]. Chin J Zoonoses, 2009, 25(7): 689-693. (in Chinese)
曹小安,邱昌慶,秦天達. 布魯氏菌毒力基因的研究狀況 [J]. 中國人獸共患病學報, 2009, 25(7): 689-693.
[7] O’Callaghan D, Cazevieille SA, Boschiroli M, et al. A homologue of theAgrobacteriumtumefaciensVirB andBordetellapertussisPtl type IV secretion system is essential for intracellular survival ofBrucellasuis[J]. Mol Microbiol, 1999, 33(6): 1210-1220.
[8] Sieira R, Comerci DJ, Sánchez DO, et al. A homologue of an operon required for DNA transfer in agrobacterium is required inBrucellaabortusfor virulence and intracellular multiplication[J]. J Bacteriol, 2000, 182(17): 4849-4855.
[9] Den Hartigh AB, Rolan HG, de Jong MF, et al. VirB3 to VirB6 and VirB8 to VirB11, but not VirB7, are essential for mediating persistence ofBrucellain the reticuloendothelial system[J]. J Bacteriol, 2008, 190(13): 4427-4436. DOI: 10.1128/JB.00406-08
[10] Sun YH, Rolan HG, den Hartigh AB, et al.BrucellaabortusvirB12 is expressed during infection but is not an essential component of the type IV secretion system[J]. Infect Immun, 2005, 73(9): 6048-6054. DOI: 10.1128/iai.73.9.6048-6054.2005
[11] Sa JC, Silva TM, Costa EA, et al. The virB-encoded type IV secretion system is critical for establishment of infection and persistence ofBrucellaovisinfection in mice[J]. Vet Microbiol, 2012, 159(1-2): 130-140. DOI: 10.1016/j.vetmic.2012.03.029
[12] Delrue RM, Martinez-Lorenzo M, Lestrate P, et al. Identification ofBrucellaspp. genes involved in intracellular trafficking[J]. Cellular Microbiol, 2001, 3(7): 487-497.
[13] Sprynski N, Felix C, O’Callaghan D, et al. Restoring virulence to mutants lacking subunits of multiprotein machines: functional complementation of aBrucellavirB5 mutant[J]. FEBS Open Bio, 2012, 2: 71-75. DOI: 10.1016/j.fob.2012.03.003
[14] Luo ZQ. Legionella secreted effectors and innate immune responses[J]. Cellular Microbiol, 2012, 14(1): 19-27. DOI: 10.1111/j.1462-5822.2011.01713.x
[15] van Schaik EJ, Chen C, Mertens K, et al. Molecular pathogenesis of the obligate intracellular bacteriumCoxiellaburnetii[J]. Nat Revi Microbiol, 2013, 11(8): 561-573. DOI: 10.1038/nrmicro3049
[16] Foulongne V, Bourg G, Cazevieille C, et al. Identification ofBrucellasuisgenes affecting intracellular survival in an in vitro human macrophage infection model by signature-tagged transposon mutagenesis[J]. Infect Immun, 2000, 68(3): 1297-1303.
[17] Lacerda TL, Salcedo SP, Gorvel JP. Brucella T4SS: the VIP pass inside host cells [J]. Curr Opin Microbiol, 2013, 16(1): 45-51. DOI:10.1016/j.mib.2012.11.005
[19] Hoppner C, Carle A, Sivanesan D, et al. The putative lytic transglycosylase VirB1 fromBrucellasuisinteracts with the type IV secretion system core components VirB8, VirB9 and VirB11[J]. Microbiology, 2005, 151(Pt 11): 3469-3482. DOI: 10.1099/mic.0.28326-0
[20] Li Z,Chen CF,Wang YZ,et al.Change of antibody and effect of related cytokines for mice vaccined by theBrucellaM5-90△VirB2 vaccine strain[J]. J Shihezi Univ (Nat Sci), 2011, 29(4): 452-455. (in Chinese)
李臻,陳創夫,王遠志,等. 布魯氏菌M5-90△virB2基因缺失株免疫小鼠抗體及相關細胞因子的檢測研究 [J].石河子大學學報,2011,29(4):452-455.
[21] Wang N,Hu HTE,Cui BY. Progress in research of immune related antigen ofBrucella[J]. Dis Surveill, 2014, 29(2): 156-162. (in Chinese)
王娜,呼和巴特爾,崔步云. 布魯氏菌免疫相關抗原研究進展 [J].疾病監測,2014, 29(2):156-162.
[22] Rouot B, Alvarez-Martinez MT, Marius C, et al. Production of the type IV secretion system differs amongBrucellaspecies as revealed with VirB5-and VirB8-specific antisera[J]. Infect Immun, 2003, 71(3): 1075-1082.
[23] Fan JM, Wang FX, Zhang B, et al. Determination of antigenic properties of VirB9, a protein of type IV secretion system ofBrucella[J]. Chin J Endemiol, 2013, 32(3): 263-266. (in Chinese)
范金明,王發興,張波,等. 布魯桿菌Ⅳ型分泌系統蛋白VirB9免疫原性檢測 [J].中華地方病學雜志,2013, 32(3): 263-266.
[24] Atmakuri K, Cascales E, Christie PJ. Energetic components VirD4, VirB11 and VirB4 mediate early DNA transfer reactions required for bacterial type IV secretion[J]. Mol Microbiol, 2004, 54(5): 1199-1211. DOI: 10.1111/j.1365-2958.2004.04345.x
[25] Mirkalantari S, Amirmozafari N, Kazemi B, et al. Molecular cloning of virB12 gene ofBrucellamelitensis 16M strain in pET28a vector[J]. Asian Pacif J Tropic Med, 2012, 5(7): 511-513. DOI: 10.1016/S1995-7645(12)60089-3
[26] De Jong MF, Sun YH, den Hartigh AB, et al. Identification of VceA and VceC, two members of the VjbR regulon that are translocated into macrophages by theBrucellatype IV secretion system[J]. Mol Microbiol, 2008, 70(6): 1378-1396. DOI: 10.1111/j.1365-2958.2008.06487.x
[27] De Jong MF, Starr T, Winter MG, et al. Sensing of bacterial type IV secretion via the unfolded protein response[J]. mBio, 2013, 4(1): e00418-12. DOI: 10.1128/mBio.00418-12
[28] Han YX, Sun ZH, Liu J, et al. Cloning and prokaryotic expression of related proteins gene RicA inBrucellatype IV secretion system and its immunogenicity analysis[J]. Acta Agriculturae Boreali-Occidentalis Sinica, 2015, 24(5): 18-23. (in Chinese)
韓玉霞,孫志華,劉娟,等. 布氏桿菌Ⅳ型分泌系統相關蛋白基因RicA的克隆、原核表達及免疫原性分析 [J].西北農業學報,2015,24(5):18-23.
[29] Nkengfac B, Pouyez J, Bauwens E, et al. Structural analysis ofBrucellaabortusRicA substitutions that do not impair interaction with human Rab2 GTPase[J]. BMC Biochem, 2012, 13(1): 1-8. DOI: 10.1186/1471-2091-13-16
[30] Herrou J, Crosson S. Molecular structure of theBrucellaabortus metalloprotein RicA, a Rab2-binding virulence effector[J]. Biochemistry, 2013, 52(50): 9020-9028. DOI: 10.1021/bi401373r
[31] De Barsy M, Jamet A, Filopon D, et al. Identification of aBrucellaspp. secreted effector specifically interacting with human small GTPase Rab2[J]. Cellular Microbiol, 2011, 13(7): 1044-1058. DOI: 10.1111/j.1462-5822.2011.01601.x
[32] Salcedo SP, Marchesini MI, Lelouard H, et al.Brucellacontrol of dendritic cell maturation is dependent on the TIR-containing protein Btp1[J]. PLoS Pathog, 2008, 4(2): e21. DOI: 10.1371/journal.ppat.0040021
[33] Salcedo SP, Marchesini MI, Degos C, et al. BtpB, a novelBrucellaTIR-containing effector protein with immune modulatory functions[J]. Front Cellular Infect Microbiol, 2013, 3: 28. DOI: 10.3389/fcimb.2013.00028
[34] Felix C, Kaplan TB, Ranaldi S, et al. TheBrucellaTIR domain containing proteins BtpA and BtpB have a structural WxxxE motif important for protection against microtubule depolymerisation [J]. Cell Communicati Signaling, 2014, 12(1): 53. DOI:10.1186/s12964-014-0053-y
[35] Myeni S, Child R, Ng TW, et al.Brucellamodulates secretory trafficking via multiple type IV secretion effector proteins[J]. PLoS Pathog, 2013, 9(8): e1003556. DOI: 10.1371/journal.ppat.1003556
[36] Marchesini MI, Herrmann CK, Salcedo SP, et al. In search ofBrucellaabortustype IV secretion substrates: screening and identification of four proteins translocated into host cells through VirB system[J]. Cell Microbiol, 2011, 13(8): 1261-1274. DOI: 10.1111/j.1462-5822.2011.01618.x
[37] Marchesini MI, Morrone Seijo SM, Guaimas FF, et al. A T4SS effector targets host cell alpha-enolase contributing toBrucellaabortusintracellular lifestyle[J]. Front Cellular Infect Microbiol, 2016, 6: 153. DOI: 10.3389/fcimb.2016.00153
[38] Newman RM, Salunkhe P, Godzik A, et al. Identification and characterization of a novel bacterial virulence factor that shares homology with mammalian Toll/interleukin-1 receptor family proteins[J]. Infect Immun, 2006, 74(1): 594-601. DOI: 10.1128/iai.74.1.594-601.2006[39] Chan SL, Low LY, Hsu S, et al. Molecular mimicry in innate immunity: crystal structure of a bacterial TIR domain[J]. J Biologic Chem, 2009, 284(32): 21386-21392. DOI: 10.1074/jbc.C109.007591
[40] Spear AM, Loman NJ, Atkins HS, et al. Microbial TIR domains: not necessarily agents of subversion[J]. Trends Microbiol, 2009, 17(9): 393-398. DOI: 10.1016/j.tim.2009.06.005
[41] Rana RR, Simpson P, Zhang M, et al.YersiniapestisTIR-domain protein forms dimers that interact with the human adaptor protein MyD88[J]. Microbial Pathogenesis, 2011, 51(3): 89-95. DOI: 10.1016/j.micpath.2011.05.004
[42] Rana RR, Zhang M, Spear AM, et al. Bacterial TIR-containing proteins and host innate immune system evasion[J]. Medic Microbiol Immunol, 2013, 202(1): 1-10. DOI: 10.1007/s00430-012-0253-2
[43] Snyder GA, Cirl C, Jiang J, et al. Molecular mechanisms for the subversion of MyD88 signaling by TcpC from virulent uropathogenicEscherichiacoli[J]. Proc Natl Acad Sci U S A, 2013, 110(17): 6985-6990. DOI: 10.1073/pnas.1215770110
[44] Askarian F, van Sorge NM, Sangvik M, et al. AStaphylococcusaureusTIR domain protein virulence factor blocks TLR2-mediated NF-kappaB signaling[J]. J Innate Immun, 2014, 6(4): 485-498. DOI: 10.1159/000357618
[45] Radhakrishnan GK, Yu Q, Harms JS, et al.BrucellaTIR domain-containing protein mimics properties of the toll-like receptor adaptor protein TIRAP[J]. J Biologic Chem, 2009, 284(15): 9892-9898. DOI: 10.1074/jbc.M805458200
[46] Sun ZH, Zhang H, Liu LZ, et al. Clone, prokaryotic expression and identification of effector molecules BPE123 and BPE275 ofBrucellaIV secretion system[J]. J Northwest Agricult Forest Univ (Nat Sci Ed), 2016, 44(5): 1-7. (in Chinese)
孫志華,張輝,劉來珍,等. 布魯氏菌Ⅳ型分泌系統效應分子BPE123和BPE275基因的原核表達與鑒定 [J].西北農林科技大學學報,2016,44(5):1-7.
[47] Liu LZ, Sun ZH, Liu J, et al. Prokaryotic expression and analysis ofBrucellaIV secretion system protein BMEI1069 gene[J]. Mod J Anim Husb Vet Med, 2015, (3): 6-11. (in Chinese)
劉來珍,孫志華,劉娟,等. 布魯氏菌Ⅳ型分泌系統蛋白BMEI1069基因的原核表達與分析 [J]. 現代畜牧獸醫,2015,(3):6-11.
[48] Zhan Y, Cheers C. Control of IL-12 and IFN-gamma production in response to live or dead bacteria by TNF and other factors[J]. J Immunol, 1998, 161(3): 1447-1453.
[49] Martirosyan A, Moreno E, Gorvel JP. An evolutionary strategy for a stealthy intracellularBrucellapathogen[J]. Immunologic Rev, 2011, 240(1): 211-234. DOI: 10.1111/j.1600-065X.2010.00982.x
[50] Von Bargen K, Gorvel JP, Salcedo SP. Internal affairs: investigating theBrucellaintracellular lifestyle[J]. FEMS Microbiol Rev, 2012, 36(3): 533-562. DOI: 10.1111/j.1574-6976.2012.00334.x
ResearchadvanceonBrucellaIVsecretionsystemproteinsanditsimmuneresponse
XIAO Qi-cheng1, TIAN Yi-nan1, PENG Guang-neng1, LI Ping2, WEI Bin1, TU Rui1, DAN Jia-ming1, REN Zhi-hua1, ZHONG Zhi-jun1
(1.CollegeofVeterinaryMedicine,SichuanAgriculturalUniversity,Chengdu611130,China;2.QionglaiAgricultureandForestryBureau,Qionglai611530,China)
Brucellais a facultative intracellular pathogen that causes infection in domestic animal and humans, mainly parasitizing in cells and macrophages of hosts.Brucellacan lead to abortion and sterility in animals. Meanwhile, it also causes arthralgia, weakness, undulat fever, hepatosplenomegaly and other symptoms in humans.Brucellarelies on immune escape mechanism in the confrontation with the host. It can helpBrucella"camouflage" to evade the identification of the immune system of the hosts and replicate within cells to persist to establish a long-term infection in the host. As a result of the existence of this mechanism, the treatment ofBrucellainfection is quite difficult. Type IV secretion system (T4SS) is a key virulence factor and it is essential forBrucellato survive in host cells. The effector proteins secreted by T4SS can help regulate the immune response againstBrucella. In this article, we reviewed the studies on related proteins of the type IV secretion system ofBrucellaand its immune response, especially the relationship between the secretions of effector proteins mediated by VirB operon and immunity of the host.
Brucella; secretory protein; immune response
Zhong Zhi-jun, Email: zhongzhijun488@126.com
10.3969/j.issn.1002-2694.2017.11.015
國家重點研發計劃(No.2016YFD0501009);國家自然科學基金資助項目(No.31000548);成都大熊貓繁育研究基金會項目(No.CPF2015-4)聯合資助
鐘志軍,Email:zhongzhijun488@126.com
1.四川農業大學動物醫學院/動物疫病與人類健康四川省重點實驗室,成都 611130;
2.邛崍市農業和林業局,邛崍 611530
R378.5
A
1002-2694(2017)11-1029-07
Supported by the National Key Research and Development Program of China (No. 2016YFD0501009), the National Natural Science Foundation of China (No. 31000548) and the Chengdu Giant Panda Breeding Research Foundation (No. CPF2015-4)
2017-02-28編輯王曉歡

