兩種高效液相色譜法測定雙黃連注射液中連翹苷含量的比較研究*
章榮葉,羅成江,湯賽飛,王彬,陳曉林,林仙軍
(1.臺州市屠宰管理所 浙江臺州318000;2.浙江省獸藥飼料監察所 杭州 311101;3.浙江建安檢測研究院有限公司 杭州 310006)
雙黃連注射液由金銀花、黃芩和連翹三味中藥材制成,主要含有綠原酸、黃芩苷和連翹苷等有效成分[1]。獸醫臨床用于預防和治療畜禽外感風寒所致的上呼吸道感染[2]、急性支氣管炎[3]、急性扁桃腺炎[4]和輕型肺炎等[5]。目前,該質量標準收載于《獸藥質量標準》2017年版(中藥卷)[6]。標準采用薄層色譜法鑒別綠原酸、黃芩苷和連翹,采用HPLC法測定黃芩苷的含量,未對連翹苷進行質量控制。目前,連翹苷含量測定的高效液相色譜方法主要有熒光檢測法[7]和紫外法[8-11]。因此,本文對連翹苷檢測的兩種方法進行了比較研究,然后利用建立的方法進行實際樣品檢測,為完善雙黃連注射液的質量控制積累數據。
1 材料與方法
1.1 試劑與儀器
連翹苷對照品購于中國食品藥品檢定研究院,批號110821-201213,含量95.3%;雙黃連注射液,規格為10mL,批號為 20180801、20180802、20180803等3批。乙腈、甲醇均為色譜純,德國默克公司;磷酸、三乙胺和磷酸二氫鉀為分析純;水為超純水。
Agilent 1260高效液相色譜儀,配VWD檢測器(美國Agilent公司);KQ-500E型超聲波清洗器(昆山市超聲儀器有限公司);Waters 2695-2475高效液相色譜儀(配Empower 2軟件);梅特勒-托利多METTLER TOLEDO XS-205電子天平(精度為0.01mg)。
1.2 高效液相色譜-熒光法
1.2.1 對照品溶液和供試品溶液的配制 取連翹苷對照品適量,加50%甲醇溶液配制成每1mL中含連翹苷約1μg/mL的溶液,為連翹苷對照品溶液;取雙黃連注射液1.00mL,于50mL量瓶中,加入50%甲醇溶液稀釋,定容;再取該溶液5.00mL,于50mL量瓶中,加入50%甲醇溶液稀釋,定容,過0.45μm有機濾膜,上機測定。
1.2.2 液相色譜參考條件 色譜柱為Waters Symmetry C18(4.6mm×250mm,5.0μm);熒光檢測條件為激發波長277nm,發射波長315nm;柱溫為30℃;流速為1.0mL/min;進樣量為20μL;流動相:乙腈-水(25∶75,v∶v)。
1.3 高效液相色譜-紫外法
1.3.1 對照品溶液和供試品溶液的配制 取連翹苷對照品適量,加50%甲醇溶液配制成每1mL中含連翹苷約100μg/mL的溶液,為連翹苷對照品溶液;取雙黃連注射液1.00mL,于5mL量瓶中,加入50%甲醇溶液稀釋,定容,過0.45μm有機濾膜,上機測定。
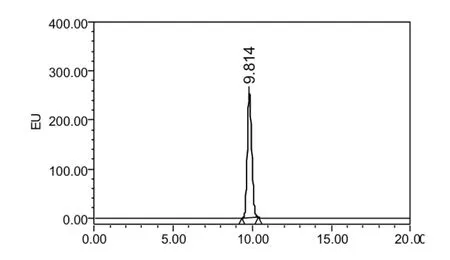
圖1 對照品溶液(濃度為1μg/mL)色譜圖(熒光檢測器)
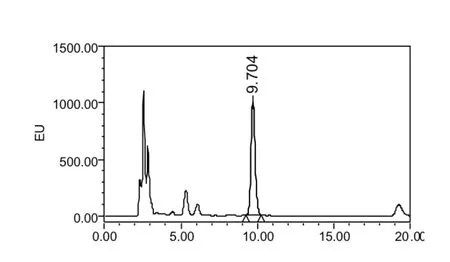
圖2 供試品溶液(批號為20180101)色譜圖(熒光檢測器)
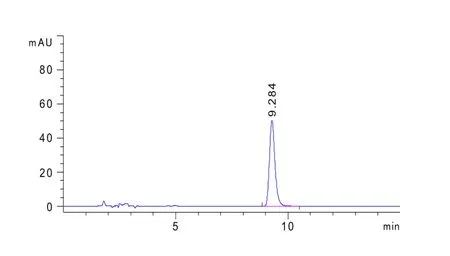
圖3 對照品溶液(濃度為1 μg/mL)色譜圖(紫外檢測器)
1.3.2 液相色譜參考條件 色譜柱為Waters Symmetry C18(4.6mm×250mm,5.0μm);檢測波長278nm,柱溫為30℃;流速為1.0mL/min;進樣量為20μL;流動相:乙腈-水(25∶75,v∶v)。
2 結果與分析
2.1 熒光檢測條件的確定
熒光檢測條件的確定及掃描方法參考文獻[12],首先將儀器的激發波長設定為200nm,發射波長掃描范圍為210~800nm,掃描后發現發射波長在277nm處有最大吸收;因此,將277nm的波長作為發射波長固定下來,做激發波長的掃描,掃描結果發現激發波長在315nm處有最大吸收。因此確定熒光檢測條件為激發波長277nm、發射波長315nm。
2.2 色譜柱的選擇
分別對Waters Symmetry C18、Waters Atlantis C18和Agilent ZORBAX Extend-C18等三種色譜柱進行檢測,結果這三種色譜柱都可以用于連翹苷的檢測。
2.3 流動相的選擇
比較了磷酸鹽緩沖液-乙腈、磷酸溶液-乙腈和水-乙腈體系,結果發現水-乙腈流動相體系連翹苷峰型最好、靈敏度最高。優化配比,使連翹苷獲得最佳保留時間,最終確定流動相為乙腈-水(25∶75,v∶v),流速為1.0mL/min。
2.4 線性考察、檢測限和定量限
取標準系列工作溶液進樣檢測,以峰面積Y對濃度X(μg/mL)作標準曲線。熒光檢測法得出回歸方程為Y=6.72×105X-2.36×104, 相 關 系 數 R2為0.9999, 在 0.01~10.0μg/mL 的濃度范圍內呈良好的線性關系;紫外檢測法得出回歸方程為Y=3.66×105X+1.06×104,相關系數R2為 0.9999, 在 1~200μg/mL 的濃度范圍內呈良好的線性關系。

表1 兩種方法測定雙黃連注射液中連翹苷含量結果比較(n=3)
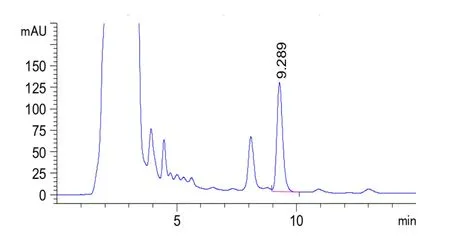
圖4 供試品溶液(批號為20180101)色譜圖(紫外檢測器)
2.5 高效液相色譜結果分析
按照上述方法測定,典型色譜圖見圖1-4。
2.6 兩種方法結果比較
對高效液相色譜-熒光檢測法和高效液相色譜-紫外檢測法的結果進行比較,每批3次測定相對標準偏差均在3.0%以內,兩種方法含量測定平均值的相對偏差在3.0%以內,表明結果無顯著差異。
3 結論
試驗結果表明,熒光法和紫外法測定雙黃連注射液中連翹苷的含量,結果無顯著差異,兩種方法都可以用于連翹苷的測定,熒光檢測法響應較高,不易受雜質干擾,對于低含量、雜質較多的樣品,影響因素較少,抗干擾強;紫外法響應低,易受雜質干擾,誤差較大。■

