5位和7位溴代橙酮衍生物的合成
沈 棣,潘國軍,蘇 超,蘆 逵
(天津科技大學生物工程學院,天津 300457)
橙酮(aurones)是植物體內的一種次生代謝產物,屬于特殊的黃酮類化合物,普遍存在于植物的根、莖、葉、花、果實中,也有報道稱少數海洋生物中也存在橙酮類化合物,橙酮母核結構為 2–(Z)–苯亞甲基–3–(2H)–苯并呋喃酮,由一個環外 C=C 雙鍵連接苯并呋喃和苯環(圖 1),是相應的黃酮(flavones)的同分異構體[1].近年來有關橙酮化合物的生物活性和藥理作用研究顯示其具有抗癌[2]、抗菌[3]、抗寄生蟲[4]、抗病毒[5]、抗炎[6]、抗瘧等活性.此外,橙酮還可以作為乳腺癌耐藥蛋白(ABCG2)抑制劑[7]、P–糖蛋白(Pgp)介導的多藥耐藥調節劑、乙酰膽堿酯酶抑制劑和腦 B型單胺氧化酶抑制劑[8]等.如圖 1所示,Hamiltron(Ⅰ)具有切割 DNA鏈的作用,化合物Ⅱ對乳腺癌白藥蛋白(ABCG2)有抑制作用;Aureusidin(Ⅲ)可作為碘化甲腺氨酸脫腆酶的抑制劑.
天然橙酮化合物多存在于植物當中,但含量低,且因為其結構復雜、作用位點多、溶解性差,導致生物利用率不高,限制了它們的廣泛應用.目前,文獻報道的有關橙酮化合物的結構修飾,主要集中在C4、C5、C7、C2'、C3'、C4'等位置.通過引入具有不同作用的基團,例如鹵素、烷(氧)基、芳基、二甲氨基、氨基、羧基、烯丙基等基團,以期改善其生物活性和提高生物利用率.
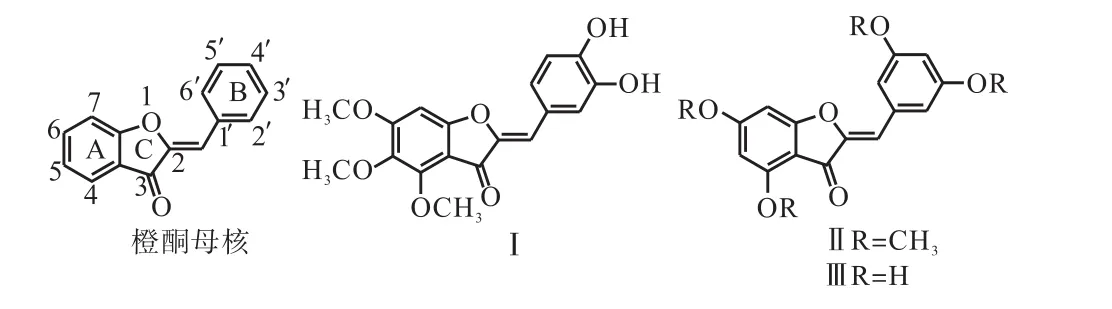
圖1 橙酮化合物的結構式Fig. 1 Structures of aurones
宋成榮等[9]在研究橙酮的抑菌活性中發現,B環上有鹵素取代的化合物對番茄灰霉病菌的抑制效果較好.黃新煒等[10]對橙酮的抗腫瘤活性研究結果表明,在B環4'位引入鹵素和3'位引入吸電子基團有利于增強抗腫瘤活性.張敏等[11]發現在 A環上 5位引入甲基可以顯著提高橙酮的除草活性.除上述文獻報道外,還發現在查爾酮化合物的3位和5位引入異戊烯基、香葉基可以顯著提高其抗腫瘤活性[12].
因此,考慮在橙酮的5位和7位進行結構改造,利用 Suzuki反應作為關鍵反應引入烷基、芳基等基團,以期改善橙酮的溶解性和生物活性.那么作為Suzuki反應關鍵底物的5位和7位的鹵代橙酮化合物的合成就成了首要解決的問題.此前,本課題組成功地在黃酮化合物的6位和8位實現了選擇性碘代和溴代[13–14],并且在使用鹵代黃酮化合物進行 Suzuki反應時,溴代黃酮的脫鹵副產物明顯少于碘代黃酮.與黃酮的選擇性鹵代研究不同,本研究目的是為了能夠簡便地合成5位與7位鹵代橙酮化合物,為之后對其不同位點進行結構改造得到大量衍生物并進行活性研究提供可能.因此,設計3個橙酮化合物母核,并以此探究5位和7位溴取代橙酮高效簡潔的合成方法.
1 材料與方法
1.1 試劑與儀器
二溴海因、N–溴代丁二酰亞胺,化學純,安耐吉化學;三氯化鋁、鹽酸、氫氧化鉀、間苯三酚、對羥基苯甲醛、3,4–二羥基苯甲醛、3,4,5–三羥基苯甲醛、1,2–二氯乙烷(DCE)、氯乙酰氯、無水硫酸鈉、無水碳酸鉀、2–碘丙烷;二氯甲烷(DCM),乙醇(EtOH)、石油醚、乙酸乙酯、N,N–二甲基甲酰胺(DMF),分析純,北京化學試劑公司.
循環水式真空泵,河南省予華儀器有限公司;集熱式恒溫加熱磁力攪拌器,鄭州長城科工貿有限公司;低溫恒溫反應浴,鞏義市京華儀器有限公司;Av–400,MHz 型核磁共振儀,瑞士Bruker公司.
1.2 合成路線
設計 5位和 7位溴代橙酮目標產物的合成線路如圖2所示.
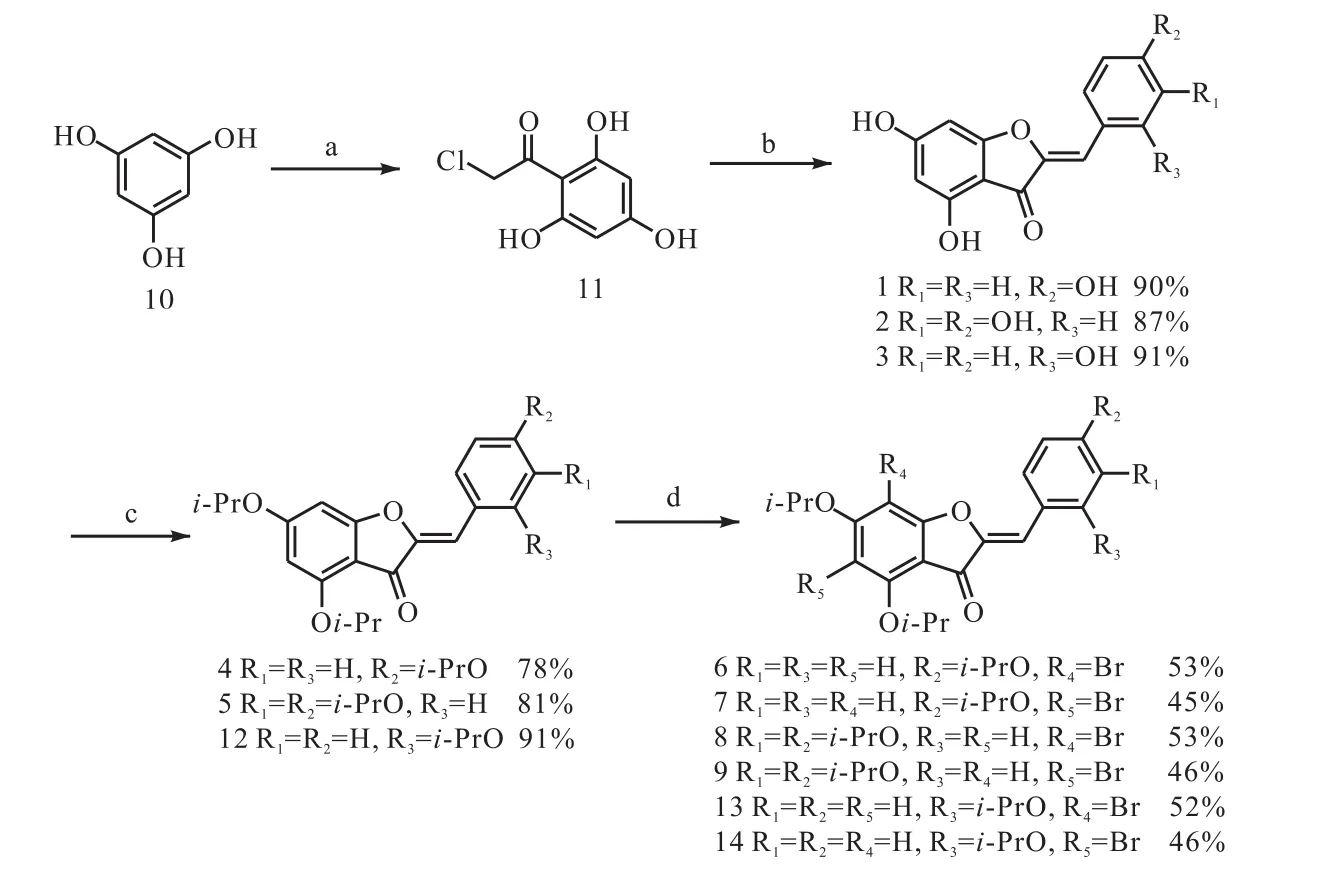
圖2 目標橙酮化合物的合成線路Fig. 2 Synthetic route of target aurones
在對橙酮進行選擇性溴代反應時,針對溴化試劑及反應條件作了篩選和優化.起初,采用 NBS作為溴化試劑,在–40,℃時幾乎不反應.之后,升溫至–20、0、25,℃時底物的轉化程度都很低.因而,考慮使用二溴海因(DBDMH)作為溴化試劑,在–40,℃條件下能達到較高的轉化率.在室溫下反應,底物幾乎可以完全轉化為5位、7位溴代的目標產物.
以異丙基全保護的金魚草素為例,在不同條件下的溴化反應(圖 3)結果見表 1.在 25,℃條件下,以二溴海因作為溴化試劑,二氯甲烷作為溶劑,就能以較高的收率同時得到 5位、7位溴代橙酮目標化合物,兩者的產率分別在53%,和46%,.
1.2.1 化合物11的合成
稱取5,g(39.65,mmol)間苯三酚溶于80,mL DCE中,在冰浴條件下,加入 10.57,g(79.30,mmol)無水三氯化鋁并攪拌 10,min,然后用恒壓滴液漏斗逐滴滴加5.37,g(47.58,mmol)氯乙酰氯,攪拌30,min后升至室溫并用堿液作尾氣吸收裝置,此后將反應體系置于100,℃油浴中加熱回流,反應 8,h.冷卻至室溫后,倒入 0,℃的濃鹽酸,攪拌 30,min后抽濾、洗滌,干燥得到4.98,g白色固體化合物11,產率62%,.
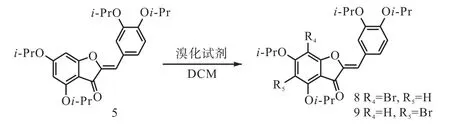
圖3 異丙基保護的金魚草素溴化反應Fig. 3 Bromination of isopropyl protected aureusidin
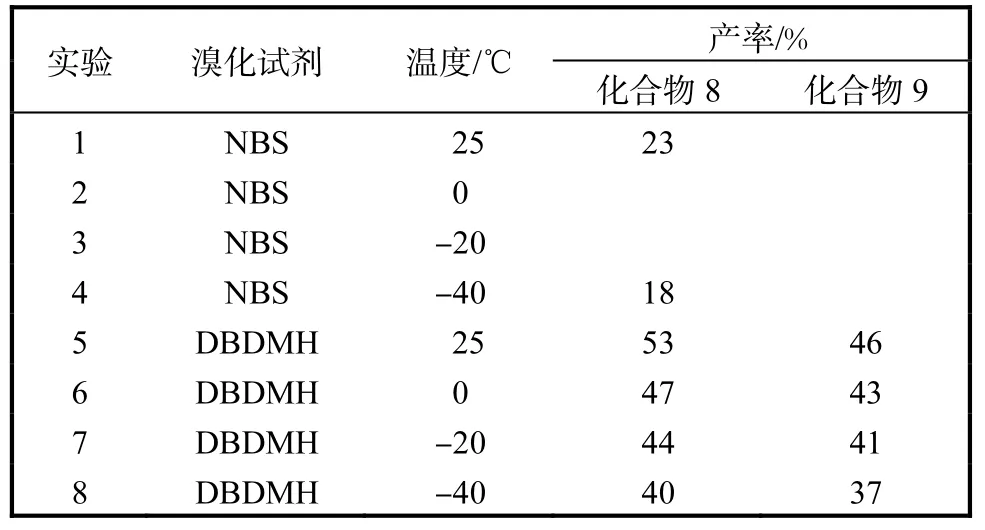
表1 溴化試劑及反應條件的篩選Tab. 1 Screening of bromide reagent and reaction conditions
1.2.2 化合物1—3的合成
稱取6.72,g(59.82,mmol)氫氧化鉀并配制成質量分數50%,的水溶液,室溫攪拌下加入3,mL乙醇以及1.22,g(9.97,mmol)對羥基苯甲醛,最后加入2.02,g(9.97,mmol)化合物 11,體系置于 60,℃油浴中反應5,h,TLC檢測反應.待反應完全后,在冰浴下慢慢加入 0,℃的稀鹽酸調 pH 至 3~4,抽濾、洗滌,干燥得到2.43,g紅色固體化合物1,產率90%,.
用3,4–二羥基苯甲醛和2–羥基苯甲醛替換對羥基苯甲醛,以相同的方法可得到化合物 2和 3,產率分別是 87%,、91%,.
1.2.3 化合物4、5和12的合成
稱取2.7,g(10,mmol)化合物1置于100,mL耐壓瓶中,加入 10,mL DMF將其溶解,在攪拌狀態下加入 5.39,g(39,mmol)無水碳酸鉀和 6.63,g (39,mmol)2–碘丙烷(i-PrI),60,℃油浴中反應 24,h.待反應冷卻至室溫后,濾除體系中固體,用乙酸乙酯洗滌并將濾液倒入 1,mol/L鹽酸中.用乙酸乙酯進行萃取,分離得到有機相并將有機相用飽和食鹽水洗滌3次,之后用無水硫酸鈉進行干燥,旋干有機相,拌樣.粗品經過硅膠柱層析(V(石油醚)∶V(乙酸乙酯)=40∶1的混合溶液為展開劑)純化后,得到 3.09,g黃色固體化合物 4,產率 78%,.
用化合物2以相同的方法可得到化合物5,產率81%,.
用化合物 3以相同的方法可得到化合物 12,產率 84%,.
1.2.4 化合物6、7、8、9、13、14的合成
稱取3.97,g(10,mmol)化合物4溶于25,mL干燥的二氯甲烷中,向其中加入 1.72,g(6,mmol)二溴海因,在室溫下攪拌反應 30,min.之后將反應體系倒入200,mL冰水中,用二氯甲烷(3×50,mL)萃取,合并有機相并用飽和食鹽水萃洗,分離得到有機相用無水硫酸鈉干燥.減壓旋干有機相,拌樣.粗品經過硅膠柱層析(V(石油醚)∶V(乙酸乙酯)=40∶1的混合溶液為展開劑)分離純化后,同時得到 2.52,g黃色固體化合物6和2.14,g黃色固體化合物7,產率為53%,和45%,.
稱取 4.00,g(8.74,mmol)化合物5,以相同的方法可同時得到2.47,g黃色固體化合物8和2.14,g黃色固體化合物9,產率為53%,和46%,.
稱取 4.00,g(9.34,mmol)化合物 12,以相同的方法可同時得到2.47,g黃色固體化合物13和2.18,g黃色固體化合物14,產率為52%,和46%,.
1.3 化合物表征數據
化合物 6:1,H NMR(400,MHz,CDCl3)δ 7.87(d,J=8.8,Hz,2H),6.96(d,J=9.2,Hz,2H),6.75(s,1H),6.20(s,1H),4.88~4.82(m,1H),4.71~4.60(m,2H),1.45(d,J=6.0,Hz,6H),1.43(d,J=6.0,Hz,6H),1.37(d,J=6.0,Hz,6H).13,C,NMR(101,MHz,CDCl3)δ 180.29,164.74,162.46,159.26,157.28,146.43,133.28,124.76,116.07,111.89,107.46,96.48,86.88,73.44,72.86,69.99,58.49,22.01,18.45. 熔點 138.6,℃.LRMS m/e C24,H27BrO5[M+H]+理論值475.1,實測值475.1.
化合物 7:1H NMR(400,MHz,CDCl3)δ 7.81(d,J=8.8,Hz,2H),6.94(d,J=8.8,Hz,2H),6.74(s,1H),6.54(s,1H),5.25~5.19(m,1H),4.73~4.60(m,2H),1.48(d,J=6.0Hz,6H),1.41(d,J=6.0,Hz,6H),1.37(d,J=6.0Hz,6H).13,C,NMR(101,MHz,CDCl3)δ 179.69,167.34,162.42,159.27,154.88,146.32,133.07,124.74,115.97,111.94,108.18,102.70,92.21,79.09,72.86,70.01,22.65,21.99,21.91. 熔點 107.1,℃.LRMS m/e C24H27BrO5[M+H]+理論值475.1,實測值475.1.
化合物 8:1H NMR(400,MHz,CDCl3)δ 7.73(d,J=2.0,Hz,1H),7.37(dd,J=8.4,2.0,Hz,1H),6.95(d,J=8.4,Hz,1H),6.72(s,1H),6.20(s,1H),4.88~4.82(m,1H),4.69~4.54(m,3H),1.44(t,J=6.0,Hz,12H),1.41(d,J=6.0,Hz,6H),1.37(d,J=6.0,Hz,6H).13,C NMR(101,MHz,CDCl3)δ 180.21,164.67,162.48,157.32,150.71,149.07,146.54,126.09,125.79,119.47,116.93,112.12,107.44,96.50,86.82,73.43,72.90,72.11,72.06,22.37,22.20,22.00. 熔點172.6,℃.LRMS m/e C27H33BrO6[M+H]+理論值 533.1,實測值533.1.
化合物 9:1H NMR(400,MHz,CDCl3)δ 7.46(d,J=2.0,Hz,1H),7.45(d,J=2.0,Hz,1H),6.95(d,J=9.0,Hz,1H),6.70(s,1H),6.52(s,1H),5.25~5.18(m,1H),4.74~4.67(m,1H),4.62~4.56(m,1H),4.54~4.48(m,1H),1.48(d,J=6.0,Hz,6H),1.41(d,J=6.0,Hz,6H),1.38(d,J=6.0,Hz,6H),1.37(d,J=6.0,Hz,6H).13C NMR(101,MHz,CDCl3)δ 179.65,167.35,162.45,154.89,151.24,148.63,146.46,126.33,125.58,121.71,116.44,112.04,108.16,102.78,92.25,79.07,72.96,72.88,71.72,22.63,22.27,22.15,21.90. 熔點 169.5,℃.LRMS m/e C27H33BrO6[M+H]+論值533.1,實測值533.1.
化合物 13:1H NMR(400,MHz,CDCl3)δ 8.35(dd,J=7.9,1.4,Hz,1H),7.38(s,1H),7.34~7.30(m,1H),7.06(t,J=15.2,Hz,1H),6.92(d,J=8.4,Hz,1H),6.21(s,1H),4.92~4.86(m,,H),4.71~4.58(m,2H),1.45(d,J=6.0,Hz,6H),1.42(d,J=6.0,Hz,6H),1.38(d,J=6.4,Hz,6H).13,C,NMR(101,MHz,CDCl3)δ 180.51,164.96,162.59,157.42,157.31,147.54,132.20,131.02,122.64,121.00,113.65,107.58,106.26,97.05,87.13,73.83,72.92,71.23,22.16,22.14,22.07. 熔點 125.2,℃.LRMS m/e C24,H27BrO5[M+H]+理論值475.1,實測值475.1.
化合物 14:1H NMR(400,MHz,CDCl3)δ 8.22(dd,J=7.8,1.4,Hz,1H),7.36(s,1H),7.32~7.28(m,1H),7.00(t,J=15.2,Hz,1H),6.91(d,J=8.4,Hz,1H),6.53(s,1H),5.28~5.21(m,1H),4.71~4.58(m,2H),1.46(d,J=6.0,Hz,6H),1.41(d,J=6.0,Hz,6H),1.37(d,J=6.0,Hz,6H).13C,NMR(101,MHz,CDCl3)δ 179.90,167.55,162.57,157.24,154.98,147.45,131.91,131.12,122.42,120.57,113.42,108.16,106.39,102.73,92.31,79.13,72.94,70.95,22.76,22.14,21.97. 熔點 124.5,℃.LRMS m/e C24H27BrO5[M+H]+理論值475.1,實測值475.1.
2 結果與討論
2.1 橙酮母核的合成
傳統的合成橙酮的方法一般有兩種:第一,以3(2H)–苯并呋喃酮為關鍵中間體;第二,通過 2′–羥基查耳酮的氧化環化.然而第一種方法中 3(2H)–苯并呋喃酮的合成實驗條件比較苛刻,且對一些底物的反應產率較低;第二種方法對底物結構有限制,且反應步驟多,較繁瑣.
以化合物2金魚草素為例,本實驗中橙酮母核的合成是通過化合物 11與 3,4–二羥基苯甲醛發生縮合、關環、消除反應得到,反應操作簡單,收率也較高.具體反應機理如圖 4所示,首先化合物 11在堿性條件下,失去羰基α 氫形成α 碳負離子進攻醛的碳正離子,氯離去,形成環氧中間體;然而由于環氧結構的不穩定,氧拉電子導致兩個位置的碳呈正電性,此外該結構中的羰基同樣具有吸電子作用,使得與之相鄰的碳更顯正電,因而苯環上的氧更容易進攻羰基的α 碳;另一方面,從空間位阻的角度考慮,在堿催化的條件下,氧更容易進攻空間位阻小的碳.所以,綜合電子效應和空間位阻兩個因素來分析,在環氧開環這一步中,氧更容易進攻羰基的α 碳,從而形成的是閉合的五元環結構,而不是六元環.最后在堿性加熱的條件下,羥基消除生成環外雙鍵,得到最終的橙酮化合物——金魚草素.
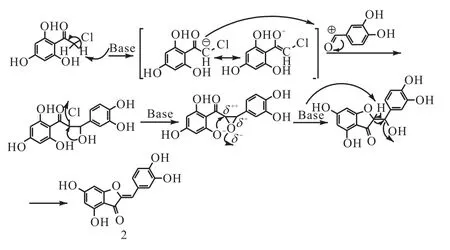
圖4 橙酮母核合成反應機理Fig. 4 Reaction mechanism of the aurone
在處理該反應的過程中,由于金魚草素上的酚羥基具有酸性,所以在氫氧化鉀的作用下,金魚草素是以水溶性很好的鉀鹽的狀態存在,然而加入鹽酸后使其變回酚羥基,溶解度降低,因此產物可以從溶液中析出,得到金魚草素的粗產品.接下來可以利用金魚草素不溶于二氯甲烷,而部分雜質溶于二氯甲烷的性質,將干燥后的粗品用二氯甲烷溶解、洗滌、抽濾,進行純化可得純度較高的金魚草素.
2.2 橙酮的溴代反應
在以二溴海因作為溴化試劑進行橙酮的選擇性溴代時,發現其選擇性較差.一般以 53%,和 45%,左右的產率分別得到 7位的溴代產物和 5位的溴代產物.分析其原因可能是:一方面橙酮與黃酮的結構相比,橙酮的中間是五元環而黃酮的中間是六元環,橙酮3位上的羰基對4位的異丙基造成的擠壓小,因而在 5位擁有了更大的空間,因此 Br原子更容易進攻5位;另一方面由于橙酮的雙鍵在環外,因此 C環上的羰基和氧對于 A環的電子云影響也不如黃酮顯著,因而5位與7位的親核性也幾乎沒太大差別.所以綜合分析兩種因素可以得出結論:橙酮化合物7位的溴代選擇性略高于5位,但兩者沒有顯著區別.
因此,可以近乎相當的產率同時得到5位和7位溴代的橙酮化合物.
3 結 語
本文首先合成了3個橙酮化合物母核,再以它們為重要中間體,通過異丙基保護后,采用二溴海因作為溴代試劑,以中等收率同時獲得 5位和 7位的 Br取代橙酮化合物,產率分別在 46%,和 53%,左右,總收率在 99%,左右.該類化合物的成功合成為進一步對橙酮化合物的 5位和 7位進行結構修飾和改造奠定了重要的基礎.
[1] Carrasco M P,Newton A S,Gon?alves L,et al. Probing the aurone scaffold against Plasmodium falciparum:Design,synthesis and antimalarial activity[J]. European Journal of Medicinal Chemistry,2014,80:523-534.
[2] Lee C Y,Chew E H,Go M L. Functionalized aurones as inducers of NAD(P)H:Quinone oxidoreductase 1 that activate AhR/XRE and Nrf2/ARE signaling pathways:Synthesis,evaluation and SAR[J]. European Journal of Medicinal Chemistry,2010,45:2957–2971.
[3] Okombi S,Rival D,Bonnet S,et al. Discovery of benzylidenebenzofuran-3(2H)-one(aurones)as inhibitors of tyrosinase derived from human melanocytes[J]. Journal of Medicinal Chemistry,2006,49(1):329-333.
[4] Kayser O,Kiderlen A F,Folkens U,et al. In vitro leishmanicidal activity of aurones[J]. Planta Med,1999,65(4):316-319.
[5] Haudecoeur R,Ahmed-Belkacem A,Yi W,et al. Discovery of naturally occurring aurones that are potent allosteric inhibitors of Hepatitis C virus RNA-dependent RNA polymerase[J]. Journal of Medicinal Chemistry,2011,54(15):5395-5402.
[6] Shin S Y,Shin M C,Shin J S,et al. Synthesis of aurones and their inhibitory effects on nitric oxide and PGE(2)productions in LPS-induced RAW264.7 cells[J]. Bioorganic & Medicinal Chemistry Letters,2011,21(15):4520-4523.
[7] Sim H M,Loh K Y,Yeo W K,et al. Aurones as modulators of ABCG2 and ABCB1:Synthesis and structureactivity relationships[J]. Chemmedchem,2011,6(4):713-724.
[8] Sheng R,Xu Y,Hu C,et al. Design,synthesis and AChE inhibitory activity of indanone and aurone derivatives[J]. European Journal of Medicinal Chemistry,2009,44(1):7-17.
[9] 宋成榮. 橙酮類似物的合成及抑菌活性研究[D]. 楊凌:西北農林科技大學,2012.
[10] 黃新煒,王征,陳巧利,等. 橙酮衍生物的合成及初步抗腫瘤活性研究[J]. 有機化學,2013(12):2565-2571.
[11] 張敏. 苯并[c]菲啶和橙酮類化合物的設計、合成與生物活性研究[D]. 天津:南開大學,2009.
[12] Wang H M,Zhang L,Liu J,et al. Synthesis and anticancer activity evaluation of novel prenylated and geranylated chalcone natural products and their analogs[J]. European Journal of Medicinal Chemistry,2015,92:439-448.
[13] Lu K,Chu J,Wang H M,et al. Regioselective iodination of flavonoids by N-iodosuccinimide under neutral conditions[J]. Tetrahedron Letter,2013,54:6345–6348.
[14] Pan G J,Yang K,Ma Y T,et al. Synthesis of 6- or 8-bromo flavonoids by regioselective mono-bromination and deprotection protocol from flavonoid alkyl ethers[J]. Bulletin of the Korean Chemical Society,2015,36:1460-1466.

