GnRH激動劑長效劑型的兩種促排卵方案在PCOS患者中的應用
李蘇萍,劉海鵬,陳藝,楊帆,賀平
(郴州市第一人民醫院生殖醫學中心,郴州 423000)
多囊卵巢綜合征(PCOS)是一種青春期和育齡期婦女最常見的內分泌紊亂性的疾病,表現為高雄激素血癥、閉經、不孕、多毛和肥胖。其中因排卵障礙而致不孕是多囊卵巢綜合征的主要臨床表現。中國近來的報告育齡期女性患病率約為5.61%[1]。在當不孕PCOS患者經歷了藥物治療和/或手術治療/人工授精等治療后仍無法妊娠時,選擇IVF/ICSI-ET治療是有效途徑。由于PCOS患者內分泌情況復雜多變,給控制性卵巢刺激(COS)帶來一定困難,因此選擇適宜的對PCOS患者進行助孕至關重要。但目前對于PCOS患者選擇理想的COS方案仍不明確。激動劑長方案在國內臨床上比較常見,根據劑型又分為短效和長效制劑,而對于在黃體中期對垂體進行降調節的GnRH激動劑長效劑型方案又有改良超長方案及減量長效長方案,文獻報道這兩種方案均有較好的治療結局。近幾年來我中心開始嘗試改良超長方案進行垂體降調節,本文回顧性分析2015年1月至2016年6月期間在我中心收治的經行IVF/ICSI的PCOS不孕患者,分別采用改良超長方案及減量長效長方案降調節,分析其臨床治療特征及妊娠結局,為PCOS患者的COS方案選擇提供思路。
資料與方法
一、一般資料
選取于2015年1月至2016年6月在我院生殖中心行IVF/ICSI的423例PCOS不孕患者。納入標準:(1)確診為PCOS患者,診斷標準按照鹿特丹標準[2];(2)其它不孕原因主要合并輸卵管因素和(或)男方因素;(3)年齡≤38歲;(4)體重指數(BMI)18~27 kg/m2。排除標準:(1)3個及以上重復周期患者;(2)有復發性流產病史;(3)子宮內膜異位癥及子宮器質性病變;(4)有嚴重子宮畸形或宮腔粘連、子宮內膜結核及既往有盆腔結核病史者;(5)促排卵周期中取消取卵者。
二、方法
1.分組及促排方案:根據垂體降調節方案的不同分為兩組:兩組患者均在接受治療前開始服用炔雌醇-環丙孕酮片(達英-35,拜耳醫藥,德國)做為預處理。自患者降調前最后一次月經第3天開始服用,每天一片,在服到第18片時開始肌肉注射促性腺激素釋放激素類似物(GnRH-a),分為改良超長方案(A組)和減量長效長方案(B組)。其中A組首次肌肉注射GnRH-a(曲普瑞林,達菲林,IPSEN,法國)1.200~1.875 mg后,于第2個月經周期的第21天再次注射相同劑量,在13~20 d后抽血查雌二醇(E2)<146.8 pmol/L、孕酮(P)<2.54 nmol/L、黃體生成素(LH)<5 U/L。行陰道B超示子宮內膜厚度<5 mm,雙側卵巢沒有直徑>10 mm的卵泡視為達到降調節標準。即開始使用促性腺激素(Gn)進行卵巢刺激,根據患者年齡、竇卵泡計數(AFC)、卵巢儲備功能、BMI值等綜合決定Gn啟動劑量(75~225 U/d),共4 d。B組則單次肌肉注射GnRH-a 0.9~1.2 mg進行垂體降調節,在13~20 d后查血清E2、P、LH及B超,結果達上述標準后使用Gn進行卵巢刺激。兩組根據卵巢反應性及卵泡生長發育的情況調整Gn劑量,當卵泡生長緩慢,卵泡增長<2 mm/3 d或者E2在Gn 6~8 d<732 pmol/L先首先考慮增加Gn,若在Gn劑量足夠的基礎上出現卵泡發育慢或E2增長緩慢,且血LH<0.5 U/L,則添加重組LH(樂芮,雪蘭諾,瑞士),通過陰道B超監測內膜和卵泡生長情況。
2.取卵和移植:兩組方案均為當至少有3個卵泡直徑≥ 18~20 mm時給予注射絨毛膜促性腺激素(HCG)5 000~10 000 U誘導卵泡成熟,36~38 h后經陰道取卵。IVF/ICSI-ET操作和黃體支持本中心按照常規進行。妊娠與否確定:胚胎移植14 d檢測血HCG>5 U/L以上視為陽性,定為生化妊娠,胚胎移植28 d后B超檢查了解孕囊個數及位置,發現孕囊者視為臨床妊娠。
3.觀察指標:主要觀察指標包括兩組年齡、不孕年限、體重指數(BMI)、基礎激素、竇卵泡計數(AFC),病因構成、促排卵情況、降調日、啟動日、HCG注射日激素變化及獲卵數、2PN受精率、卵裂率、優胚率、移植胚胎數、子宮內膜厚度、遲發性中重度OHSS發生率、OHSS風險取消移植率、種植率、臨床妊娠率、早期流產率、抱嬰率等。
三、統計學方法

結 果
一、患者臨床一般資料及基礎狀況
兩組患者年齡、不孕年限、體重指數(BMI)及基礎FSH、LH、T值、AFC計數、病因構成比較均無統計學差異(P>0.05)(表1、表2)。
二、兩組患者促排卵情況比較
統計結果表明,兩組患者降調日血清FSH、LH、E2,啟動日FSH、E2及HCG日LH、E2、P比較,差異均無統計學意義(P>0.05);啟動日血清LH水平A組顯著低于B組,有統計學差異(P<0.05);兩組患者Gn天數、啟動Gn劑量、Gn總量比較,差異均無統計學意義(P>0.05),r-hLH量A組顯著高于B組,差異有統計學意義(P<0.05)(表3)。
三、兩組患者的臨床結局
統計結果表明,兩組患者獲卵數、2PN受精率、卵裂率、優胚率、移植胚胎數、子宮內膜厚度、OHSS風險取消移植率比較,差異均無統計學意義(P>0.05);A組種植率、臨床妊娠率、抱嬰率顯著高于B組,A組早期流產率顯著低于B組,差異均有統計學意義(P<0.05);遲發性中重度OHSS發生率兩組比較,差異無統計學意義(P>0.05)(表4)。
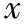
表1 兩組患者一般資料比較(-±s)

表2 兩組患者病因構成的比較[%(n)]
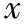
表3 兩組患者促排卵情況比較(-±s)
注:與B組比較,*P<0.05
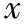
表4 兩組患者臨床結局比較[(-±s),%(n)]
注:與B組比較,*P<0.05
討 論
GnRH-a最早用于治療內異癥、性早熟、子宮肌瘤等疾病。于1984年開始被應用于輔助生殖技術的促排卵治療,目前廣泛用于各種垂體降調節方案。長效長方案、改良超長方案就是利用其抑制垂體效果或者降調節效應,有效降低卵泡期LH水平,避免卵泡過早黃素化,提高卵母細胞質量,從而獲得更多優質胚胎,改善妊娠結局[3]。對于PCOS患者,國內常采用降調節方案促排卵,也取得了一定的成效。但是因PCOS患者常常伴有FSH分泌不足、LH分泌異常增高、高胰島素血癥、高雄激素血癥等內分泌和代謝異常,OHSS發生率高[4],給COS帶來了一定程度的困難。在尋找合適的PCOS患者的COS方案過程中,龔斐等[5]研究率先國內外指出改良超長方案可能適合PCOS不孕患者。但除外該醫院,國內其他生殖中心關于該方案在PCOS患者中的使用情況報道較少。我中心在通過近幾年對該方案學習和摸索的基礎上,對近1年半的PCOS患者治療情況做了一個回顧性分析。
PCOS患者的內分泌特點其中一個表現為LH異常升高、FSH/LH比值倒置,致使較多的學者贊同使用LH/FSH比值作為PCOS的補充診斷依據[6],研究認為異常的LH水平,導致過早黃素化、卵母細胞發育不良、質量差,使胚胎著床率和臨床妊娠率都降低[7]。Evans等[8]的研究認為GnRH-a通過對垂體的長效降調節,增加子宮內膜LH受體的數量,增加對雌、孕激素的反應性。根據PCOS的內分泌特點,我中心歷年來多采用長效GnRH-a降調節,而從本研究中的數據可以看出,經過垂體兩次降調節后改良超長方案組啟動日LH值明顯低于減量長效長方案組,說明改良超長方案降調節時間延長,垂體抑制較深,使PCOS患者體內的LH水平控制在一個較低的范圍,可以穩定地抑制PCOS患者的異常內分泌水平,使卵泡處于穩定的反應期,充分的降調節可以避免PCOS患者在促排卵中的大量卵泡募集,減少OHSS相關風險。因PCOS患者是輔助生殖技術過程中易導致OHSS的高風險人群,據文獻報道可達15%[9]。近來也有研究認為PCOS患者為了降低OHSS發生率,可以選擇拮抗劑方案COS,但有較多研究同時也表明拮抗劑方案妊娠率低于激動劑方案,拮抗劑方案在國內起步晚,其廣泛應用還需一個學習的過程,對于PCOS來說仍待商榷。而在本研究中中重度OHSS發生率改良超長方案組與減量長效長方案組分別為2.24%和2.0%,未超出文獻報道的OHSS發生率(3%~6%)[10],說明如果改良超長方案及減量長效長方案掌握得當,即使在對于較敏感的PCOS人群中,也未明顯增加OHSS發生率,這與楊蕊等[11]的研究一致。
“兩細胞-兩促性腺激素”的學說認為,卵泡的正常發育和卵母細胞成熟需要LH和FSH的相互協同作用,且卵泡的發育及成熟和類固醇激素的合成均需要最低水平的LH。有學者證實,降調節后LH值過低可能影響卵泡的發育和卵母細胞質量,并對治療結局造成負面影響,此外LH還可以直接作用于子宮內膜的LH受體和黃體細胞,支持內膜和黃體的發育,減弱長效GnRH-a的溶黃體效應,改善子宮內膜容受性,因而提高胚胎種植率和臨床妊娠率,降低早期流產率。因此,晚卵泡期適當的LH水平對IVF/ICSI的結局至關重要[12]。在本研究中,改良超長方案組的降調后血LH值較減量長效長方案組低,差異具有統計學意義(P<0.05),因考慮該方案對垂體抑制程度更深,部分患者在其促排卵過程中需額外添加外源性LH以糾正卵泡中的LH水平,帥振虹等[12]、朱桂金[13]及Huarte等[14]的研究認為補充LH對臨床結局可以帶來益處。Humaidan等[15]的研究認為在血LH<0.5 U/L時對卵巢的反應性及妊娠結局均有顯著益處,但是否需要全部添加LH以及添加LH的時機,目前仍無公認的標準,其具體的發生機制,仍需要設計更多大樣本的前瞻性研究。
本研究中通過對比發現改良超長方案組臨床妊娠率及種植率顯著高于減量長效長方案組,早期流產率改良超長方案組顯著低于減量長效長方案組,差異均具有統計學意義(P<0.05),而其他相關指標分別比較均無明顯統計學意義。通過進一步分析及查閱相關文獻認為,GnRH-a通過延長降調時間,有使卵巢及子宮內膜處于一個較長靜止狀態的作用,可以改善子宮內膜容受性及盆腔微環境。龔斐等[16]的研究顯示改良超長方案組著床期子宮內膜上表達的胞飲突增加,著床相關因子COX2、LPAR3、HOXA10的表達增加,改善了子宮內膜容受性。因此本研究提示可能改良超長方案妊娠結局的提高是由于改善了子宮內膜容受性。但本研究中兩組方案內膜厚度相比較,無顯著性差異,這與某些文獻報道不一致,分析可能是因為本研究選擇的均是GnRH-a激動劑長效劑型,且研究設計與文獻不盡相同有關。
綜上所述,本研究認為,在PCOS患者IVF/ICSI-ET的治療中,改良超長方案有較好的臨床結局,可以為PCOS的輔助生殖治療提供一個選擇。但該方案也存在一些缺點,如治療周期延長,降調時間長可能帶來的低雌激素癥狀,延長促排卵天數及促排卵過程中需要添加更多LH。而本文為回顧性研究,存在其所固有的研究設計缺陷,其結果及所得出的結論可能存在偏倚,還需進一步大量數據及高質量研究分析論證。
[1] Li R,Zhang Q,Yang D,et al.Prevalence of polycystic ovary syndrome in women in China:a large community-based study[J].Hum Reprod,2013,28:2562-2569.
[2] Rotterdam ESHRE/ASRM-Sponsored PCOS consensus workshop group.Revised 2003 consensus on diagnostic criteria and long-term health risks related to polycystic ovary syndrome (PCOS) [J].Hum Reprod,2004,19:41-47.
[3] Lainas TG,Sfontouris IA,Zorzovilis IZ,et al.Flexible GnRH antagonist protocol versus GnRH agonist long protocol in patients with polycystic ovary syndrome treated for IVF:a prospective randomised controlled trial (RCT)[J].Hum Reprod,2010,25:683-689.
[4] Franks S,Stark J,Hardy K.Follicle dynamics and anovulation in polycystic ovary syndrome[J].Hum Reprod Update,2008,14:367-378.
[5] 龔斐,羅克莉,盧光琇.改良的超長方案在PCOS不孕患者IVF/ICSI-ET中的療效[J].基礎醫學與臨床,2010,30:984-987.
[6] Ning N,Balen A,Brezina PR,et al.How to recognize PCOS:results of a web-based survey at IVF-worldwide.com[J].Reprod Biomed Online,2013,26:500-505.
[7] Heijnen EM,Eijkemans MJ,Hughes EG,et al.A meta-analysis of outcomes of conventional IVF in women with polycystic ovary syndrome[J].Hum Reprod Update,2006,12:13-21.
[8] Evans J,Salamonsen LA.Too much of a good thing? Experimental evidence suggests prolonged exposure to HCG is detrimental to endometrial receptivity[J].Hum Reprod,2013,28:1610-1619.
[9] Pundir J,Sunkara SK,El-Toukhy T,et al.Meta-analysis of GnRH antagonist protocols:do they reduce the risk of OHSS in PCOS?[J].Reprod Biomed Online,2012,24:6-22.
[10] Marzal A,Holzer H,Tulandi T.Future developments to minimize ART risks[J].Semin Reprod Med,2012,30:152-160.
[11] 楊蕊,羅莉,王穎,等.多囊卵巢綜合征患者初次IVF/ICSI-ET助孕臨床方案選擇[J].生殖與避孕,2015,35:241-246.
[12] 帥振虹,連方.補充黃體生成素對控制性超促排卵過程中卵巢慢反應患者臨床結局的影響[J].現代婦產科進展,2014,23:716-723.
[13] 朱桂金.黃體生成素在卵泡發育中的作用和黃體生成素峰[J].生殖醫學雜志,2007,16:312-313.
[14] Huarte M,Rinn JL.Large non-coding RNAs:missing links in cancer?[J].Hum Mol Genet,2010,19:R152-R161.
[15] Humaidan P,Bungum L,Bungum M,et al.Ovarian response and pregnancy outcome related to mid-follicular LH levels in women undergoing assisted reproduction with GnRH agonist down-regulation and recombinant FSH stimulation[J].Hum Reprod,2002,17:2016-2021.
[16] 龔斐,郭慧,彭炬,等.改良超長方案改善多囊卵巢綜合征(PCOS)不孕患者子宮內膜容受性的研究[J].生殖與避孕,2015,35:300-309.

