握力與中老年2型糖尿病患者認知障礙的關系
王 琎,修雙玲,王 立
(首都醫科大學宣武醫院內分泌科,北京 100053;*通訊作者,E-mail:wangli@mail.bjhb.gov.cn)
2型糖尿病是一種以慢性高血糖為主要表現的代謝性疾病。已有研究顯示糖尿病是導致認知損害的獨立危險因素[1],與正常人群相比,糖尿病患者認知功能障礙發病率更高,程度更為嚴重,來自南京的一項調查發現糖尿病患者認知障礙的患病率約為29.8%[2]。糖尿病認知功能障礙的危險因素包括年齡、病程、血糖控制程度、胰島素抵抗程度,藥物、運動、炎性指標、合并相關血管疾病、基因等諸多因素。目前尚無有效改善認知障礙的治療方法。
肌肉減少癥是近年來被認識到的老年綜合征[3],即隨著年齡的增長,骨骼肌數量和質量下降而引起的疾病,發病機制復雜,涉及例如激素水平改變,胰島素抵抗,全身炎癥反應,去神經支配等多方面因素影響。有研究顯示糖尿病患者肌肉減少癥的發病率較高[4],糖尿病患者肌少癥發病率約為非糖尿病患者2-4倍[5]。研究發現糖尿病認知功能障礙與肌少癥發病機制都存在胰島素抵抗、全身炎癥反應,二者可能存在更多更緊密的關系。有研究[6]發現認知較好的老年人其握力大,且握力下降速度也相對慢。
目前國內尚缺少糖尿病認知功能與握力、身體成分的研究,本文旨在進一步探討握力與糖尿病患者認知障礙的關系。
1 對象與方法
1.1 研究對象
選擇2016-04~2016-09首都醫科大學宣武醫院內分泌科病房收治的2型糖尿病患者,符合入組標準的患者共100例,根據蒙特利爾認知評估MoCA(北京版)[7]分為認知障礙組(n=56)和認知功能正常組(n=44)。入組標準:年齡≥55歲的2型糖尿病患者;所有患者均符合中華醫學會《2013年中國2型糖尿病防治指南》中2型糖尿病診斷標準。排除標準:心功能不全,慢性阻塞性肺疾病,骨關節疾病等影響活動能力的疾病;糖尿病急性并發癥;嚴重肝腎功能不全;急性腦血管病、既往腦梗死遺留肢體活動障礙、顱內占位、顱內感染、癲癇、癡呆;嚴重聽力障礙。
1.2 研究方法
1.2.1 一般資料 記錄入組患者性別、年齡、身高、體質量、血壓、腰圍、臀圍、臂圍、腿圍,并發癥及合并疾病情況。計算每位患者BMI(BMI=體質量/身高2,kg/m2)、腰圍臀圍比、腿圍、臀圍等。所有測量人員均經過統一培訓,采用統一血壓計、皮尺等工具對患者進行測量。腰圍測量位置在水平位髂前上棘和第12肋下緣連線的中點。臀圍測量位置在恥骨聯合和背后臀大肌最凸處。
1.2.2 認知障礙評估 使用MoCA量表對所有患者認知功能進行評價。教育程度≤12年的患者加1分,總分≥26分為正常,<26分為認知障礙。
1.2.3 實驗室檢查 所有入組患者均禁食8 h,次日晨起抽取空腹靜脈血,化驗血糖(FPG)、胰島素(FINS)、C肽(CP)、糖化血紅蛋白(HbA1c)、甘油三酯(TG)、總膽固醇(TC)、高密度脂蛋白(HDL-C)、低密度脂蛋白(LDL-C)、促甲狀腺激素(TSH)、游離T3(FT3)、游離T4(FT4)、肌酐(Cr)、尿酸(UA)、同型半胱氨酸(HCY)、C反應蛋白(CRP)、白介素6(IL-6)、維生素D(VitD)、睪酮、雌二醇、生長激素、皮質醇水平。以上檢驗均由我院檢驗科進行。計算肌酐清除率、胰島素抵抗水平(HOMA-IR=FPG×FINS/22.5)。
1.2.4 肌肉數量、功能測量,骨密度檢查 采用雙光能X線骨密度儀,測量患者全身身體組成(上肢肌肉質量、上肢脂肪質量、下肢肌肉質量、下肢脂肪質量),兩側股骨頸、腰椎1-4椎體骨密度。計算四肢肌肉含量,骨骼肌肌肉質量指數(ASMI,四肢骨骼肌肌肉質量除以身高的平方,單位:kg/m2)。肌肉力量評價指標為握力、步速。握力測試使用Jamar握力計,結果單位為kg,精確到0.1。測試時采用美國手治療協會(American Society of Hand Therapists)所推薦的姿勢[8],即患者坐位,屈膝屈髖成90°,雙足置于水平地面,上臂緊貼胸部,前臂中立位,伸腕0°-30°,尺偏0°-15°,測定優勢手握力3次,取其最大值。步速測試為6 m步行試驗,即記錄患者于水平地面以正常速度行走6 m的時間,重復進行2次,取最短時間為試驗結果。
1.3 統計學方法
采用SPSS 19.0軟件進行統計分析,定量資料用均數±標準差表示,比較采用t檢驗,計數資料采用卡方檢驗。以認知障礙為因變量,以t檢驗中有差異的變量為自變量進行Logistic回歸分析,評價2型糖尿病認知障礙的危險因素。以P<0.05為差異具有統計學意義。
2 結果
2.1 兩組一般資料比較
入組100例中老年2型糖尿病患者,認知功能障礙者為56例(56.0%),MoCA得分為21.45±3.51;認知正常者44例(44.0%),MoCA得分為27.36±1.45。兩組年齡、體質量、肌酐清除率、上肢肌肉質量、上肢脂肪質量、四肢肌肉質量、骨骼肌肌肉質量指數(ASMI)、下肢上肢肌肉質量比、左上肢臂圍、右上肢臂圍、左下肢大腿圍、右下肢大腿圍、握力、左股骨頸骨密度比較差異有統計學意義(見表1-4)。兩組病程、血糖控制情況、激素水平、步速、右股骨頸、腰椎骨密度等差異無統計學意義。
2.2 多因素Logistic回歸分析
以單因素分析具有統計學意義的指標為自變量,以認知功能障礙為因變量,進行Logistic回歸分析,結果顯示,影響中老年2型糖尿病患者認知功能的危險因素為上肢脂肪質量(OR=0.51,P=0.014)、握力(OR=0.933,P=0.003,見表5)。
3 討論
國內外尚缺乏糖尿病人群認知功能與握力及身體成分的研究。本研究發現握力水平高、上肢脂肪質量高是認知障礙的保護性因素。
表1認知障礙與認知正常患者一般資料比較
Table1Comparisonofgeneralcharacteristicsbetweenpatientswithdifferentcognitionstatus

指標 認知障礙組認知正常組 t/χ2 P年齡(歲)65.88±7.9963.02±6.01-2.042 0.044體質量(kg) 70.06±11.41 75.19±10.082.3470.02身高(m) 1.66±0.08 1.68±0.071.2080.23BMI(kg/m2)25.30±3.5426.57±2.961.9190.06腰圍(cm)95.50±9.8496.55±9.550.5340.56臀圍(cm) 97.62±15.09102.11±7.96 1.7860.07腰臀比 0.96±0.06 0.94±0.05-0.8930.17左上肢臂圍(cm)28.35±2.8630.13±3.492.8070.00右上肢臂圍(cm)28.84±3.2630.21±3.462.0260.04左下肢大腿圍(cm)50.53±5.1053.10±5.372.4460.02右下肢大腿圍(cm)50.76±4.9153.21±5.182.4170.02左下肢小腿圍(cm)35.24±3.5736.18±2.921.4430.15右下肢小腿圍(cm)35.20±3.47 36.41±3.1171.7860.08糖尿病病史(年)14.66±9.0114.63±8.05-0.0230.98高血壓[例(%)]44(78.5)28(63.6)2.7260.099周圍神經病變[例(%)]25(0.44)20(0.45)0.0070.935糖尿病腎病[例(%)]10(0.18)8(0.18)0.0020.967糖尿病視網膜[例(%)]20(0.36)18(0.41)0.2820.595吸煙[例(%)]22(0.39)17(0.39)0.0040.947
表2認知障礙與認知正常患者肌肉數量、功能比較
Table2Comparisonofthemusclemassandfunctionbetweenpatientswithdifferentcognitionstatus
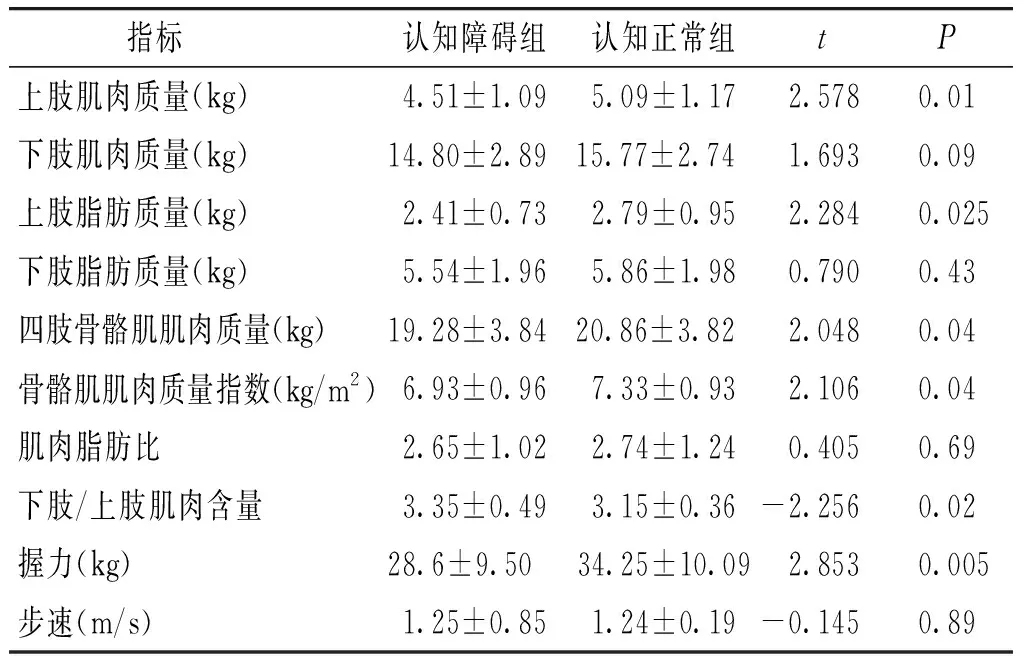
指標 認知障礙組認知正常組tP上肢肌肉質量(kg)4.51±1.095.09±1.172.5780.01下肢肌肉質量(kg)14.80±2.8915.77±2.74 1.6930.09上肢脂肪質量(kg)2.41±0.732.79±0.952.2840.025下肢脂肪質量(kg)5.54±1.965.86±1.980.7900.43四肢骨骼肌肌肉質量(kg)19.28±3.8420.86±3.82 2.0480.04骨骼肌肌肉質量指數(kg/m2)6.93±0.967.33±0.932.1060.04肌肉脂肪比2.65±1.022.74±1.240.4050.69下肢/上肢肌肉含量3.35±0.493.15±0.36-2.2560.02握力(kg)28.6±9.5034.25±10.092.8530.005步速(m/s)1.25±0.851.24±0.19-0.1450.89
表3認知障礙與認知正常患者骨密度水平比較
Table3ComparisonofBMDbetweenpatientswithdiffe-rentcognitionstatus
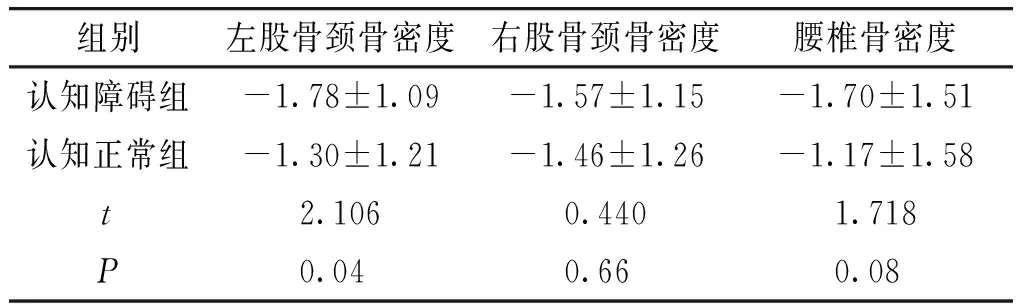
組別左股骨頸骨密度右股骨頸骨密度腰椎骨密度認知障礙組-1.78±1.09-1.57±1.15-1.70±1.51認知正常組-1.30±1.21-1.46±1.26-1.17±1.58t2.1060.4401.718P0.040.660.08
表4認知障礙與認知正常患者實驗室檢查比較
Table4Comparisonofthelaboratoryexaminationbetweenpatientswithdifferentcognitionstatus
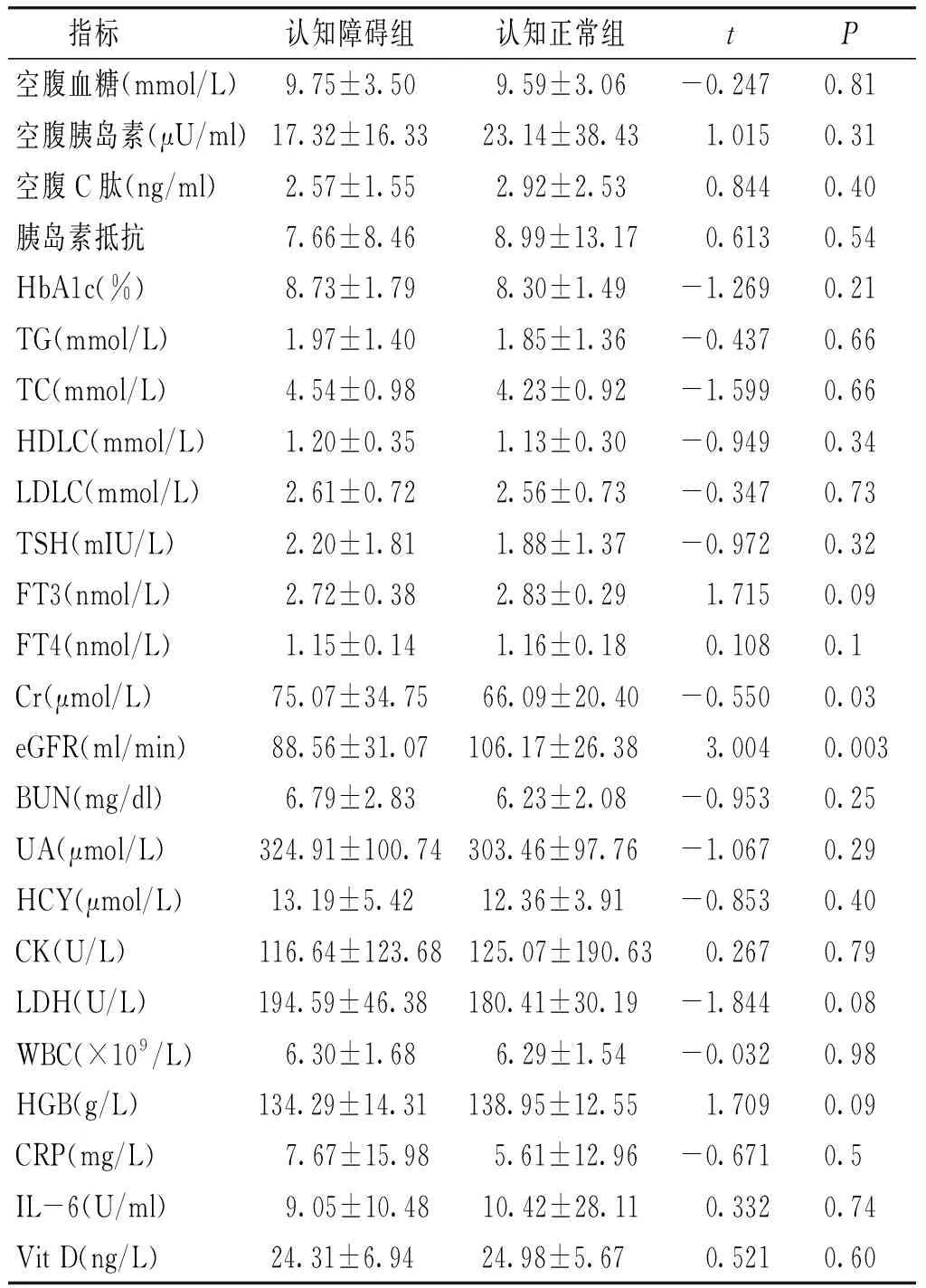
指標 認知障礙組認知正常組tP空腹血糖(mmol/L)9.75±3.509.59±3.06-0.247 0.81空腹胰島素(μU/ml)17.32±16.3323.14±38.431.0150.31空腹C肽(ng/ml)2.57±1.552.92±2.530.8440.40胰島素抵抗7.66±8.46 8.99±13.170.6130.54HbA1c(%)8.73±1.798.30±1.49-1.2690.21TG(mmol/L)1.97±1.401.85±1.36-0.4370.66TC(mmol/L)4.54±0.984.23±0.92-1.5990.66HDLC(mmol/L)1.20±0.351.13±0.30-0.9490.34LDLC(mmol/L)2.61±0.722.56±0.73-0.3470.73TSH(mIU/L)2.20±1.811.88±1.37-0.9720.32FT3(nmol/L)2.72±0.382.83±0.291.7150.09FT4(nmol/L)1.15±0.141.16±0.180.1080.1Cr(μmol/L)75.07±34.7566.09±20.40-0.5500.03eGFR(ml/min)88.56±31.07106.17±26.38 3.0040.003BUN(mg/dl)6.79±2.836.23±2.08-0.9530.25UA(μmol/L)324.91±100.74303.46±97.76 -1.0670.29HCY(μmol/L)13.19±5.42 12.36±3.91 -0.8530.40CK(U/L)116.64±123.68125.07±190.630.2670.79LDH(U/L)194.59±46.38 180.41±30.19 -1.8440.08WBC(×109/L)6.30±1.686.29±1.54-0.0320.98HGB(g/L)134.29±14.31 138.95±12.55 1.7090.09CRP(mg/L) 7.67±15.98 5.61±12.96-0.6710.5IL-6(U/ml) 9.05±10.4810.42±28.110.3320.74Vit D(ng/L)24.31±6.94 24.98±5.67 0.5210.60
表5中老年2型糖尿病患者認知功能障礙的Logistic分析
Table5Logisticregressionanalysisforriskfactorsassociatedwithcognitiveimpairmentinmiddleagedandelderlypatientswithtype2diabetes
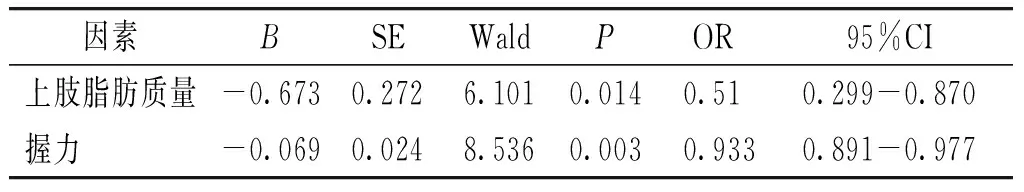
因素BSEWaldPOR95%CI上肢脂肪質量-0.6730.2726.1010.0140.510.299-0.870握力 -0.0690.0248.5360.0030.9330.891-0.977
國外研究發現[9],握力水平與65歲以上人群認知能力改變有關(語言能力、空間能力、思考速度、記憶),認為握力的下降可能與生活方式的改變相關,例如65歲以上人群因為退休等原因,其雙手工作較前減少,可能加快認知水平的下降。另外,胰島素抵抗作為認知障礙重要的危險因素,對握力也有影響,有研究[10]發現肌肉質量與胰島素抵抗指數呈負相關。具體機制可能與胰島素相對不足,抑制蛋白質分解作用減弱而導致肌纖維分解加快,數量減少,進而造成握力下降。
關于肢體肌肉脂肪含量對認知的影響,國內尚無報道,國外研究結論也不盡相同。日本一項研究發現[11],四肢肌肉質量低的男性、下肢肌肉質量低的女性認知障礙發生率高,上肢肌肉質量對認知的影響僅在男性人群體現。該研究認為男性上肢肌肉比例雖高于女性,但受到男女生活習慣不同的影響,女性每日進行烹調、清潔的工作時間多于男性,上肢肌肉運動多于男性,總體肌肉下降速度較男性慢,進而造成認知差異。另外,荷蘭的一項研究[12]發現,對于全體被研究的老年人,大腿肌肉質量多者其癡呆發生率低,但腹部皮下脂肪(非內臟脂肪)多的女性其癡呆發病率低。從胰島素抵抗角度分析,脂肪含量低肌肉含量高認知障礙的發生應越低,但與實際研究結果不完全相符,考慮其受性別影響可能性大,已有大量研究證實女性體內雌激素是認知的保護性因素[13]。但身體各部位不同的成分對認知產生不同的影響,機制還不明確。
年齡作為認知障礙另一危險因素已被廣泛認識。大量研究發現高齡患者認知障礙發病率高且病情嚴重,本研究雖也發現兩組患者年齡存在差異,但當校正其他因素后這種差異消失,可能與本研究樣本量較小有關。另外隨著年齡增長,人類進食量下降,缺少合成肌肉原料,導致肌肉數量、功能的下降。Yamada等[14]對日本糖尿病患者研究發現握力與血紅蛋白水平、身高、年齡呈正相關。Kim等[15]的隨機對照試驗通過對老年肌少癥患者進行每日增加兩次3 g亮氨酸飲食,患者肌力得到改善。以上兩項研究證實了營養與肌力的關系,而運動同樣與肌力相關,阻力訓練[16]被認為可以改善老年肌少癥患者肌肉質量及力量。營養與運動同時作為握力影響因素。通過研究握力的影響因素利于尋找改善認知功能的方法。
與其他研究結果不同,在一般資料比較時發現兩組患者血糖控制情況、血脂水平、胰島素抵抗指數不存在差異,這與多數研究相悖,分析原因如下:本研究為橫斷面研究,采用糖化血紅蛋白反映血糖控制水平,僅能反映近2-3個月血糖水平,難以體現出整個病程中血糖控制情況。若以糖化水平對患者進行分組并隨訪評估認知水平,可能會得出更合理的結果。我科住院患者大多數已存在血管病變(斑塊形成、血管狹窄),長期服用他汀類藥物者較多,通過定期監測一部分患者血脂已達標,故不能以一次血脂水平作為評價依據。同樣由于患者服用二甲雙胍,吡格列酮等改善胰島素抵抗的藥物,本研究無法解釋胰島素抵抗對患者認知及肌肉含量的影響。關于藥物因素影響,目前已有研究證實吡格列酮[17]可改善糖尿病患者的認知功能,其詳細機制尚不明確。
既往研究對糖尿病認知障礙的分析多集中在不良生活習慣、血生化指標、合并慢性病、并發癥,本研究率先在我國2型糖尿病人群中分析握力、身體成分與認知功能的關系,發現握力、上肢脂肪含量與認知功能障礙的發生明顯相關,并校正更多影響因素。提示2型糖尿病患者認知障礙還可能與肌肉功能、身體成分的改變相關,可通過運動、阻力訓練、飲食改善握力水平進而改善認知。但本研究為橫斷面研究,無法解釋認知障礙與握力下降的因果關系,且樣本量較小,無法排除其余混雜因素影響,更不能代表整體2型糖尿病人群,雖然對多個因素進行校正,仍可能遺留某些未知的變量影響觀察數據。需要進一步設計完善的大樣本的前瞻性研究去探索握力與認知障礙的關系。
綜上所述,本研究發現中老年2型糖尿病患者握力、上肢脂肪質量可能是認知障礙的危險因素,對于糖尿病患者可能通過進行握力訓練改善認知功能。
參考文獻:
[1] CuklermanT, Gersteln HC, Willamson JD,etal.Cognitive decline and dementia in diabetes: systematic overview of prospective observational studies[J]. Diabetologla,2005,48(12):2460-2469.
[2] 陶艷,于衛華,魏小飛,等.2型糖尿病住院病人認知障礙發病現況調查[J].護理研究,2013,27(10):3116-3118.
[3] Chen LK, Liu LK, Woo J,etal.Sarcopenia in Asia: consensus report of the Asian Working Group for Sarcopenia[J]. J Am Med Dir Assoc,2014,15(2):95-101.
[4] Kim TN, Choi KM. Sarcopenia: definition, epidemiology, and pathophysiology[J]. J Bone Metab, 2013, 20(1): 1-10.
[5] Kim TN, Park MS,Yang SJ,etal.Prevalence and determinant factors of sarcopenia in patients with type 2 diabetes: the Korean sarcopenia Obesity Study(KSOS)[J].Diabetes Care,2010,33(7):1497-1499.
[6] Taekema DG,Ling CHY, Kurrle SE,etal. Temporal relationship between handgrip strength and cognitive performance in oldest old people[J].Age Aging,2012,41(4):506-12.
[7] 溫洪波,張振馨,牛富生,等.北京地區蒙特利爾認知量表的應用研究[J].中華內科雜志,2008,47(1):36-39.
[8] Fess EE.Clinical Assessment Recommendations[M]. 2nd ed.Chicago: American Society of Hand Therapists, 1992: 41-45.
[9] SternangO, Reynolds CA, Finkel D,etal. Grip strength and cognitive abilities:Association in old age[J].J Gerontol B Psychol Sci Soc Sci,2016,71(5):841-848.
[10] Bijlsma AY,Meskers CG,van Heemst D,etal. Diagnostic criteria for sarcopenia relate differently to insulin resistance[J].Age (Dordr),2013,35(6):2367-2375.
[11] Bae S, Shimada H, Park H,etal. Association between body composition parameters and risk of mild cognitive impairment in older Japanese adults[J].Geriatr Gerontol Int,2017,17(11):2053-2059.
[12] Spauwen PJ,Murphy RA,Jonsson PV,etal. Associations of fat and muscle tissue with cognitive status in older adults:the AGES-Reykjavik Study[J]. Age Ageing,2017, 46(2): 250-257.
[13] 徐潔.雌激素對女性認知功能的影響[J].國際婦產科學雜志,2012,39(2):112-114.
[14] Yamada E,Takeuchi M,Kurata M,etal. Low hemoglobin levels contribute to low grip strength independent of low-grade inflammation in Japanese elderly women[J]. Asia Pac J Clin Nutr,2015,24(3):444-451.
[15] Kim HK,Suzuki T,Saito K,etal.Effects of exercise and amino acid supplementation on body composition and physical function in community-dwelling elderly Japanese sarcopenic women: a randomized controlled trial[J]. J Am Geriatr Soc,2012,60(1):16-23.
[16] Liu CJ, Latham NK. Progressive resistance strength training for improving physical function in older adults[J]. Cochrane Database Systematic Reviews(online),2009;3(3):CD002759.
[17] 于海燕,王群松,張梓威,等.吡格列酮治療2型糖尿病輕度認知功能障礙患者的臨床療效[J].中國老年學雜志,2017,37(17):4224-4226.

