紫外照射下氧氟沙星在蒙脫石懸浮液中的去除研究
黃曉丹,饒艷英,吳丹丹,賴貴滿,陳國平
(1.莆田學院 環境與生物工程學院,福建 莆田351100;2.福建省新型污染物生態毒理效應與控制重點實驗室,福建 莆田351100)
氟喹諾酮類抗生素是廣譜抗菌藥,具有易于口服的優點,因而在臨床醫學、水產養殖以及畜禽疾病防治等方面得到了廣泛應用[1].但氟喹諾酮類抗生素通常在生物體內大約只有20%~80%會代謝和降解,剩余藥物將會隨尿液和糞便排出體外,進入環境[2].近年來,國內外均報道了在城市污水[3]、自然水體[4-5]、水體沉積物[6-7]以及土壤[8]中發現氟喹諾酮類抗生素.而氟喹諾酮類抗生素在環境中的滯留和積累將導致環境中生物的耐藥性增強,加大環境風險.傳統的生物污水處理工藝無法有效地去除氟喹諾酮類抗生素,因此研究安全有效地去除水體中氟喹諾酮類抗生素技術具有重要意義.
蒙脫石(KSF)是層狀硅酸鹽粘土礦物,是土壤粘土的主要成分之一,也是大氣、水體中漂浮顆粒物和沉積物的重要組成,在自然界里廣泛存在.由于特殊的物化結構,具有較高的離子交換容量和吸水膨脹能力,蒙脫石作為一種環境友好型礦物材料在環境污染治理中得到了廣泛應用[9-10].本實驗以氧氟沙星(OFLX)作為氟喹諾酮類抗生素代表,研究其在紫外光照下蒙脫石懸濁液中的去除情況及其影響因素.
1 材料與方法
1.1 主要儀器及試劑
電子天平(Cp213,上海奧斯),紫外分光光度計(UVmini-1240,島津)、酸度計(pHS-2S,上海偉業),254 nm紫外燈(北京博朗特),離心機(TDL80-2B,上海安亭).
KSF、OFLX(98%)購自上海晶純有限公司,30%H2O2、NaOH、NCl、C3H8O 等所有試劑均為分析純,實驗用水為純水.
1.2 實驗方法
配制一定濃度的OFLX與KSF的混合溶液,調整實驗所需參數,以24 W主波長254 nm紫外燈作為光源進行照射反應,間隔30 min取樣,所取樣品在4 000 r·min-1的離心機中離心30 min后取上清液過0.45 μm濾膜后,用UVmini-1240紫外分光光度計于OFLX的最大吸收波長296 nm處測其吸光度,而后進行去除率計算.
OFLX的去除率計算如下:
去除率=[(C0-Ct)/C0]×100%.
式中:C0—OFLX初始濃度,單位mg/L;Ct—反應t時刻時OFLX濃度,單位mg/L.
2 結果與分析
2.1 對照試驗
在OFLX=20 mg/L,KSF=0.1 g/L,H2O2=8 mL/L,pH=7.0,紫外光照為24 W的實驗條件下進行了系列對照試驗.實驗結果如圖1所示.UV/KSF/H2O2體系中OFLX的降解率最大,達到84.6%.其它體系如單獨UV、單獨KSF、UV/H2O2、UV/KSF、KSF/H2O2對 OFLX的降解率均不如 UV/KSF/H2O2體系.蒙脫石 KSF對OFLX有一定的吸附去除作用,反應240 min后,OFLX吸附去除率達44.3%.單獨UV照射對OFLX去除率只有7.3%,UV/H2O2體系對OFLX去除率也只有25.8%.UV/KSF/H2O2體系對OFLX的去除率高于體系中各因素的單獨作用之和,由此可見各因素之間存在著一定的協同作用.
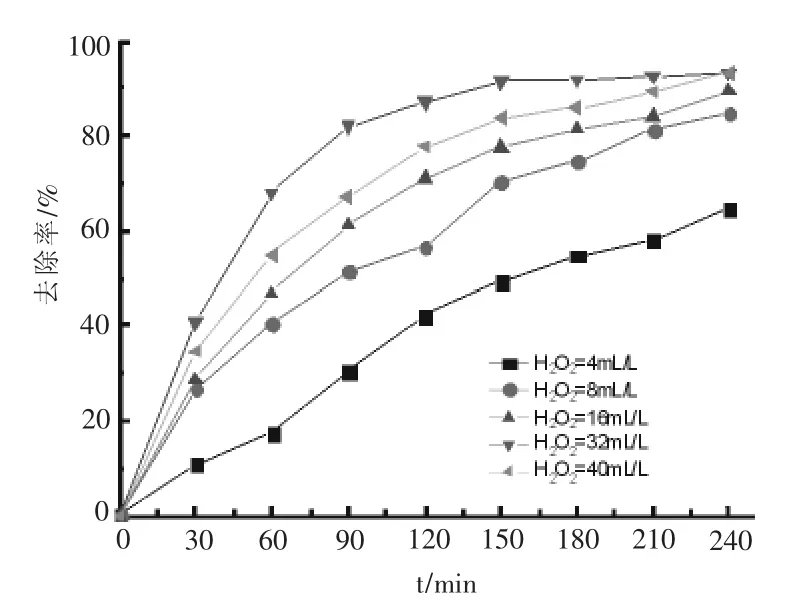
圖1 OFLX在不同體系中的去除效果
2.2 H2O2的影響
在OFLX=20 mg/L,KSF=0.1 g/L,pH=7.0,紫外光照為24 W的實驗條件下考察H2O2投加量影響,實驗結果如圖2所示.起初隨著H2O2投加量增加,OFLX去除率隨之顯著提高,當H2O2投加量從4 mL/L增加到8 mL/L時,OFLX去除率從64.6%增大到84.6%.但隨著H2O2投加量進一步增加,H2O2投加量從8 mL/L增加到40 mL/L時,OFLX去除率只是略有提高,從84.6%增加到93.4%.H2O2在紫外照射和蒙脫石KSF中鐵成分[11-13]催化下均會產生強氧化性的OH·自由基.OH·自由基可氧化降解OFLX,但過量的H2O2反而會猝滅體系中的OH·自由基,從而使體系對OFLX的去除率難以進一步提高.
2.3 KSF的影響
在OFLX=20 mg/L,H2O2=8 mL/L,pH=7.0,紫外光照為24 W的實驗條件下考察KSF投加量影響,實驗結果如圖3所示.隨著KSF投加量逐漸增加,OFLX去除率先升高而后下降.當KSF投加量從0.02 g/L增加到0.1 g/L時,OFLX去除率從32.6%增加到84.6%,而后進一步提高KSF投加量到0.5 g/L,OFLX去除率反而下降為32.5%.KSF能吸附一定量的OFLX,同時由于KSF含有微量鐵[9-10],可以催化H2O2產生OH·自由基,因而一定范圍內KSF投加量增加可以使OFLX去除率隨之提高.但當KSF濃度過高,一方面降低了溶液的透明度,影響體系對紫外光的利用效率,另一方面高濃度的KSF在溶液中容易發生團聚,也進一步降低了OFLX的去除率.

圖3 KSF投加量對OFLX去除率的影響

圖4 溶液pH值對OFLX去除率的影響
2.4 溶液pH值的影響
在OFLX=20 mg/L,H2O2=32 mL/L,KSF=0.1 g/L,紫外光照為24 W的實驗條件下考察溶液pH的影響,實驗結果如圖4所示.在溶液初始pH值為3.0、5.0和7.0時,OFLX去除率分別為88.9%、90.1%和93.1%.但隨著溶液初始pH值進一步增加,從9.0到11.0,OFLX去除率隨著pH值的增加而減小,從85.6%降低到67.1%.究其原因,強氧化性的OH·自由基是體系去除OFLX的主要氧化劑,而在堿性條件下OH·自由基會被氫氧根猝滅,因而堿性條件下OFLX的去除率下降.同時,KSF表面一般呈負電狀態,在pH3.0~7.0區間,OFLX分子呈質子化狀態帶正電[14],電性引力可提高KSF吸附能力,而在pH9.0~11.0區間,OFLX分子去質子化帶負電[14],電性相斥也降低了KSF對OFLX的吸附能力.因此,UV/KSF/H2O2體系對OFLX的去除可在中性條件下進行.
2.5 OFLX去除反應動力學分析
在H2O2=32 mL/L,KSF=0.1 g/L,pH=7.0,紫外光照為24 W的實驗條件下考察不同OFLX初始濃度在UV/KSF/H2O2體系的去除,實驗結果如圖5所示.隨著OFLX的濃度升高,OFLX去除率下降,但去除的OFLX絕對數量是不斷增加的.對不同OFLX初始濃度的去除反應進行一級和二級動力學分析,分析結果如表1所示.
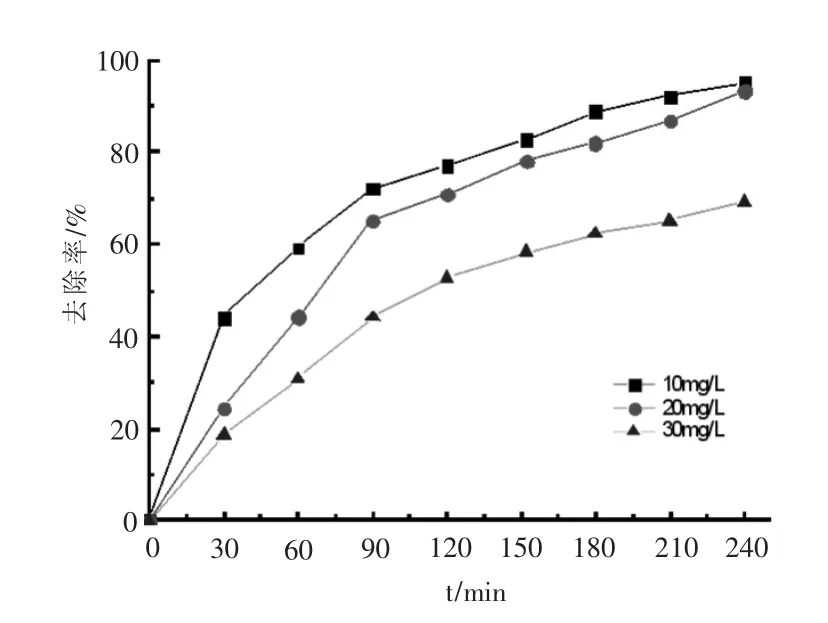
圖 5 不同初始濃度OFLX在UV/KSF/H2O2中的去除

表1 OFLX的去除反應動力學分析
從表1可以看出,UV/KSF/H2O2體系對OFLX去除反應的二級動力學方程擬合相關系數R2均在0.98以上,比一級動力學方程擬合相關系數更高,因此UV/KSF/H2O2體系對OFLX去除反應可用二級動力學方程來描述.
2.6 OFLX去除機制研究
在UV/KSF/H2O2體系中,OFLX的去除應該主要通過兩種途徑,一種是KSF的吸附作用,還有一種是體系中產生的氧化性OH·自由基對OFLX的降解作用.為了驗證假設,在OFLX=20 mg/L,H2O2=32 mL/L,KSF=0.1 g/L,pH=7.0,紫外光照為24 W的實驗條件下,加入一定量的異丙醇猝滅溶液中的OH·自由基,考察此時的OFLX去除率,實驗結果如圖6所示.
從圖6可以看出,體系中加入5 mL異丙醇之后,OFLX的去除率劇烈下降,從原來的93.4%下降到49.7%.進一步提高異丙醇的投加量到20 mL,OFLX的去除率進一步下降到41.7%,由此可見,體系中OH·自由基對OFLX的氧化是主要去除途徑之一.而體系剩余的去除作用則是由KSF吸附貢獻.因此,OFLX在UV/KSF/H2O2體系中的去除由氧化去除和吸附去除共同完成.

圖6 異丙醇投加量對OFLX去除率的影響
3 結論
OFLX在UV/KSF/H2O2體系中可以有效地被去除.KSF和H2O2有最優投加量.當溶液pH值為7.0,KSF投加量為0.1 g/L,H2O2投加量為32 mL/L,OFLX去除率達最大值93.4%.在溶液pH值3.0~7.0范圍內,OFLX去除率均在85%以上,進一步提高溶液pH值,去除效率則大幅下降.二級反應動力學可較好地描述OFLX在UV/KSF/H2O2體系中的去除反應.OFLX在UV/KSF/H2O2的去除有兩種途徑,一種是OH·自由基的氧化去除,另一種是KSF的吸附去除.

