農桿菌介導的胡麻轉化因子的優化
李淑潔,羅俊杰,林玉紅,裴懷弟,李聞娟
(1.甘肅省農業科學院 生物技術研究所,蘭州 730070;2.甘肅省農業科學院 作物研究所,蘭州 730070)
農桿菌介導的轉基因技術因具有轉化機理清楚、整合外源基因拷貝數低、整合位點穩定、外源基因表達和遺傳穩定性好、操作簡單、所需儀器少和試驗成本低而成為目前最有效的基因轉化方法之一[1]。該技術轉化率主要受多個轉化因子,諸如受體系統中的再生體系、選擇劑及篩選濃度、農桿菌轉化系統中的菌株、表達載體、侵染菌液濃度及時間等影響。
胡麻(LinumusitatissimumL.)即油用亞麻,是亞麻科亞麻屬1 a生草本植物,其種子富含α -亞麻酸和木酚素,是具有重要營養價值和保健功能的油料作物。因其植株小、生育期短、自花授粉,種子繁殖、種子小且量大、基因組小(2n=30,約700 Mb)等特點成為麻類作物功能基因組學研究的代表作物[2]。轉基因技術是研究基因功能及作物改良的重要技術,因此,胡麻轉基因技術體系的建立對于研究其功能基因組學和遺傳改良具有重要意義。
亞麻轉基因研究主要采用外源DNA導入法和農桿菌介導法。其中農桿菌介導的胡麻轉基因研究始于1983年Hepburm等[3]用根癌農桿菌侵染亞麻上胚軸得到亞麻腫瘤株系,表明亞麻是易于被農桿菌侵染轉化的。之后,優化轉化體系、提高轉化效率一直是國內外的一個研究熱點,并對外植體[4-5]、培養基成份[2,6-8]、篩選基因的選擇[5,9-12]等開展了大量工作。本研究以甘肅省主推胡麻品種‘定亞22號’和‘隴亞10號’為受體,在已報道的國內外亞麻(包括纖維用亞麻和油用亞麻)遺傳轉化體系基礎上,選取一些還未達成一致的轉化因子參數進行優化,如草銨膦選擇壓、下胚軸的是否剝表皮處理、預培養時間、高效農桿菌菌株的篩選和侵染時間等,以期建立高效、穩定的胡麻轉化系統,為后續的胡麻功能基因組學研究和遺傳改良奠定基礎。
同時本研究中以gus表達率或表達頻率、抗性苗分化率作為衡量遺傳轉化率的代換指標,其相關性高、檢測方便,在轉化初期和中期都能快速統計分析,便于參數優化,快速建立高效穩定的遺傳轉化體系。
1 材料與方法
1.1 材料及受體準備
基因轉化受體‘隴亞10號’和‘定亞22’為油用亞麻品種。胡麻種子用流水沖洗30 min,φ=75%乙醇快速殺菌30 s,φ=2% NaClO浸泡12 min,無菌水沖洗3~5次,接種于1/2 MS培養基。20 ℃黑暗培養3 d后轉移至光照條件下,16 h/d 光周期培養。剪取6~7 d苗齡的無菌苗下胚軸(長度約0.5~1 cm)作為外植體。
農桿菌菌株和質粒:農桿菌菌株AGL1、C58c1、EHA105、GV3101和LBA4404, pCAMBIA3301質粒T-DNA區帶有CaMV35S啟動子驅動的gusA報告基因和bar選擇標記基因(圖1)。
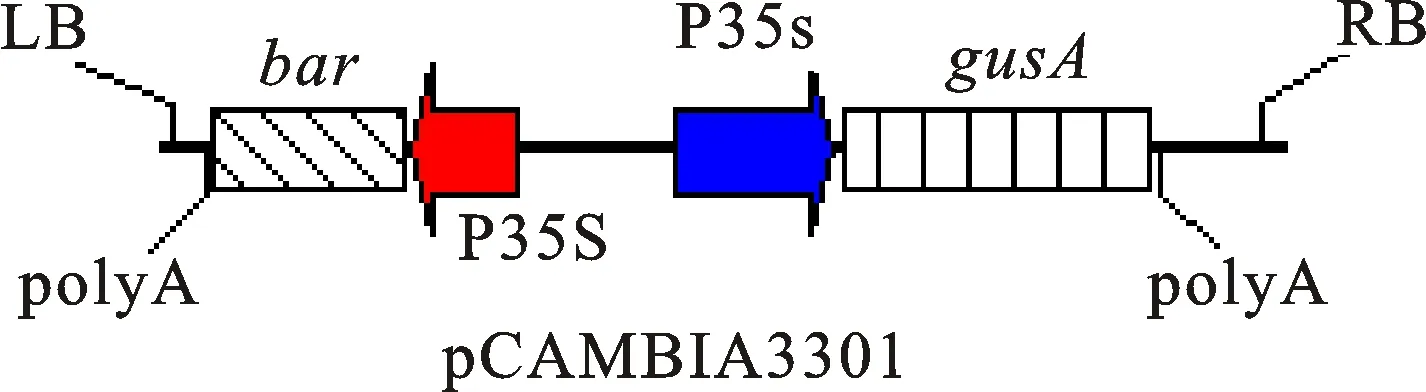
圖1 pCAMBIA3301植物表達載體結構簡圖Fig.1 General frame of plasmid pCAMBIA3301
1.2 農桿菌菌液的制備及侵染
侵染菌液的制備:將pCAMBIA3301植物表達載體分別轉化農桿菌菌株AGL1、C58c1、EHA105、GV3101和LBA4404,并挑取單菌落接種于含有利福平(rif)、鏈霉素(str)和卡那霉素(kan)各50 mg/L 的YEP液體培養基中,28 ℃、220 r/min 振蕩培養24 h左右。然后取2 mL菌液加入到50 mL YEP液體培養基進行擴大培養,待菌液的濃度達到OD600=0.5~0.6 后,4 ℃、5 000 r/min 離心5 min收集菌體。將菌體重懸于1/2 MS液體培養基(pH = 5.4)至OD600=0.5~0.6 備用。
農桿菌侵染轉化程序:下胚軸接種于愈傷誘導分化培養基(MS + 6-BA 1.0 mg/L + NAA 0.1 mg/L,pH 5.8),26/22℃(日/夜)、16/8 h(光/暗)預培養3 d后,用制備好的菌液侵染10 min,侵染結束后用無菌濾紙吸干多余菌液,接種于共培養基(同愈傷誘導分化培養基),25 ℃黑暗培養3 d。
1.3 各轉化因子的優化
1.3.1 草銨膦(PPT)臨界選擇壓 分別進行了愈傷組織誘導、分化苗伸長生長和生根階段草銨膦臨界選擇壓篩選,每個階段設PPT 0 mg/L、2 mg/L(僅限生根階段有)、5 mg/L、10 mg/L、20 mg/L和40 mg/L處理,統計愈傷組織誘導率、分化率、白化苗率、生根率,篩選出不同階段的草銨膦臨界選擇壓。每個處理設3次重復,下同。
1.3.2 外植體預處理 下胚軸分2種預處理:用解剖刀輕輕剝去約30%表皮,對照為不剝表皮處理;預培養設0 d和3 d。預處理后程序同“1.2”中農桿菌侵染轉化程序。
1.3.3 農桿菌侵染和共培養 不同菌株侵染處理:以預培養3 d的下胚軸為受體,分別用攜帶有目標質粒的AGL1、C58c1、EHA105、GV3101和LBA4404侵染10 min。共培養程序同“1.2”所述。
侵染時間處理:以農桿菌C58c1侵染15 min、30 min和60 min,分別統計不同侵染時間對gus表達和抗性苗分化的影響。
1.3.4 乙酰丁香酮(AS) AS處理:將預培養3 d的下胚軸分別用上述的5種菌株侵染10 min,侵染結束后共培養于含100 μmol/L AS的共培養基,以不含AS為對照,25 ℃黑暗培養3 d。分析AS對gus表達率或表達頻率及抗性苗分化率的影響。
1.4 轉化體的篩選及抗性植株再生
共培養結束后下胚軸在含有羧芐青霉素(Carb)350 mg/L及PPT 5~10 mg/L的篩選培養基上培養3~7 周。分化出的抗性苗移至含有PPT 2 mg/L的生根篩選培養基(1/2 MS + 3%蔗糖+瓊脂粉0.5%+ Carb 200 mg/L,pH 5.8) 誘導生根。
1.5 轉化體的gus染色檢測
參照王關林等[13]組織化學染色法檢測培養30 d后抗性愈傷組織和抗性植株中gus表達率和表達頻率。
gus表達率=gus染色陽性外植體數/總檢測外植體數×100%
gus表達頻率=檢測外植體中gus染色陽性總點數/總檢測外植體數
抗性苗率=抗性苗數/接種外植體數×100%
1.6 數據分析
利用Microsoft Excel 2003繪圖,并用SPSS 17.0進行數據的顯著性分析。
2 結果與分析
2.1 草銨膦(PPT)臨界選擇壓的確定
如表1所示,在愈傷組織誘導和分化階段,添加草銨膦致使愈傷組織誘導受到很大的抑制,草銨膦質量濃度為5 mg/L時愈傷組織誘導率為45.5%、分化率為0;10 mg/L時愈傷組織誘導率為4.16%、分化率仍為0;質量濃度為20和40 mg/L時愈傷組織誘導率和分化率均為0,因此胡麻愈傷組織誘導階段草銨膦的篩選質量濃度為10 mg/L,愈傷組織分化階段草銨膦的篩選質量濃度為5 mg/L。
胡麻分化苗伸長生長和生根階段,只有不添加草銨膦的培養基上分化苗才能正常生長和生根(生根率98.5%),因此分化苗伸長生長和生根階段草銨膦的篩選質量濃度為2 mg/L。

表1 草銨膦臨界選擇壓的篩選Table 1 Appropriate mass concentration selection of phosphinothricin
2.2 受體預處理
根據下胚軸剝表皮預處理的gus表達率和抗性苗率(圖2)得出,下胚軸剝表皮處理顯著影響抗性分化苗率,其抗性苗率是未剝表皮細胞處理的20%。剝表皮處理對gus表達率的影響未達到統計學的顯著水平,是未剝表皮細胞處理的54.6%,所以以下胚軸為受體的胡麻遺傳轉化中不宜對外植體進行去表皮處理。
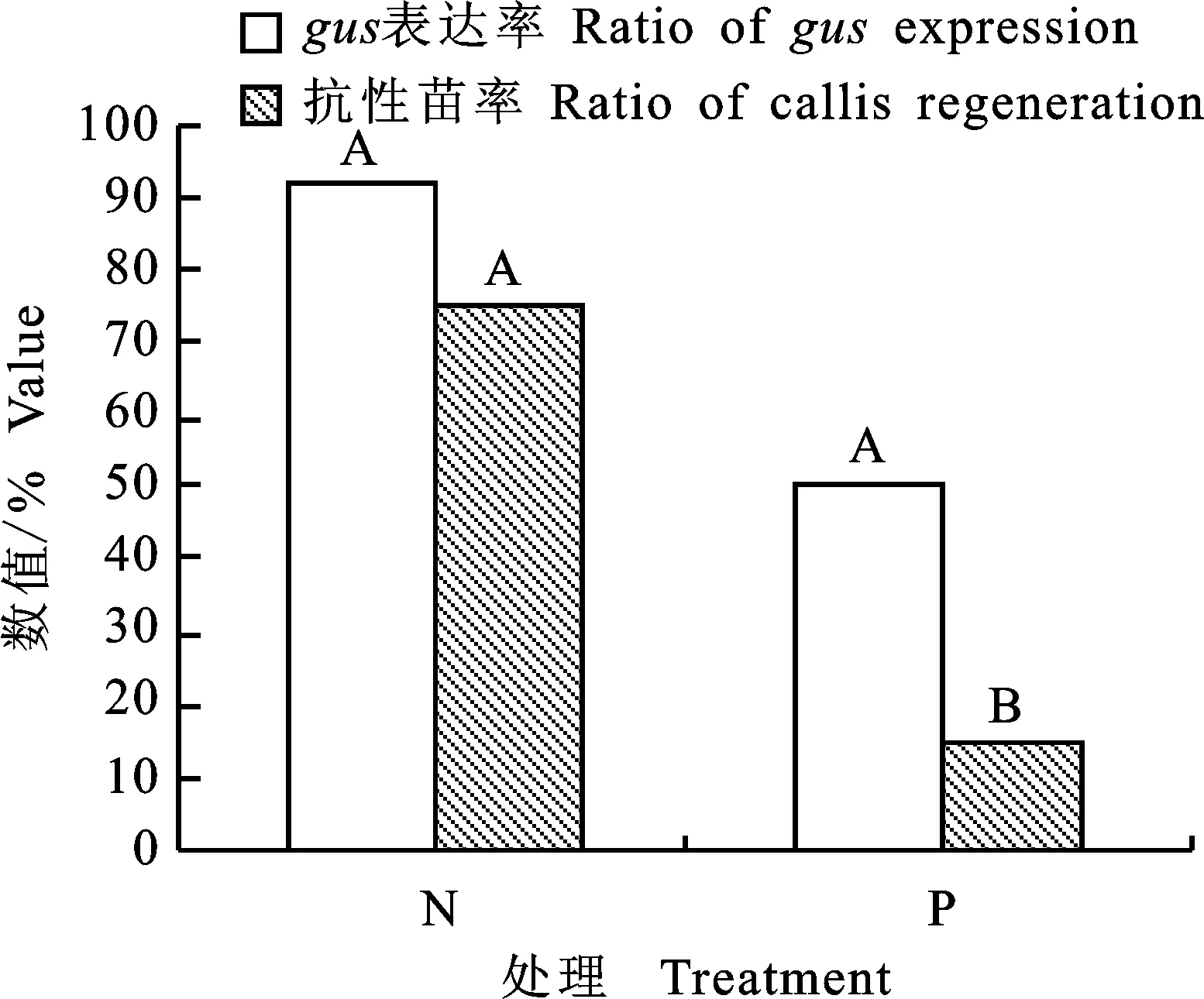
N.未做剝表皮處理的下胚軸 Common hypocotyl; P.剝表皮處理的下胚軸 Hypocotyl that removal of partial epidermal cell;圖中不同大寫字母表示P<0.01水平差異顯著 Different capital letters indicate significant difference at level 0.01;下同 The same below
圖2下胚軸剝表皮處理的gus表達率和抗性苗率
Fig.2Ratioofgusexpressionandcallisregenerationafterremovingepidermalcell
預培養0 d和3 d的下胚軸侵染30 d后轉化愈傷組織gus染色檢測都呈藍色,預培養3 d的愈傷組織gus表達頻率高于0 d處理,但不存在顯著差異(圖3)。
預培養時間對抗性苗率影響極顯著。不同的外植體經農桿菌介導轉化后誘導的愈傷組織質量和愈傷組織分化率有很大差異,抗性苗率存在極顯著差異。預培養0 d處理的愈傷組織表面光滑、堅硬、不易分散,易玻璃化,分化率很低;而預培養3 d處理的胚性愈傷組織率高,愈傷組織表面呈許多小顆粒密集狀,易分散,分化率很高。預培養3 d處理抗性苗率達60.3%,而0 d抗性苗率僅為5.2%(圖3)。由此得出,下胚軸預培養3 d 對于獲得高轉化率至關重要。

圖3 預培養0 d和3 d的gus表達頻率和抗性苗率Fig.3 Frequency of gus expression and ratio of callis regeneration at different preculture time
2.3 農桿菌菌株及侵染時間
分別用攜帶有pCAMBIA3301質粒的AGL1、C58c1、EHA105、GV3101和LBA4404侵染胡麻下胚軸,相同轉化條件下,侵染30 d后gus表達率都高達80%~100%,但各菌株侵染后愈傷組織的分化率差異很大,抗性苗率存在極顯著差異。其中 C58c1侵染后分化的抗性苗最多,達73株,抗性苗率高達280.77%,其次為LBA4404和GV3101,分別為13(抗性苗率44.83%)和11株(抗性苗率40.74%),AGL1和 EHA105抗性苗低于10%(圖4),因此確定C58c1作為后續胡麻遺傳轉化中的侵染菌株。
研究以OD600=0.5~0.6作為侵染濃度,侵染時間設15、30和60 min 3個處理。侵染30 d后各處理gus表達率均為100%,抗性苗率無顯著差異,但處理間gus表達頻率存在極顯著差異,侵染60 min時gus表達頻率最高,為7.5,其抗性苗率為60.3%(圖5),因此將60 min作為最佳侵染時間。
2.4 乙酰丁香酮(AS)
在胡麻下胚軸的遺傳轉化中,添加AS后顯著提高了C58c1和GV3101侵染gus表達頻率(圖6),添加AS處理的gus表達頻率分別是不添加處理的16倍和10倍。
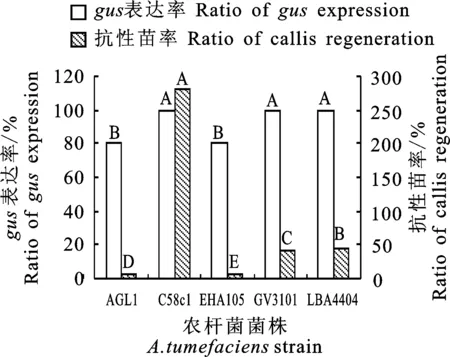
圖4 不同侵染菌株的gus表達率和抗性苗率 Fig.4 Ratio of gus expression and callis regeneration mediated by different A.tumefaciens strains
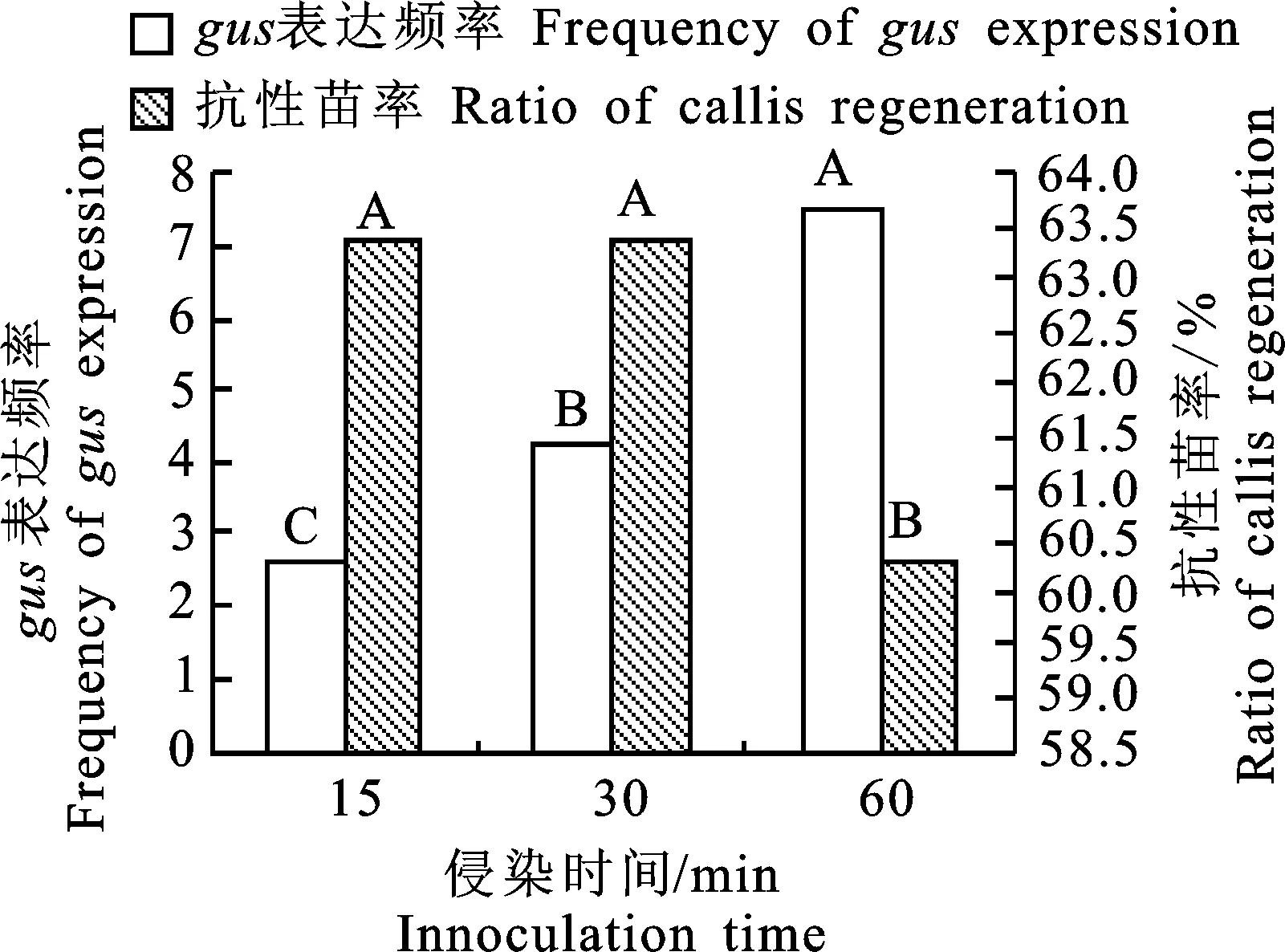
圖5 不同侵染時間的gus表達頻率和抗性苗率Fig.5 Frequency of gus expression and ratio of callis regeneration at different innoculation time

圖6 共培養階段使用AS時不同轉化菌株的gus表達頻率Fig.6 Frequency of gus expression when AS is added in co-culture media
2.5 轉化植株的gus染色檢測
將抗性愈傷組織進行不定芽分化和生根培養(圖7),并對抗性苗的莖、根和葉分別進行gus染色檢測,如圖8所示,轉化愈傷組織和轉化植株的莖、根和葉中都檢測到了gus基因的表達,說明外源基因在胡麻中成功轉化并表達。
3 討 論
根癌農桿菌只有在植物創傷部位生存16 h后才能誘發“腫瘤”,才能進行T-DNA的轉移。因此,制造外植體創傷是實現農桿菌介導轉化成功的必要條件,考慮到下胚軸只有前后端兩個切口,而亞麻下胚軸再生體系中90%以上不定芽的分化部位位于兩切口之間的胚軸上,所以Vrbová等[14-15]在農桿菌侵染前將下胚軸剝去50%~60%表皮細胞或用200 mg/L的纖維素酶預處理下胚軸,轉化率分別提高了11.75%和1.6倍。本研究參考Vrbová 等[14-15]方法,將下胚軸剝去約30%表皮細胞以制造機械損傷,但去表皮后抗性苗分化率顯著下降,抗性苗分化率是未剝表皮細胞處理的20%,gus表達率下降,是未剝表皮細胞處理的54.6%,推測同樣處理得到相反結論的主要原因在于受體材料的不同,雖然同是亞麻下胚軸,但Vrbová等[14-15]所用的基因型為纖維用亞麻,纖維用亞麻表皮富含纖維素,農桿菌不易滲入,所以提高了剝去部分表皮后轉化率。而本試驗所用的‘隴亞10號’和‘定亞22號’都是油用亞麻品種,其表皮層薄,纖維素含量低,剝表皮對下胚軸造成了較大創傷,使不定芽分化率下降,抗性苗數量也急劇下降。
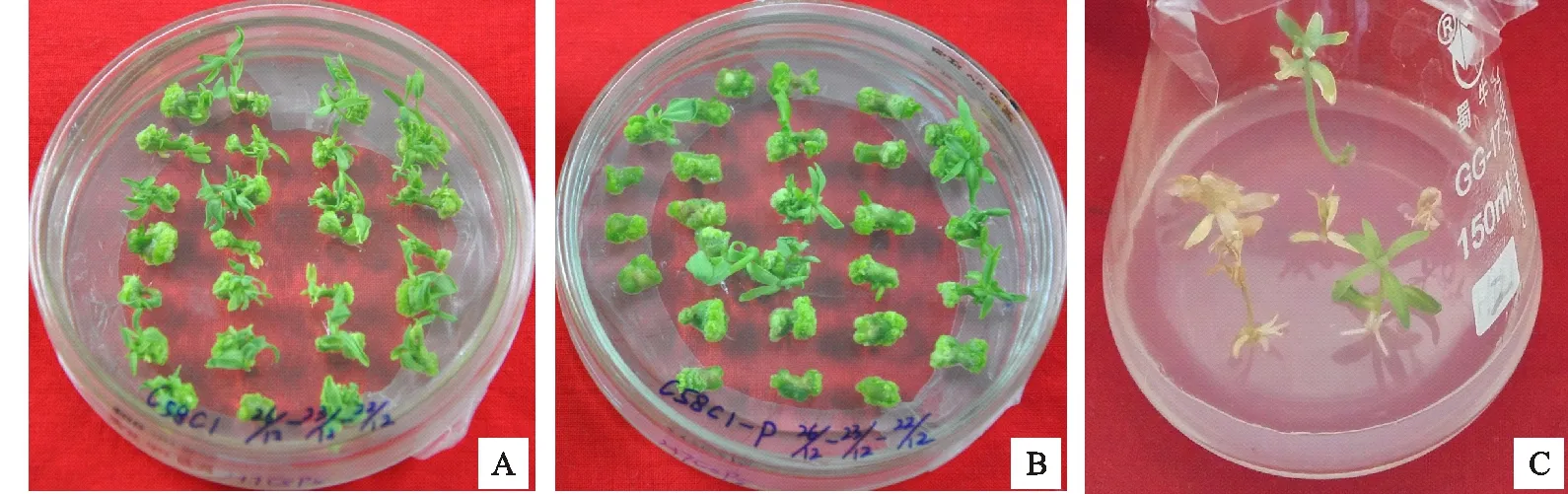
A.轉化受體為未剝表皮處理的下胚軸愈傷組織分化 Regeneration of transgenic callis induced by hypocotyl inoculation withA.tumefaciensC58c1;B.轉化受體為剝部分表皮處理的下胚軸愈傷組織分化 Regeneration of transgenic callis induced by removing hypocotyl partial epidermal cell;C.轉化植株生根 Rooting of transgenic plants
圖7抗性愈傷組織分化及轉化植株生根
Fig.7Regenerationoftransgeniccallisandrootingoftransgenicplants
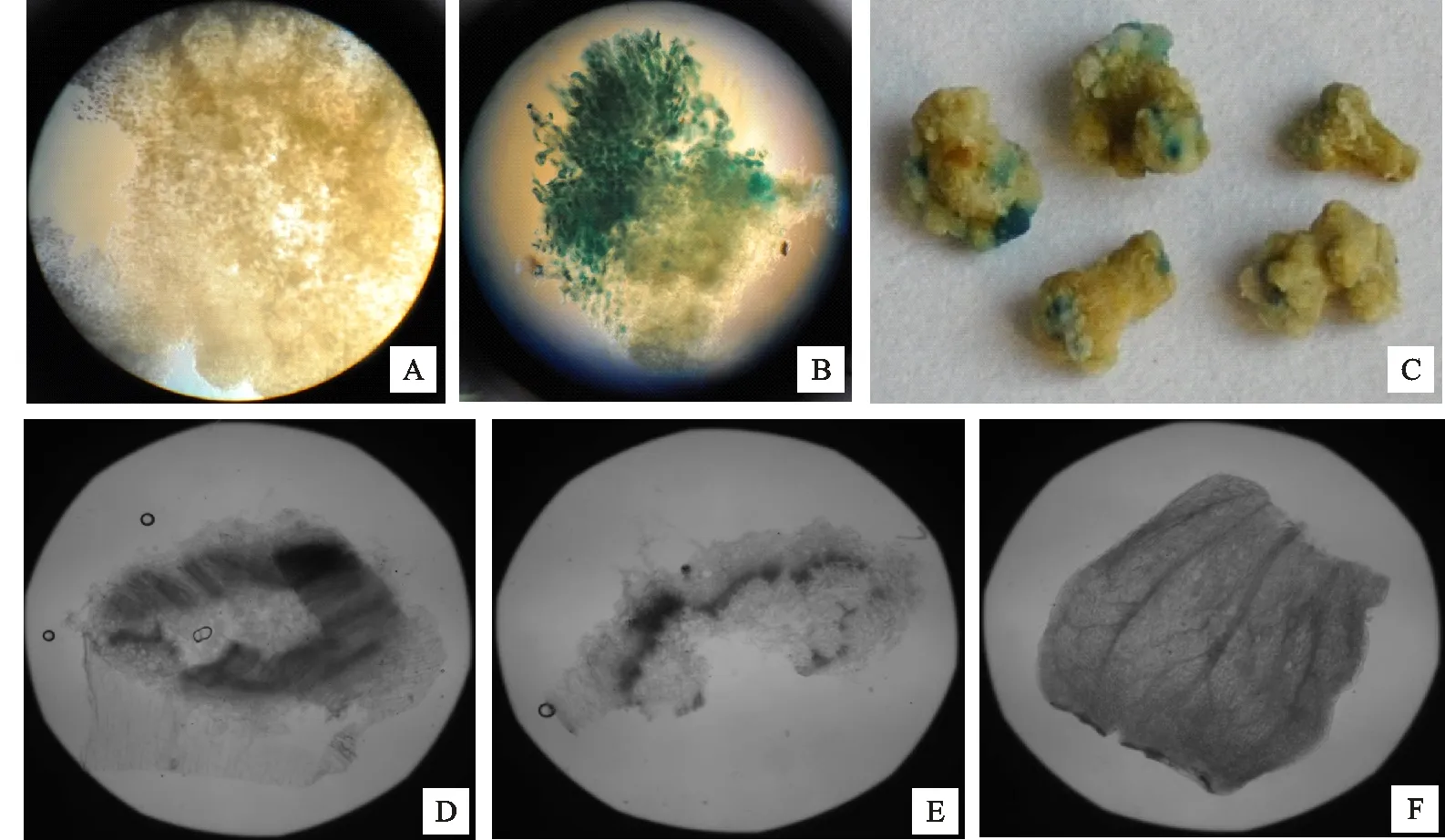
A.CK Control(Non-transgenic plant);B、C.轉化愈傷 Transgenic callis;D.轉化株莖 Stem of transgenic plant;E.轉化株根部 Root of transgenic plant;F.轉化株葉片 Leaf of transgenic plant
圖8轉化材料的gus活性檢測
Fig.8gusexpressionintransgenicflax
農桿菌菌株與表達載體的組合共同影響T- DNA的轉移效率。有研究指出,即使是同一農桿菌菌株介導的遺傳轉化,表達載體不同,轉化效率也有差異[16]。本研究中將同一表達載體與不同的農桿菌菌株組合,篩選與pCAMBIA3301表達載體組合的高轉化率農桿菌菌株。本試驗中采用的5種農桿菌菌株來自于3類不同的農桿菌菌系,菌株對植物的侵染能力由該菌株農桿菌染色體基因的調控、農桿菌中的Ti質粒和vir基因的活化能力等因素決定。C58c1菌株為胭脂堿型,其染色體背景為C58,具有生長速度快,轉化實驗中易操作等特點。Wróbel等[17]曾用C58c1:pGV2260組合將PHB合成基因導入亞麻,此外,該菌株在小麥、大麥遺傳轉化中被廣泛使用。AGL1和EHA105為農桿堿型,是具有超強侵染力的菌株,在單子葉植物、尤其是AGL1在禾本科作物的轉基因研究中應用較多,但在本實驗中,這2個菌株侵染的愈傷組織的分化率低。LBA4404屬于章魚堿型,普遍用于雙子葉植物和部分單子葉植物的遺傳轉化中,是植物轉基因中運用最廣泛的菌株,Shisha等[18]曾利用LBA4404:pBI121組合將GFP-TUA6 基因成功導入白俄羅斯和烏克蘭的纖維用亞麻品種。本研究中LBA4404侵染后抗性苗率為44.83%,是胡麻下胚軸轉化體系中僅次于C58c1的又一高轉化率菌株。
農桿菌侵染強度是侵染菌液濃度、侵染時間和共培養3個綜合因子的組合,對遺傳轉化效率至關重要。Gurlitz 等[19]認為,植物細胞有一個可承受的農桿菌侵染強度的閾值,超過該閾值,植物遺傳轉化率下降。增加侵染菌液濃度、延長侵染時間或共培養時間都可加大農桿菌侵染強度。因此,本研究在固定侵染濃度和共培養時間的基礎上探索適宜的侵染時間和乙酰丁香酮對轉化率的影響,通過比較gus表達率/表達頻率和抗性苗率篩選出了C58c1介導胡麻下胚軸遺傳轉化的侵染強度,這與周蘊薇等[20]在農桿菌介導的地被菊遺傳轉化體系研究中的分析方法一致。
4 結 論
胡麻轉化因子中的草銨膦選擇濃度、下胚軸預處理、農桿菌菌株、侵染時間,以及乙酰丁香酮都影響著胡麻的遺傳轉化效率。經過對上述各轉化影響因子的參數優化篩選,說明胡麻下胚軸再生的不同階段對草銨膦的敏感性不同,愈傷組織誘導、分化和再生苗生根階段草銨膦選擇壓分別是10 mg/L、5 mg/L和2 mg/L;對胡麻下胚軸進行去表皮預處理和預培養都顯著影響抗性苗分化率,對gus表達率無顯著影響;農桿菌菌株和侵染時間同時影響gus表達率/頻率和抗性苗率:AGL1、C58c1、EHA105、GV3101和LBA4404 5個菌株中C58c1為最優侵染菌株,侵染60 min時gus表達頻率最高,在共培養階段添加100 μmol/L乙酰丁香酮能顯著提高轉化愈傷組織的gus表達頻率。

