快速協同濁點萃取-熒光分光光度法 測定5種食品塑料包裝材料中的浸出苯酚
羅幸玲,鄭 涵,洪佳佳,王 梅,周之榮
(廣東藥科大學公共衛生學院,廣東廣州 510310)
近年來,塑料由于具有良好的性能和低成本被廣泛用作食品包裝材料,但其使用安全性問題也成為研究熱點[1-2]。苯酚作為塑料制作的化工原料之一,具有高毒性,因此苯酚的浸出所帶來的安全性問題不容忽視[3-4]。食品包裝材料的原材料種類多,基質復雜,且苯酚的浸出量常在痕量水平,這為苯酚的測定帶來了一定的困難。因此,盡管現有儀器分析方法具有較高的靈敏度,在上機檢測前仍需對樣品進行凈化、分離、富集處理。
快速協同濁點萃取(Rapid synergistic cloud point extraction,RS-CPE)是在傳統濁點萃取基礎上,通過加入濁點的誘導協同劑,室溫下即可完成萃取的一種快速有效分離富集方法。該方法既保留了傳統濁點萃取成本低、綠色環保、萃取效果好、易與多種分析儀器聯用等優點,又省去了耗時較長的水浴過程,前處理更為簡單、省時。誘導協同劑還可輔助表面活性劑萃取目標物,提高萃取率。RS-CPE最早由Wen在2011年提出,與分光光度法聯用測定食品和水樣中痕量銅[5]。目前,RS-CPE已與原子吸收光譜、電感耦合等離子體發射光譜法等結合用于各種金屬離子的測定[6-9],尚未見RS-CPE應用于苯酚分離富集的報道。熒光分光光度法作為測定苯酚常用的分析手段,具有儀器操作簡單、運行成本低、抗干擾能力強、靈敏度高(通常比紫外分光光度法高2~3個數量級)等優點。且經RS-CPE所得的富集相可直接轉移至比色皿中進行檢測,省去了稀釋過濾步驟,進一步簡化了實驗操作。因此,熒光分光光度法與RS-CPE聯用用于苯酚測定是較優的選擇。然而目前已報道的RS-CPE法中,選用的表面活性劑為Triton X系列,含有苯環結構,會對用熒光分光光度法測定苯酚帶來較大的熒光干擾信號。在現有的CPE與熒光分光光度法聯用的文獻報道中[10],通過扣除Triton X-100空白值對測量值進行校正,導致實驗誤差較大,特別在苯酚含量低時,嚴重影響方法靈敏度和準確度。因此,亟需尋找一種對苯酚測定無干擾且萃取效果好的表面活性劑。
聚乙二醇 6000(PEG 6000)作為一種直鏈型的非離子型表面活性劑,具有無毒、來源廣、成本低、無苯環結構、不產生熒光干擾信號、易降解、對環境友好等優點,現已被逐漸應用于濁點萃取中[11]。Samaddar選取PEG 6000作萃取劑,用于汞的形態分析[12];Ulusoy使用PEG 6000萃取食品中的維生素B9,獲得良好效果[13]。但是由于PEG 6000的濁點溫度高(100 ℃),實驗中常需要通過大量電解質的使用和耗時較長的高溫水浴條件才能產生濁點現象。然而溫度是影響熒光強度的一個重要因素,當隨著溫度的上升,分子的內部能量轉換作用以及分子間的碰撞幾率增加,熒光強度減弱。而且過高的水浴溫度,也易導致半揮發性苯酚的損失,影響結果的準確性和重現性。目前,PEG 6000尚未應用于苯酚的預富集。
本文選用直鏈型的非離子表面活性劑PEG 6000為萃取劑,正辛醇為濁點的誘導協同劑,以苯酚的熒光強度為檢驗指標,考察了聚乙二醇 6000、無水硫酸鈉和正辛醇的用量、溶液pH等因素對其的影響,建立了RS-CPE-熒光分光光度法聯用測定5種食品塑料包裝材料中浸出苯酚的分析方法,為食品塑料包裝材料中苯酚的測定提供一種簡單、快速、基質干擾少、靈敏度高、廉價的新方法。
1 材料與方法
1.1 材料與儀器
苯酚標準品 純度大于99%,德國Dr. Ehrenstorfer公司;PEG 6000 美國Sigma公司;5種食品塑料瓶 從本地超市購買5種聚對苯二甲酸類(PET)不同牌子的飲料瓶,用自來水和超純水進行清洗,自然干燥,備用;實驗試劑 均為分析純及以上;實驗用水 為超純水(電阻率18.2 mΩ·cm);實驗所用器皿 均用10%(v/v)硝酸和10%(v/v)乙醇的溶液浸泡過夜,再用自來水和純水沖洗干凈,并晾干后使用。
F-2500熒光分光光度計 日本日立高新技術公司;TG12Y臺式加熱離心機 湖南湘立科學儀器有限公司;PHS-3C精密級數字式酸度計 上海虹益儀器儀表有限公司;QB-228臺式搖勻機 海門Kylin-bell實驗室儀器有限公司;CPA225D型十萬分之一電子天平 北京賽多利斯科學儀器有限公司;Synergy超純水系統 默克密理博公司。
1.2 實驗方法
1.2.1 苯酚檢測波長的確定 移取一定量的苯酚標準溶液,用純甲醇稀釋定容后,用1 cm石英比色皿裝待測溶液,并放入熒光分光光度計,激發和發射狹縫均為5 nm,光電倍增管負高壓400 V,掃描速度1500 nm/min,固定激發波長為275 nm,在波長為280~400 nm范圍內掃描,獲得發射光譜;固定發射波長為300 nm,在波長為240~290 nm范圍內掃描,獲得激發光譜。光譜圖中最大熒光強度對應的激發波長和發射波長選作苯酚的檢測波長。
1.2.2 樣品預處理 參照相關文獻[14-15],在已洗凈干燥的塑料瓶中注入超純水,在60 ℃恒溫水浴箱中水浴2 h,獲得待檢樣品的浸泡液。
1.2.3 RS-CPE和熒光分光光度計檢測條件 取25.0 μL 1.00 mg/mL的苯酚標準溶液于50 mL離心管中,依次加入8.0 mL 0.2 g/mL PEG 6000,3.0 g無水硫酸鈉,5.0 mL正辛醇,2.0 mL pH6.0檸檬酸-磷酸氫二鈉緩沖溶液,用超純水定容。充分振蕩混勻后,3500 r/min離心3 min。分相后,直接轉移富集相至1 cm石英比色皿中,在激發波長/發射波長(λex/λem)=275/300 nm條件下測定其熒光強度。
1.2.4 RS-CPE條件的單因素實驗 在λex/λem=275/300 nm的最佳檢測波長條件下,固定其他條件不變(溶液pH6.0,8.0 mL 0.2 g/mL PEG 6000,5.0 mL正辛醇,3.0 g無水硫酸鈉),采用單因素實驗法分別考察了pH(1.0、2.0、3.0、4.0、5.0、6.0、7.0、8.0、9.0)、0.2 g/mL PEG 6000添加量(5、6、7、8、9 mL)、正辛醇添加量(4、5、6、7、8 mL)、無水硫酸鈉添加量(0、1、2、3、4 g)對苯酚熒光強度的影響,每個實驗重復3次。
1.2.5 方法的分析特征實驗 分別加入1、2.5、5、10、25、50、75、80 μL 1.00 mg/mL的苯酚標準溶液于50 mL離心管中,用1.2.3的條件進行萃取和檢測。以苯酚的質量濃度(ρ,μg/mL)為橫坐標,熒光強度(F)為縱坐標繪制標準曲線,獲得方法的線性回歸方程和相關系數。對10份苯酚空白溶液按照1.2.3的條件進行萃取測定,計算測定值的3倍標準偏差(s)與標準曲線斜率(k)的比值(3s/k),獲得方法的檢出限(LOD)。對苯酚濃度為0.5 μg/mL的溶液用1.2.3的條件平行萃取測定8次,獲得方法的精密度,用相對標準偏差(RSD)表示。
1.2.6 共存離子的干擾實驗 按照1.2.3的實驗條件,在此基礎上分別加入一系列濃度的共存離子,將系列濃度所得的苯酚熒光強度值與不添加干擾離子的熒光強度值進行對比,若測定值間的相對標準偏差在±5%范圍內,則定義為不會干擾苯酚的測定。而此濃度與0.5 μg/mL苯酚的比值,則為其濃度倍數關系。
1.2.7 樣品分析和加標回收實驗 取1.2.2中的樣品浸泡液25.0 mL于50 mL離心管中,用1.2.3的條件進行萃取檢測。同時,向樣品中分別加入兩個濃度(0.02、0.20 μg/mL)的苯酚標液,按照1.2.3實驗條件做加標回收實驗。
1.2.8 分布系數的計算 HA表示平衡溶液中某化合物的分子形式,A-表示平衡溶液中該化合物的一元離子形式。對于一元弱酸而言,在溶液中主要存在HA和A-兩種形式,故其分子形式的分布系數δ(HA)=[H+]/{[H+]+Ka},其中[H+]=10-pH;Ka=10-pKa;離子形式的分布系數δ(A-)=Ka/{[H+]+Ka}=1-δ(HA)。
1.3 數據處理
使用Excel 2003對實驗數據進行處理,實驗結果以測定平均值±標準差表示。
2 結果與分析
2.1 苯酚檢測波長的確定
激發光譜和發射光譜是熒光物質的特征光譜,而最佳激發波長和發射波長是熒光強度最大時的波長,可作為定性和定量分析的依據,也能夠有效提高檢測靈敏度和選擇性。通過掃描苯酚溶液的激發光譜和發射光譜,確定檢測的最佳激發波長為275 nm,發射波長為300 nm,結果見圖1。

圖1 苯酚光譜圖 Fig.1 Fluorescence spectra of phenol
2.2 pH對苯酚熒光強度的影響
苯酚的熒光強度隨著pH增大,先逐漸升高后呈下降趨勢(見圖2)。苯酚在溶液中主要以C6H5OH(HA)和C6H5O-(A-)兩種形態存在。據報道,苯酚以離子狀態存在時不產生熒光,只有中性形式才能產生熒光[10]。苯酚的pKa為9.89,屬于一元弱酸物質,故根據1.3公式可以計算出在不同pH溶液中苯酚的不同存在形式所占的比例,從而得出分布系數δ與溶液pH間的關系曲線(圖3)。當pH小于9.89(pH

圖2 pH對熒光強度的影響 Fig.2 The effect of pH on the fluorescene intensity

圖3 苯酚分布系數圖 Fig.3 The distribution coefficient diagram of phenol
2.3 表面活性劑添加量對苯酚熒光強度的影響
篩選合適的表面活性劑是實現RS-CPE與熒光分光光度法聯用測定苯酚的關鍵所在。在預實驗中,本研究選取了兩種直鏈型的非離子表面活性劑PEG 6000和Tergitol 15-S-7作RS-CPE萃取劑。結果表明,兩者在本研究檢測波長范圍內均無任何熒光信號,故避免了富集相中表面活性劑熒光干擾信號的問題,提高了方法的靈敏度和準確度,使結果更加可靠。兩者在水溶液中均可形成膠束,將苯酚萃取至富集相中,但PEG 6000所得的熒光強度高于Tergitol 15-S-7。故本研究選擇PEG 6000作為萃取劑,并考察了不同用量的0.2 g/mL PEG 6000對苯酚熒光強度的影響,結果如圖4所示。苯酚熒光強度隨著0.2 g/mL PEG 6000用量的增大而增大,當使用體積為8.0 mL時,熒光強度達到峰值,隨后有輕微下降趨勢。這是因為,使用少量萃取劑時,形成的膠束數較少,對目標物的萃取效果差,所得的熒光強度小;但若使用過量的萃取劑,則會使富集相體積增大明顯,目標物被過度稀釋,從而導致熒光強度有所下降。因此,為確保有足夠的表面活性劑形成膠束萃取目標物,本研究選擇8.0 mL 0.2 g/mL PEG 6000用于后續實驗。
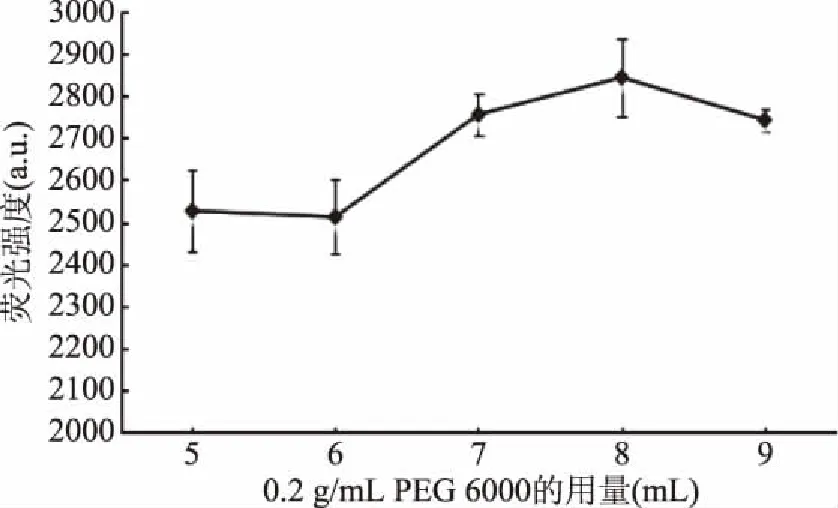
圖4 0.2 g/mL PEG 6000對熒光強度的影響 Fig.4 The effect of 0.2 g/mL PEG 6000 on the fluorescence intensity
2.4 正辛醇添加量對苯酚熒光強度的影響
經預實驗發現,在甲醇、無水乙醇、正辛醇協同萃取劑中,正辛醇效果最好,使用少量即可將濁點溫度降至室溫,快速完成萃取過程,故進一步考察了正辛醇用量對苯酚熒光強度的影響,結果見圖5。正辛醇用量在4.0~5.0 mL時,苯酚的熒光強度逐漸增大,當用量大于5.0 mL時,苯酚的熒光強度相對穩定。這是因為,一方面使用較少量的正辛醇時,不足以將全部表面活性劑的濁點降至室溫,形成的膠束少,這與Wen等人的研究結果是一致的[5]。另一方面,正辛醇可輔助表面活性劑萃取目標物至富集相中,因此隨著其用量的增加,苯酚的熒光強度也逐漸增大。故本研究選擇正辛醇的最優用量為5.0 mL。

圖5 正辛醇對熒光強度的影響 Fig.5 The effect of octanol on the fluorescence intensity
2.5 電解質對苯酚熒光強度的影響
在RS-CPE過程中加入適量的無機電解質,可以改變溶液的濁點溫度,促使表面活性劑聚集成更大的膠團,促進分相[16]。實驗中觀察到,在本研究考察的四種常用無機電解質中,需要使用5.3 g氯化鈉方能達到與其他三種鹽一樣的鹽析效果;但是由于碳酸鈉和磷酸鈉是強堿弱酸鹽,其水溶液呈強堿性,由2.2可知,苯酚在堿性條件下主要以離子A-形式存在,導致萃取效率低,熒光強度弱。氯化鈉和硫酸鈉為中性鹽,它們的加入不影響溶液pH。而且相同物質的量濃度的電解質,單電荷離子在水中的電荷密度比多電荷離子低,打斷PEG 6000與水的作用力的能力弱,萃取率低[12]。結果表明,無水硫酸鈉的使用量少,萃取效果最好,更適用于本實驗。從圖6可知,熒光強度隨無水硫酸鈉量的增加而增加,當加入的無水硫酸鈉質量為3.0 g時,苯酚的熒光強度達到最大。因此選擇加入3.0 g無水硫酸鈉。

圖6 電解質對熒光強度的影響 Fig.6 The effect of electrolyte on the fluorescence intensity
2.6 方法的分析特征
在上述的最優實驗條件下,即溶液pH6.0,8.0 mL 0.2 g/mL PEG 6000,5.0 mL正辛醇,3.0 g無水硫酸鈉,進行了方法的分析特征實驗。在0.02~1.60 μg/mL范圍內,RS-CPE法萃取苯酚的線性回歸方程為F=5675.6ρ-2.0598,R2為0.9998,檢出限為0.0064 μg/mL,相對標準偏差為4.49%(n=8),表明該方法線性關系良好,靈敏度高,重現性高,精密度好。在最優實驗條件下,按被萃取進入富集相的苯酚的量與總量的百分比,計算得出苯酚的萃取率為89.8%,表明該方法的萃取效果佳。
2.7 共存離子對苯酚熒光強度的影響

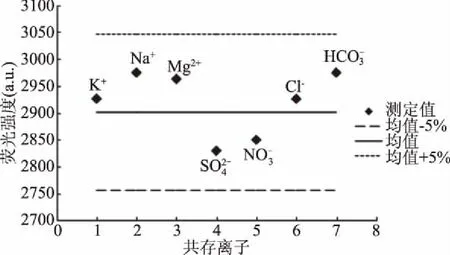
圖7 共存離子的干擾 Fig.7 The interference test of coexisting ions
2.8 實際樣品分析和加標回收實驗
為了驗證該方法的實際應用性,對本地超市購買5種不同牌子的飲料瓶按1.2.2和1.2.3進行萃取測定,結果見表1。其中在樣品2中檢測到苯酚濃度為0.0310 μg/mL,但其未超過GB 9685-2016規定食品接觸材料及制品中苯酚含量均不得大于3 μg/mL的標準,而其他4種牌子的包裝材料則均未檢出。向樣品中分別加入兩個濃度(0.02、0.2 μg/mL)的標液,計算其加標回收率。苯酚的回收率為90.5%~109.5%,表明該方法適用于實際樣品中苯酚的分析檢測。

表1 樣品加標回收率(n=3)Table 1 The recovery of sample(n=3)
3 結論
本研究建立了RS-CPE-熒光分光光度法快速測定食品塑料包裝材料中浸出苯酚的方法。在正辛醇與無水硫酸鈉的協同作用下,直接將濁點溫度高達100 ℃的直鏈型非離子表面活性劑PEG 6000降至室溫,實現快速濁點萃取與相分離,并用熒光分光光度計直接進行測定。該方法具有操作簡單、環保安全、靈敏度高、檢出限低的特點(LOD=0.0064 μg/mL),在0.02~1.60 μg/mL范圍內具有良好的線性(R2=0.9998),精密度好(RSD=4.49%,n=8)。在溶液pH6.0,8.0 mL 0.2 g/mL PEG 6000,5.0 mL正辛醇,3.0 g無水硫酸鈉的最優條件下,苯酚的萃取率可達89.8%。通過添加兩種濃度(0.02、0.2 μg/mL)作加標回收實驗,獲得較好的加標回收率(90.5%~109.5%),該方法適用于食品塑料包裝材料中浸出苯酚的分析測定。

