膽囊結石患者血液中檢出1株O1群霍亂弧菌
肖麗華,傅慶萍,唐芹芳,顏冬梅,金浩,孫明忠
(東南大學醫學院附屬鹽城醫院檢驗科,江蘇鹽城224001)
霍亂弧菌為革蘭陰性弧菌,棲居于海洋水產品及小海鮮類動物腸道和體表。根據菌體脂多糖抗原的不同,目前可將其分為210多個血清群[1],其中O1群和O139群是引起急性腸道傳染病的病原菌,感染后可導致嚴重的腹瀉和嘔吐[2]。歷史上出現過的7次世界性霍亂大流行均由O1群引起。
2017年8月本實驗室從1例膽囊結石患者血培養中分離出霍亂弧菌O1群小川型,并經江蘇省疾病預防控制中心確證。因為從血培養中檢出霍亂弧菌O1群,國內罕見[3],現予以報告。
1 病例資料
患者,男,64歲,已婚,因右上腹痛伴發熱、皮膚黃染3 d就診。患者無明顯誘因下出現右上腹持續性脹痛不適,逐漸加重,伴惡心嘔吐、畏寒發熱、尿黃、皮膚黃染,體溫最高39.0℃,大便2~3次/d,為黃色水樣便。入院時白細胞計數為13.22×109/L,中性粒細胞百分比為 93.3%,總膽紅素 93.28 μmol/L;CT檢查示膽囊結石,膽囊炎,膽總管擴張。
入院后規范采集患者血標本進行細菌培養,16 h后需氧瓶與厭氧瓶提示細菌生長,及時轉種至血平板、巧克力平板和麥康凱平板。24 h后血平板上見濕潤、光滑、具有綠色金屬光澤且呈β溶血的菌落生長(圖1);麥康凱平板上見光滑、邊緣整齊、不發酵乳糖菌落生長。菌落涂片為革蘭陰性,弧形或逗點狀細菌(圖2);挑取單個菌落制成懸滴,在鏡下呈中速或快速穿梭狀運動。全自動微生物鑒定儀VITEK-2 Compact鑒定結果為霍亂弧菌,生物編號為0425611350506201,置信度94%。玻片法血清凝集試驗(寧波天潤生物藥業有限公司)發現該分離株生理鹽水不自凝,O139群不凝,O1群多價凝集,小川型出現凝集,明確該分離株為霍亂弧菌O1群小川型。
參照臨床微生物實驗室操作規程進行藥敏試驗,該分離株對16種抗生素均敏感。左氧氟沙星的最小抑菌濃度(minimum inhibitory concentration,MIC)≤0.25μg/mL,頭孢他啶、頭孢曲松、頭孢吡肟、氨曲南、慶大霉素以及妥布霉素的MIC均≤1μg/mL,氨芐西林、氨芐西林舒巴坦和阿米卡星MIC均≤2μg/mL,哌拉西林他唑巴坦、頭孢唑林、頭孢替坦和亞胺培南均≤4μg/mL,呋喃妥因≤16μg/mL,復方新諾明≤20μg/mL。對患者行腹腔鏡下膽囊切除術后,予以環丙沙星等抗感染、保肝、補液對癥治療,生命體征平穩,恢復良好,保肝抗炎后總膽紅素為18.74μmol/L,白細胞計數為 7.15×109/L,中性粒細胞百分比為69.9%。后續復查血培養3套,均未檢出細菌;同時送檢糞便標本培養,未檢出霍亂弧菌。

圖1 血平板菌落形態
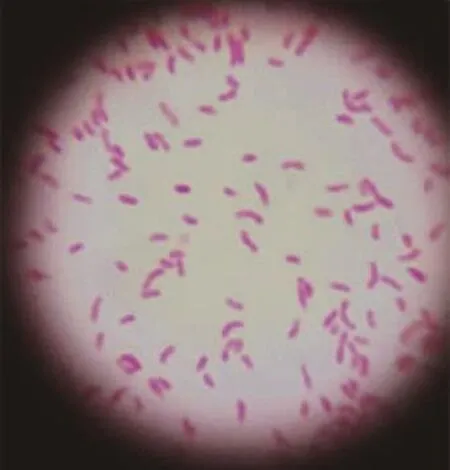
圖2 菌落涂片革蘭染色鏡檢(×1 000)
2 討論
O1群霍亂弧菌引起菌血癥的原因至今尚不明確,目前報道的菌株大多從免疫力低下的患者血液中分離。本例從膽囊結石患者血液中分離出O1群霍亂弧菌為江蘇報道的首例,其侵入血液途徑機制尚不清楚[4]。患者出生并生長于江蘇鹽城,否認有血吸蟲疫水疫區接觸史,否認工業毒物、粉塵、放射性物質等接觸史。發病前未接觸過海水、河水,未接觸過腹瀉患者,家人也未發生過腹瀉,同時否認發病前曾生食或食用未經煮熟的海產品或水產品,其居住地附近也未發生過水污染事件。
患者入院治療后總膽紅素逐漸下降至正常,推測黃疸的原因之一可能是O1群霍亂弧菌侵入血液。肝病或免疫力低下患者若被霍亂弧菌感染容易導致菌血癥或敗血癥。Restrepo等[5]研究指出hlyA編碼的霍亂溶血素在疾病的發生過程中可能起到一定作用,使得腸道中的霍亂弧菌通過腸黏膜侵入血液,提示霍亂弧菌的溶血能力也可能是重要的致病因素;同時,rtx編碼的細胞毒素可引起炎癥反應[6]。本例患者初入院時白細胞計數為13.22×109/L,中性粒細胞百分比93.3%,治療后白細胞計數為7.15×109/L,中性粒細胞百分比為69.9%,恢復至正常;本例患者伴有發熱而沒有嚴重腹瀉,有待于進一步研究其致瀉性毒力基因如 ctxA、ctxB、ace、cep、zot、tcpA和 cri等[7-8]。
研究發現不同血清群霍亂弧菌的毒力因子在外環境中容易發生轉移。大多數非致病性霍亂弧菌經過復雜的進化和變異,可獲得毒力而有效地定殖在人類小腸并釋放腸毒素致病;同時非流行株和非產毒株也可感染人體引起腹瀉。霍亂弧菌毒力基因的分布特性為毒力因子的轉移提供了環境毒力貯存庫,成為霍亂持續流行的重要因素之一。

