元素及其化合物專項訓練(A卷)
■湖南省長沙縣實驗中學 唐梓雲(yún)
■湖南省辰溪縣第二中學 蔡俊來
1.化學在綠色發(fā)展、循環(huán)發(fā)展、低碳發(fā)展及推進生態(tài)文明建設中正發(fā)揮著積極作用。下列做法不正確的是( )。
A.研制開發(fā)燃料電池汽車,降低機動車尾氣污染,某種程度可以減少PM2.5污染
B.綠色化學的核心是應用化學原理對環(huán)境污染進行治理
C.鐵強化醬油可通過膳食補充人體所需的鐵元素
D.地溝油由于混有一些對人體有害的雜質而不能食用,可加工制成生物柴油,生物柴油成分與從石油中提取的柴油成分不同
2.化學反應中,反應物用量、濃度或反應條件不同可能對生成物產(chǎn)生影響。下列反應的生成物不受上述因素影響的是( )。
A.銅與硝酸反應
B.鈉與氧氣反應
C.氫氣與氯氣反應
D.氯化鋁與氫氧化鈉溶液反應
3.C、Si、S都是自然界中含量豐富的非金屬元素,下列有關說法中正確的是( )。
A.三種元素在自然界中既有游離態(tài)又有化合態(tài)
B.元素的+4價氧化物都屬于酸性氧化物,都能與堿反應而不能與任何酸反應
C.最低價的氣態(tài)氫化物都具有還原性,易與O2發(fā)生反應
D.其最高價氧化物對應的水化物的酸性強弱:H2SO4>H2SiO3>H2CO3
4.下列各組物質,不能按a→b→c(“→”表示反應一步完成)關系轉化的是( )。

選項 a b cA Al2O3 NaAlO2 Al(OH)3 B AlCl3 Al(OH)3 NaAlO2 C Al Al(OH)3 Al2O3 D MgCl2 Mg(OH)2 MgO
5.下列離子方程式正確的是( )。
①氯氣與水反應:Cl2+H2O==2H++Cl-+ClO-
②氯氣與氫氧化鈉溶液反應:Cl2+2OH-==Cl-+ClO-+H2O
③濃鹽酸與二氧化錳共熱:MnO2+
④漂白粉溶液中通入少量的二氧化碳氣體:Ca2++2ClO-+H2O+CO2==CaCO3↓+2HClO
A.①③ B.②④ C.②③ D.①④
6.從淡化海水中提取溴的流程如下:
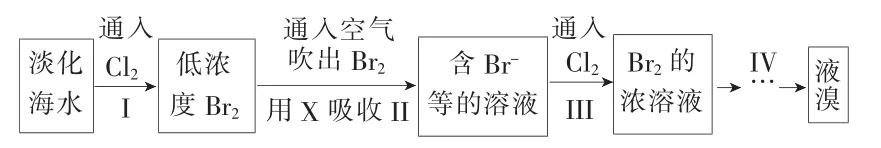
下列有關說法不正確的是( )。
A.X試劑可以為Na2SO3飽和溶液
B.步驟Ⅲ的離子反應:2Br-+Cl2==2Cl-+Br2
C.工業(yè)上每獲得1 molBr2,需要消耗Cl244.8L
D.步驟Ⅳ包含萃取、分液和蒸餾
7.圖1是檢驗氣體性質的實驗裝置。向裝置中緩慢通入氣體X,若關閉活塞K,品紅溶液無變化,澄清石灰水變渾濁;若打開活塞K,品紅溶液褪色。據(jù)此判斷,氣體X和液體Y可能是( )。
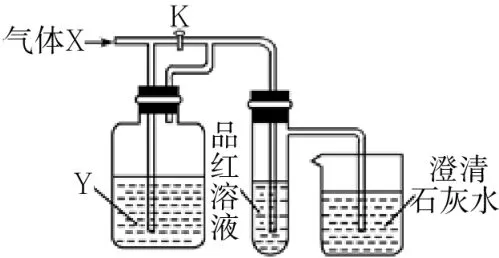
圖1
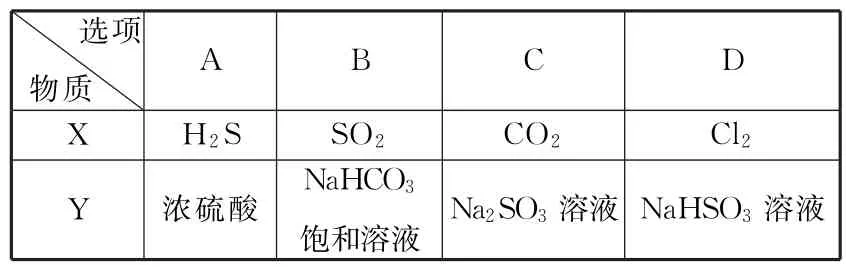
A B C DX H2S SO2 CO2 Cl2 Y 濃硫酸 NaHCO3飽和溶液 Na2SO3溶液 NaHSO3溶液
8.砷(As)及其化合物可用于制半導體材料及除草劑等。回答下列問題:
(1)砷是氮的同族元素,比氮多2個電子層,砷在周期表中的位置為第____周期第____族;AsH3的熱穩(wěn)定性比NH3________(填“強”或“弱”)。砷在自然界中豐度最大的核素的中子數(shù)為40,該核素為____(用元素符號表示)。
(2)砷化鎵是常見的半導體材料,Ga與As同周期,Ga最外層有3個電子,砷化鎵的化學式為____。
(3)某工業(yè)廢水中含有少量的As2O3,向該廢水中通入硫化氫可將其轉化為更難溶的As2S3,該反應的化學方程式為____。
9.食用堿是人們生活中常用的食品疏松劑和肉類嫩化劑,其成分為純堿和小蘇打。甲、乙兩位同學想根據(jù)高中階段學習的知識設計實驗,測定食用堿中小蘇打的質量分數(shù)。
甲同學認為可以根據(jù)食用堿中兩成分的熱穩(wěn)定性差異,利用加熱前后的質量差求小蘇打的質量分數(shù)。
(1)寫出小蘇打受熱分解的化學方程式:____。
(2)甲同學的實驗方案中需要使用的儀器有____(填字母)。
①三腳架 ②托盤天平 ③瓷坩堝④坩堝鉗 ⑤泥三角 ⑥石棉網(wǎng) ⑦燒杯⑧蒸發(fā)皿 ⑨鐵坩堝 ⑩干燥器 ?酒精燈
A.①②③④⑤⑥? B.①②④⑤⑨⑩?
C.①②⑥⑦⑧?
(3)如果該食用堿在測定前已經(jīng)受潮,則用甲同學的實驗方案測得的NaHCO3的質量分數(shù)會____(填“偏大”“偏小”或“無影響”)。
乙同學設計了另一種實驗方案來測定13.7g食用堿中NaHCO3的質量分數(shù),其流程如下。
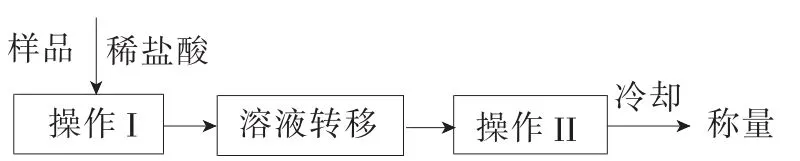
(4)操作Ⅱ的名稱是____,最終稱量的物質的化學式是____。
(5)如果最終稱量固體質量為11.7g,則該食用堿中NaHCO3的質量分數(shù)為____。
10.工業(yè)上利用菱鎂礦 MgCO3(含雜質Al2O3、FeCO3)制取鎂的工藝流程如下。
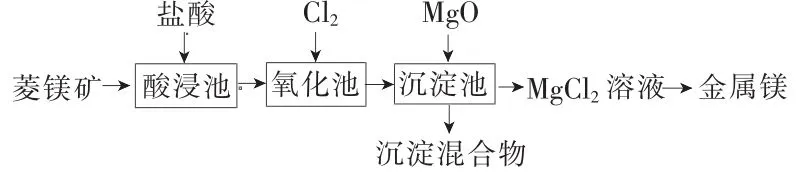
回答有關問題:
(1)菱鎂礦送入酸浸池前需要粉碎,目的是____。
(2)氧化池中通入氯氣的目的是氧化____,工業(yè)上不選用硝酸作氧化劑的原因是____和____。
(3)沉淀混合物為____和____(填化學式)。
(4)利用熔融氯化鎂制取金屬鎂,選用的方法是____(填字母)。
A.電解法 B.氫氣還原法
C.碳還原法 D.分解法
11.圖2是實驗室制備氯氣并進行一系列相關實驗的裝置(夾持裝置已略)。
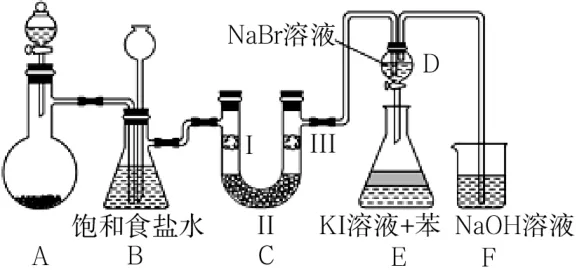
圖2
(1)制備氯氣選用的藥品為漂粉精固體和濃鹽酸,則相關反應的化學方程式為____。
(2)裝置B中飽和食鹽水的作用是____。同時裝置B也是安全瓶,監(jiān)測實驗進行時裝置C是否發(fā)生堵塞,請寫出發(fā)生堵塞時裝置B中的現(xiàn)象:____。
(3)裝置C的實驗目的是驗證氯氣是否具有漂白性,為此裝置C中Ⅰ、Ⅱ、Ⅲ處依次放入____(選填表1中字母選項)。
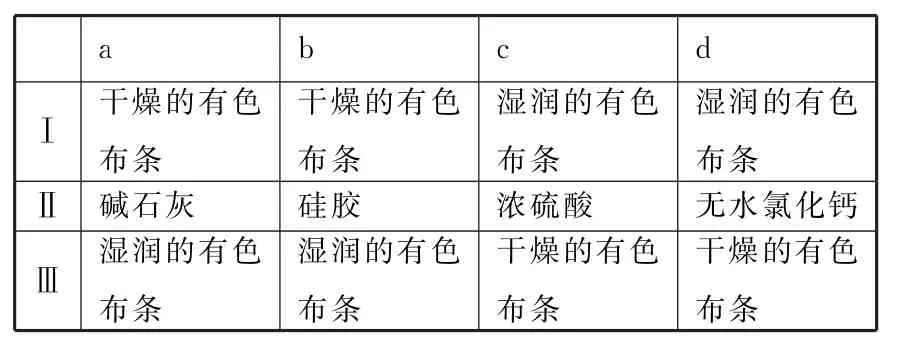
表1
(4)設計裝置D、E的目的是比較氯、溴、碘的非金屬性。當向D裝置中緩緩通入一定量氯氣時,可以看到無色溶液逐漸變?yōu)開___色,說明氯的非金屬性強于溴。
(5)打開活塞,將裝置D中少量溶液加入裝置E中,振蕩后靜置。觀察到的現(xiàn)象是____。

