前列腺癌主動監(jiān)測期間組織ERG蛋白表達與腫瘤進展的關(guān)系*
周文浩 龔志勇 廖波 程樹林
(川北醫(yī)學院附屬醫(yī)院泌尿外科,四川 南充 637000)
前列腺癌已成為威脅男性健康最常見的惡性腫瘤,在歐美國家其發(fā)病率高居男性惡性腫瘤首位,死亡率僅次于肺癌[1]。前列腺特異性抗原(prostate specific antigen, PSA)的篩查,以及經(jīng)會陰前列腺穿刺活檢使前列腺癌成了最易于被檢測到的男性惡性腫瘤之一,雖然多數(shù)前列腺癌不發(fā)生進展、轉(zhuǎn)移,但仍有一部分進展甚至導致患者死亡[2-3]。 與主動監(jiān)測或觀察等待的患者相比,對低危前列腺癌患者實施根治性治療,并不顯著降低患者全因死亡率或腫瘤特異性死亡率,且在總生存率上并無明顯優(yōu)勢[4],對低風險前列腺癌實施主動監(jiān)測可能對于一部分患者是更為合理的選擇[5]。主動監(jiān)測期間前列腺癌進展風險的評估,及時對進展風險較高的患者進行干預,是主動監(jiān)測方案能否順利實施的關(guān)鍵[6]。目前,臨床上較為常用的前列腺癌進展預測因素包括組織學分級,臨床分期及PSA水平,但這些指標在腫瘤進展的預測效能上均不能達到令人滿意的效果[7-8]。因此,前列腺癌新的進展預測因子研究很有必要。2005年Tomlins團隊首次報道了位于21q22.3的跨膜絲氨酸蛋白酶2(Transmembrane serine protease,TMPRSS2)基因與一系列擁有鳥類白血病病毒E26同源序列基因特異性轉(zhuǎn)錄調(diào)控(E26 transformation-specific,ETS)因子家族融合的現(xiàn)象[9],其中又以TMPRSS2基因與ETS家族中的ERG基因融合最為常見;TMPRSS2-ERG基因融合直接導致前列腺癌組織ERG蛋白表達升高,已有研究探討ERG蛋白在前列腺癌診斷及預后的作用。本研究將探討ERG蛋白的表達與前列腺癌主動監(jiān)測期間進展的關(guān)系。
1 資料和方法
1.1 一般資料 納入川北醫(yī)學院附屬醫(yī)院2012年3月~2016年2月前列腺穿刺證實為前列腺癌,符合主動監(jiān)測條件或有意愿行主動監(jiān)測方案的56例患者作為研究對象,通過住院電子病歷系統(tǒng),門診病歷及社交軟件獲取研究對象相關(guān)資料。 納入患者年齡61~84歲,平均(74±4)歲;平均隨訪時間37.5個月,中位隨訪時間28個月(1~57);其他臨床病理學參數(shù)見表1。
1.2 納入與排除標準 納入研究的患者需滿足活檢穿刺為前列腺癌,PSA≤10ng·ml-1,影像學分期≤cT2a,GS≤6,超出納入標準但患者行主動監(jiān)測意愿較強者,仍納入本次研究。合并其他系統(tǒng)原發(fā)性腫瘤如胃癌、肺癌、膀胱癌等或慢性基礎(chǔ)疾病患者則被排除。納入患者參照2014版《中國泌尿外科疾病診斷治療指南》前列腺癌主動監(jiān)測方案定期監(jiān)測PSA水平,根據(jù)PSA倍增時間、PSA速率、患者焦慮狀況、年齡及影像學(MRI)情況重復穿刺。
1.3 前列腺癌進展定義 參照Klotz等[10]的經(jīng)驗,組織學進展定義為GS≥3+4或4+3(若確診GS=3+4),PSA進展定義為PSA倍增時間<3年,若患者行血清PSA檢測期間服用5α還原酶抑制劑,或合并尿路感染及尿潴留等則該次PSA結(jié)果不納入分析。
1.4 主要試劑與方法 ERG兔抗人單克隆抗體(clone EPR3864)購于Epitmics公司,染色用即用型試劑盒及DAB顯色劑購于美國Tucson公司。所有穿刺活檢標本均行中性福爾馬林溶液固定及石蠟包埋,3μm連續(xù)切片,免疫組織化學染色嚴格按照說明書進行,ERG蛋白表達陽性定義為細胞核染為棕黃色,其余為非特異性染色[11]。
表1納入研究患者的臨床和病理學特點[n(×10-2)]
Table1Clinicopathologicfeaturesoftheentirestudycohortof56patients
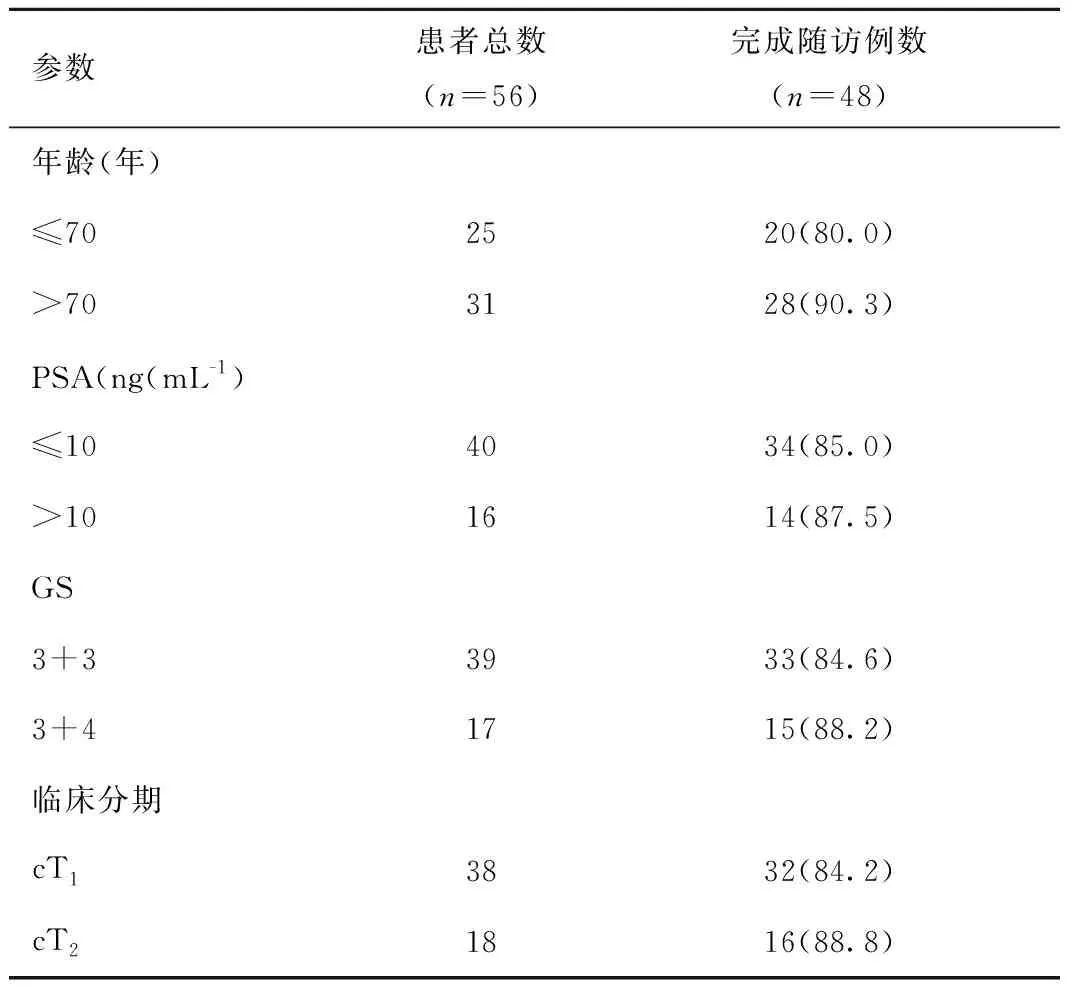
參數(shù)患者總數(shù)(n=56)完成隨訪例數(shù)(n=48)年齡(年)≤702520(80.0)>703128(90.3)PSA(ng(mL-1)≤104034(85.0)>101614(87.5)GS3+33933(84.6)3+41715(88.2)臨床分期cT13832(84.2)cT21816(88.8)
1.5 統(tǒng)計學分析 采用SPSS23.0軟件進行統(tǒng)計分析及作圖,ERG蛋白表達與患者臨床病理學間的差異采用2檢驗,ERG陽性及陰性表達組生存函數(shù)間的差異采用log-rank檢驗,主動監(jiān)測期間前列腺癌進展風險采用Cox比例風險模型分析,P<0.05為差異有統(tǒng)計學意義。
2 結(jié)果
2.1 ERG蛋白表達與前列腺癌進展 本研究共納入前列腺穿刺證實為前列腺癌并行主動監(jiān)測方案的患者48名,平均隨訪時間37.5(1~57)個月,患者中ERG陽性表達18例,陰性30例,陽性表達率37.5%(圖1)。組織學進展18例,ERG陽性表達組10例(55.6%),陰性表達組8例(44.4%),其中重復穿刺1次34例(60.7%),2次18例(32.1%),3次4例(7.2%)。PSA進展16例,ERG蛋白陽性組9例(56.2%),陰性組7例(43.8%)。ERG蛋白表達狀態(tài)與患者年齡、確診PSA水平、Gleason評分均無相關(guān)(P>0.05),與前列腺癌臨床分期相關(guān)(P<0.05),見表2。
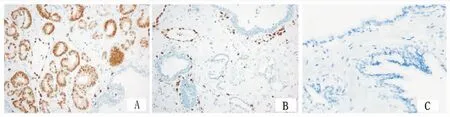
圖1ERG蛋白的表達情況(×20)
Figure1ImmunohistochemicaldetectionofERGproteinexpression.ERGproteinwasfoundpositiveexpressioninprostatecancertissues(A),negativeexpressioninprostatecancer(B)andbenignprostatichyperplasiatissues
注:A.前列腺癌中陽性表達;B.前列腺癌中陰性表達;C.前列腺增生組織中陰性表達
表2ERG蛋白表狀態(tài)與各參數(shù)間的關(guān)系
Table2CorrelationofERGproteinexpressionwithclinicopathologicparameters
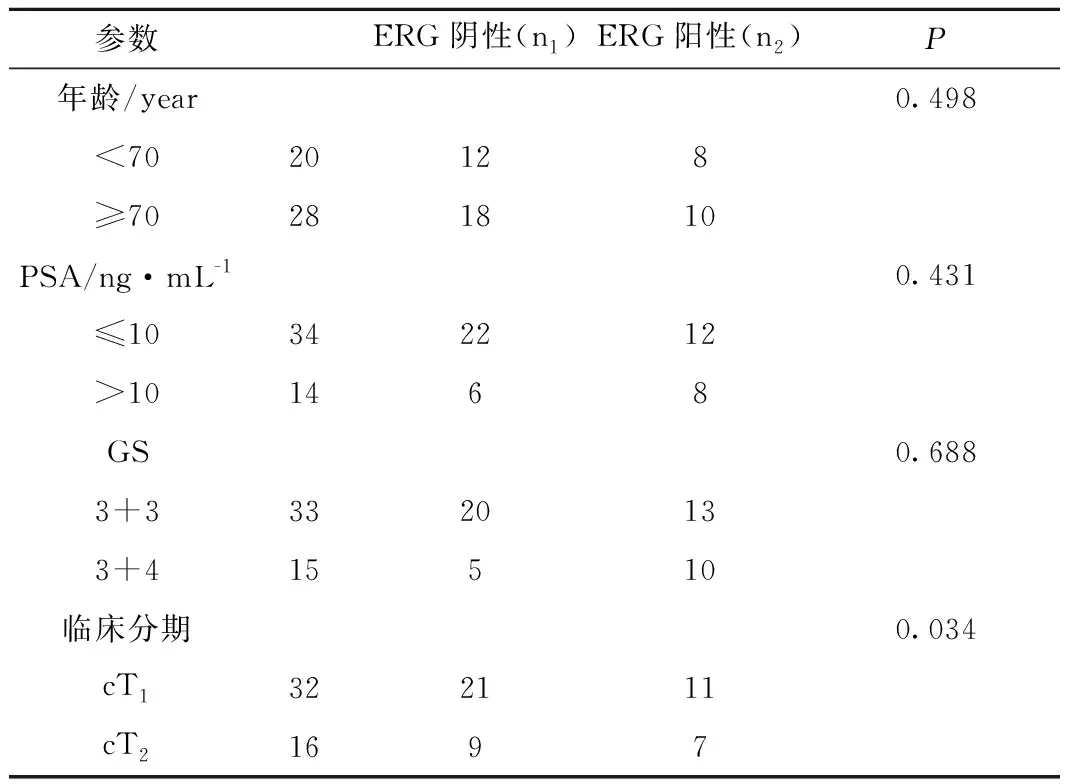
參數(shù)ERG陰性(n1)ERG陽性(n2)P年齡/year0.498<7020128≥70281810PSA/ng·mL-10.431≤10342212>101468GS0.6883+33320133+415510臨床分期0.034cT1322111cT21697
2.2 生存分析與Cox回歸分析 納入研究的患者ERG蛋白陽性和陰性表達組平均組織學無進展生存時間分別為33.8個月和42.5個月;中位組織學無進展生存時間分別為32個月及48個月,Log-rank檢驗2=4.476,P=0.034;兩組平均PSA無進展生存時間分別為21.5個月及24.8個月,無進展中位生存時間分別為21個月及26個月,Log-rank檢驗(2=4.272,P=0.039(圖2)。Cox回歸模型中確診時年齡、PSA、GS及臨床分期均與前列腺癌進展無關(guān),而ERG蛋白陽性表達是前列腺癌主動監(jiān)測期間腫瘤進展的獨立危險因素,見表3。
3 討論
前列腺癌作為嚴重影響男性健康的惡性腫瘤,其管理與治療已成為各國臨床工作者關(guān)注的焦點。盡管臨床局限性前列腺癌可以通過根治性手術(shù)及放療達到較好的腫瘤控制效果,但較高的手術(shù)風險,以及患者的經(jīng)濟、心理負擔同樣應納入方案評估中。因此,對部分低風險前列腺癌進行主動監(jiān)測可能是更為合理的選擇。國外兩項隨機對照研究(PIVOT和SPCG-4),對臨床局限性前列腺癌患者行根治性手術(shù)及主動監(jiān)測進行了比較,在總生存率上兩種方案并無統(tǒng)計學差異[12-13],這說明對低風險前列腺癌患者行根治性治療不僅須面對治療相關(guān)的風險及并發(fā)癥,且僅有極少數(shù)患者獲益。另一方面,在主動監(jiān)測期間,約30%的患者會接受進一步的治療[14]。然而,部分患者及外科醫(yī)師對主動監(jiān)測方案接受度較低的主要原因是目前臨床尚缺乏可靠的前列腺癌進展預測因子[15]。因此,新的進展預測因子及生物標記物的研究顯得很有必要。
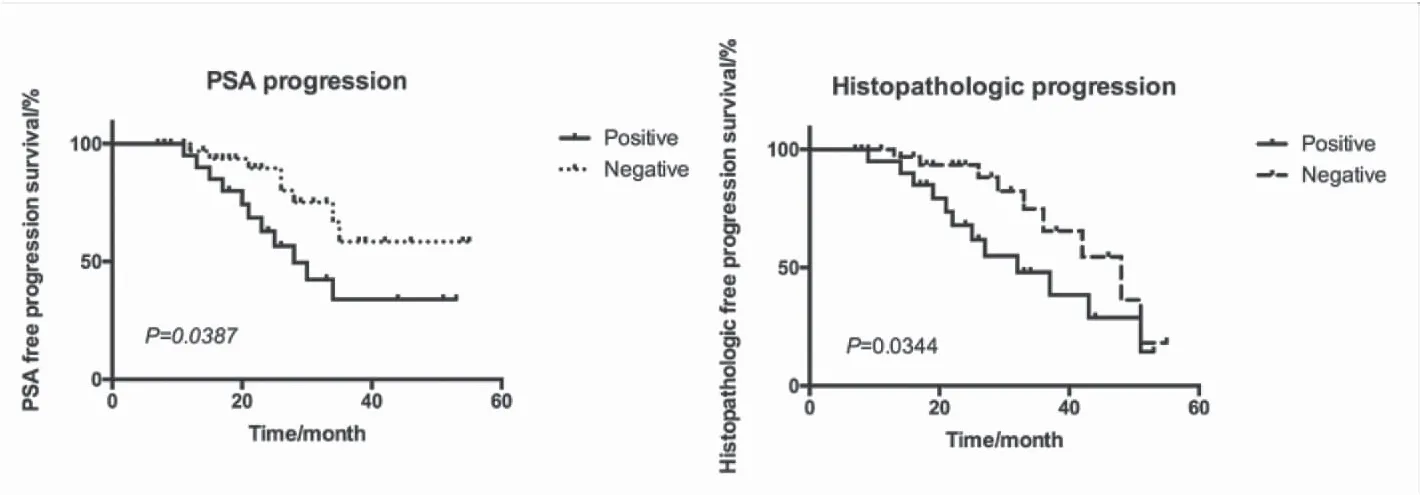
圖2 基于ERG蛋白表達與前列腺癌組織學、PSA進展的生存曲線Figure 2 Kplan-Meier survival curves of patients based on PSA progression, GS and ERG protein expression
表3各臨床病理學參數(shù)對前列腺癌主動監(jiān)測期間進展的預測作用
Table3PredictivevalueofERGproteinandclinicopathologicparemetersforcancerprogression
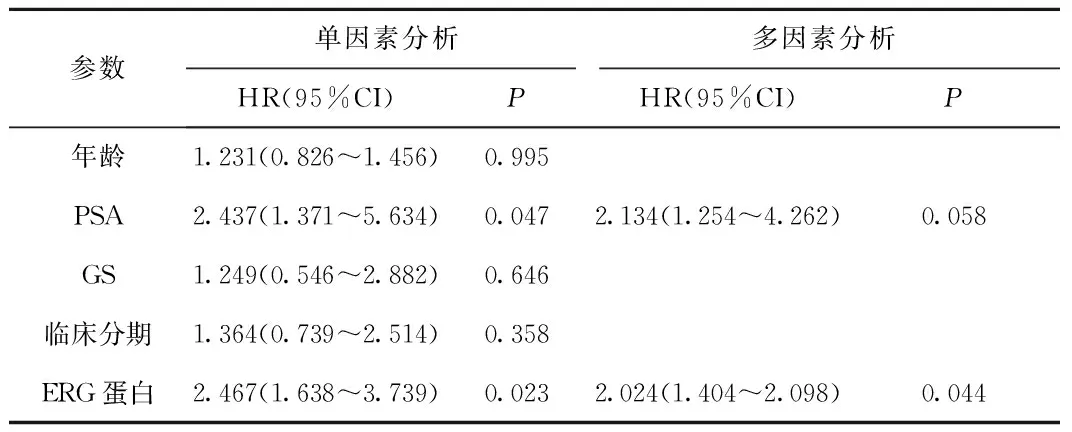
參數(shù)單因素分析多因素分析HR(95%CI)PHR(95%CI)P年齡1.231(0.826~1.456)0.995PSA2.437(1.371~5.634)0.0472.134(1.254~4.262)0.058GS1.249(0.546~2.882)0.646臨床分期1.364(0.739~2.514)0.358ERG蛋白2.467(1.638~3.739)0.0232.024(1.404~2.098)0.044
2005年Tomlins團隊首次報道了前列腺癌組織中TMPRSS2-ERG基因融合及ERG蛋白表達,為前列腺癌的診斷及治療提供了新的思路。國外研究人員通過對45名患者行前列腺穿刺及尿TMPRSS2-ERG融合基因檢測得出TMPRSS2-ERG診斷前列腺癌特異度為87%[16]。易發(fā)現(xiàn)等[17]檢測前列腺活檢穿刺標本中ERG蛋白表達發(fā)現(xiàn)其診斷前列腺癌特異度高達94%,靈敏度為45%。這一系列研究確定了ERG蛋白在前列腺癌組織中的高表達和特異性,同時其也具備了作為新的診斷前列腺癌的分子生物標記物的特征。同時,ERG蛋白的表達與前列腺癌預后的關(guān)系也引起了各國學者的關(guān)注。采用免疫組織化學的方法檢測161例前列腺癌患者組織ERG蛋白的表達,分析其與前列腺癌組織學分級、臨床分期以及腫瘤進展間的關(guān)系后發(fā)現(xiàn),組織ERG蛋白陽性的患者往往提示腫瘤的高侵襲性以及較低的腫瘤特異性生存率[11],而國內(nèi)研究人員則發(fā)現(xiàn)前列腺癌患者在雄激素最大限度阻斷治療后ERG蛋白陽性表達組較陰性表達組更易發(fā)生生化復發(fā)[18]。
本研究納入了56名接受主動監(jiān)測的前列腺癌患者,通過免疫組化檢測ERG蛋白在穿刺組織中的表達,收集患者臨床病理學參數(shù),最終獲得48例完整隨訪資料。37.5%的患者前列腺癌組織ERG蛋白表達陽性(18/48),通過統(tǒng)計學分析發(fā)現(xiàn),穿刺組織ERG蛋白表達陽性是前列腺癌進展的獨立危險因素。
Berg等[19]通過對265名接受主動監(jiān)測的前列腺癌患者進行規(guī)律的血清PSA水平監(jiān)測、重復穿刺活檢以及臨床影像學評估,分析ERG蛋白的表達對主動監(jiān)測期間前列腺癌進展的風險。在競爭風險模型中,ERG蛋白陽性表達組無論組織學還是PSA進展的風險均高于ERG蛋白表達陰性組。Vainer團隊發(fā)現(xiàn)前列腺癌穿刺標本中ERG蛋白陽性表達組較陰性表達組有更高進展風險,但關(guān)于腫瘤無進展生存時間該學者并未提及[20]。本實驗在48例行主動監(jiān)測的前列腺癌患者中,ERG蛋白陽性表達18例,陰性30例,陽性表達比例與現(xiàn)有研究結(jié)果一致[21]。通過單因素及多因素分析發(fā)現(xiàn)穿刺組織ERG蛋白陽性表達是前列腺癌主動監(jiān)測期間進展的獨立預測因素。本研究主要的局限在于通過免疫組織化學的方法檢測前列腺癌組織ERG蛋白的表達是一種定性評價,結(jié)論還需進一步的研究加以證實;其次,本研究采用回顧性研究的方法,其本身存在的局限性可能導致在納入研究對象時產(chǎn)生選擇性偏倚。
4 結(jié)論
穿刺組織ERG蛋白表達增加了主動監(jiān)測前列腺癌進展的風險,通過對組織ERG蛋白的表達狀態(tài)的檢測及分析有望為患者制定個體化的主動監(jiān)測方案,以降低過度治療為患者帶來的心理及經(jīng)濟負擔。

