二氧化硅干凝膠塊的吸附過程及性能研究
劉 璐,劉世權
(濟南大學 材料科學與工程學院,山東 濟南 250022)
1 引言
染料被應用于很多工業生產中,如紡織業[1]、造紙業[2]、皮革制造業[3]以及印刷業[4]等。由于染料的難降解性,導致其成為重要的污染物[5]。水中的染料使水體著色,阻擋陽光的進入和水中光合作用的進行,進而影響水體生物的生存,并通過污染水體影響人類食物鏈及健康[6]。
染料廢水的處理有很多的方法,如生物法[7]、電化學處理[8]、膜分離法[9]、吸附法[10]等。其中吸附法是利用吸附劑對廢水中的染料進行吸附以達到除去染料并使水體脫色的目的。該法處理染料廢水有效、操作簡便,是目前處理染料廢水較成熟的方法之一。由于不同吸附劑對染料的吸附有選擇性的差異,因此在吸附脫色研究中有關吸附劑的研究是重要內容之一[11]。最常用的為活性炭、多孔SiO2等吸附劑[12]。多孔SiO2材料因其具有孔道多、比表面積大的特點,以及具有良好的熱穩定性、耐酸(HF除外)等優良特性,在吸附方面具有很大的優勢[13]。如劉國強等[14]通過溶膠-凝膠法制備了高比表面積的塊狀SiO2凝膠,并通過等溫吸附實驗研究了SiO2凝膠對亞甲基藍(MB)的吸附性能,吸附過程符合偽二級動力學方程,驗證了SiO2凝膠表面帶有負電荷,吸附陽離子MB主要推動力應是靜電引力,同時還可能存在SiO2凝膠表面的-Si-OH基團及四面體配位的水分子和MB骨架中N原子形成的氫鍵及范德華力。單層吸附量較高,達到了218.82mg/g。Li[15]制備了高比表面積的二氧化硅凝膠,并探究了其對羅丹明B的吸附能力,由于其高的比表面,從而具有更多的吸附位點,能吸附較多的染料分子,對羅丹明B的吸附量達到41mg/g。
2 實驗材料與方法
實驗使用以下試劑:正硅酸乙酯(C8H20O4Si,TEOS,分析純,國藥化學試劑有限公司),無水乙醇(C2H5OH,EtOH,≥99.7%,天津富宇精細化工有限公司),一正丁胺(≥99.0%,阿拉丁試劑),亞甲基藍MB(C16H18C13S.3H2O,97%,天津大茂化學試劑有限公司)。
在丁胺中通過TEOS的水解和縮合反應制備SiO2凝膠。將EtOH和去離子水混合,磁力攪拌10分鐘,向溶液中加入正丁胺,在劇烈攪拌30分鐘后加入TEOS。繼續攪拌5分鐘后,隨著透明混合物逐漸變成不透明白色,形成SiO2溶膠,陳化得到凝膠,然后置于烘箱中,在80℃烘干4h后取出為干凝膠塊體。
稱取一定量的MB,在燒杯中用蒸餾水溶解,制備不同濃度的亞甲基藍溶液。
稱取0.5g二氧化硅凝膠,置于不同濃度的MB溶液中,不同的吸附時間后,用可見分光光度計(JH722,上海菁華科技有限公司)測量了MB溶液的吸光度,對照標準曲線及方程確定凝膠對亞甲基藍的吸附率和吸附量。研究了時間、染料濃度等對吸附性能的影響,并進行了吸附等溫模型分析和吸附動力學研究。
3 結果與討論
3.1 凝膠材料表征
所得凝膠材料為毫米及厘米尺度的塊體,如圖1所示。其氮氣等溫吸附曲線及孔徑分布曲線如圖2所示。計算可得,干凝膠的表面積、孔容、孔徑分別為 601m2/g、1.72cm3/g、30.1nm。
3.2 時間對吸附的影響
二氧化硅凝膠材料吸附MB的實驗在25℃下進行,固定亞甲基藍溶液初始濃度為20mg/L,SiO2凝膠材料投加量為0.5g,在水浴恒溫振蕩器中振蕩反應。探究吸附劑在不同的吸附時間(1、2、3、4、5、6、8、10、12、24h)對亞甲基藍溶液吸附效果的影響。
圖3為時間對SiO2凝膠材料吸附亞甲基藍的影響。如圖所示,隨著時間從1h增加到5h,SiO2凝膠材料對亞甲基藍的去除效率增加較快,在5-12h時,吸附逐漸趨于平衡,雖然吸附率仍有增加,但增加較緩慢。在12h之后基本不增加。所以綜合考慮效率和能耗,選擇了5h作為以下吸附實驗的時間。

圖1 烘干后的SiO2干凝膠
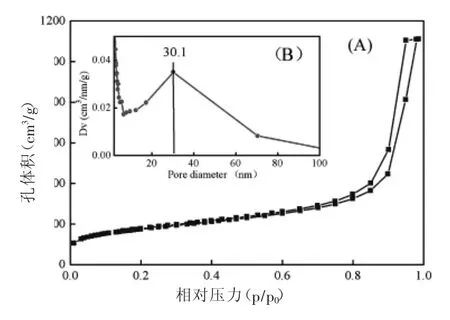
圖2 SiO2凝膠材料的N2吸附等溫線(A)和孔徑分布曲線(B)
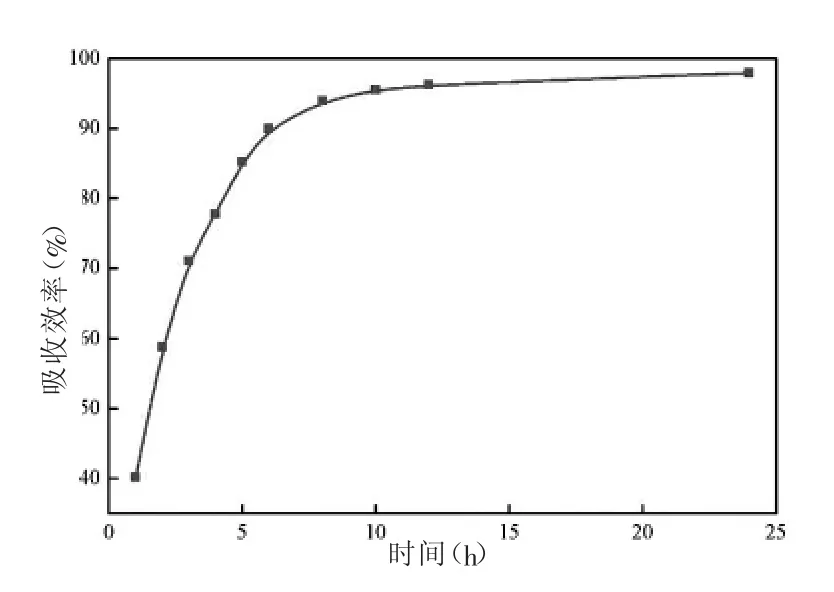
圖3 時間對SiO2凝膠材料吸附亞甲基藍的影響
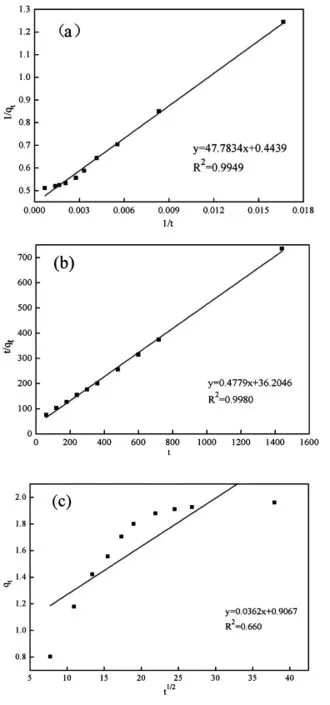
圖4 SiO2凝膠對亞甲基藍吸附動力學模型擬合:(a)偽一級動力學;(b)偽二級動力學;(c)顆粒內擴散模型
利用常用的吸附動力學模型偽一級動力學[16],偽二級動力學[17]和顆粒內擴散模型[18]分別對吸附數據進行擬合,結果如圖4所示。

表1 SiO2凝膠材料對亞甲基藍吸附的動力學模型數據
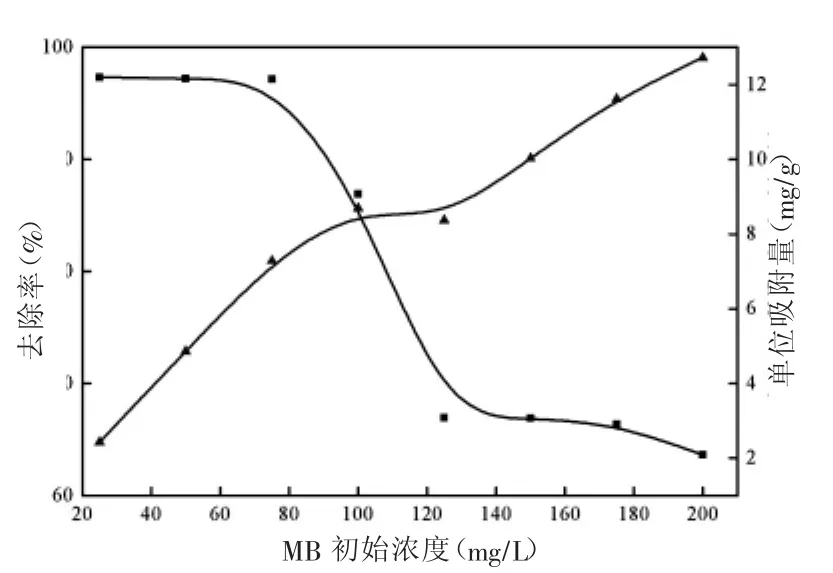
圖5 亞甲基藍初始濃度對SiO2凝膠吸附率及吸附量的影響
表1列出了經各模型擬合所得的數據。從表1中數據可以看出,偽二級動力學擬合的相關系數R2的值最高,更符合SiO2凝膠材料對亞甲基藍的吸附行為。
3.3 初始濃度對吸附的影響
研究了MB的初始濃度(10-200mg/L)對吸附的影響,溫度為25℃,吸附劑量為0.5g,在水浴恒溫振蕩器中振蕩反應5h。結果如圖5所示,從圖中可以看出,隨著MB初始濃度的增大,MB的去除率逐漸降低,但是單位吸附量逐漸增加。這是由于在溶液中存在更多的MB,在相同的條件下,凝膠的有效吸附位點周圍具有更多的MB分子。此外,較高的MB初始濃度增加了濃度梯度,增加了質量傳遞的驅動力,導致MB分子與吸附劑之間碰撞的概率較高,這導致MB吸附量較高[19]。實驗條件下的最大吸附率為97.34%,最大吸附量為12.72mg/g。
對上述吸附數據采用 Langmuir[20]、Freundlich[21]和 Temkin[22]等溫吸附模型進行擬合。結果如圖6所示。
擬合后的相關數據列于表2中,從表中數據得出,三種等溫模型的相關系數R2分別為0.9425、0.7722和0.8362。由此可知,SiO2凝膠材料對亞甲基藍的吸附更符合Langmuir模型,屬于單分子層吸附。雖然實驗材料的單層最大吸附量并不高,但所得凝膠材料為小塊體,具有易于使用和分離回收的優點。
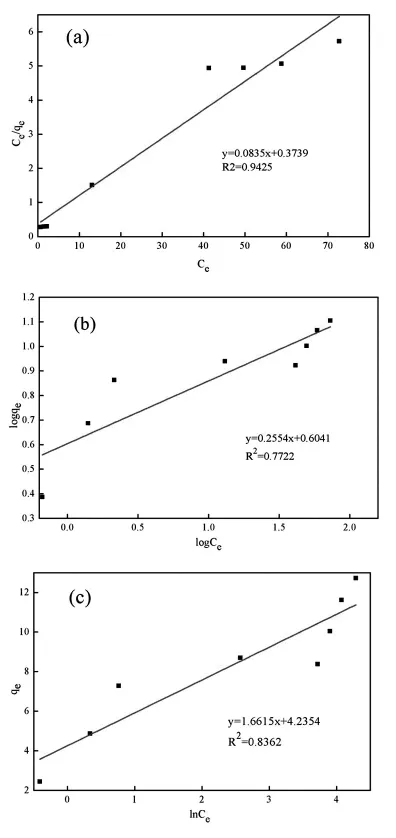
圖6 SiO2凝膠材料對亞甲基藍吸附的等溫吸附模型擬合:(I)Langmuir模型;(II)Freundlich 模型;(III)Temkin 模型
3.4 吸附機理
SiO2凝膠材料對亞甲基藍吸附的過程可分為三步,第一步為亞甲基藍從溶液中遷移到SiO2凝膠材料的表面,第二步為亞甲基藍擴散進入到復合材料的孔道內,最后一步為亞甲基藍在吸附劑的吸附位點發生上吸附[17]。由于所得凝膠材料表面具有羧基及部分化學結合的氨基吸附位,分別與離子型染料亞甲基藍發生靜電吸附或絡合,因而對水中的染料具有較高的吸附能力。
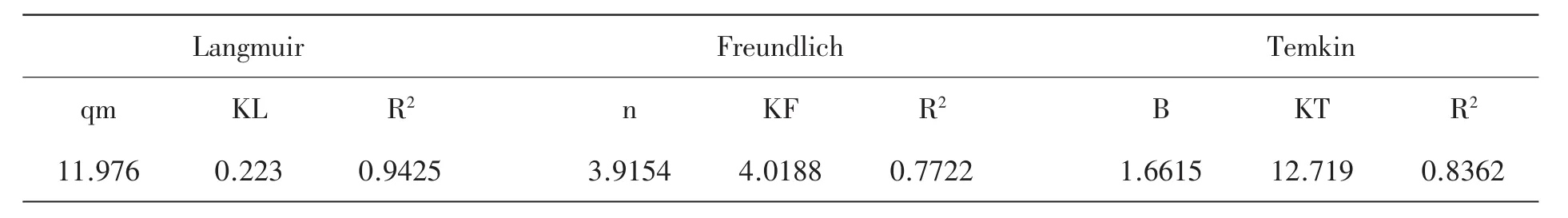
表2 SiO2凝膠材料對亞甲基藍吸附的等溫吸附模型數據
4 結論
實驗所得二氧化硅凝膠對亞甲基藍染料具有良好的吸附性能,吸附率最高可達到97.34%。吸附過程符合Langmuir模型和偽二級動力學模型。所得凝膠材料為小塊體,具有易于使用和分離回收的優點。
可折疊鋰離子電池:定向碳納米管膜替代傳統金屬集流體
柔性鋰離子電池是可穿戴電子器件的基礎元件。常用的鋰離子電池以金屬箔(銅箔、鋁箔等)作為集流體,受其本身固有的剛性所限,難以滿足可穿戴電子器件對柔性電源的要求。近年來,以碳納米管、石墨烯等為代表的碳納米材料,以其優異的導電性、柔性被廣泛地運用于柔性鋰離子電池的研究。碳納米管具有高導電率、保持高力學性能的同時還具有優異的柔性,將其制備成膜是實現鋰離子電池柔性集流體的一種理想選擇。通常制備碳納米管膜的方法有抽濾法、干拉法、液相沉積法等。但是這些方法制備的碳納米管膜不僅力學性能不佳,而且難以實現大規模批量生產。
同時,在鋰離子電池發生形變過程中,保持電池的電化學性能穩定是柔性鋰離子電池的另一個基本問題。在承受較大形變時,傳統的金屬箔集流體光滑的表面極易使得活性材料與集流體發生分離,同時限制了活性材料的負載量。構造多孔的集流體是解決這個問題的一個簡易有效的方法。
近期,江西理工大學吳子平教授團隊與華中科技大學夏寶玉教授團隊研究了碳納米管基集流體對鋰離子電池的電化學性能的影響并提出了以定向碳納米管膜作為集流體的解決辦法。該工作以紙作為基底,通過表界面改性成功地實現了定向碳納米管膜的規模化制備,該膜面積高達1800mm×1000mm,且具有大量的三維孔結構。將其用作電池正負極的集流體,不僅使得電池展現出卓越的柔性、電化學穩定性和倍率性能;同時還提升了活性物質的載量,其單層全電池容量高于700mAh(比容量160mAh/g),在模擬不同溫度(-40~70℃)及低壓條件下,電池仍保持穩定的電化學性能。
該工作實現了定向碳納米管膜的規模化制備;成功地通過表界面工程對碳納米管膜改性,改善了其導電性和對電解液的浸潤性;以該膜作為集流體,提升了全電池在不同溫度(-40~70℃)及低壓條件下的循環穩定性和倍率性能。

