異位胰腺38例診治分析
黃湘輝 武鴻彪 丁小云 嚴志龍 袁旦平
異位胰腺又稱迷走胰腺或副胰,是一種在解剖上與正常胰腺無關聯(lián)的孤立胰腺組織。異位胰腺的發(fā)病機制仍不清楚,目前得到認可的有錯位理論和化生理論。錯位理論認為異位胰腺的形成是胚胎時期內胚層腸管在旋轉過程中發(fā)生的變異,化生理論認為異位胰腺是在胚胎發(fā)育過程中遷移到黏膜下層的內胚層所化生的胰腺組織[1]。異位胰腺是一種少見的先天畸形,其臨床表現不典型或缺乏特異性,故術前診斷困難,易被漏診、誤診。在尸體檢查中異位胰腺的檢出率為0.5%~13%,多見于30~50歲人群,男性發(fā)病率高于女性[2]。隨著內鏡檢查的普及,異位胰腺的檢出率有所升高。本研究回顧性分析寧波市第一醫(yī)院2011—2016年經病理檢查證實的38例異位胰腺患者的臨床資料,結合近年相關進展探討其診斷和治療方法,旨在進一步提高對異位胰腺的認識。
1 對象與方法
1.1 研究對象 回顧性分析2011-2016年在寧波市第一醫(yī)院診斷并接受治療的異位胰腺患者38例,男、女各19例,年齡20~64歲,平均年齡為(42.0±3.6)歲。所有患者均經病理檢查確診,即具備正常胰腺組織學上的胰腺泡、胰管、胰島結構,但缺乏主胰腺的解剖、血管結構。
1.2 研究方法 統(tǒng)計38例患者的臨床表現、診斷過程、病灶特征、治療方法和預后情況,分析異位胰腺的臨床病理特征。
2 結 果
2.1 臨床表現 38例患者中,34例患者有消化系統(tǒng)癥狀,其中腹痛12例,腹脹4例,腹痛、腹脹4例,腹脹、噯氣伴反酸5例,腹脹、噯氣伴饑餓痛3例,腹痛伴黑便3例,腹脹、腹痛伴惡心嘔吐1例,腹脹伴腹瀉1例,腹脹、納差1例(出現癥狀后8個月體重減輕5 kg);3例患者表現為消化道出血,糞便潛血陽性,血紅蛋白水平輕度降低,呈慢性貧血表現。余4例患者無特殊不適,因其他疾病在術中或術后經病理檢查發(fā)現。
2.2 病灶位置和大小 36例異位胰腺位于胃,其中胃竇24例(63.2%)、胃體11例(28.9%)、胃底1例(2.6%);有2例(5.3%)位于十二指腸球部。37例病灶為單發(fā),直徑為0.4~4.0 cm,平均直徑為(1.49±0.16)cm;1例有2處病灶,直徑分別為1.2和0.8 cm,均位于胃體大彎下段前壁。
2.3 輔助檢查 38例患者行常規(guī)腹部多普勒超聲檢查,肝、膽、胰、脾均未見異常。12例患者行消化道鋇劑造影檢查,其中3例發(fā)現胃占位。10例患者行腹部增強CT檢查,其中6例提示胃壁局部隆起或增厚,增強后強化;4例未發(fā)現異常。34例患者行普通胃鏡檢查,均未提示異位胰腺,其中6例胃鏡診斷為胃間質瘤;28例診斷為黏膜下隆起性病變,無法定性。34例患者行超聲內鏡(EUS)檢查,表現為均勻或不均勻低回聲27例(79.4%)、高回聲5例(14.7%)、不均質回聲2例(5.9%),中位直徑為1.5 cm(0.7~4.0 cm);其中10例EUS檢查診斷為異位胰腺(診斷準確率29.4%),11例誤診為間質瘤,2例誤診為脂肪瘤,2例誤診為胃息肉,1例誤診為神經內分泌瘤,1例誤診為胃囊腫,1例誤診為胃囊腫伴潰瘍(黏膜下均勻低回聲,黏膜表面表現為炎性反應、潰爛),其余6例無法定性(均為黏膜下層低回聲病變)。
2.4 治療方法 34例患者接受內鏡黏膜下剝離術(ESD)治療,應用奧林巴斯GIF-XQ240電子胃鏡、Olympus GIF UM-2000內鏡超聲系統(tǒng)、UM-25R超聲探頭、高頻電凝裝置、氬氣刀等,手術過程見圖1~6。全部獲得完全切除,無患者術中出現活動性出血,5例患者術后出現明顯腹痛,4例糞便隱血陽性,經對癥處理后均好轉,無其他ESD相關并發(fā)癥。
4例患者接受外科手術治療。1例患者病灶位于胃竇后壁,大小為4.0 cm×1.5 cm,術前診斷為胃囊腫伴潰瘍(圖7A、7B),行遠端胃切除術+畢Ⅰ式吻合,病理檢查確診為異位胰腺,周圍伴胃黏膜慢性炎性反應,區(qū)域急性活動、腸化生(圖7C),同時胃大彎側淋巴結反應性增生。1例病灶位于十二指腸球部后壁(圖8A、8B),行腹腔鏡胃部分切除術+畢Ⅰ式吻合術,病理檢查證實異位胰腺組織位于肌層(圖8C)。1例因術前增強CT檢查發(fā)現胃大彎處增厚,范圍約3 cm,行胃鏡腹腔鏡聯(lián)合胃部分切除術。1例腫物位于胃底,行胃楔形切除術。4例經外科手術治療的患者術中出血量為50~400 m L,術后并發(fā)癥主要是腹腔感染、上呼吸道感染和肺部感染,經抗感染治療后均好轉。
2.5 病理檢查結果 38例標本經組織病理學檢查發(fā)現,異位胰腺組織2例位于黏膜層,30例發(fā)生于黏膜下層,1例發(fā)生于黏膜和黏膜下層,3例位于肌層,1例位于漿膜層,1例貫穿胃壁全層。
2.6 預后 38例患者術后經胃腸減壓、抑酸、抗感染和對癥支持治療后,均恢復順利,隨訪至2018年1月,無1例死亡,患者均無明顯消化道癥狀,復查胃鏡均未見明顯異常,無1例復發(fā)。

圖7 男性,48歲,以腹痛、黑便為首發(fā)癥狀
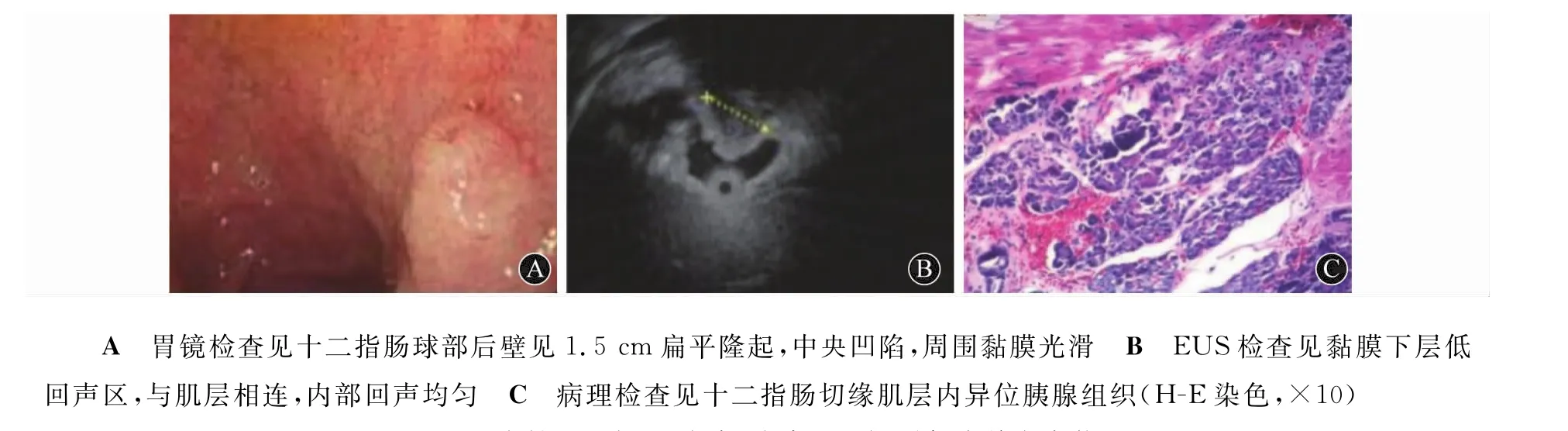
圖8 女性,36歲,以腹脹、腹痛、反酸、噯氣為首發(fā)癥狀
3 討 論
異位胰腺可發(fā)生于消化道的任何部位,最常見于胃(25%~38%),其次是十二指腸(17%~36%)和空腸(15%~21.7%),食管、膽總管、脾、腸系膜、縱隔和輸卵管等部位少見[3],不發(fā)生于結腸[4]。本研究中38例中僅2例發(fā)生于十二指腸,其余均發(fā)生于胃。異位胰腺大多為直徑<30 mm的圓形或橢圓形隆起灶[5],一般位于黏膜下層、肌層或漿膜層,臨床表現與異位胰腺的發(fā)生部位、大小等因素有關,也可無臨床表現,出現并發(fā)癥可引起相應癥狀[6],最常見癥狀是腹痛,其次為腹脹、惡心嘔吐、反酸噯氣、消化道出血等。Pessaux等[7]認為具有分泌功能的異位胰腺可形成囊性病變,本組有1例異位胰腺主要表現為腹脹、腹痛伴惡心嘔吐,胃鏡檢查見胃竇后壁4.0 cm×1.5 cm半球狀隆起,EUS檢查表現為黏膜下層低回聲區(qū),提示伴囊性變,由于異位胰腺的導管與胃腔連接不通暢,胰腺外分泌液滯留導致急性梗阻性胰腺炎反復發(fā)作,從而引起腹痛,形成的假性囊腫引起胃排空障礙,出現腹脹、惡心嘔吐癥狀。
異位胰腺的術前定性診斷較為困難,需與胃腸間質瘤、平滑肌瘤、脂肪瘤、血管瘤等相鑒別。氣鋇雙重對比造影檢查可見局灶黏膜充盈缺損,消化道造影檢查對診斷此病的意義不大。異位胰腺在CT檢查中表現為圓形或類圓形腫塊,平掃密度均勻,與正常胰腺密度相等或稍低,增強掃描多數強化,同時可提示異位胰腺有無胰腺炎、囊性變、癌變等[8-9]。有研究[10]發(fā)現,CT檢查病變位于胃竇前區(qū)或十二指腸,突向腔內,邊界模糊,黏膜增強掃描后強化,病變長徑與短徑比值>1.4,這5項CT表現同時存在2項以上時診斷特異度為82.5%,存在4項以上時診斷特異度為100%。本組中6例異位胰腺在CT檢查表現為病變位于黏膜下,局部隆起增厚,增強后強化。
診斷異位胰腺的首選方式是EUS檢查,可觀察到異位胰腺的典型表現,即黏膜隆起性病變上見開口和臍樣凹陷,這是與其他類型病變的重要區(qū)別,有助于鑒別診斷。臍樣凹陷系異位胰腺導管引流外分泌液到黏膜表面的開口,但僅<50%的病灶有此開口[11-13]。EUS檢查可觀察到異位胰腺位于消化道的黏膜下層、肌層和(或)漿膜層中,特征為回聲不均或無回聲區(qū),邊界不清[14],異位胰腺的組織成分有胰腺腺泡、導管和胰島,構成比例不全相同,因此在EUS檢查中的物理學特征也可存在差異,可有不典型表現[5]。EUS檢查與術后病理檢查診斷的符合率可達73.0%~83.0%[15-16],因此術前完善EUS檢查具有重要意義。本組中EUS檢查的診斷準確率僅為29.4%,遠低于文獻報道,可能與內鏡醫(yī)師對異位胰腺認識不足有關,也可能與樣本量較小有關。EUS引導細針穿刺術(EUS-FNA)能夠將診斷準確率提高至80%以上[17-19]。
本病發(fā)病率較低,臨床癥狀差異較大,部分患者長期無明顯不適,故是否所有異位胰腺均需要治療,目前存在爭議,但部分異位胰腺可發(fā)生急、慢性胰腺炎,以及假性囊腫、壞死、出血,甚至惡變(惡變率為0.7%~1.8%)[20-21]。目前,積極的觀點認為無論有無癥狀或病理改變均應手術切除[8];保守的觀點認為有臨床癥狀的異位胰腺予以手術切除,沒有癥狀的可定期隨訪[22]。本組4例異位胰腺患者無臨床癥狀且病灶較小(直徑<1.5 cm),考慮到本病行ESD治療的風險較小,而且患者大多不能堅持長期定期復查,故同樣予以手術切除。治療首選微創(chuàng)手術[23],如ESD治療。對于病灶較小、臨床癥狀輕微或無明顯臨床癥狀且耐受性差的患者,可暫予隨訪觀察;對于病灶直徑>10 cm或累及肌層、漿膜層者,不適合行ESD治療[24];對于病灶位于十二指腸、空腸的患者行ESD切除的風險較高,且不易完整切除,若切除過深可能導致出血、穿孔等并發(fā)癥發(fā)生,穿孔率可達20.0%,總體并發(fā)癥發(fā)生率達40%[25],此時應行腹腔鏡或開腹手術;對于病灶位于漿膜層或體積較大且貫穿胃壁全層者,可行胃鏡腹腔鏡聯(lián)合下胃部分切除術。本組有1例患者行胃鏡腹腔鏡聯(lián)合下胃部分切除術,術后病理檢查證實黏膜、黏膜下、肌層和漿膜層廣泛發(fā)現異位胰腺組織。
綜上所述,異位胰腺的臨床表現缺乏特異性,且常規(guī)檢驗、檢查手段均不易鑒別,術后病理檢查仍是唯一的確診方法。進一步提高對異位胰腺的認識,遇到黏膜下隆起型病變時,應結合EUS和CT檢查,考慮是否存在異位胰腺的可能性[8],一經發(fā)現,無論有無癥狀或病理損害,均應根據病變部位、大小、深度、生物學特性,以及手術難度和患者耐受性等綜合選擇治療方式。對于有內鏡下治療條件者,首選內鏡下微創(chuàng)手術。

