心臟病合并糖尿病患者圍術期自噬微管相關蛋白輕鏈3抗體Ⅱ水平變化及其與炎性因子水平、心肌缺血再灌注損傷的相關性研究
謝恒韜,夏中元,王娟,賈強,賈一帆
據最新全球流行病學調查顯示,2型糖尿病是常見且高發的慢性疾病之一,其較難治愈并易引起并發癥發生[1]。目前,全球約4.25億糖尿病患者,糖尿病發病率約為9%[2],我國是全世界糖尿病發病大國,患病人數約1.1億,城鎮糖尿病患者約為農村的2倍,預計到21世紀中葉,患病人數將增加至1.2億人,且呈年輕化趨勢[3-4]。2017年一項統計結果顯示,全球約400萬人死于糖尿病(我國約100萬人),其病死率位居全球死因前列,已成為威脅我國居民乃至全球公共衛生健康的主要疾病種類[5]。
糖尿病并發癥主要為全身血管病變,包括局部微血管及大血管病變,也是導致患者致殘或致死的病因。研究表明,我國糖尿病合并心血管疾病患者約占糖尿病患者總數的15%,且糖尿病引起全身代謝紊亂更增加了大血管疾病發病風險[6-7]。有研究證實,細胞自噬在心肌缺血再灌注損傷過程及2型糖尿病發生發展過程中發揮著重要作用,且適量細胞自噬能有效保護心肌,而過度細胞自噬則會加重心肌損傷[8]。細胞自噬還可通過炎性反應而影響患者術中心肌缺血再灌注損傷[9]。本研究旨在探討心臟病合并糖尿病患者圍術期自噬微管相關蛋白輕鏈3抗體Ⅱ(LC3Ⅱ)水平變化及其與炎性因子水平、心肌缺血再灌注損傷的相關性,以期為提高圍術期心臟病合并糖尿病患者心肌保護效果提供參考。
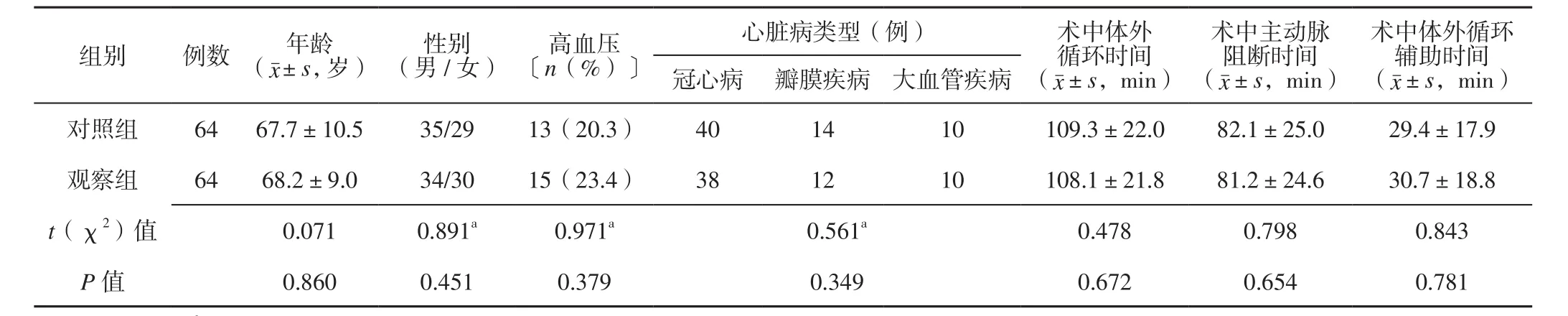
表1 兩組患者一般資料及術中體外循環時間、主動脈阻斷時間及體外循環輔助時間比較Table 1 Comparisons of general information,intraoperative duration of cardiopulmonary bypass,aortic cross clamping and auxiliary of cardiopulmonary bypass between the two groups
1 資料與方法
1.1 一般資料 選取2016—2017年武漢大學人民醫院心胸外科收治的心臟病合并糖尿病患者64例作為觀察組,均經心臟超聲、臨床體征、冠狀動脈CT造影確診;均符合糖尿病診斷標準[3]。同期選取未合并糖尿病的心臟病患者64例作為對照組。納入標準:(1)手術均在心臟停搏下進行;(2)首次心臟手術者;(3)年齡20~80歲;(4)無腫瘤、神經系統疾病者;(5)血糖控制良好者;(6)無肝、腎功能不全者。排除標準:(1)伴有凝血功能障礙者;(2)合并免疫系統疾病者;(3)住院前兩周無感染者;(4)住院前使用免疫抑制劑者。兩組患者年齡、性別、高血壓發生率、心臟疾病類型、術中體外循環時間、術中主動脈阻斷時間及術中體外循環輔助時間比較,差異無統計學意義(P>0.05,見表1),具有可比性。本研究經武漢大學人民醫院醫學倫理委員會審核批準,所有患者對本研究知情并簽署知情同意書。
1.2 手術方法 兩組患者根據冠狀動脈、瓣膜及血管病變情況選擇相應手術方法,術中給予高鉀晶體停跳液聯合血液(晶 ∶血 =1∶4)15~20 ml/kg,采用經典ST THOMAS法自制停搏液:500 ml復方氯化鈉溶液、25%硫酸鎂20 ml,10%氯化鉀30.75 ml,5%碳酸氫鈉40 ml,2%利多卡因10 ml;根據手術方式選擇根部順行灌注和經冠狀動脈開口直接灌注,同時在心臟放置冰屑進行心臟保護,待心內操作完成后,逐步減少體外循環流量,直至脫離體外循環。
1.3 LC3Ⅱ水平及炎性因子檢測 分別于手術前后抽取兩組患者清晨空腹外周靜脈血6~8 ml,加入抗凝試管,3 000 r/min 離心 10 min(離心半徑 10 cm),留取上清液并置于-80 ℃冰箱中保存待測,采用酶聯免疫吸附法檢測LC3Ⅱ、白介素6(IL-6)及白介素8(IL-8)水平,試劑盒均購自湖北黃石研科生物科技有限公司,嚴格按照試劑盒說明書進行操作。
1.4 乳酸脫氫酶(LDH)、心肌肌鈣蛋白T(cTnT)及肌酸激酶同工酶(CK-MB)水平檢測 兩組患者于術后24 h后抽取靜脈血,采用免疫化學發光法檢測LDH、cTnT及CK-MB水平。
1.5 統計學方法 采用SPSS 20.0統計學軟件進行數據分析,計量資料以(±s)表示,組間比較采用兩獨立樣本t檢驗;計數資料比較分析采用χ2檢驗;LC3Ⅱ水平與圍術期心臟病合并糖尿病患者IL-6、IL-8、LDH、cTnT、CK-MB水平的相關性分析采用Pearson相關分析。以P<0.05為差異有統計學意義。
2 結果
2.1 兩組患者手術前后LC3Ⅱ及炎性因子水平比較 兩組患者術前LC3Ⅱ、IL-6、IL-8水平比較,差異無統計學意義(P>0.05);術后觀察組患者LC3Ⅱ、IL-6、IL-8水平高于對照組,差異有統計學意義(P<0.05,見表2)。
2.2 兩組患者術后24 h LDH、cTnT、CK-MB水平比較術后24 h觀察組患者LDH、cTnT、CK-MB水平高于對照組,差異有統計學意義(P<0.05,見表3)。
2.3 相關性分析 Pearson相關分析結果顯示,LC3Ⅱ水平與圍術期心臟病合并糖尿病患者IL-6(r=0.955)、IL-8(r=0.962)、LDH(r=0.981)、cTnT(r=0.964)、CK-MB(r=0.969)水平呈正相關(P<0.01,見圖1)。
表2 兩組患者手術前后LC3Ⅱ及炎性因子水平比較(±s,ng/L)Table 2 Comparison of LC3 Ⅱ and inflammatory cytokines between the two groups before and after operation
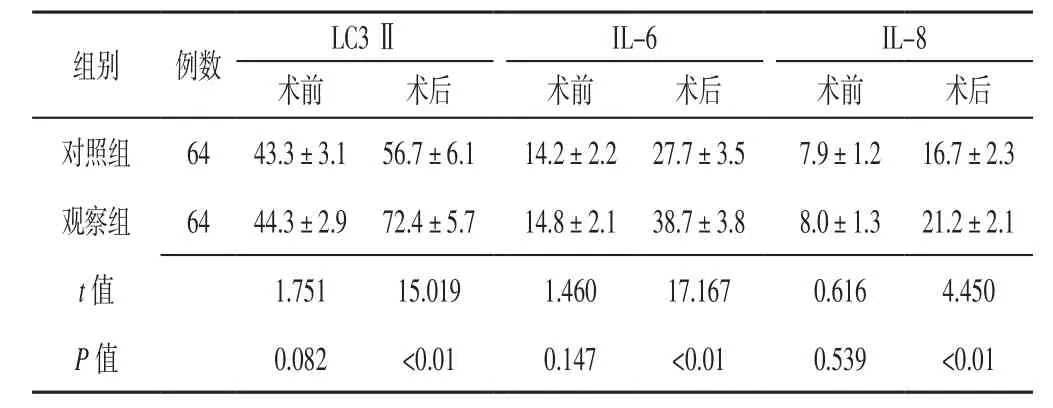
表2 兩組患者手術前后LC3Ⅱ及炎性因子水平比較(±s,ng/L)Table 2 Comparison of LC3 Ⅱ and inflammatory cytokines between the two groups before and after operation
注:LC3Ⅱ=自噬微管相關蛋白輕鏈3抗體Ⅱ,IL-6=白介素6,IL-8=白介素8
組別 例數 LC3Ⅱ IL-6 IL-8術前 術后 術前 術后 術前 術后對照組 64 43.3±3.1 56.7±6.1 14.2±2.2 27.7±3.5 7.9±1.2 16.7±2.3觀察組 64 44.3±2.9 72.4±5.7 14.8±2.1 38.7±3.8 8.0±1.3 21.2±2.1 t值 1.751 15.019 1.460 17.167 0.616 4.450 P 值 0.082 <0.01 0.147 <0.01 0.539 <0.01
表3 兩組患者術后24 h LDH、cTnT、CK-MB水平比較(±s)Table 3 Comparison of LDH,cTnT and CK-MB levels at 24 h after surgery
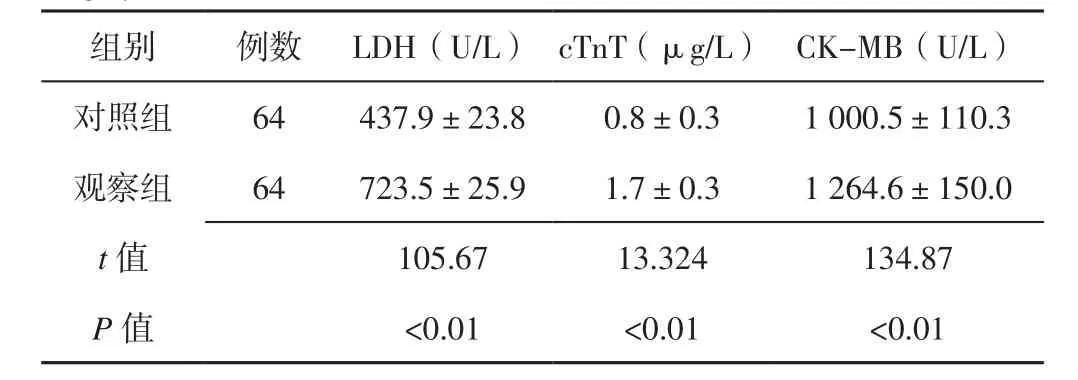
表3 兩組患者術后24 h LDH、cTnT、CK-MB水平比較(±s)Table 3 Comparison of LDH,cTnT and CK-MB levels at 24 h after surgery
注:LDH=乳酸脫氫酶,cTnT=心肌肌鈣蛋白T,CK-MB=肌酸激酶同工酶
組別 例數 LDH(U/L) cTnT(μg/L) CK-MB(U/L)對照組 64 437.9±23.8 0.8±0.3 1 000.5±110.3觀察組 64 723.5±25.9 1.7±0.3 1 264.6±150.0 t值 105.67 13.324 134.87 P值 <0.01 <0.01 <0.01
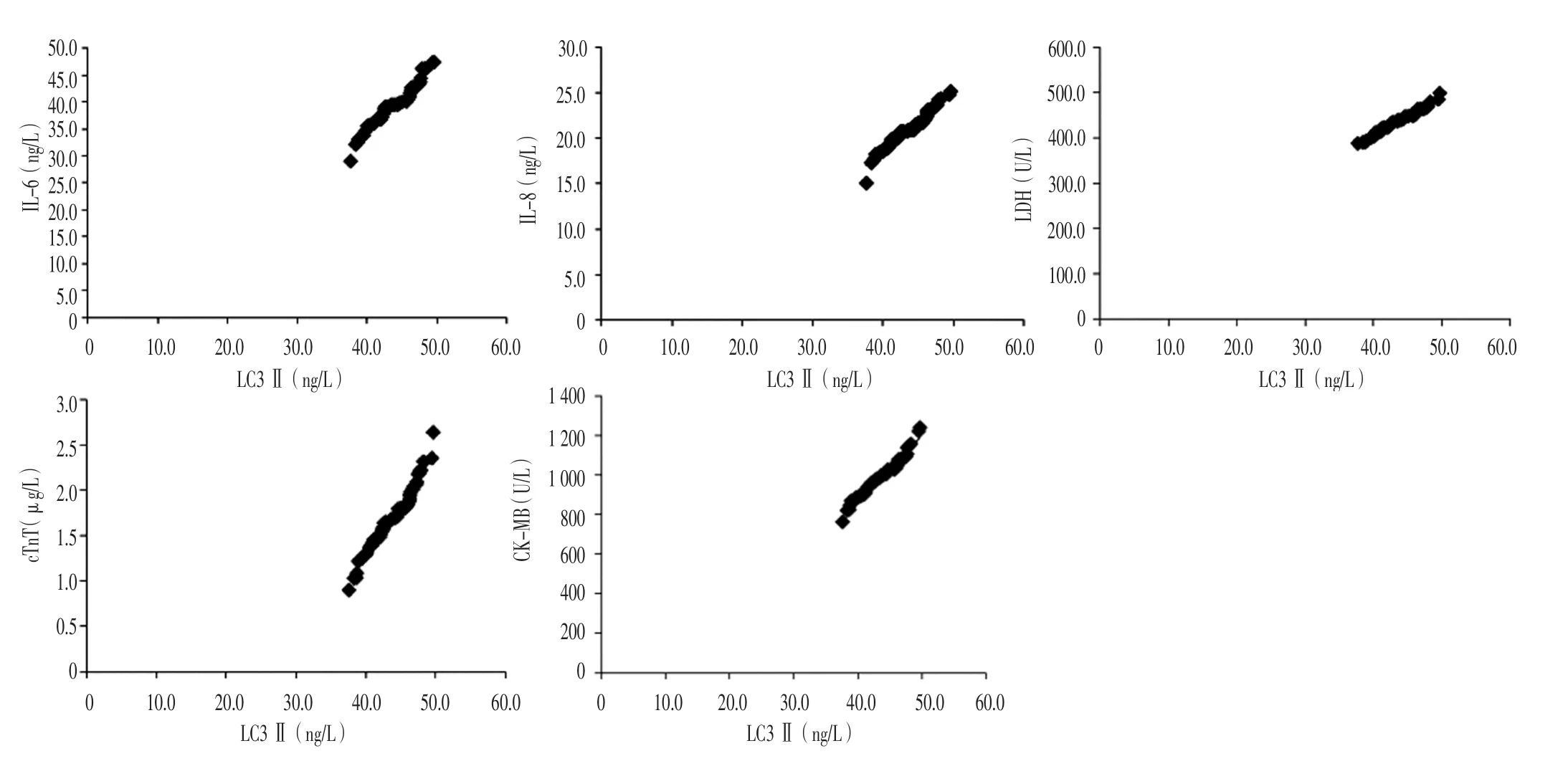
圖1 LC3Ⅱ水平與圍術期心臟病合并糖尿病患者IL-6、IL-8、LDH、cTnT、CK-MB水平相關性的散點圖Figure 1 Scatter diagramfor correlations of LC3 Ⅱwith IL-6,IL-8,LDH,cTnT,CK-MB in perioperative heart disease patients merged with diabetes
3 討論
糖尿病是一類以血糖及胰島素增高為臨床表現的代謝性疾病,長期高血糖可使機體各組織產生大量自由基,進而激發過度氧化應激反應,最終加重心臟缺血再灌注損傷[10-12]。研究表明,2型糖尿病患者心臟術后心肌再灌注損傷是非糖尿病患者的5倍[13],且術后病情危重,預后不佳,因此積極探討圍術期心臟病合并糖尿病患者自噬作用具有重要意義[14]。
研究表明,細胞自噬在心肌缺血再灌注損傷中的主要機制是細胞回收細胞質、處理多余或存在缺陷細胞器過程并轉化能量供應,對緩和心肌缺血缺氧損傷具有重要作用,但過度細胞自噬會導致細胞損傷[15-17]。LC3Ⅱ是細胞自噬的代表蛋白之一。本研究結果顯示,術后觀察組患者LC3Ⅱ水平高于對照組,提示圍術期心臟病合并糖尿病患者的自噬作用高于心臟病合并非糖尿病患者,與既往研究結果一致[18];分析其發生病理機制可能是:糖尿病患者細胞發生無氧代謝引起細胞表面膜蛋白、突觸蛋白、信號激酶及細胞凋亡因子和促炎因子等異常改變,自噬作用增強,進而影響細胞穩態,破壞細胞器正常功能,從而觸發線粒體細胞凋亡通路,引起細胞能量代謝,最終加重細胞損傷。細胞自噬還可抑制中性粒細胞功能,加重心肌缺血再灌注早期炎性反應。本研究結果顯示,術后觀察組患者IL-6、IL-8水平高于對照組,且LC3Ⅱ水平與圍術期心臟病合并糖尿病患者IL-6、IL-8水平呈正相關,提示心臟病合并糖尿病患者圍術期過度的自噬作用會增加機體炎性因子水平[19]。
LDH、cTnT、CK-MB是評估心臟損傷的主要標志物。本研究結果顯示,觀察組患者術后24 h LDH、cTnT、CK-MB水平高于對照組,且LC3Ⅱ水平與圍術期心臟病合并糖尿病患者LDH、cTnT、CK-MB水平呈正相關,提示與心臟病合并非糖尿病患者相比,心臟病合并糖尿病患者術后心肌缺血再灌注損傷程度較重,且與過度自噬作用有關[20];分析其發生機制可能是由于糖尿病加重機體的自噬作用,而過度自噬又會損傷內皮細胞而加重炎性反應,進而加重患者心臟缺血再灌注損傷[21-22]。
綜上所述,心臟病合并糖尿病患者圍術期LC3Ⅱ水平較高,且LC3Ⅱ水平與炎性因子水平及心肌缺血再灌注損傷有關;但本研究為單中心研究,且樣本量較小,未來仍需聯合多中心、擴大樣本量進一步研究自噬作用在心臟病合并糖尿病患者中的作用機制。
作者貢獻:謝恒韜進行試驗設計與實施、資料收集整理、撰寫論文并對文章負責;王娟、賈強、賈一帆進行試驗實施、評估、資料收集;夏中元進行質量控制及審校。
本文無利益沖突。

