基于線粒體COⅠ序列的南海北部櫛江珧遺傳多樣性分析
于非非 鐘智明 牛素芳 杜曉東 許開航 林子騰 張穎懿 王家晉 劉漫玲
(廣東海洋大學水產學院, 湛江 524088)
櫛江珧(Atrina pectinata), 隸屬于軟體動物門(Mollusca), 瓣鰓綱(Lamellibranchia), 貽貝目(Mytiloida), 江珧科(Pinnidae), 江珧屬(Atrina)[1], 有帶子、大海紅、海锨、大海蕎麥、土杯、馬蹄等俗稱。櫛江珧為一種廣溫、廣鹽的穩居性貝類, 廣泛分布于溫、熱帶泥沙質近海地區, 我國的渤海、黃海、東海和南海四大海域均有分布, 其中南海是我國櫛江珧分布種類最多、產量最高的海區[1]。櫛江珧閉殼肌肥大、肉質鮮嫩, 具有較高的經濟價值和藥用價值[2], 在我國南海沿岸地區備受歡迎。然而, 櫛江珧的人工養殖技術尚不完善, 一般采用半人工養殖方法, 即采捕野生櫛江珧苗種、然后選擇合適海區進行集中養殖的方式[3]。多年的過度捕撈和人工養殖的相對滯后使櫛江珧的野生資源遭到大量破壞, 種質資源明顯退化[4]。這與南海沿岸日益上升的需求量相違背, 對南海櫛江珧資源進行調查和保護成為亟待解決的科學問題。
細胞色素氧化酶亞單位Ⅰ(Cytochrome Oxidase Ⅰ,COⅠ)是一種線粒體DNA標記, 因其結構簡單、進化速度快、母系遺傳、易于擴增等特點,被廣泛應用于不同生物群體的遺傳多樣性分析[5]。近年來有研究者基于COⅠ序列對不同地理位置櫛江珧的群體遺傳性進行了分析, 如嚴加坤等[4]調查了長島、日照、文登、湛江、海口五個城市的野生櫛江珧資源, 發現南方群體和北方群體之間存在極大遺傳分化, 而南北方群體內部幾乎沒有遺傳分化。Xue等[6]利用COⅠ基因分析了遼寧獐子島、山東蓬萊、山東劉公島、山東榮成、山東紅島、山東日照、江蘇連云港、浙江舟山、福建福州和韓國海州(Haeju)8個地區的櫛江珧資源, 發現來自中國北方海域的7個群體雖然遺傳多樣性較高, 但沒有遺傳分化; 而中國和韓國樣品間存在明顯的遺傳分化。以上利用COⅠ基因對櫛江珧的研究多聚焦在中國北部海域, 或者更關注南北方海域群體的差異, 而對于櫛江珧分布種類最多、產量最高的南海北部海域群體內部的資源調查研究較少。
本研究基于COⅠ基因序列對我國南海北部7個沿海城市的櫛江珧群體進行群體遺傳學研究,從遺傳多樣性、遺傳分化和歷史動態探討南海北部櫛江珧的系統地理格局, 以期闡明南海北部櫛江珧的群體遺傳特征, 評估其遺傳資源狀況, 為資源保護、人工養殖和良種選育提供理論儲備。
1 材料與方法
1.1 樣品采集
采集了汕頭(ST)、陽江(YJ)、湛江(ZJ)、海口(HK)、瓊海(QH)、北海(BH)、防城港(FCG)近海等7個海區野生群體, 共191只櫛江珧個體(圖1和表1)。對所有樣品進行形態學鑒定后取其閉殼肌,-80℃保存備用。

圖1 南海北部櫛江珧7個群體的采樣地點Fig. 1 Sample locations for seven A. pectinata populations from the Northern South China Sea
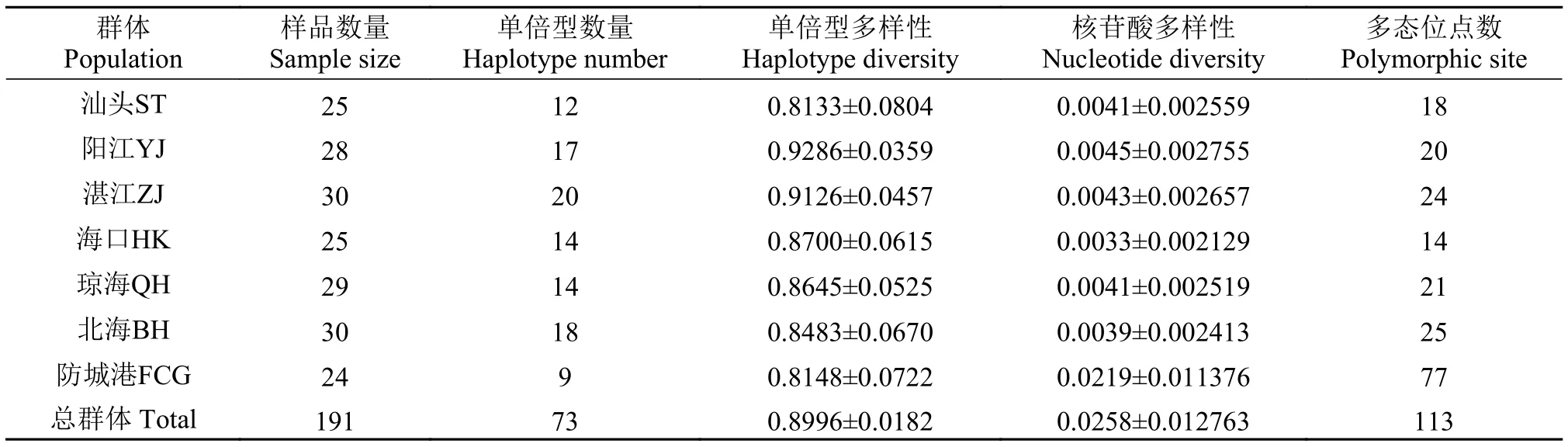
表1 南海北部櫛江珧7個群體的采樣信息和遺傳多樣性參數Tab. 1 The sampling information and genetic diversity indices for 7 A. pectinata populations from the Northern South China Sea
1.2 DNA提取和目的基因的擴增
用E.Z.N.A.R Tissue DNA試劑盒(OMEGA)提取各樣品基因組DNA, 1%瓊脂糖凝膠電泳檢測DNA的純度和濃度。COⅠ基因片段擴增所用引物序列為: LCO1490 (GGTCAACAAATCATAAA GATATTGG)和HCO2198 (TAAACTTCAGGGT GACCAAAAAATCA)。PCR反應體系為25 μL 2×EasyTaqPCR SuperMix (TransGen)、正反引物(10 μmol/L)各1 μL, 基因組DNA (100 ng/μL) 2 μL,ddH2O補齊50 μL。PCR反應程序為: 94℃預變性3min; 94℃變性30s, 57℃退火30s, 72℃延伸1min,35個循環; 最后72℃延伸10min。PCR產物經1%瓊脂糖凝膠電泳檢測后由生工測序。
1.3 數據處理
利用DNAStar 7.1和Clustal X 1.81[7]進行序列校對和編輯; 利用DnaSP 5.10.01[8]計算單倍型數目、單核苷酸變異位點數和多態簡約信息位點數;利用Arlequin 3.5.1.2[9]統計序列的平均堿基組成, 計算單倍型多樣性(h)和核苷酸多樣性(π)等群體遺傳學參數; 利用MEGA 6.06[10]計算轉換百分比、顛換百分比和轉換/顛換比率(Ts/Tv), 選擇DNA序列的最佳替換模型。利用MrBayes 3.2.6構建單倍型系統進化樹, 利用Network5.0.0.1(http://www.fluxus-engineering.com/share-net.htm)中的中介連接網絡法構建單倍型網絡支系圖[11]
群體遺傳結構采用3種方法進行分析: (1)采用分化固定指數Fst評價兩兩群體間的遺傳差異, 檢驗結果的顯著性; (2)根據樣品來源、遺傳學參數和Fst, 將7個櫛江珧群體劃分為2個組: 汕頭(ST)、陽江(YJ)、湛江(ZJ)、海口(HK)、瓊海(QH)和北海(BH)6個櫛江珧群體為一組(L1組), 防城港群體(FCG)單獨為一組(L2組), 通過AMOVA分析估算遺傳變異在組群間、組群內群體間和群體內的分布,進行顯著性分析; (3)通過Exact檢驗檢測單倍型在群體間分布頻率的差異。
群體歷史動態采用2種方法進行檢測: (1)采用Tajima'sD檢驗和Fu'sFs檢驗檢測中性假說是否成立, 并進行顯著性分析; (2)基于核苷酸不配對分布檢驗南海北部櫛江珧群體是否存在數量和空間擴張, 并通過擬合優度檢驗(Goodness of fit test)檢測核苷酸不配對的觀測分布和預期分布之間的一致性, 并估算群體歷史擴張時間。在本研究中,COⅠ基因的分化速率采用2.4%/MY (Million year, MY)[6],世代時間設置為1年[12]。
2 結果
2.1 序列分析
本研究共獲得7個群體191條長度為600 bp的COⅠ基因部分序列, 其G、C、A、T的平均含量分別為24.05%、14.81%、19.18%和41.96%。共檢測到113個核苷酸變異位點(18.8%), 包括14個單核苷酸變異位點, 99個多態簡約信息位點, 無插入和缺失位點。轉換數共有107次, 明顯高于顛換數(19次),Ts/Tv=15.33。轉換和顛換在G、C、A、T之間均有發生, 其中C-T (53.68%)轉換多于G-A(40.88%)轉換, T-G (1.79%)和T-A (1.66%)顛換稍多于C-G (1.05%)和C-A (0.92%)顛換。突變位點均勻地分布在COⅠ基因上, 但在群體間的分布差異較大, 77個多態位點來源于FCG群體。
2.2 單倍型和遺傳多樣性分析
COⅠ單倍型在7個群體中的分布見表1和表2。113個核苷酸變異位點共定義73個單倍型(Gen-Bank登錄號為MH536017—MH536089), 包括58個獨有單倍型和15個共享單倍型。在共享單倍型中,3個單倍型(H23、H36和H44)為6個群體所共有,1個單倍型(H2)為5個群體所共享, 1個單倍型(H29)為3個群體所共享, 10個單倍型(H1、H18、H20、H34、H47、H51、H52、H54、H61和H62)為2個群體所共享。H44出現的頻率最高(占總樣品的31.41%), 這表明這個單倍型是南海北部櫛江珧在長期進化過程中形成的較為穩定的優勢基因型。值得注意的是, 防城港群體具有9個單倍型(H65-H73), 均為獨有單倍型。
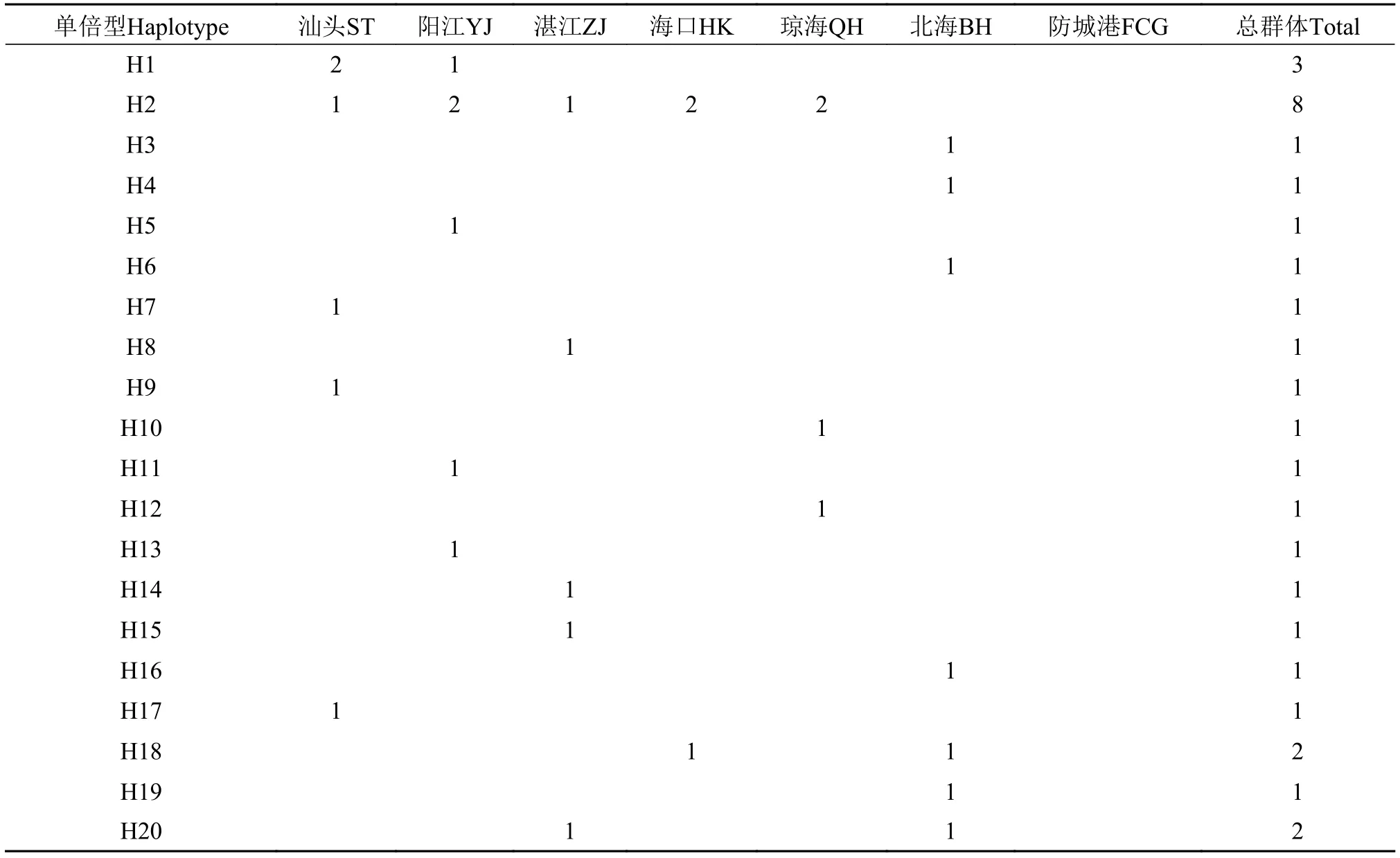
表2 南海北部櫛江珧7個群體的單倍型分布情況Tab. 2 Haplotype distribution of 7 A. pectinata populations from the Northern South China Sea

續表2
遺傳多樣性參數如表1所示, 南海北部櫛江珧總群體的單倍型多樣性和核苷酸多樣性分別為0.8996和0.0257, 表明南海北部櫛江珧群體的遺傳多樣性目前仍處于較高的水平。在7個群體中,L1組6個群體的單倍型多樣性為0.8133—0.9286, 核苷酸多樣性為0.0033—0.0045, 表現出高h低π遺傳多樣性模式; 而防城港群體的單倍型多樣性為0.8148, 核苷酸多樣性較高(0.0219), 表現出高h高π遺傳多樣性模式。
2.3 群體遺傳學關系分析
以旗江珧(Atrina vexillum)COⅠ基因序列為外群, 構建櫛江珧73個單倍型的貝葉斯推理樹(圖2)。結果顯示, L1組6個群體的各單倍型交叉出現在系統發育樹中, 并未表現出與地理位置相對應的譜系結構; L2組的獨有單倍型(H65-H73)聚為一個獨立的進化分支, 顯示了較遠的遺傳距離。單倍型網絡支系圖(圖3)具有1個主體單倍型(H44), 該主體單倍型在6個群體中均有分布, 且出現頻率較高,說明它可能是起源于母系祖先的主體單倍型; 其他單倍型呈輻射狀分布在主體單倍型周圍, 其中L2組的9個獨有單倍型作為一個獨立分支, 與其他單倍型具有較遠的遺傳距離。這暗示著南海北部櫛江珧北部灣的防城港群體與其他群體間存在顯著的遺傳結構。

圖2 南海北部櫛江珧COⅠ單倍型貝葉斯推理樹Fig. 2 Bayesian inference tree for A. pectinata from the Northern South China Sea based on COⅠ
2.4 群體遺傳結構
由表3可知, L1組6個群體間的Fst值均較小(-0.0200— -0.0055), 且統計學差異不顯著(P>0.05);但L 2組與L 1組6個群體間的Fst值均較大(0.8729—0.8821), 且統計學差異極顯著(P<0.01)。分子方差分析(Analysis of molecular variance, AMOVA)結果顯示(表4), 組群間、組群內群體間和群體內個體間的遺傳變異比例分別為97.01%、-0.1%和3.09%, 組群間、組群內群體間和群體內個體間的固定系數Fct、Fsc和Fst分別為0.9701 (P>0.05)、-0.0324 (P>0.05)和0.9691 (P<0.01)。Fst值和AMOVA結果表明, L1組6個群體間在分子水平不存在明顯的遺傳分化, 但L2組與L1組6個群體間存在顯著遺傳分化。Exact檢驗結果顯示, 單倍型在L1組6個群體間的分布頻率并無顯著差異, 但在L2組與L1組間差異顯著。
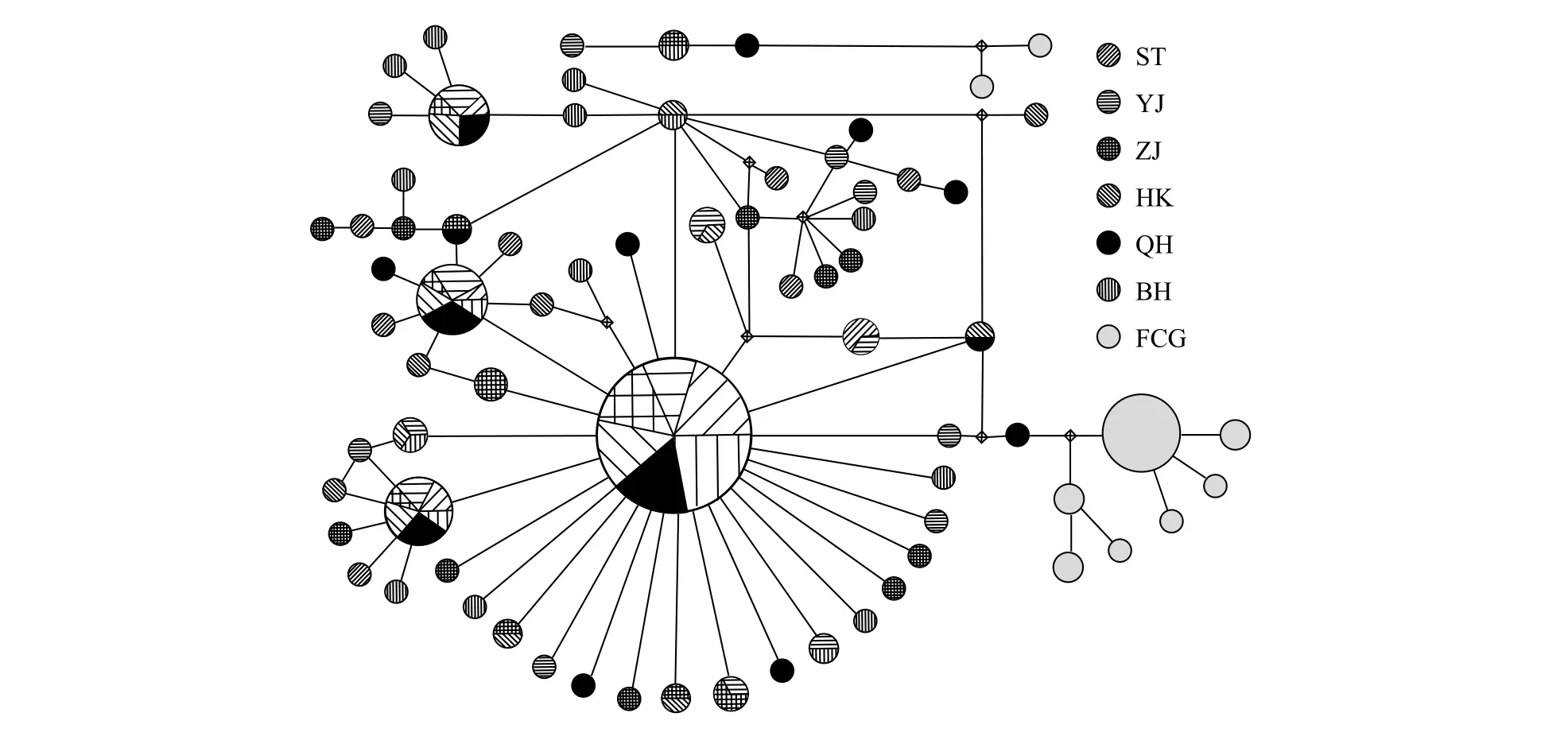
圖3 南海北部櫛江珧COⅠ單倍型支系圖Fig. 3 Haplotype network of A. pectinata from the Northern South China Sea based on COⅠ
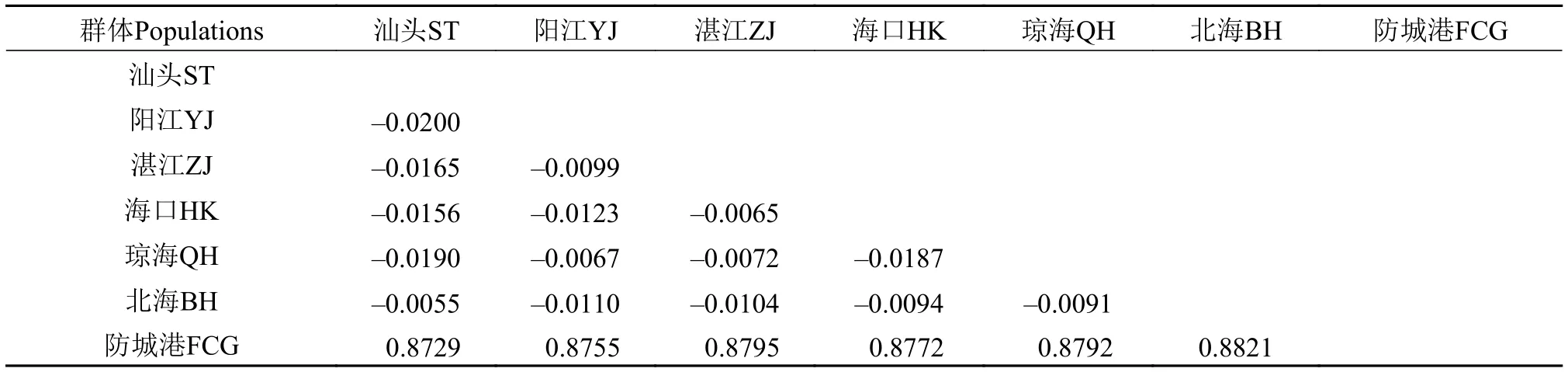
表3 南海北部櫛江珧7個群體間的遺傳分化指數FstTab. 3 The pairwise Fst among seven populations of A. pectinata from the Northern South China Sea

表4 南海北部櫛江珧7個群體間的AMOVA分析Tab. 4 Analysis of molecular variance (AMOVA) among seven populations of A. pectinata from the Northern South China Sea
2.5 群體歷史動態
由于FCG群體與其他6個群體間具有顯著的遺傳分化, 故將FCG群體單獨進行歷史動態分析。中性檢驗結果顯示, FCG群體所在L2組的Tajima'sD檢驗(D= -1.4320,P=0.0565)為不顯著負值, Fu'sFs檢驗(Fs=4.9540,P=0.9620)為不顯著正值, 說明FCG群體進化符合中性假說。L1組6個群體間無顯著的遺傳分化, 故將其合并為一個大群體進行歷史動態分析。結果顯示, Tajima'sD檢驗(D= -2.3190,P=0)和Fu'sFs檢驗(Fs= -26.8316,P=0)均為顯著負值。基于數量擴張模型和空間擴張模型的核苷酸不配對分布均呈單峰分布(圖4), 且觀測分布和期望分布擬合優度較好(SSD),Hri值小且不顯著(表5)。中性檢驗和核苷酸不配對分布結果均提示南海北部櫛江珧L1組6個群體在歷史上可能發生過數量和棲息地擴張事件。數量擴張模型和空間擴張模型下的τ值分別為1.2830和1.0880 (表5), 據此推算南海北部櫛江珧群體擴張時間約在75500—89000年前。
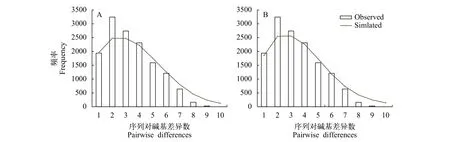
圖4 南海北部櫛江珧總群體COⅠ核苷酸不配對分布圖Fig. 4 Mismatch distributions of A. pectinata from the Northern South China Sea based on COⅠ
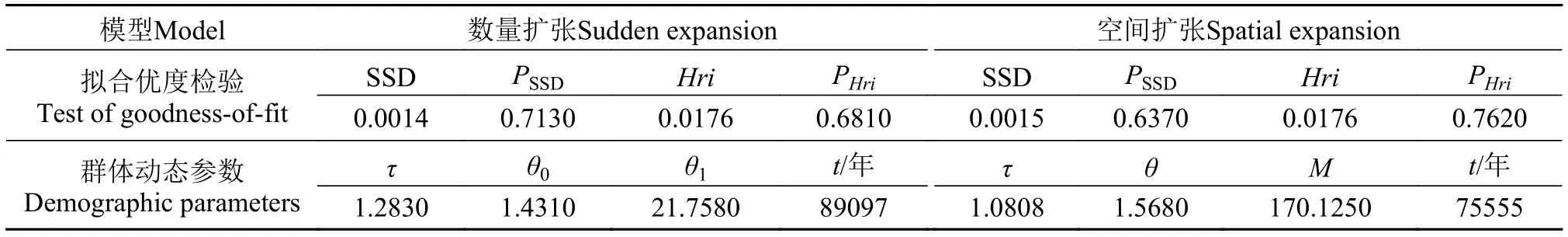
表5 南海北部櫛江珧總群體COⅠ核苷酸不配對分布參數Tab. 5 Mismatch distribution indices of A. pectinata from the Northern South China Sea based on COⅠ
3 討論
3.1 群體遺傳多樣性
單倍型多樣性(h)和核苷酸多樣性(π)是衡量物種遺傳多樣性的2個重要指標[13]。在本研究中, 南海北部櫛江珧L1組群呈現出較高的單倍型多樣性(0.8133—0.9286)和較低的核苷酸多樣性(0.0033—0.0045), 即高h低π模式。這種高h低π的遺傳參數特征通常是由一個較小的有效群體經過近期快速擴張成一個大的群體所引起的[14]。在末次冰盛期, 南海海平面下降約100—120 m, 變成一個半封閉的內陸海(圖1), 成為眾多海洋生物的冰期避難所[15,16]。在冰期惡劣的環境下, 南海櫛江珧的分布范圍和數量可能經歷了一定程度的收縮; 隨著間冰期氣溫回升, 海平面上升, 產生大量近岸棲息地, 冰期避難所內殘留的櫛江珧可能發生快速擴張重新進入南海大陸架。此過程南海櫛江珧群體積累了單倍型的多樣性, 但尚缺乏足夠的時間積累核苷酸序列的多樣性[11]。而防城港群體顯示了較高的單倍型多樣性(0.8148)和核苷酸多樣性(0.0219), 這暗示著北部灣豐富的生態資源和相對穩定的生存環境對櫛江珧保持遺傳多樣性產生了重要影響。
單倍型多樣性和核苷酸多樣性分析結果表明,南海北部櫛江珧群體的遺傳多樣性目前仍處于較高的水平, 這可能與櫛江珧廣闊的生境范圍有關。櫛江珧在我國東海、渤海、黃海和南海海域均有分布, 廣闊的生境范圍使其面臨較小的自然選擇壓力, 積累較多的遺傳變異。雖然自第四紀以來, 全球溫度的大幅度升降使許多物種的遺傳多樣性損失嚴重[17], 但櫛江珧作為一種底棲動物可能受到的影響較小, 保留了較高的遺傳多樣性。
3.2 群體遺傳結構
在本研究中, AMOVA分析、Fst值、單倍型系統發育樹和網絡支系圖結果均表明, L1組6個櫛江珧群體的遺傳差異不顯著, 不存在顯著的群體遺傳結構。造成L1組6個群體遺傳分化不顯著的原因可能有三點: 一是擴散生活史特征。對于有幼蟲階段的海洋生物, 浮游期(Pelagic larval duration, PLD)對于基因交流和遺傳結構具有重要影響[18,19]。櫛江珧的浮游期約30d左右, 比櫛孔扇貝(Chlamys farreri)(約15d)、中國蛤蜊(Mactra chinensis)(約10d)等雙殼類具有更長的浮游期[18], 這暗示著櫛江珧具有較強的擴散能力, 可以越過地理環境和水深條件,產生更多的基因交流。二是洋流的輸送作用。南海沿岸櫛江珧5月份進入成熟期和排放期, 排放期可一直延續到12月份, 在此期間櫛江珧的性腺分批多次排放[20]。西南季風漂流、南海暖流、粵東沿岸流和海南島以東沿岸流等北向海流[21,22]有利于QH、ZJ等地方群體卵和幼蟲的的北上擴散; 而東北季風漂流、廣東沿岸流和黑潮南海分支等南向海流[21,22]則可促進ST群體向南遷移, 從而進行基因交流。三是目前一般認為海洋生物是從海洋到陸地的遷移方式, 陸地周圍的淡水、濁流和人類活動對生物體的擴散形成一個地理和生態的障礙[23]。但櫛江珧適應能力強, 從潮下帶到水下100 m、泥質或砂質海區皆可分布[24,25], 這意味著櫛江珧比其他貝類具有更強的克服地理和生態障礙的能力, 能夠被洋流輸送更遠的距離, 產生更多的基因交流。
值得一提的是防城港群體與其他6個群體間產生了明顯的遺傳分化, 具有顯著的遺傳結構, 有3個可能的解釋: 一是北部灣是一個半封閉的海域, 位于大陸架邊緣, 于古近系斷陷期形成, 南海櫛江珧很可能在此時期發生了分化[26], 其中L1組群隨后進行了大規模擴散, 而防城港群體由于地理位置所限,擴散程度則相對較小, 經過多年積累形成了遺傳分化。二是基于生態競爭不相容原理。當兩個相近的物種或個體共存于一個相對狹小的生境中時, 他們可能會劃分生存空間和食物資源, 以最大程度地減少生態位重疊和競爭[27,28]。長期空間和食物的差異導致兩個物種最終產生遺傳分化, 尤其體現在防城港群體和北海群體間。三是北部灣的自然資源對于櫛江珧群體而言非常豐富, 尤其是紅河的匯入帶來了豐富的海底沉積物。北部灣的紅樹林資源亦很豐富, 空間異質性強, 可以作為雙殼類幼蟲的天然屏障, 不但給幼蟲提供了多樣性的食物和小生境, 也減少其他物種對幼蟲的掠奪[26,29], 從而使北部灣狹小空間內產生多樣性的系統分化成為可能。
3.3 資源管理
目前, 南海北部櫛江珧種質資源明顯退化[4], 而物種的遺傳多樣性是生存和進化的前提, 豐富的遺傳多樣性意味著較大的進化潛力, 也是生物適應環境變化的必要條件[30]。本研究表明, 北部灣防城港櫛江珧群體COⅠ的遺傳多樣性水平較高; 汕頭、陽江、湛江、海口、瓊海和北海6個群體的遺傳多樣性相對偏低, 其中海口群體的遺傳多樣性最低。為避免櫛江珧種質資源嚴重衰退的現象, 應當加強櫛江珧的管理和保護, 尤其是面臨較大捕撈壓力的南海北部沿岸群體。

