小麥穗部性狀和株高的QTL定位及T6VS·6AL易位效應分析
胡文靜,高德榮,,陸成彬,梁秀梅,石宜宗,程順和,
(1.江蘇里下河地區農業科學研究所/農業農村部長江中下游小麥生物學與遺傳育種重點實驗室,江蘇揚州 225007; 2.長江大學農學院,湖北荊州 434023)
迄今,已有諸多國內外學者利用不同的群體對小麥總小穗數、千粒重、穗粒數、穗長和株高進行了QTL定位[1-6]。但由于穗部性狀間關系錯綜復雜,都是受多基因控制的數量性狀,且受環境影響較大[7-8],導致前人在一些穗部性狀的研究上結果差異較大,很大程度上限制了其在遺傳育種中的應用。
穗粒數是重要的產量構成因素,而總小穗數和每小穗結實粒數共同決定了穗粒數,因此,通過減少不育小穗數,并增加穗頂部和基部小穗的結實粒數,可進一步增加小麥產量。Ma等[9]利用望水白和南大2419構建的RIL群體和IF2群體對小麥穗基部不育小穗數進行了QTL定位,在13個染色體區段檢測到與基部不育小穗數相關的位點。Li等[10]利用川35050和山農483構建的RIL群體檢測到8個控制不育小穗數的QTL。Wu等[11]利用旱選10號和魯麥14構建的DH群體在不同干旱脅迫條件下檢測到24個控制不育小穗數的QTL。Xu等[12]利用小偃54和京411構建的RIL群體在不同的氮肥和磷肥環境下檢測到控制不育小穗數的QTL。Cui等[13]利用溫麥8號和煙農19、溫麥8號和濟麥20構建的兩個RIL群體檢測到與可育小穗數相關的QTL。株高與小麥產量的提高密切相關,國內外學者在小麥21條染色體上相繼定位出50多個株高相關QTL[14-16],且已經命名了27個主效的矮稈基因(Rht),Rht1、Rht2、Rht3和Rht10分別被克隆[17-18],其他矮稈基因研究也取得了一定的進展[19-21]。目前育種中利用最多的矮稈基因是Rht1、Rht2、Rht8、Rht9和Rht10。
揚麥17和揚麥18是江蘇里下河地區農業科學研究所育成的抗病優質小麥品種和矮稈大穗白粉病免疫小麥品種,本研究利用揚麥17和揚麥18創制的206個單株組成的F2群體為材料構建遺傳連鎖圖譜,并結合F2和F2:3群體的表型數據進行小麥穗部性狀和株高QTL定位,以期發掘新的穗部性狀和株高QTL,為分子標記輔助育種提供材料和技術支撐。
1 材料與方法
1.1 材 料
1.1.1 植物材料
以普通小麥揚麥18為父本,揚麥17為母本雜交獲得F1代,F1自交得到206株F2植株,F2按單株收種,獲得F2:3群體。揚麥18的穗頂部、基部結實性狀明顯好于揚麥17。簇毛麥( 2n = 14,VV) 種質來自英國劍橋植物園。抗性供體南農P045是由南京農業大學細胞遺傳研究所培育的T6VS·6AL抗白粉病易位系(含PM21)。
1.1.2 引物
所用的2 403對SSR引物可覆蓋小麥全基因組,全部由農業部長江中下游小麥生物學與遺傳育種重點實驗室(江蘇里下河地區農業科學研究所)提供,由上海捷瑞生物有限公司合成。其引物序列和退火溫度通過GrainGenes數據庫或Somers 等(2004)公布的遺傳圖譜可查。
1.2 方 法
1.2.1 田間試驗和表型調查
親本材料、F2及其F2:3家系分別于2015-2016年度、2016-2017年度種植于江蘇里下河地區農業科學研究所灣頭基地試驗田。其中,F2群體按單株種植;F2:3家系按株行種植,2次重復;行長1.3 m,行距35 cm,每行點播30粒,栽培管理同大田生產,小麥生長季未見嚴重病蟲害和倒伏。
2016和2017年分別于小麥灌漿后期調查主莖的穗粒數、總小穗數、不育小穗數、穗頂部結實粒數、穗基部結實粒數、穗長和株高。其中,穗頂部結實粒數為頂部第一小穗、第二小穗和第三小穗結實粒數之和;穗基部結實粒數為基部第一小穗、第二小穗和第三小穗結實粒數之和。親本P1和P2分別調查50株;F2群體調查每個單株;F2:3群體按株行調查,每行隨機選取10株,取平均值,并調查2個重復。
教學中筆者發現,學生對1平方分米的表象往往停留在邊長為1分米的小正方形上,觀察后感悟:原來1平方分米不一定是邊長1分米的正方形,可以是相應的其他圖形。這一做法幫助學生突破思維定勢,發展面積守恒觀念。
1.2.2 DNA提取和PCR擴增
取親本和F2群體的苗期葉片,采用常規CTAB法提取DNA,PCR體系與程序參考Taq酶(北京天根生化科技有限公司)說明書,循環數35,延伸時間為45 s,退火溫度取決于不同引物。采用8%的非變性聚丙烯酰胺凝膠電泳分離PCR擴增產物,銀染檢測,觀察記錄結果并拍照保存。F2群體苗期用能夠追蹤T6VS·6AL易位染色體的6V染色體短臂末端共顯性標記MBH1[22]進行鑒定,其正向引物序列為5′-GCCATTATAGTCAAGAGTGCACTAGCTGT-3′,反向引物序列為5′-AGCTCCTCTCGTTCTCCAATGCT-3。
1.2.3 數據分析
用 Microsoft Excel 2013對數據進行整理,用SPSS 22.0對親本的穗部相關性狀和株高進行獨立樣本t測驗,并同時對 F2和 F2:3群體中所調查的性狀進行統計和相關性分析。
1.2.4 連鎖圖譜的構建和QTL分析
利用JoinMap 4.0軟件并采用Kosambi函數構建遺傳圖譜,用WinQTLCart 2.5軟件選擇復合區間作圖法進行QTL定位分析[23],若LOD值>2.5,就認為該處存在一個有效的QTL,同時分析其加性效應和貢獻率。以“Q+性狀名稱縮寫+群體英文縮寫+染色體名稱+QTL次序”[24]對QTL進行命名。
2 結果與分析
2.1 表型性狀及相關性分析
由表1可知,除總小穗數外,揚麥17與揚麥18在穗部相關性狀和株高上均具有顯著或極顯著差異。其中,揚麥18的穗頂部結實粒數、穗基部結實粒數和穗粒數在表型上屬于高值親本,而揚麥17的總小穗數、不育小穗數和株高在表型上屬于高值親本。此外,穗長性狀表現為揚麥17<揚麥18。F2:3群體中的偏度和峰度的絕對值都小于1,即滿足正態分布。同時,各性狀存在明顯的雙向超親分離現象,表明均為多基因控制的數量性狀。
相關性分析結果(表2)表明,在揚麥17/揚麥18的F2:3群體中,穗粒數與不育小穗數呈極顯著負相關,而與總小穗數、穗頂部結實粒數、穗基部結實粒數以及穗長均呈極顯著正相關,與株高呈顯著正相關;穗頂部、基部結實粒數與不育小穗數呈極顯著負相關,尤其穗基部結實粒數與不育小穗數之間呈高度負相關。以上結果表明,不育小穗數的減少,穗頂部結實粒數、穗基部結實粒數、穗長以及總小穗數的增加,均有利于穗粒數的增加。
2.2 遺傳連鎖圖譜的構建
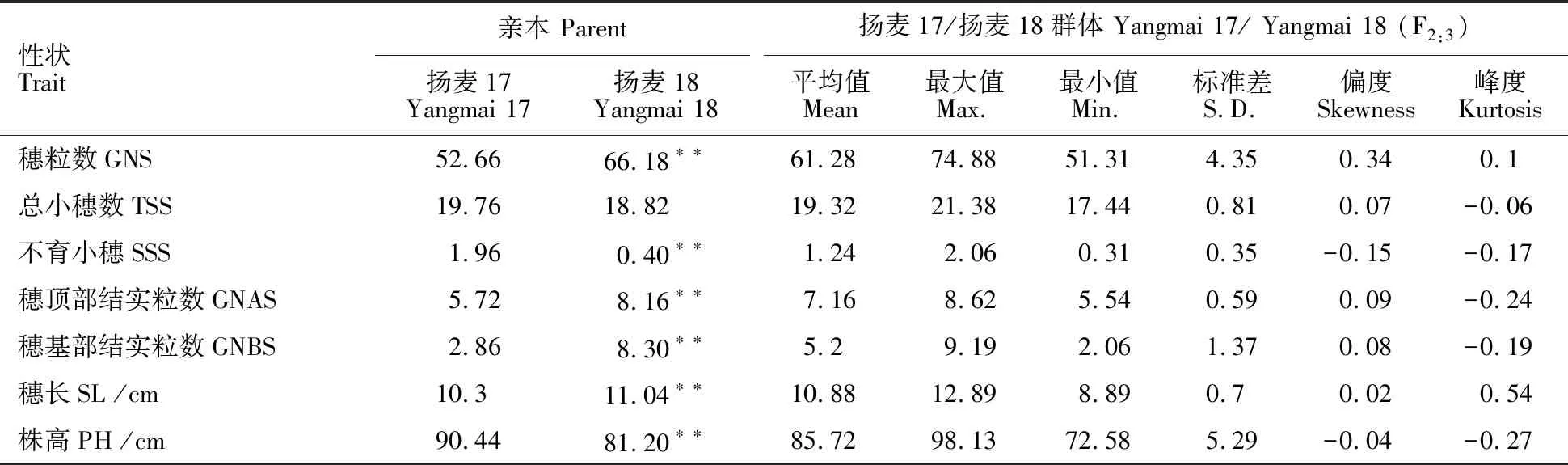
表1 揚麥17/揚麥18的F2:3群體穗部性狀和株高的變異Table 1 Phenotypic variation of spike traits and plant height in the F2:3 population of Yangmai 17/Yangmai 18
GNS:Grain number per spike; TSS:Total spikelet number per spike; SSS:Sterile spikelets; GNAS:Grain number in top spikelet;GNBS:Grain number in basal spikelet; SL:Spike length; PH:Plant height.The same in tables 2-4.
** 表示與揚麥17的差異達到極顯著水平(P<0.01)。
** indicates the difference reached to the extremely significant level compared with Yangmai 17(P<0.01).

表2 揚麥17/揚麥18F2:3群體中穗部各性狀之間的相關系數Table 2 Correlation coefficients for all traits in the F2:3 population of Yangmai 17/Yangmai 18
*和** 分別表示相關性達到顯著(P<0.05)和極顯著(P<0.01)水平。
*and ** indicate the correlation reaching the significant level at 0.05 and 0.01 levels,respectively.
2.3 QTL定位分析
基于復合區間作圖法,共定位到15個控制穗部性狀和株高的QTL,分布在2B、2D、4B、5A、5B、7A染色體上(圖1和表3)。
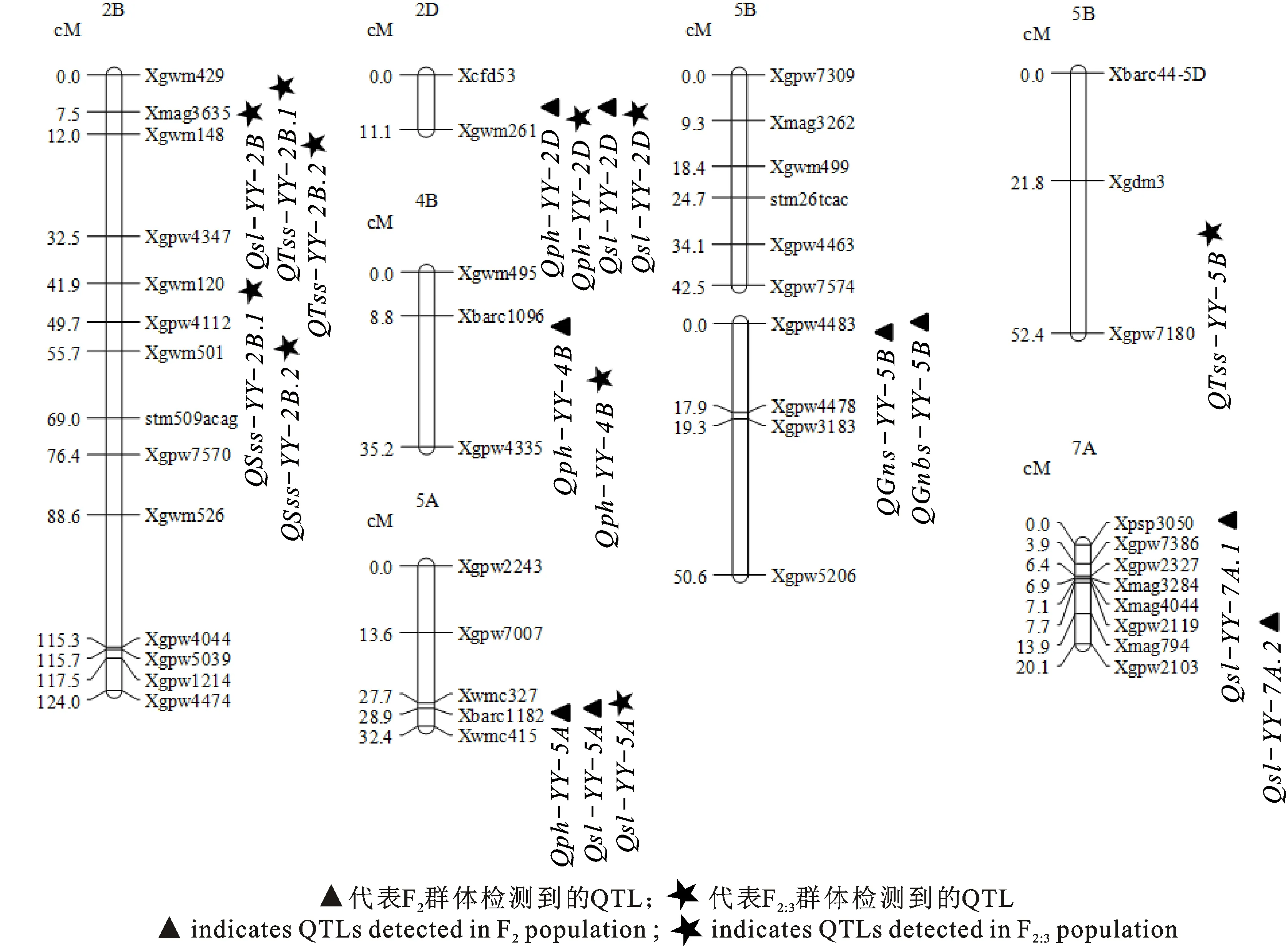
圖1 (揚麥17/揚麥18)F2和F2:3群體穗部性狀和株高QTL在染色體上的分布
2.3.1 穗部性狀QTL
1個控制穗粒數的QTL位于5B染色體上的Xgpw4483~Xgpw4478標記之間,僅能在F2代檢測到,可解釋9.92%的表型變異,其增效等位基因來自揚麥18。3個控制總小穗數的QTL分別位于2B和5B染色體上,僅在F2:3代被檢測到。其中,QTss-YY-5B位于Xgdm3~Xgpw7180之間,表型變異解釋率為7.28%,增效基因來源于揚麥17;QTss-YY-2B.1和QTss-YY-2B.2分別位于Xgwm429~Xmag3635和Xgwm148~Xgpw4347之間,兩個QTL的峰值在20 cM以內,推測是相同QTL,表型變異解釋率分別為6.77%和9.21%,增效等位基因均來自揚麥18。2個控制不育小穗數的QTL均位于2B染色體上,僅在F2:3代檢測到,分別位于Xgwm120~Xgpw4112和Xgpw4112~Xgwm501之間,Xgpw4112是二者共同緊密連鎖的分子標記,兩個QTL的峰值在20 cM以內,推測是相同QTL,QTL表型變異解釋率分別為7.05%和7.65%,增效等位基因均來自揚麥18。1個控制穗基部結實粒數的QTL位于5B染色體上,位于Xgpw4483~Xgpw4478之間,僅在F2代檢測到,表型變異解釋率為6.43%,增效等位基因來源于揚麥18。未能檢測到控制穗頂部結實粒數及其構成性狀的QTL。
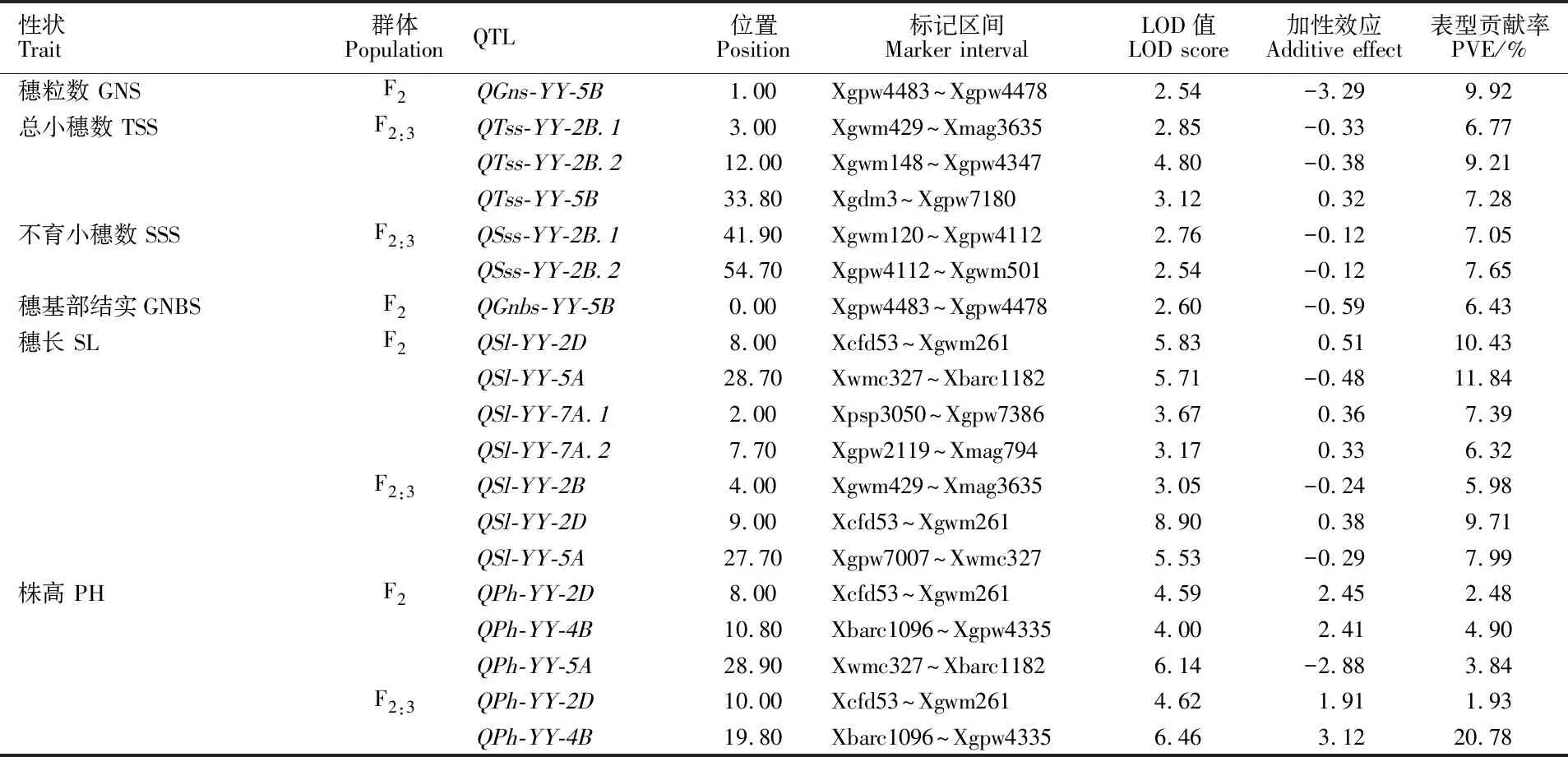
表3 揚麥17/揚麥18 F2和F2:3群體穗部性狀以及株高的QTL定位結果Table 3 QTLs for spike traits and plant height in the F2 and F2:3 populations of Yangmai 17/Yangmai 18
加性效應值中,正值表示增效基因來自揚麥17,負值表示增效基因來自揚麥18。
Positive additive effect values indicate increased effects from Yangmai 17,and negative additive effect values indicate increased effects from Yangmai 18.
5個與穗長相關的QTL分別位于2B、2D、5A和7A(2)染色體上。其中,QSl-YY-7A.1、QSl-YY-7A.2分別位于Xpsp3050~Xgpw7386和Xgpw2119~Xmag794之間,僅在F2代檢測到,兩個QTL的峰值在20 cM以內,推測是相同QTL,表型變異解釋率分別為7.39%和6.32%,增效等位基因均來自揚麥17;QSl-YY-2B位于Xgwm429~Xmag3635之間,僅在F2:3代下檢測到,表型變異解釋率為5.98%,增效等位基因來源于揚麥18;QSl-YY-2D和QSl-YY-5A在兩代中均能被檢測到,前者在兩代中都位于Xcfd53~Xgwm261之間,表型變異解釋率分別為9.71%和10.43%,增效等位基因均來自揚麥17,后者在兩世代中分別位于Xgpw7007~Xwmc327、Xwmc327~Xbarc1182之間,表型變異解釋率分別為7.99%和11.84%,增效等位基因均來自揚麥18。
2.3.2 株高QTL
3個控制株高的QTL被定位在2D、4B和5A染色體上。其中,QPh-YY-2D和QPh-YY-4B分別位于Xcfd53~Xgwm261和Xbarc1096~Xgpw4335之間,在兩世代中均被檢出,表型變異解釋率分別為1.93%和20.78%,增效等位基因均來自揚麥17;QPh-YY-5A位于Xwmc327~Xbarc1182之間,僅能在F2代中檢測到,表型變異解釋率為3.84%,增效等位基因來自揚麥18。
2.4 小麥-簇毛麥易位染色體T6VS·6AL在F2群體中的傳遞及對小麥穗部性狀的影響
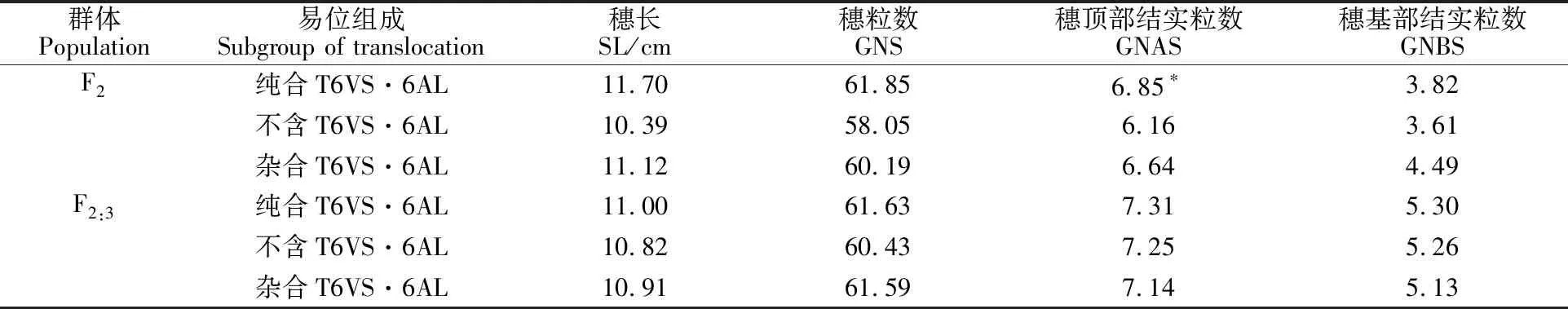
表4 兩世代中含有純合T6VS·6AL、雜合T6VS·6AL和不含T6VS·6AL的個體間穗部性狀比較Table 4 Comparison of spike traits among homologous T6VS·6AL,heterozygous T6VS·6AL and non T6VS·6AL subgroups in two generations
*表示兩世代中含有純合T6VS·6AL與不含T6VS·6AL類群間的差異達到顯著水平(P<0.05)。
* indicates the difference between homologous T6VS·6AL and non T6VS·6AL subgroups in two generations reaching a significant level(P<0.05).
3 討 論
3.1 QTL位點的一致性
本研究結果表明,穗長QTL分別位于2D、5A、7A和2B上, 增效等位基因QSl-YY-2D位于Xcfd53和Xgwm261之間,這與Heidari等[25]和Sourdille等[1]的研究結果一致;增效等位基因QSl-YY-5A位于Xbarc327~Xbarc1182之間,與Liu等[26]檢測到與穗長相關的QTLQSL-5A.2所屬區段相同,推測是同一QTL;在7A上檢測到的穗長QTL與前人報道[26-27]相距較遠,推測是一個新的QTL;QSl-YY-2B所屬標記區間Xgwm429~Xmag3635位于2BS上,標記Xgwm429落在侯立江[28]定位到的Qsl2B區段內,但是因為另一標記不在此區段,因此無法推斷是否是同一QTL。
株高QTL分別位于2D、4B和5A上,QPh-YY-2D位于Xcfd53~Xgwm261區段內,增效等位基因來自揚麥17,已有報道顯示Xgwm261可以作為2DS上矮稈基因Rht8的特異分子標記[29],推測此QTL是Rht8。QPh-YY-4B位于Xbarc1096~Xgpw4335區段內,F2:3代表型貢獻率達到20.78%,增效基因來自揚麥17,經過與中國春(CS)V1.0 版本參考基因組(http://plants.ensembl.org/Triticum_aestivum/Info/Index)比對發現該QTL位于4BL上,與已報道4BS上矮稈基因Rht-B1b的物理位置相距較遠,推測此處是一個新的矮稈QTL。QPh-YY-5A位于Xwmc327~Xbarc1182區段內,增效基因來自揚麥18,與Gao等[30]報道的5AS上株高QTL位置不同,與已知矮稈基因Rht12相距較遠[31],推測是一個新的株高QTL。
總小穗數QTLQTss-YY-2B.1位于Xgwm429~Xmag3635區段,增效等位基因來自揚麥18,此QTL與梁秀梅等[32]檢測到的總小穗數QTLQTSS-2B區段具有共同分子標記Xgwm429,推測是同一QTL。另一總小穗數QTLQTss-YY-5B,表型貢獻率7.28%,增效基因來自揚麥17,所屬區段為Xgdm3~Xgpw7180,未見前人報道。
5B長臂末端同時定位到穗粒數和穗基部結實粒數QTL,增效等位基因均來自揚麥18,標記區間為Xgpw4483~Xgpw4478,這與王健勝[33]定位到的控制穗粒數的QTLQGns.wa-5B.e3所屬標記區段位置相近[27],推測是同一QTL。有關穗基部結實粒數QTL研究罕見,已知梁秀梅等[32]在3D上檢測到穗基部結實粒數QTLQGnbs-YN-3D,其他未見報道,因此本研究定位到的QGnbs-YY-5B是一個新的穗粒數QTL。
3.2 QTL 位點的表型貢獻率和穩定性
定位結果顯示大多數穗部性狀QTL的貢獻率較低,只有QSl-YY-2D、QSl-YY-5A、QPh-YY-2D和QPh-YY-4B能夠同時在兩世代中被檢測到,其他位點只能在單一世代被檢測到,而QPh-YY-2D在F2:3世代表型貢獻率達到20.78%,F2代表型貢獻率只有4.9%。這是因為穗部性狀大都屬于數量遺傳性狀,由微效多基因控制,且受環境影響,并且供試群體F2和F2:3屬于低世代臨時性群體,表型調查誤差大,導致大多數穗部性狀在不同世代中檢測到的QTL有差異。我們后續會增加重組自交系群體多環境試點以提高結果的可靠性和穩定性,尋找在不同環境下穩定表達的穗部相關性狀QTL。
3.3 QTL位點的“一因多效性”或者緊密連鎖
相關性狀的QTL往往存在于相同或相近染色體區,表現出“一因多效”或緊密連鎖效應,通過不同性狀的QTL同時定位可以在一定程度上解釋復雜性狀及其構成要素或相關性狀之間的關系,也在一定程度上證明了該位點的穩定性。本研究在2D、5A染色體同一區段發現了控制穗長和株高的QTL,在5B染色體同一區段發現控制穗粒數和穗基部結實粒數的QTL,在2B染色體相近區段發現控制總小穗數和穗長的QTL。利用這些“一因多效”或者緊密連鎖的QTL,結合穩定表達的位點,通過回交和分子標記輔助選擇,可同時聚合不同位點上控制多個性狀的等位基因,從而創制出優異的小麥種質資源。
3.4 T6VS·6AL易位系的遺傳效應
李桂萍等[34]的研究結果表明,T6VS·6AL易位染色體對后代的穗長和千粒重表現出一定的正向效應,對其他產量構成要素及產量沒有表現出明顯的影響。本研究供試親本揚麥18與揚麥17雜交后獲得的F2代中T6VS·6AL類群的穗頂部結實粒數顯著高于非T6VS·6AL類群,而穗長、穗粒數和穗基部結實粒數在兩個類群之間無顯著差異,與以往的報道不完全一致,這是因為外源染色體導入小麥背景后產生的遺傳效應有可能受小麥不同遺傳背景、不同世代的影響。
F2代中,含有純合T6VS·6AL類群的穗長、穗粒數、穗頂部結實粒數最高,含雜合T6VS·6AL類群的穗長、穗粒數、穗頂部結實粒數和穗基部結實粒數均高于另兩個類群的平均值,不含T6VS·6AL類群的穗長、穗粒數、穗頂部結實粒數和穗基部結實粒數最低。而F2:3代中含有純合T6VS·6AL類群的穗長、穗粒數最高,含雜合T6VS·6AL類群的穗長、穗粒數均高于另兩個類群的平均值,初步推測6VS上攜帶有增加穗長、穗粒數的基因,且為部分顯性。由于研究所用的群體為尚未穩定的分離群體,特別是F2群體缺少生物學重復鑒定,因此本研究獲得的有關T6VS·6AL對產量性狀的效應還需進一步利用穩定的重組自交系群體通過多年多點試驗進行驗證。
致謝:感謝中國農業科學院作物科學研究所夏先春研究員在 KASP 基因分型方面提供的技術支持!

