鎂鋁水滑石的水熱合成及表征
呂 品 ,施春輝 ,李 偉 ,仲劍初
(1.遼寧省人民政府工業特種資源保護辦公室,遼寧沈陽110032;2.大連理工大學精細化工國家重點實驗室,化工學院材料化工系)
水滑石(LDH)是20世紀80年代開發的一種新型無機熱穩定劑,與已有熱穩定劑相比具有無毒、清潔、價廉和高效等優點。但是,一直以來困擾水滑石工業化大規模連續生產的問題是水滑石形貌不規整、顆粒易團聚、生產成本高等。水滑石常用的合成方法是共沉淀法,但是該方法容易出現類似球體的“sand rose”形貌[1];水熱法能避免 face-edge 現象,制備的產品形貌是規整的六方片狀[2],但是合成出的水滑石尺寸較小,一般不超過500 nm。綜上,筆者選用共沉淀法與水熱法結合,一方面可以合成出尺寸較大的納米晶,另一方面可以解決face-edge導致的“sand rose”形貌,合成出分散性較好的水滑石。
近年來,對水滑石類熱穩定劑的研究主要集中在新型陰陽離子組合水滑石,如MgZnAl-maleate-LDH、ZnAlLa-CO3-LDH、MgAlCe-CO3-LDH、十四烷酸插層稀土類水滑石等[3-7],對傳統鎂鋁水滑石的研究則主要集中在改性、方法改良等方面。水滑石的PVC(聚氯乙烯)熱穩定性能與其比表面積息息相關,只有比表面積小于30 m2/g的水滑石才具有熱穩定效果[8]。然而針對水滑石比表面積方面的研究很少,國內外雖有人進行過研究[9-12],但是難以得到比表面積在10~20 m2/g的水滑石。筆者采用高過飽和共沉淀水熱法,利用價廉的化工原料合成小比表面積的水滑石,系統考察了反應溫度、原料性質、晶種等條件對合成MgAl-LDH晶體結構、比表面積、水合粒徑等的影響。
1 實驗部分
1.1 樣品制備
以分析純氯化鎂(MgCl2·6H2O)、硫酸鋁[Al2(SO4)3·18H2O]、無水碳酸鈉(Na2CO3)和氫氧化鈉(NaOH)為原料,采用高過飽和共沉淀水熱法制備MgAl-LDHs。 稱取 35.45 g MgCl2·6H2O 和 14.00 g NaOH 分別置于燒杯中,分別加入去離子水配成100 mL的溶液,將兩種溶液混合均勻后轉移到水熱釜中,在一定溫度下反應3 h,將所得產物Mg(OH)2過濾,洗滌至pH=7。將氫氧化鎂濕濾餅置于燒杯中,加入去離子水攪拌均勻,配成200 mL Mg(OH)2懸濁液。按照n(Mg)∶n(Al)=2∶1 稱取相應量的 Al2(SO4)3·18H2O 置于燒杯中,加入去離子水溶解并定容至150 mL。將Mg(OH)2懸濁液與 Al2(SO4)3溶液混合均勻得到混合液。配制一定比例的Na2CO3和NaOH混合溶液置于三口燒瓶中,調節水浴溫度為60℃,在劇烈攪拌條件下將上述混合液迅速倒入三口燒瓶中,在60℃水浴中攪拌反應2 h,然后將反應液趁熱快速轉移至水熱釜中水熱反應一段時間,反應結束后冷卻、過濾,用去離子水洗滌至pH=7,所得產物在65℃烘箱中干燥24 h得到產品。
1.2 樣品表征
采用D/MAX-2400型X射線衍射儀(XRD)分析樣品的晶相組成。用JSM6360-LV型掃描電子顯微鏡(SEM)觀察樣品的表面形貌。用AUTO SORB-1-MP型物理吸附儀對樣品進行比表面積分析。用DTS 5101型激光粒度儀對樣品進行粒徑分析。晶粒尺寸通過謝樂公式計算:D=Kλ/βcos θ。式中:K取0.89;θ為衍射角;λ為 X射線波長 0.154 056 nm;β為半峰寬。
2 結果與分析
2.1 反應溫度對合成水滑石的影響
固定水熱時間為12 h,不同水熱溫度制得水滑石的XRD譜圖見圖1。原料Mg(OH)2的合成條件:水熱溫度為150℃、水熱時間為3 h。由圖1看出,不同水熱溫度制得的產物均具有明顯的水滑石特征衍射峰(003)(006)(012)(015)(018)(110)(113),并且峰形尖銳、對稱性好、強度高,說明產物的結構規整性強;隨著水熱溫度的升高,特征峰強度不斷增大,說明水滑石的結構規整性增強。

圖1 不同水熱溫度合成LDHs的XRD譜圖
表1為不同水熱溫度制得水滑石的晶體結構參數。由表1可知,隨著水熱溫度升高,晶胞參數a、c、d逐漸增大。這是因為,隨著水熱溫度升高,Mg(OH)2水解速率逐漸增大,所以沉淀產物中實際n(Mg)∶n(Al)增大,所以a增大;同時,由于層板上正電荷密度降低,所以晶胞厚度c增大。另外,晶粒尺寸沿a軸方向的D110逐漸增大,沿c軸方向的D003也增大,但是D110比D003變化大,說明溫度升高使得產物徑向增大比厚度增大明顯,從而導致徑厚比D110/D003大大增加。
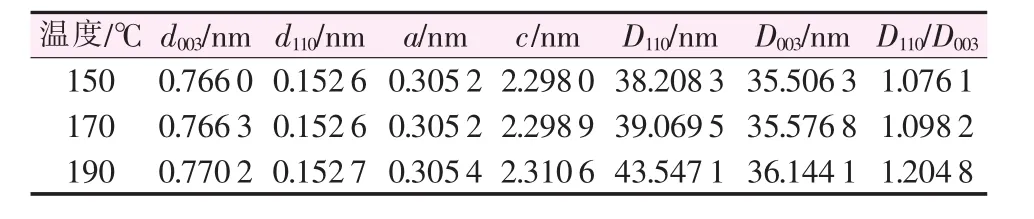
表1 不同水熱溫度合成LDHs的晶體結構參數
圖2為不同水熱溫度制得水滑石的SEM照片。從圖2看出,產物均呈片狀形貌,規整性、均一性、分散性較好;隨著溫度升高顆粒尺寸逐漸增大。當溫度為170℃時,晶粒棱角不分明,形狀類似圓餅形,表面不光潔;當溫度為190℃時,晶粒為規整的六方片狀結構,表面光潔,分散性也有所提高。因此,最佳的水熱溫度為190℃。
表2為不同水熱溫度合成水滑石的比表面積和水合粒徑。由表2看出:隨著水熱溫度由150℃升高到170℃,水滑石的水合粒徑增大,由于粒徑越大比表面積越小,所以反應溫度越高比表面積越小。但是,隨著溫度的進一步升高,水滑石的比表面積減小的程度降低。

圖2 不同水熱溫度合成LDHs的SEM照片

表2 不同水熱溫度合成LDHs的比表面積和水合粒徑
2.2 氫氧化鎂原料合成條件對合成水滑石的影響
固定水滑石的水熱反應時間為12 h、水熱反應溫度為190℃,以不同水熱溫度制得的Mg(OH)2為原料制得水滑石的XRD譜圖見圖3。由圖3看出,利用不同溫度制得的Mg(OH)2為原料,所得水滑石的物相組成有差異。隨著原料合成溫度的升高,原料晶型變好,得到水滑石的衍射峰也越來越尖銳,說明產品的晶體結構更加規整。其中以60℃合成的Mg(OH)2為原料時,合成的產物中除了有水滑石物相外,還有明顯的 Al(OH)3特征峰;隨著原料 Mg(OH)2合成溫度的升高,水滑石產物中Al(OH)3特征峰越來越弱。

圖3 以不同水熱溫度制得的Mg(OH)2為原料制得LDHs的XRD譜圖
圖4為以不同水熱溫度制得的Mg(OH)2為原料制得水滑石的SEM照片。從圖4看出,采用150℃合成的Mg(OH)2為原料時,所得水滑石表面光潔;采用170℃合成的Mg(OH)2為原料時,所得水滑石厚度大、分散性好,但是成形性差,有晶粒破碎現象。綜上可以看出,原料Mg(OH)2的合成適宜條件為150℃,3h。

圖4 以不同水熱溫度制得的Mg(OH)2為原料制得LDHs的SEM照片
表3為以不同水熱溫度制得的Mg(OH)2為原料制得水滑石的比表面積和水合粒徑。由表3看出:當Mg(OH)2合成溫度由60℃驟變成130℃時,水滑石的水合粒徑減小、比表面積增大;但是當Mg(OH)2合成溫度由130℃逐漸升高到170℃時,水滑石的水合粒徑卻逐漸增大、比表面積逐漸減小。

表3 以不同水熱溫度制得的Mg(OH)2為原料制得LDHs的比表面積和水合粒徑
2.3 硼雜質含量對合成水滑石的影響
在工業生產中,氯化鎂原料多采用成本較低的鹽湖MgCl2。由于鹽湖中含有硼,因此鹽湖MgCl2中含有硼雜質,如中國青海鹽湖氯化鎂中就含硼[13],三氧化二硼質量分數為0.006%~0.030%。而Mg(OH)2吸附能力較強,極易吸附硼,所以硼含量會對產品造成不同程度的影響。表4為以不同硼含量的MgCl2為原料制得水滑石的晶體結構參數。其他條件同2.1節。由表4看出,隨著原料中B2O3質量分數由0.006%增加至0.020%,晶胞參數a、c、d逐漸減小,說明水滑石結構中實際 n(Mg)∶n(Al)減小;當硼含量過大(B2O3質量分數達到0.030%)時,晶胞參數增大。另外,晶粒尺寸D110、D003先增大后減小,徑厚比D110/D003先減小后增大。這說明適量的硼雜質有利于水滑石徑向尺寸和厚度的增大,存在最佳硼含量。由表4看出,將B2O3質量分數控制在0.020%左右可以合成大尺寸的晶粒。

表4 以不同硼含量的氯化鎂為原料制得LDHs的晶體結構參數
圖5為以不同硼含量的MgCl2為原料制得LDHs的SEM照片。從圖5看出,產物均呈規整的六方片狀形貌,棱角分明,晶粒分散性和均一性較好,晶粒尺寸沒有大的差異,介于500~700 nm。從晶粒形貌上看,不同硼含量的原料制得的水滑石并沒有明顯差異。
表5為以不同硼含量的氯化鎂原料制得水滑石的比表面積和水合粒徑。由表5看出:當采用分析純試劑為原料時,水滑石的水合粒徑為772 nm;當原料中加入越來越多的硼酸時,水滑石的水合粒徑和比表面積雖然有所改變,但是變化程度非常小。

圖5 不同硼含量的氯化鎂原料制得LDHs的SEM照片

表5 以不同硼含量的氯化鎂原料制得LDHs的比表面積和水合粒徑
2.4 晶種對合成水滑石的影響
以150℃水熱 3 h合成的 Mg(OH)2為原料,固定水熱溫度為190℃、水熱時間為12 h,合成過程中加入不同量的晶種(以質量分數計),制得水滑石的XRD譜圖見圖6。由圖6看出,隨著晶種加入量增大,水滑石特征峰強度逐漸增大,說明加入少量晶種可以誘導晶體成型。

圖6 加入不同量晶種制得LDHs的XRD譜圖
表6為添加不同量晶種制得水滑石的晶體結構參數。由表6看出,隨著晶種加入量增大,晶胞參數a、c、d大致呈減小趨勢,表明產物的結構規整性也降低。晶胞參數a減小,說明在晶種的誘導下同時進入骨架的Al3+的量比Mg2+的量大,所以層板上正電荷密度增大,層板與層間陰離子的相互作用增強,所以晶胞厚度c會減小。另外,晶粒尺寸D110減小,但D003增大,所以徑厚比D110/D003減小。

表6 加入不同量晶種制得LDHs的晶體結構參數
圖7為加入不同量晶種制得水滑石的SEM照片。從圖7看出:當晶種加入量為0.5%時,水滑石形貌為非常規整的六方片狀,表面光潔,且尺寸顯著增大;當晶種加入量為1.0%時,水滑石的形狀變得極不規則,尺寸極不均一,所以晶種過多反而不利于晶粒形成規整的形狀。綜上可以得出,晶種添加量選擇0.5%較適宜。
表7為添加不同量晶種制得水滑石的比表面積和水合粒徑。由表7看出:當加入少量晶種(10.5%)時,水滑石的水合粒徑增大,比表面積大大減小;隨著晶種加入量繼續增加(1.0%),水滑石的水合粒徑反而減小,比表面積增大。

表7 加入不同量晶種制得LDHs的比表面積和水合粒徑

圖7 加入不同量晶種制得LDHs的SEM照片
3 結論
采用高過飽和共沉淀水熱法合成的鎂鋁水滑石晶體結構規整,晶粒形貌完整。實驗結果表明:1)隨著反應溫度升高、反應時間延長,產物的晶粒尺寸和徑厚比逐漸增大,最佳合成條件為水熱時間為12 h、水熱溫度為 190℃;2)Mg(OH)2原料的合成條件不同會直接影響水滑石物相組成和形貌,最佳Mg(OH)2原料水熱合成條件為150℃、3 h;3)原料中適量硼雜質可以促進晶體生長,最佳B2O3質量分數為0.020%;4)添加適量晶種有利于水滑石形成,晶種添加過多不利于形貌規整,最佳晶種添加量為0.50%左右。在上述最佳條件下,制得水滑石比表面積為10.33 m2/g、水合粒徑為878 nm。

