含銫鹵化鈣鈦礦的研究進展
(濟南大學材料科學與工程學院,山東濟南250022)
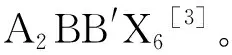
鈣鈦礦材料包括有機-無機鈣鈦礦和全無機鈣鈦礦2種。有機-無機鈣鈦礦是指在ABX3結構中,A位陽離子由MA+、FA+等有機小分子占據。由于這類鈣鈦礦的尺寸、形狀、元素組成等都可以發生改變[9],通過簡單調節電子結構就可以得到不同的帶隙[10],加之具有發光色域廣、色度高等特點[11],在太陽能電池,光探測器等器件的吸收層材料、發光器件上有著廣泛的應用。盡管有機-無機鈣鈦礦有許多優點,但是,由于有機小分子的穩定性較差,當這類鈣鈦礦受到熱應力,或者在空氣、光照下曝露較長時間時,結構與性能會發生很大的的變化,甚至產生降解[12-15],因此,將A位陽離子由有機小分子替換為其他較為穩定的陽離子具有極高的應用價值。經研究發現,將有機小分子替換為Cs+,制備的全無機鈣鈦礦在250 ℃下依然能夠保持結構穩定,熱穩定性大大提高[16],并且由于Cs+的激子結合能較高,躍遷速度快,電荷載流子遷移率和光致發光量子產率也較有機-無機鈣鈦礦有了明顯的提高。目前,含銫鹵化鈣鈦礦成為發光二極管中最廣泛采用的發光層之一[17]。
本文中綜述了含銫鹵化鈣鈦礦的研究進展,包括合成方法、主要性能、應用等,并分別對含鉛與不含鉛鈣鈦礦的研究現狀進行了調研分析,旨在為今后含銫鹵化鈣鈦礦的性能的提高和應用的擴展提供參考。
1 鹵化銫鉛鈣鈦礦的研究現狀
鹵化銫鉛鈣鈦礦在全無機鈣鈦礦中占有非常重要的地位,對它的研究報道也非常多,目前主要集中于CsPbX3(X=Cl、Br、I)。到目前為止,就形態而言,CsPbX3在微觀上已被合成為納米晶(NCs)、納米片(NPL)、納米線和納米籠,宏觀上長成了單晶(SCs);就成分而言,研究主要集中于離子交換,包括陰離子(Cl-、Br-、I-)、一些等價物(Sn2+、Mn2+、Cd2+、Ba2+、Ge2+)和異價陽離子(Rb+、Ag+、Cu+、Bi3+)等[18];就性能而言,CsPbX3的研究主要集中于熒光、光電轉換等方面。
1.1 CsPbX3的熒光性能
CsPbX3(X=Cl、Br、I) 鹵化鉛鈣鈦礦具有帶隙可調節(1.77~3.10 eV)、發光范圍廣(波長405~700 nm)、光致發光量子產率(PLQY)高(40%~99%)、缺陷形成能低且光學良性等優點,加之僅通過使用不同的鹵族元素(Cl、Br、I)和控制反應溫度來就改變發射波長,實現從藍光、綠光到紅光的發射[19],因此CsPbX3具有優異的熒光性能,在LED等領域的應用中具有明顯優勢。
Jurow等[20]通過熱注射技術合成了具有深藍色光發射的CsPbBr3納米片,并利用鈣鈦礦電子躍遷對介電環境的敏感性,通過等離子體沉積工藝將氧化鋁薄膜覆蓋于發光顆粒之上,使平均躍遷偶極矩與表面之間的角度從50°減小到僅14°,從而減小了因過渡偶極矩的隨機取向對光輸出耦合效率的限制,使納米片的PLQY高于70%。
Chen等[21]將Cs2CO3、1-十八烯、油酸混合,并先后在真空和Ar下加熱保溫制備Cs-油酸酯前驅體溶液,之后采用熱注射技術制備了室溫下為立方體結構的CsPbX3納米晶,PLQY達到了70%。研究后發現,通過調節鹵素比例,可以將發射峰從波長407 nm調節到680 nm,這幾乎覆蓋了整個可見光的范圍。
Ye等[22]開發了一種在90 ℃的空氣中合成CsPbX3納米晶的簡便方法。該方法選擇在非極性溶劑——辛烷中進行,合成的納米晶PLQY超過了90%。 他們通過在成核之前,將特定金屬有機鹽溶解在前驅體溶液中來控制形態,制得了納米立方體、 量子點、 納米片、 納米棒和納米線等不同形態的CsPbX3。 除此之外,他們開發了一種原位陰離子交換方法,使用PbX2溶于辛烷中作為鹵化物源來調節CsPbX3的光致發光發射,從而實現了從波長410~680 nm的精確控制。
Adhikari等[23]將銫前驅體的生產過程從脂肪酸與銫鹽的反應轉換為銫堿與脂肪酸酯反應。通過皂化沉淀,使反應不再需要真空烘箱或者是惰性氣體環境,簡化了實驗設備,降低了實驗的要求。他們研究發現,由于量子限制,調節合成溫度可以使納米晶體的尺寸發生變化,進而使帶隙在2.21~2.83 eV范圍可調節,具體表現為隨著合成溫度的升高,帶隙持續減小,吸收光譜發生了紅移,實現了藍、 綠光的調節。
1.2 CsPbX3的光電性能
憑借吸收系數高、載流子壽命長、激子結合能低等特點[24],CsPbX3不僅具有優異的熒光性能,還具有優秀的光電性能,使其在太陽能電池、激光、光電探測器等方面得到了廣闊的應用。
在太陽能電池中,一般選擇CsPbI3和CsPbBr3,因為它們具有合成簡單、電荷傳輸性能優越、載流子的壽命長、帶隙合適等優點[25];但是,由于CsPbX3在水分和極性溶劑下,會出現相不穩定性和降解等狀況,因此限制了太陽能電池的能量轉化效率(PCE)。2014年,Choi等[26]報道的黃相CsPbI3由于外來晶相和寬的帶隙導致PCE僅為0.09%。Murugadoss等[27]制備的黃相CsPbI3和CsPbBr3的PCE分別為0.75%、1.16%,但是在制備過程中通過摻雜Sn可以將CsPbI3的PCE提高到5.12%。Sanehira等[28]課題組通過在CsPbI3量子點薄膜上涂覆甲脒碘化物,將PCE提高到了13.4%。Ghosh等[29]通過改善鹵素的配比,合成了PCE為7.94%的CsPbBr1.5I1.5,將其在相對濕度為55%的空氣中曝露35 h后,PCE僅下降了12%,這說明其可在較長時間內穩定存在。
激光器是基于受激發射的電磁輻射通過光學放大過程發光的裝置。鈣鈦礦材料具有尺寸可調、合成簡便以及對溫度不敏感的光學特性,并且CsPbX3具有由最小粒徑引起的量子限制效應,在激光器中展現了廣闊的應用潛力。2007年,Kondo等[30]首次證明了通過從非晶相中結晶制備的微晶CsPbBr3薄膜具有室溫刺激發射的特性。在室溫條件下,其閾值激發強度為50 kW/cm2(77 K)和100 kW/cm2(295 K),盡管鈣鈦礦的PLQY較低,這項工作沒有提供更好的結果,但它揭示了在金屬鹵化物中尋找新激光介質的可能性。在2015年,Kovalenko等[31]報告了基于回音壁模式(WGM)的激光,他們使用PbX2和Cs-油酸酯在非極性溶劑介質中,通過簡單的一步反應合成了鈣鈦礦CsPbX3納米晶,并將其涂覆到二氧化硅球體上,測試后發現室溫光學放大可以在整個可見光譜范圍(波長440~700 nm)內獲得,其閾值低至5 μJ/ cm2,高模態凈增益值至少為(450±30)cm-1,脈沖持續時間高達10 ns。
光電探測器是用來將光信號轉化為電信號的裝置,CsPbX3憑借其高吸收效率(2×105cm-1)和較大的載流子遷移率,在光電探測器領域有著廣泛應用。Ramasamy等[32]在2016年首次展示了基于CsPbI3的光電探測器,他們選擇紅色發射的CsPbI3納米晶作為活性材料,這是因為CsPbI3納米晶具有相對長的輻射壽命,并且可以產生高光電流。他們合成CsPbBr3納米晶后將其溶解在己烷中,然后在溶液中加入LiI以形成CsPbI3納米晶,之后將獲得的納米晶在預先制備好的Si襯底上滴鑄,并在N2氣氛中退火后制得了具有CsPbI3膜的光電探測器裝置。該裝置具有非常好的光敏性 、相對快速的上升(24 ms)和衰減時間(29 ms)。Huang等[33]首次報道了基于無機鈣鈦礦CsPbBr3量子點的分子印跡聚合物(MIP)熒光傳感器,主要用于氧化樂果(OMT)的檢測。通過壓印技術與溶膠-凝膠反應合成的CsPbBr3,由于具有高的PLQY和高MIP選擇性,顯示出了對OMT測定的高靈敏度:可以測定濃度低至18.8 mg/L的OMT,這說明了全無機鈣鈦礦作為傳感器在生物和環境檢測中的巨大潛力。
1.3 其他的鹵化銫鉛鈣鈦礦
在鹵化銫鉛鈣鈦礦中,除了CsPbX3結構外,還有其他的結構被研究,如Cs4PbX6、CsPb2X5等。以銫鉛溴鈣鈦礦為例,除CsPbBr3外,還有Cs4PbBr6、CsPb2Br5等鈣鈦礦衍生物,它們之間具有具有不同的結構和性質:CsPbBr3是一種三維結構[34],而Cs4PbBr6具有零維結構[35],CsPb2Br5則顯示出各向異性的二維分層結構[36]。一般認為Cs4PbBr6、CsPb2Br5是由CsPbBr3通過相變轉化而來的,例如,Alivisatos等[37]使用胺引發從CsPbBr3到Cs4PbBr6的相轉變。Jiang等[38]探討了從CsPbBr3到CsPb2Br5的形狀變化和相轉變。Manna等[39]在CsPbBr3和Cs4PbBr6之間實現可逆的合成后轉化。
需要特別指出的是Li等[40]利用熱注射技術,通過控制溫度、時間和Pb和Cs物質的量比制備了CsPbBr3、Cs4PbBr6、CsPb2Br5,首次系統地研究了三者的轉變過程并對其相組成、形態、光致發光(PL)的性質進行了觀測。他們的研究發現,隨著溫度、Pb與Cs的物質的量之比的增加或時間的延長,Cs4PbBr6相與未反應的PbBr2反應形成CsPbBr3相;在高溫(超過160 ℃)且Pb和Cs的物質的量之比大于3時,樣品從Cs4PbBr6變為CsPbBr3,延長時間最終得到了CsPb2Br5納米片。3種相僅CsPbBr3具有高熒光PL和在波長520 nm附近的窄且對稱的發射峰,而CsPb2Br5和Cs4PbBr6沒有觀察到發射峰。
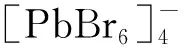
1.4 鹵化銫鉛鈣鈦礦面臨的挑戰
盡管鹵化銫鉛鈣鈦礦有著諸多的優點,但也存在2個關鍵的問題阻礙了其應用和發展:一是穩定性;二是鉛的毒性。尤其是鉛的毒性,成為制約鹵化銫鉛鈣鈦礦發展的最大因素[42]。
鹵化銫鉛鈣鈦礦雖然相比有機-無機鈣鈦礦在熱穩定方面有了很大提高,但是,當接觸到極性溶液(如水、醇等)或長時間置于空氣、紫外線照射時,依然容易分解,導致性能變差。為了提高CsPbX3的穩定性,通常采用的方法是使用聚合物、惰性材料、半導體材料、碳材料等進行表面包覆。例如Meyns等[43]使用馬來酸酐和1-十八烯的混合溶液(PMA)與CsPbX3前體溶液,制備了PMA封端的鈣鈦礦納米晶,可以用于制造具有窄帶寬的單色綠色或白色發光二極管。Liu等[44]通過將CsPbX3納米晶與孔徑為12~15 nm的介孔SiO2直接混合,將NCs納入SiO2的孔隙中,提高了光穩定性,防止了陰離子交換,目前已經應用于背光顯示器和片狀LED器件中,顯示出比以前報道的更好的性能。Xu等[45]報道了通過將窄帶隙CsPbBr3與寬帶隙Cs4PbBr6相結合的I型異質結構,與純CsPbBr3相比,基于復合材料的LED的最大電流效率和EQE分別增加了100倍和68倍,目前已成功應用于LED。石墨烯和碳納米管也可用于包覆鈣鈦礦NCs,主要原因是碳材料的高導電性能夠實現有效的電子提取和光誘導載流子的快速分離,Xu等[46]將CsPbBr3納米晶和石墨烯的復合物應用在光催化CO2還原中,表現出比裸露的CsPbBr3納米晶更好的性能。
相比穩定性,毒性不僅是鹵化銫鉛鈣鈦礦最大的問題,也是所有含鉛鈣鈦礦不得不面對的問題。鉛中毒是最嚴重的環境危害之一。這是因為鉛會對人的造血、腎臟、生殖和中樞神經系統產生各種有害的影響,并且這些影響通常是不可恢復的;此外,Pb會與體內的鈣競爭,破壞神經遞質釋放,減小骨礦物質密度; 更重要的是來自鈣鈦礦中的鉛可能會形成水溶性化合物,這些化合物會隨著食物鏈的積累而進入人體,在人類成年人的身體中,大約10%的攝入鉛會被吸收,但在兒童的身體中,這個數字可能會高出4~5倍。 由于鉛對公共健康和生態系統的威脅比含鎘材料更嚴重[47],因此,降低鉛的含量或者設計出新型無鉛的鈣鈦礦成為當前被廣泛關注的課題。
2 無鉛鹵化銫鈣鈦礦的研究現狀
如前所述,鉛的毒性對人體的危害很大,為了減少鉛的含量,研究者從化學組成晶體結構出發,尋找鉛的替代元素。到目前,根據相關文獻的報道,取代Pb2+的金屬離子主要有以下3種報道:一是選擇2價的IIA族、IVA族或者過渡族的金屬離子,如Sr2+、Sn2+、Ge2+、Cu2+等;二是選擇原子序數與Pb相近的非2價金屬離子,如Bi3+等;三是選擇1價和3價金屬離子共同形成雙鈣鈦礦結構,如Ag+和Bi3+等[42,48]。
2.1 CsSnX3的合成及應用
在APbX3的取代元素中,被認為最具有潛力的是錫元素。錫的2價離子半徑為1.02 ?,與Pb2+的離子半徑1.19 ?非常接近,并且錫基鈣鈦礦具有鉛基鈣鈦礦優良的光電性能,相比鉛基鈣鈦礦具有更窄的帶隙。早在1999年,錫被用在有機-無機鈣鈦礦上制得了半導體鈣鈦礦(C6H5C2H4NH3)2SnI4的旋涂薄膜,展現出了良好的性質[49]。而錫在鹵化鈣鈦礦中的應用較晚,且以CsSnI3居多。
Jellicoe等[50]通過使用不同的鹵化物源直接合成納米結構,或混合合成的純鹵化鈣鈦礦顆粒進行合成后的陰離子交換等2種方法制備CsSnX3(X=Cl、 Cl0.5Br0.5、 Br、 Br0.5I0.5、 I)鈣鈦礦納米晶。 他們利用量子限制效應和在鈣鈦礦晶體中使用不同的鹵化物來調整光學帶隙,將帶隙從2.8 eV調整到1.3 eV,從而跨越了可見光到近紅外的區域。Chen等[51]首次將CsSnI3作為光吸收劑應用到太陽能電池中,使用熱退火工藝來沉積CsSnI3薄膜,制備了肖特基型的器件,但由于受到了低分流的影響,其PCE僅為0.9%。 Chung等[52]利用CsSnI3半導體固體材料替代染料敏化太陽能電池(DSC)中的有機液體電解質,首次報道了全固態染料敏化太陽能電池。 他們制備了由CsSnI3、多孔納米TiO2和染料N719組成的太陽能電池。原始的CsSnI3電池顯示出優異的光電流密度-電壓特性,其PCE為3.72%。在摻雜SnF2后,其PCE可達10.2%。Marshall等[53]報道了在室溫下從溶液中制備正交CsSnI3薄膜的開創性論證:通過使用CsI和過量的SnI2制備前驅體,在DMF中旋轉澆鑄CsSnI3來制備CsSnI3膜。所獲得的CsSnI3膜缺陷密度非常低,PCE達到了1.5%,可用作聚合物太陽能電池(PSC)中的有效光吸收劑。 Li等[54]引入次磷酸(HPA)作為絡合劑,制備了CsSnIBr2薄膜。 HPA能夠加速成核過程,并在CsSnIBr2薄膜的形成過程中,起到限制Sn4+形成的還原劑的作用。 他們制備的CsSnIBr2的PCE為3.2%,在環境條件下儲存的封裝PSC經過77 d后,依然能夠保持較高的效率,是迄今為止報道的最穩定的CsSnI3裝置。
盡管錫基鈣鈦礦不含鉛,降低了毒性,但在實際應用中卻存在著一個嚴重的問題,即Sn2+易氧化成Sn4+形成Sn空位,導致Sn基鈣鈦礦的氧化穩定性很差,因此,錫基鈣鈦礦的一個研究熱點就是如何提高Sn2+的穩定性。最常見的策略是在鈣鈦礦薄膜的沉積過程中添加還原劑,如SnF2[52]。SnF2可以提高Sn基鈣鈦礦在空氣中的氧化穩定性,增加載流子長度和改善器件的界面能量排列。除了SnF2之外,常用的添加劑還有其他種類的錫鹽(如SnCl2、SnBr2和SnI2等)和還原劑如肼、吡嗪、HPA、哌嗪等[53-58],這些添加劑不僅可以作為有效的還原劑,還可以協助形成均勻形態的錫基鈣鈦礦膜。除了添加還原劑,常見的方法還有溶劑工程、熱退火、氣相沉積等[57,59-60]。
2.2 Cs3Bi2X9的合成及應用
Bi與Pb是同周期相鄰的2種元素,Bi3+與Pb2+具有相同的6s26p0電子構型,相近的半徑,并且相比Sn2+,Bi3+的氧化穩定性更好[61]。Cs3Bi2X9(X=Cl,Br,I)是二維層狀結構的有序空位鈣鈦礦,其晶胞數量是普通鈣鈦礦的3倍,鹵化鉍八面體可以形成角、邊和面共享的鉍鹵陰離子的單核或多核無機骨架,并且只有2/3的八面體空位被占據,剩余八面體保持空置并分離[62],從而產生廣泛的結構和可調的電子或光學性質。
Yang等[63]在室溫下合成了在空氣狀態下可穩定存在30 d的Cs3Bi2X9(X=Cl,Br,I)NCs,其發射波長范圍為400~560 nm。 無配體的Cs3Bi2Br9顯示藍色發射,光致發光量子效率(PLQE)約為0.2%。 當在合成過程中添加油酸(OA)做配體后,PLQE可以增加至4.5%。他們將PLQE的提高歸因于OA可以鈍化快速捕獲過程,延長了發射時間。值得注意的是,他們認為陷阱狀態也可以在潮濕條件下鈍化。
Tang等[64]使用乙醇做為溶劑合成了Cs3Bi2Br9量子點。其在波長410 nm處顯示藍色發射,PLQY高達19.4%。他們發現Cs3Bi2Br9量子點水解后的產物BiOBr能夠實現自我鈍化,大大提高了穩定性。他們在Cs3Bi2Br9外包覆了SiO2,并與Y3Al5O12磷光體組合,制造出白光發射的發光二極管。此外,他們通過混合前體溶液制備了全系列的Cs3Bi2X9(X=Cl、Br、 I),發射峰波長可以覆蓋393~545 nm。
Lian等[65]通過熱注射技術首次合成全無機的平行四邊形Cs3Bi2Br9鈣鈦礦納米片,并借助陰離子交換調節Cs3Bi2Br9的組成。通過非原位透射電子顯微鏡研究生長過程,證明了Cs3Bi2Br9納米片在單分散的平行四邊形核中各向異性地生長。由于大的激子結合能和量子限制,該NPL顯示出極其尖銳的吸收峰,其峰值位于380 nm,與Cs3Bi2Br9單晶相比,藍移95 nm。它的FWHM為39 nm,比報道的Cs3Bi2Br9(48 nm)或MA3Bi2Br9(62 nm)納米晶體的窄得多,這是NPL的優勢所在,但是NPL的PL強度非常弱,PLQY僅為0.54%。
Bass等[66]通過將BiBr3和CsBr溶解在熱的HBr水溶液中制備Cs3Bi2Br9。在真空過濾、冷卻后收集亮黃色粉末,通過旋轉澆鑄溶解在二甲基亞砜中的粉末溶液,并在Br2氣氛中退火制備藍光發射的薄膜。他們主要研究了Cs3Bi2Br9的光學性質,并根據密度泛函理論,計算確定的其電子結構。通過研究發現,在吸收光譜中產生尖銳的激子峰結合能近似為940 meV,顯著強于在其他鹵化鈣鈦礦中發現的值,這種大的結合能使激子耦合到晶格的振動過程中產生室溫下的高度結構化發射。
Pazoki等[67]同樣利用密度泛函理論以及實驗評估,計算出Cs3Bi2I9的直接帶隙和間接帶隙值分別為2.17 、2.0 eV,并通過數據說明了Cs3Bi2I9具有較低的光捕獲能力、較低的介電常數和載流子遷移率,以及可能較低的電荷分離效率,這解釋了在太陽能電池中其與鉛基鈣鈦礦相比具有較低的PCE的原因。
Cs3Bi2X9也存在這一些問題,最主要的問題就是效率低。在不添加配體時,其PLQY一般很低[63],在添加配體后,盡管PLQY有所增加,但依然遠低于鹵化銫鉛鈣鈦礦的PLQY(40%~99%)。目前,還沒有鹵化鉍銫鈣鈦礦的PLQY可以與鹵化銫鉛鈣鈦礦相媲美的報道。Cs3Bi2X9不僅PLQY較低,PCE也很低,Ghosh等[68]發現不管太陽能電池是何種結構,Cs3Bi2X9的PCE都低。盡管導致其PCE低的原因被發現,但如何大幅提高還沒有很好的辦法。
2.3 無鉛含銫雙鈣鈦礦的合成及使用
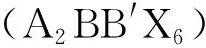
2016年,3個不同的課題組幾乎同時報告了Cs2AgBiX6(X=Cl或Br)的研究情況。Mcclure等[70]從固態和溶液路線合成了雙鈣鈦礦Cs2AgBiBr6和Cs2AgBiCl6,并對其穩定性進行了研究。結果表明,2種化合物在曝露于空氣時都是穩定的,但當曝露于光照下時,Cs2AgBiBr6會在數周內降解。Giustino等[71]成功合成了面心立方的Cs2AgBiCl6,并使用單晶X射線衍射發現其晶格參數10.50 ?,通過光學吸收光譜和Tauc圖估計間接光學帶隙在2.3~2.5 eV范圍內。Slavney等[72]報告了具有高熱穩定性和水分穩定性的Cs2AgBiBr6,該材料的室溫PL壽命達到了660 ns,遠高于高質量(MA)PbBr3薄膜(170 ns)的壽命。通過PL衰減曲線發現,該材料從單晶轉變為粉末只有6%的PLQY損失,表明位于表面的缺陷不會對材料的光伏性能產生不利影響。到目前,隨著Cs2AgBiX6的研究逐漸深入,其性能和應用不斷發展,但局限性也逐漸顯現出來,主要是存在著滯后問題。為了克服滯后問題,Pantaler、Gao等分別從合成方法、晶體結構等方面做出了改善,取得了一定的成果[73-74]。
得到較多研究的還有具有直接帶隙的Cs2AgInCl6。Volonakis等[75]通過結合第一性原理計算和實驗,首次報道了具有3.3 eV直接帶隙的Cs2InAgCl6。研究發現,這種新化合物在2.1 eV左右顯示PL,并且具有光致變色行為,即在紫外線照射下,顏色可逆地由白色變為橙色。 Luo等[76]采用水熱法合成了Cs2AgInCl6單晶,其陷阱密度僅為8.6×108cm-3,該值小于一般鹵化鉛鈣鈦礦SCs中報道的值。他們還借助系統光學和電子表征,通過實驗驗證了Cs2AgInCl6中奇偶禁止躍遷的存在,并確定了氧在控制其光學性質中的作用。Lee等[77]通過溶劑熱法合成的Cs2AgInCl6納米晶,具有在3.33 eV處從價帶最大值(VBM)到導帶最小值(CBM)的奇偶校驗禁止轉變和在4.88 eV處第三價帶層和CBM之間的奇偶校驗允許的高階躍遷,發射狀態也分為350 nm處的帶邊發射和395 nm出的缺陷態發射。
除了以上2種外,被報道的含銫鹵化雙鈣鈦礦還有許多,如Wang等[78]通過超聲波剝離技術,首次制備具有1.6 eV窄帶隙的單層Cs4CuSb2Cl12納米晶體,發現層間范德華力和平面內化學鍵在剝離過程中起著關鍵作用,微晶剝離成NCs后,導致間接帶隙轉變為直接帶隙和電子有效質量的減小。Zhang等[79]首次報道了Cs2NaBiI6(CNBI)的合成和表征,并通過各種測試方法確定了晶體結構和光學性質。他們發現CNBI具有1.66 eV的低帶隙,并且對空氣中的水分和氧氣具有高穩定性。Deng等[80]用溶液法合成了雙鈣鈦礦Cs2AgSbCl6并通過水熱法制備了包含Cs2AgSbCl6和TiO2的異質結納米粒子,實驗測量顯示Cs2AgSbCl6具有立方結構,晶格常數為10.699 ?,電子從雙鈣鈦礦層流到TiO2,該型太陽能電池的PCE較以往有了很大的提高。
含銫鹵化雙鈣鈦礦材料在水、熱和光中具有優異的穩定性,在光電領域具有廣闊的應用前景。盡管理論上存在的鹵化物雙鈣鈦礦材料有許多,但目前能夠通過實驗探索到的數量卻十分有限。此外,對這些材料的合成方法也局限在固態和濕化學路線上[69],因此,如何獲得更多結構的雙鈣鈦礦材料以及擴展其合成方法將是以后研究的重點。
3 結論與展望
相比于有機-無機雜化鈣鈦礦,全無機的含銫鹵化物鈣鈦礦在穩定性上具有壓倒性的優勢。由于鹵化銫鉛鈣鈦礦具有PLQE、PCE高的特點,使它的應用前景非常廣闊,但鉛的毒性和在極性溶液中的穩定性卻成為制約其發展的重要因素。無鉛鈣鈦礦成功地減小了毒性,增加了在極性溶液中的穩定性;但隨之而來的是PLQE和PCE的大幅度降低,因此如何繼續提高鹵化銫鉛的穩定性和如何提高無鉛含銫鹵化鈣鈦礦的PLQE和PCE將是未來工作的重點。由于鹵化銫鉛鈣鈦礦鉛的毒性無法避免,因此無鉛鈣鈦礦可能會擁有更加廣闊的應用前景。相信通過科研工作者的努力,具有高效率的無鉛含銫鹵化鈣鈦礦終會被開發出來并得到應用和推廣。

