超聲引導下周圍神經阻滯后暴發痛的臨床特征及影響因素分析
施蕓岑, 方 婕, 倉 靜, 張曉光
復旦大學附屬中山醫院麻醉科,上海 200032
周圍神經阻滯(peripheral nerve blocks,PNBs)廣泛應用于四肢手術,尤其是接受日間手術的患者。PNBs聯合鎮靜用于多種四肢手術,避免了氣道操作和椎管內麻醉。與全身麻醉術后靜脈鎮痛相比,PNBs具有減少阿片類藥物的用量及相應的不良反應、提供良好的術后早期鎮痛、縮短住院時間等優勢[1]。近年來,超聲引導下神經阻滯技術在臨床應用日益廣泛,同既往根據解剖定位或使用神經刺激儀相比,超聲引導下的PNBs操作可以減少血管穿刺的幾率、減少局部麻醉藥的用量、減少局麻藥全身毒性反應的風險[2]。最近一項回顧性隊列研究結果[3]顯示,超聲引導下操作可以減少短期內可恢復的神經損傷的發生率。
神經阻滯麻醉有許多優點,但在臨床上觀察到在實施了單次神經阻滯(single-shot peripheral nerve blocks,sPNBs)麻醉的患者,相當一部分在阻滯消退的過程中會經歷短暫劇烈的疼痛。Brian等[4]首次提出了暴發痛評分(rebound pain score,RPS):自患者主訴神經阻滯失效起12 h內最高疼痛數字評分(numerical rating scale,NRS)減去最后一次評估神經阻滯效果存在時的NRS評分。該研究發現通過延長阻滯時間可以降低RPS,阻滯時間每延長1 h,RPS降低0.03分(P<0.001)。其后的神經阻滯相關臨床研究中,無論是臂叢神經阻滯、股神經阻滯、腘窩坐骨神經阻滯,均提及暴發痛的現象,但是并未做具體描述和分析。比較神經阻滯麻醉和全身麻醉患者的術后疼痛情況發現[5]:接受神經阻滯的患者在術后8 h內的疼痛評分顯著低于全身麻醉組,但術后24 h的疼痛評分則顯著高于全身麻醉組。全身麻醉后疼痛呈逐漸下降趨勢,而神經阻滯后早期因阻滯的作用仍存在而完全無痛,在阻滯消退期則可能突然出現劇烈疼痛,并且由于局部麻醉藥的作用時效所致,這種劇烈疼痛經常發生在手術當晚。目前針對單次神經阻滯后暴發痛的臨床研究較少。因此,本研究觀察了sPNBs復合鎮靜進行麻醉的四肢手術術后暴發痛的發生情況及特點并探討暴發痛可能的危險因素。
1 資料與方法
1.1 一般資料 本研究是一項觀察性、前瞻性隊列研究。研究通過復旦大學附屬中山醫院倫理委員會批準(B2016-079R)。研究對象是2016年6月至12月在復旦大學附屬中山醫院在神經阻滯復合鎮靜、喉罩全身麻醉或者腰麻下進行擇期骨科手術的患者。納入標準:年齡大于18歲;能夠理解NRS評分并給出反饋信息;術后采用阿片類藥物進行患者自控靜脈鎮痛(patient control intravenous analgesia,PCIA);取得書面知情同意。排除標準:術前口服止痛藥物大于2周;長期使用糖皮質激素;雙側肢體同期手術;嚴重的復合外傷;認知功能障礙;妊娠期婦女。中途退出標準:在麻醉后復蘇室(post anesthesia care unit,PACU)內出現中、重度疼痛的患者(NRS≥4);隨訪過程中患者因除疼痛以外的原因要求退出。
1.2 麻醉及鎮痛方法 麻醉訪視時取得書面知情同意,并向患者解釋疼痛NRS評分的使用方法,記錄術前NRS評分。患者進入麻醉誘導室后開放上肢靜脈,面罩吸氧,靜脈注射1~2 mg咪達唑侖,50 μg芬太尼。根據手術部位選擇阻滯方式,在超聲引導下進行神經阻滯,并記錄阻滯完成的時間。在神經阻滯后大約30 min通過針刺法測定痛覺阻滯區域,確定手術區域阻滯完全。術中由負責麻醉的主治醫師判斷是否聯合喉罩全身麻醉、鎮靜或腰麻。術畢給予丙帕他莫2 g 靜脈滴注,靜注特耐40 mg或氟比洛芬酯40 mg。術后鎮痛采用舒芬太尼PCIA,持續劑量2 μg/h,患者自控給藥4 μg/次,鎖定時間6 min。PCIA作為患者出現中、重度疼痛的補救措施。
1.3 術后隨訪 在神經阻滯完成后,在24 h和48 h隨訪2次,詢問患者出現疼痛峰值的時間并采用NRS法描述峰值疼痛。如患者描述峰值疼痛達到中、重度疼痛(NRS≥4),請患者回憶疼痛發生的時間以及疼痛的性質、持續時間和緩解措施。
1.4 統計學處理 由于這是一項觀察性的研究,本研究并沒有進行樣本量估計。對有序分類變量采用中位數描述,采用非參數檢驗進行變量比較。采用單因素及多因素logistic回歸比較各因素與中、重度疼痛發生的相關性。所有統計資料采用SPSS 24.0統計軟件包進行分析處理,檢驗水準(α)為0.05。
2 結 果
2.1 一般資料 共納入了31例骨科手術患者。患者的人口統計學數據及手術、麻醉的資料見表1。神經阻滯使用的局麻藥物為濃度0.375%的羅哌卡因(單純神經阻滯)或0.25%的羅哌卡因(神經阻滯聯合全身麻醉或腰麻)。所有患者術后均無嚴重的不良反應發生。
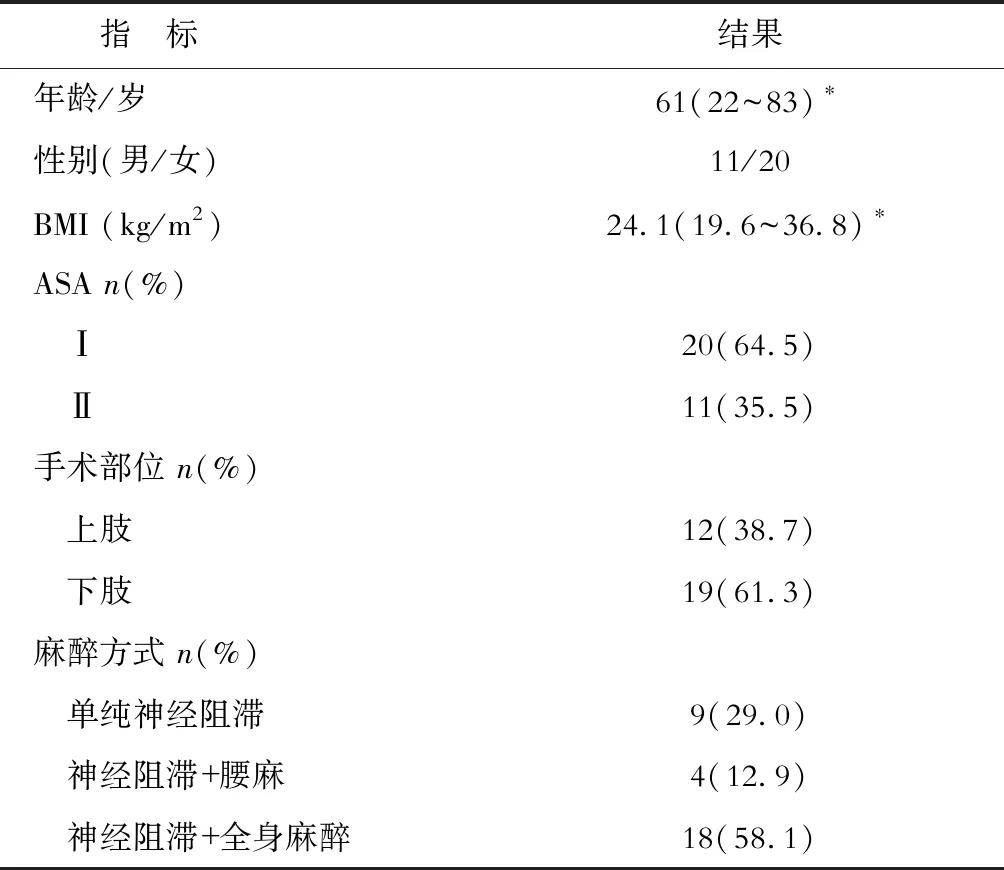
表1 患者一般臨床資料 N=31
BMI:體質指數;ASA:美國麻醉醫師協會.*中位數(范圍)
2.2 術后疼痛情況 31例患者中,術后峰值疼痛達到中、重度疼痛(NRS≥4)的患者25例(80.6%),其中重度疼痛(NRS≥7)15例(48.4%),中度疼痛(4≤NRS<7)10例(32.2%)。6例患者描述峰值疼痛NRS<4,對睡眠和活動都不造成影響,無法提供疼痛開始的具體時間。峰值疼痛NRS評分為7(6~8)[中位數(四分位距)](圖1A),峰值疼痛發生時間點距離阻滯時間點的間隔為16.8 h(12.3~22.9 h)[中位數(四分位距)](圖1B)。患者描述的疼痛峰值評分和其對應發生的時間見圖2,疼痛出現的時間越晚,NRS評分越低(P<0.05)。NRS大于或等于4時,患者幾乎都能明確說出疼痛開始的確切時間。NRS≥7時,尤其當疼痛在夜間出現時,患者往往表述是被疼痛驚醒,為刺痛并且疼痛令其難以再次入睡,阿片類藥物無法緩解這種暴發性的重度疼痛。經30 min~1 h疼痛緩解。
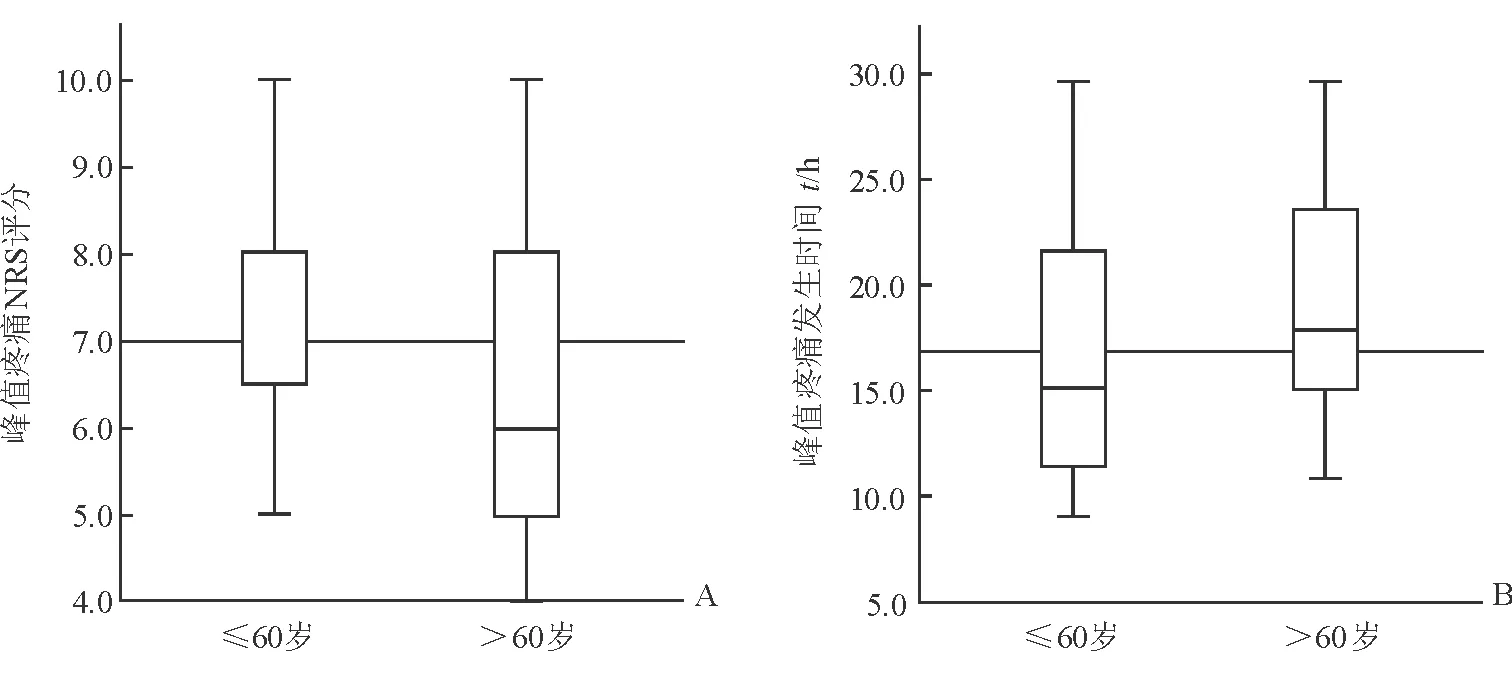
圖1 發生中、重度疼痛患者的峰值疼痛評分(A)和峰值疼痛發生時間(B)

圖2 患者峰值疼痛發生時間和NRS評分r=-0.239,P=0.011
為進一步分析不同年齡階段疼痛發生的情況,我們將患者按照是否大于60歲分為兩組:年齡≤60歲組(n=15)和年齡>60歲組(n=16)。兩組患者術后中、重度疼痛的發生率見表2,發生率的差異有統計學意義(P=0.01)。對發生中重度疼痛的患者的數據進一步分析發現,年齡≤60歲組的峰值疼痛NRS評分高于年齡>60歲組,峰值疼痛出現的時間也早于年齡>60歲組,但差異無統計學意義(表3)。

表2 兩組患者峰值疼痛情況比較 n (%)
NRS:疼痛數字評分

表3 兩組中重度疼痛患者情況比較
NRS:疼痛數字評分
2.3 暴發痛的危險因素 用單因素logistic相關系數分析對發生中、重度疼痛的危險因素進行篩選,其中與性別、BMI、ASA分級、手術部位是上肢或下肢的相關性無統計學意義,年齡和麻醉方式的相關性有統計學意義(表4)。單純進行PNBs麻醉的患者暴發痛的發生率要高于PNBs聯合腰麻或全身麻醉的患者,年齡增長暴發痛現象減少。

表4 中、重度疼痛的危險因素分析
BMI:體質指數;ASA:美國麻醉醫師協會
3 討 論
周圍神經阻滯是四肢手術中常用的麻醉方式。關于神經阻滯的研究常提及阻滯消退期的重度疼痛,但是對這一類暴發痛并無明確的定義和診斷標準,將其稱為“rebound pain”。本研究對神經阻滯恢復期疼痛進行了深入的研究,發現在術后使用阿片類藥物PCIA的情況下,實施了PNBs麻醉的骨科手術患者在阻滯效果消退后出現中、重度疼痛(NRS≥4)的比例達到80.6%(25/31),其中重度疼痛(NRS≥7)的比例為48.4%。這與Sort和Brorson等[6]在研究腘窩坐骨神經阻滯下實施急診踝關節骨折切開復位內固定術后產生中度(80%)和重度(35%)疼痛的比例相似。本研究在隨訪過程中詳細記錄了患者對疼痛的描述,發現NRS<4的患者往往不能明確回憶起疼痛開始的時間,對疼痛的描述通常是在患肢活動過程中感到的不適。當NRS≥4時,患者幾乎都能明確說出疼痛開始的確切時間,與之前阻滯完善時存在明顯的分界。而當NRS≥7時,尤其當疼痛在夜間出現時,患者往往表述是被疼痛驚醒,且疼痛令其難以再次入睡,阿片類藥物無法緩解這種暴發性的重度疼痛。這種從“無”到“有”的暴發式疼痛,除了生理上的不適,更帶來了心理上的恐慌,超過了患者對術后疼痛的心理預期,降低了患者對整體醫療的滿意度。對于合并心血管疾病的患者更可能增加術后心血管事件的發生率。Galos等[5]比較了全身麻醉和神經阻滯下行橈骨遠端骨折切開復位內固定術的術后疼痛的特點:術后2 h全身麻醉組的疼痛評分超過神經阻滯組,12 h時間點神經阻滯組疼痛評分超過全身麻醉組。也有研究發現暴發痛一般出現在術后12~24 h[4,7]。本研究記錄了從阻滯完成后到出現峰值疼痛的時間中位數為16.8 h(IQR12.3~22.9 h),在進行四肢手術的麻醉選擇時應該將術后暴發痛的發生納入考量因素,與患者充分進行溝通,提前交待術后12~24 h內發生暴發痛的可能并指導做好橋接鎮痛。
本研究還觀察到年齡≤60歲的患者術后暴發痛發生率高于60歲以上的患者,可能與隨年齡增長痛覺閾值變化有關[8],年輕組出現峰值疼痛的時間要早于年長患者;還發現峰值疼痛發生的時間與疼痛評分之間存在聯系,峰值疼痛出現的時間越晚,疼痛的NRS評分越低。這提示通過延長神經阻滯的時間可能會減輕暴發痛的嚴重程度。在已知的可以延長阻滯時間的措施中,連續周圍神經阻滯操作和術后管理的難度較大,通過在局麻藥中添加佐劑來延長阻滯時間則更容易實施。可樂定、右美托咪定、地塞米松等在既往的研究中都被認為能夠延長神經阻滯的持續時間,其對于暴發痛的影響尚待研究[9]。進一步嘗試篩選術后發生中、重度疼痛可能的危險因素,發現患者的性別、體質指數(BMI)、ASA分級、手術部位是上肢或是下肢與暴發痛的發生無關,僅與麻醉方式和年齡可能相關。單純進行PNBs麻醉的患者暴發痛的發生率要高于PNBs聯合腰麻或全身麻醉的患者。在既往相關的臨床研究中并未見到類似報道,推測可能是聯合麻醉時使用的局部麻醉藥濃度較低相關。Janda等[10]的動物研究發現,盡管超聲下進行PNBs可以減少直接的神經損傷,但是阻滯時的穿刺和注射藥物時的壓力創傷都會引起神經周圍的炎性反應。另外,全身麻醉時為了減少術后惡心嘔吐的發生會使用地塞米松。有Meta分析顯示地塞米松無論靜注還是作為局麻藥佐劑用于神經周圍,均可延長神經阻滯時間。是否因此減少了術后暴發痛的發生仍需要進一步的臨床研究證實[11]。
本研究首次對PNBs麻醉術后產生暴發性疼痛的現象進行了詳細描述,發現進行PNBs麻醉的骨科手術術后暴發性中、重度疼痛的發生率較高,尤其是≤60歲的患者發生率高于年齡>60歲的患者。暴發痛通常在阻滯后的12~24 h發生,隨著發生時間的延后,暴發痛的程度有所下降。單純的PNBs麻醉術后比聯合麻醉更容易發生暴發痛。這些觀察結果為今后的隨機對照臨床研究提供一定的思路,以進一步探索減少暴發痛的措施,提高術后鎮痛的質量。

