苓澤合劑對急性痛風性關節炎大鼠血清 IL-6、TNF-α含量的影響
趙用 劉佳 馬寶東 陳巖松 張宏 喬敏 甘雨
〔摘要〕 目的 觀察苓澤合劑對尿酸鈉誘導的大鼠痛風性關節炎的抗炎作用,并探討其作用機制。方法 將80只Wistar大鼠隨機分為空白組、模型組、芬必得組、苯溴馬隆組、痛風定組及苓澤合劑低、中、高劑量組,每組10只。用尿酸鈉誘導大鼠痛風性關節炎,測定血清中白細胞介素-6(interlenkin 6, IL-6)、腫瘤壞死因子-α(tumor necrosis factor-α, TNF-α)的含量。結果 與模型組比較,各給藥組血清中IL-6與TNF-α的含量均顯著降低(P<0.01) 。苓澤合劑中劑量組、高劑量組與低劑量組比較,血清中 IL-6、TNF-α的含量明顯下降(P<0.05)。結論 苓澤合劑可抑制急性痛風性關節炎大鼠IL-6、TNF-α的表達,治療痛風性關節炎。
〔關鍵詞〕 苓澤合劑;痛風性關節炎;IL-6;TNF-α。
〔中圖分類號〕R285.5;R684.3? ? ? ?〔文獻標志碼〕A? ? ? ?〔文章編號〕doi:10.3969/j.issn.1674-070X.2019.01.007
Effect of Lingze Mixture on Serum Levels of IL-6 and TNF-α in Rats with Acute Gouty Arthritis
ZHAO Yong, LIU Jia, MA Baodong*, CHEN Yansong, ZHANG Hong, QIAO Min, GAN Yu
(Department of Rheumatology, The Second Affiliated Hospital of Liaoning University of Traditional Chinese Medicine, Shenyang, Liaoning 110034, China)
〔Abstract〕 Objective To explore the anti-inflammatory effect of Lingze Mixture on monosodium urate (MSU) crystal-induced gouty arthritis in rats and its mechanism of action. Methods Eighty Wistar rats were randomly divided into blank group, model group, fenbid group, benzbromarone group, Tongfengding group, and traditional Chinese medicine (TCM) Lingze Mixture groups (low, medium, and high doses), with ten rats in each group. A rat model of gouty arthritis was established by MSU crystals. Then the serum levels of interleukin-6 (IL-6) and tumor necrosis factor-α (TNF-α) were determined. Results Compared with the model group, levels of IL-6 and TNF-α in serum in each model group were significantly decreased (P<0.01). Compared with the low-dose Lingze Mixture group, the medium-and high-dose Lingze Mixture groups had significantly reduced serum levels of IL-6 and TNF-α (P<0.05). Conclusion Lingze Mixture can inhibit the expression of IL-6 and TNF-α in rats with acute gouty arthritis, thus achieving the aim of preventing and alleviating gouty arthritis.
〔Keywords〕 Lingze Mixture; gouty arthritis; interleukin-6; tumor necrosis factor-α
痛風性關節炎是由于血尿酸升高而導致尿酸鹽(monosodium urate,MSU)在關節囊、滑囊、軟骨、骨質和其他組織中形成微晶體沉淀,引起非特異性的炎性反應[1],MSU在關節周圍組織沉積,刺激局部組織細胞膜形成破裂,引起白細胞的活化和吞噬,產生大量炎性細胞,釋放白細胞介素-6(interlenkin 6, IL-6)、腫瘤壞死因子-α(tumor necrosis factor-α, TNF-α)等細胞因子,導致如局部血管擴張、白細胞集聚、血漿滲出、滲透性增加等一系列的連鎖炎癥反應,局部組織易被溶解侵蝕,使痛風性關節炎患者出現劇烈疼痛,局部紅腫發熱的癥狀[2-4]。本病在中醫學屬于“歷節病”“痹證”等范疇[5],苓澤合劑為我院協定方,臨床用治痛風性關節炎十余年,由土茯苓、澤瀉、蒼術等9味中藥組成,有清熱消腫、利濕除痹、通絡止痛之功。本實驗采用MSU引起急性痛風性關節炎動物模型[6],觀察苓澤合劑對急性痛風性關節炎大鼠血清中IL-6和TNF-α含量的影響,以探討苓澤合劑對痛風性關節炎治療的部分作用機制。
1 材料與方法
1.1? 實驗動物
80只健康雄性Wistar大鼠,質量(200±20)g,由遼寧長生生物技術有限公司購入,公司許可證號:SCXK(遼)2015-0001。
1.2? 實驗藥物
苓澤合劑(組成:土茯苓30 g,澤瀉30 g,川黃柏20 g,蒼術15 g,知母25 g,生姜10 g,當歸20 g,白芍15 g,紅花15 g),由遼寧中醫藥大學制劑中心制備,生藥濃度4.3 g/mL;芬必得,由中美天津史克制藥有限公司生產,批號:16110441,規格:0.3 g/粒;苯溴馬隆片,Excella GmbH(德國,昆山龍燈瑞迪制藥有限公司分裝),批號:1604591,規格:50 mg/片;痛風定膠囊,四川升和藥業股份有限公司,批號:1609104,規格:0.4 g/粒;尿酸鈉,美國Sigma公司,批號:1122B052,規格:10 mg/瓶。
1.3? 儀器與試劑
BS6005型電子天平(上海友聲衡器有限公司),BSZOOS型電子天平(北京賽多利斯天平有限公司),RB-200型智能熱板儀(淮北正華生物儀器有限公司),UV1700紫外可見分光光度計(日本島津公司),Anke TDL-60C離心機(上海安亭科學儀器廠),IL-6、TNF-α試劑盒(北京奇松生物科技有限公司)。
1.4? 造模方法
取尿酸鈉研磨成粉,過篩,用滅菌注射用水制成100 mg/mL尿酸鈉溶液。參考相關文獻[6],在無菌條件下,模型組和各給藥組將配制好的尿酸鈉溶液0.1 mL用6號注射針注入大鼠右后足跖皮下。空白組大鼠給予同體積生理鹽水。
1.5? 給藥方法
按照“人與動物體表面積換算的等效劑量”換算方法計算大鼠給藥量,將80只大鼠按每組10只隨機分成空白組、模型組、芬必得組(0.144 g/kg)、苯溴馬隆組(18 mg/kg)、痛風定組(0.86 g/kg)、苓澤合劑中劑量組(33.30 g/kg)、低劑量組(50%中劑量組藥量,即16.65 g/kg)、高劑量組(200%中劑量組藥量,即66.60 g/kg)。給藥組大鼠按上述劑量口服給予相應藥物20 mL/kg,空白組和模型組給予同體積的蒸餾水,1次/d,連續給藥7 d。末次給藥后30 min造模,24 h后取血檢測相應檢查指標。
1.6? 指標檢測
造模后4 h眼眶取血2 mL,以4 000 r/min離心15 min,按試劑盒檢測步驟及方法,采用酶聯免疫法(ELISA)成批檢測大鼠血清中IL-6、TNF-α的含量。
1.7 統計學處理
運用SPSS 17.0統計學軟件進行實驗數據分析,計量資料用“x±s”表示,采用單因素方差分析比較多組樣本的差異,以P<0.05為差異有統計學意義。
2 結果
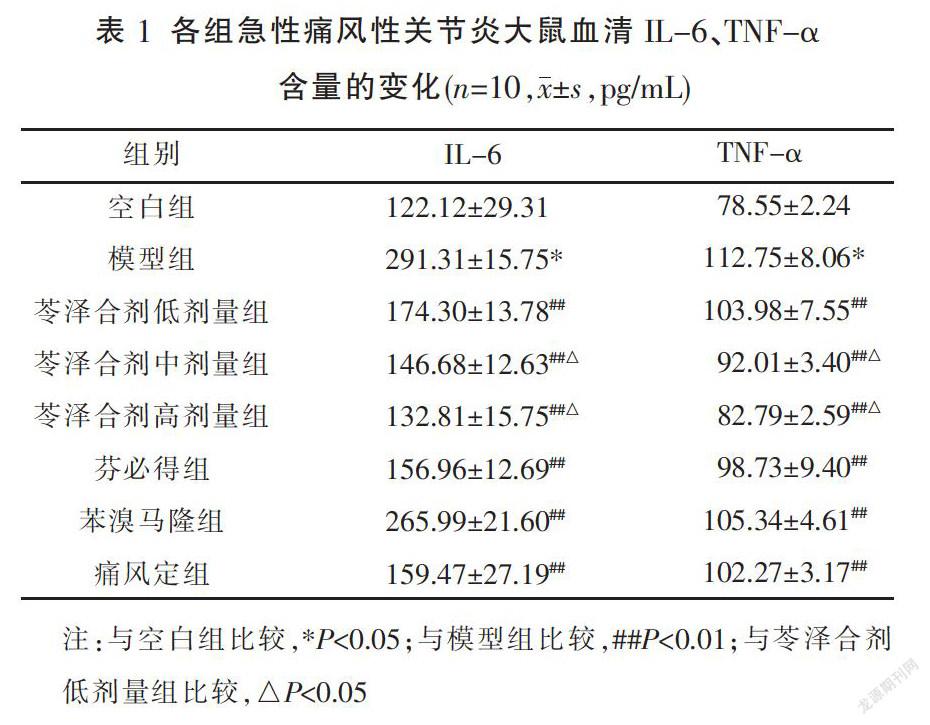
與空白組相比較,模型組血清IL-6、TNF-α含量均顯著升高(P<0.05),表明造模成功;與模型組相比較,各給藥組血清中IL-6、TNF-α含量均顯著降低(P<0.01);與苓澤合劑低劑量組比較,苓澤合劑中、高劑量組血清中IL-6、TNF-α含量顯著降低(P<0.05);苓澤合劑中劑量組和高劑量組比較差異無統計學意義(P>0.05)。結果見表1。
3 討論
現代研究認為,急性痛風性關節炎的根本原因是高尿酸血證及其導致的關節局部MSU結晶的析出。在急性痛風性關節炎的發生及發展過程中,作為炎癥趨化因子和激活因子的IL-6、TNF-α起重要作用。IL-6是多功能炎性細胞因子,是炎性介質網絡的關鍵成分,在炎癥反應中起重要作用。IL-6不僅參與炎癥反應,增加滑膜組織的炎癥細胞,而且直接導致炎癥,同時也通過促進其他炎癥介質的釋放間接導致炎癥,并可趨化激活中性粒細胞。由此可見,IL-6既是炎癥反應的重要介質,更是調節炎癥的始動因素,在急慢性痛風性關節炎的病程中,都起著極為重要的作用,更有學者將 IL-6作為判斷痛風性關節炎疾病活動性和嚴重程度的指標[7]。TNF-α主要由單核巨噬細胞和中性粒細胞分泌,為介導炎癥反應的核心物質和前炎癥網鏈中的一級細胞因子。一般認為,中性粒細胞、內皮細胞黏附是急性痛風性關節炎產生的本質,TNF-α可增加中性粒細胞的募集,上調內皮細胞選擇素活性,使中性粒細胞和內皮細胞表面的黏附分子結合,為促炎癥介質,可對局部部位產生浸潤,導致炎性介質釋放,引起關節局部如紅腫熱痛等炎癥反應。TNF-α水平的變化既是急性痛風性關節炎發病的機制,也可反映關節炎癥反應的輕重,已被用于治療痛風藥物療效評價[8-9]。由上述發病機制可見,IL-6、TNF-α在痛風性關節炎的炎癥病情中發揮著重要的作用。因此,抑制兩者產生并阻斷其所介導和激發的炎癥過程,對緩解急性痛風性關節炎病情有積極意義。
中醫學認為本病的病因或為飲食不節,嗜食肥甘厚味;或為脾腎虧虛,導致濕熱內蘊,由外感風寒或日久化瘀,致營衛行澀,濕熱瘀阻,經絡不通,痹阻經絡[10]。治療應以清熱消腫、利濕除痹、通絡止痛為主。苓澤合劑由土茯苓、澤瀉、知母、蒼術、川黃柏、當歸、紅花、生姜和白芍九味中藥組成。方中土茯苓、澤瀉清熱、消腫、利濕,為君藥,兩者均具有較強的抗炎作用,土茯苓鎮痛作用較強,澤瀉亦可利尿[11-12]。知母、蒼術、川黃柏清熱、利濕,為臣藥。三者均有減輕炎癥損傷的藥理作用,知母還可保護血管內皮、抑制血管通透性、減輕水腫,蒼術有明確的抑制IL-6、TNF-α及IL-8、PGE2等炎性因子的作用,川黃柏還可保護腎臟、抑制免疫等[13-15]。當歸、紅花活血除痹、通絡止痛,為佐藥。兩者除減輕炎癥損傷及拮抗多種炎癥因子外,當歸還具有鎮痛等功效[16-17]。生姜、白芍一溫中化濕,一緩急止痛,為使藥,兩者均具抗炎等功效,白芍還有調和諸藥、鎮痛、抗自身免疫病等作用[18-19]。上述諸藥合用,共奏清熱消腫、利濕除痹、通絡止痛之功,其現代藥理學作用也部分揭示苓澤合劑在治療痛風性關節炎過程中的基本作用機制。
近年來,我國高尿酸血癥及痛風的患病率逐年增加。西醫目前用于治療急性痛風性關節炎的藥物主要為秋水仙堿和非甾體類抗炎藥,其胃腸道不良反應較多,常有肝腎損害,嚴重者可出現骨髓抑制。中藥湯劑苓澤合劑藥味組合簡單常見,有較高的安全性,且性價比適宜,治療痛風性關節炎療效明確,值得臨床推廣。
參考文獻
[1] 劉安寧,張高生,黃? 晶,等.香芹酚對大鼠痛風性關節炎中血清炎性因子及軟骨細胞凋亡的影響[J].臨床和實驗醫學雜志,2017,16(6):531-534.
[2] TONY M. Genomic Influences on Hyperuricemia and Gout[J].Rheumatic Disease Clinics of North America, 2017,43(3):389-399.
[3] 陸小龍,曾? 朋,向黎黎,等.蠲痹歷節清酊對大鼠急性痛風性關節炎模型滑膜組織中ICAM-1、NF-κB表達的影響[J].湖南中醫藥大學學報,2017,37(12):1299-1302.
[4] 周? 彪,郭玉星,陸小龍,等.蠲痹歷節清方對大鼠痛風性關節炎關節腫脹指數和滑膜組織中炎癥因子的影響[J].云南中醫學院學報,2017,40(3):15-18,32.
[5] 張劍勇,王? 輝,謝靜靜,等.痛風泰顆粒對急性痛風大鼠IL-1、IL-6及TNF-α含量的影響[J].新中醫,2016,48(12):201-203.
[6] DHANASEKAR C,RASOOL M. Morin, a dietary bioflavonol suppresses mon-osodium urate crystal-induced inflammation in an animal model of a-cute gouty arthritis with reference to NLRP3 inflammasome,hypo-xan-thine phosphor-ribosyl transferase,and inflammatory mediators[J]. Eur J Pharmacol,2016,7(86): 116-127.
[7] FERNANDO M, GIEMBYCZ M, MC K. Bidirectional crosstalk via IL-6,PGE2 and PGD2 between murine myofibroblasts and alternative-ly activated macrophages enhances anti-inflammatory phenotype in both cells[J]. Br J Pharmacol,2016,173(5): 899-912.
[8] 劉昌盛,陳? 昉,何? 穎,等.白子菜提取物對急性痛風性關節炎大鼠模型抗炎作用的研究[J].湖南中醫藥大學學報,2016,36(8):26-29,81.
[9] GAO F, YANG Y, FENG X, et al. Interleukin-27 is elevated in sepsis-induced myocardial dysfunction and mediates inflammation[J]. Cyto-kine,2016,8(8): 1-11.
[10] 謝興文,王春亮,徐世紅,等.忍冬藤痛風顆粒對痛風性關節炎模型大鼠MMP-3和LP-PLA2的影響[J].中國中醫骨傷科雜志,2016,24(2):6-8.
[11] 侯瑋婷,羅佳波.復方茯苓多糖口服液抗腫瘤作用和免疫調節功能的初步研究[J].中藥藥理與臨床,2017,32(2):78-81.
[12] 汪錦飄,劉永茂,何志超,等.澤瀉乙醇提取物對氧嗪酸鉀鹽致大鼠高尿酸血癥模型的影響[J].中成藥,2017,39(3):605-608.
[13] 林? 彬.黃柏生品與各種炮制品滋陰及抗痛風作用比較[J].醫學理論與實踐,2017,29(19):3304-3305.
[14] 龐? 雪,劉玉強,才? 謙,等.蒼術麩炒前后活性部位藥效比較研究[J].中國藥房,2016,27(10):1308-1311.
[15] 司曉麗,王? 燕,黨文呈,等.百合知母湯對支氣管哮喘大鼠氣道炎癥的影響[J].中醫雜志,2017,58(14):1499-1502.
[16] 李? 琴.當歸拈痛湯加減聯合刺絡放血法治療急性痛風性關節炎臨床觀察[J].云南中醫中藥雜志,2017,38(3):18-19.
[17] 張彥麗,張碩峰,華國棟,等.紅花對華法林抗凝作用的影響[J].中醫藥信息,2016,33(1):32-35.
[18] 姜衛星,王海燕,索成云,等.生姜醇提取物對肝臟缺血再灌注大鼠氧化應激損傷的保護作用[J].中醫藥信息,2017,34(2):9-13.
[19] 李振彬,馬? 旭,楊? 靜,等.白芍總苷治療大鼠急性痛風性關節炎的作用及對血清IL-1β、IL-6、TNF-α的影響[J].新醫學,2017,48(6):380-384.

