微波輔助酸處理桉木預水解液純化制備低聚木糖
董吉冉 楊桂花 吉興香 徐豐 陳嘉川



摘 要:為利用桉木預水解液制備低聚木糖,對經過Ca(OH)2和活性炭處理的二級處理預水解液進行微波輔助酸處理,探討了處理過程中酸類型、酸用量、處理溫度和處理時間對預水解液中木糖及聚合度為2~4低聚木糖(低聚木糖DP2~4)含量的影響,并對處理后預水解液中的低聚木糖進行了分析與表征。結果表明,微波輔助酸處理二級處理預水解液較優工藝條件為:硫酸用量1.4%、處理溫度120℃、處理時間 20 min,在此條件下,經過微波輔助酸處理所制備的三級處理預水解液中低聚木糖DP2~4含量為9.25 g/L,與未經微波輔助酸處理二級處理預水解液相比,其低聚木糖DP2~4含量提高了38.1%,預水解液中低聚木糖DP2~4組分得到了進一步純化。傅里葉變換紅外光譜(FT?IR)和熱重分析(TGA)結果表明,微波輔助酸處理桉木預水解液純化制備的低聚木糖含有部分阿拉伯糖及糖醛酸側鏈,且該低聚木糖具有較高的熱穩定性。
關鍵詞:桉木;預水解液;低聚木糖;微波;酸水解
中圖分類號:TS79
文獻標識碼:A
DOI:10.11980/j.issn.0254?508X.2019.06.002
Improvement of Xylo?oligosaccharides Content of Eucalyptus Pre?hydrolysis
Liquor with Microwave?assisted Acid Treatment
DONG Jiran YANG Guihua* JI Xingxiang XU Feng CHEN Jiachuan*
(State Key Lab of Bio?based Materials and Green Papermaking/Key Lab of Pulp & Paper Science and Technology of Education
Ministry of China,
Qilu University of Technology (Shandong Academy of Sciences), Jinan, Shandong Province, 250353)
(*E?mail: ygh@qlu.edu.cn;chenjc@qlu.edu.cn)
Abstract:In this work,microwave?assisted acid treatment was used to prepare xylo?oligosaccharides(XOS) from the secondary Eucalyptus pre?hydrolysis liquid(PHL) which had been treated by Ca(OH)2 and activated carbon successively. The effects of the kinds of acid, acid dosage, treatment temperature and treatment time on xylose and XOS DP2~4 contents were investigated and the prepared XOS DP2~4 were characterized. The results showed that the optimal treatment conditions were sulfuric dosage of 1.4%(based on the weight of secondary Eucalyptus PHL), 120℃ and 20 min, the content of XOS DP2~4 of the third PHL was 9.25 g/L, increased by 38.1% compared to the secondary PHL without microwave?assisted acid treatment.Analyses of Fourier Transform infrared spectroscopy(FT?IR) and Thermo gravimetric(TGA) showed that XOS from the microwave?assisted sulfuric acid treatment process contained part of side?chains of arabinose and uronic acid, and showed a high thermal stability.
Key words:Eucalyptus; pre?hydrolysis liquid; xylo?oligosaccharides; microwave; acid treatment
溶解漿作為一種高純度精制漿,廣泛應用于黏膠纖維、醋酸纖維、玻璃紙、紡織品等生產領域,其市場需求量不斷提高[1]。在利用闊葉木生產硫酸鹽法溶解漿的過程中,為降低木質纖維組分分離過程中的化學品消耗量,提高溶解漿質量,通常先對原料進行預水解溶出部分半纖維素,因此預水解過程會產生大量的預水解液[2]。預水解液中含有豐富的半纖維素糖類、少量木素、糠醛、乙酸等[3]。一些企業將預水解液與黑液混合燃燒產生熱量,一定程度上造成了半纖維素資源的浪費。闊葉木預水解液中含有的半纖維素糖類主要是低聚合度木糖,因而預水解液成為生產低聚木糖的良好資源,具有較高的利用價值[4]。
低聚木糖(xylo?oligosaccharides,XOS)又稱木寡糖,是由2~7個木糖分子通過β?14糖苷鍵連接而成的功能性低聚糖,其主要有效成分為木二糖、木三糖和木四糖[5]。低聚木糖具有良好的理化性質,如可選擇性增殖腸道益生菌、改善腸道功能、降低膽固醇、促進鈣吸收及脂質代謝等。另外,由于低聚木糖不能被人體消化吸收,因而可滿足肥胖癥人及糖尿病人對甜度的需求[6?8]。因此近年來,低聚木糖產品廣泛應用于醫藥、食品等領域。
目前,國內外制備低聚木糖的方法主要有熱水抽提法、酶解法、酸解法及微波降解法[9]。熱水抽提法操作簡單、無污染,但是反應過程需要高溫高壓的環境,對設備要求較為苛刻,產物含量低且純化工藝較為繁瑣[10];酶解法反應條件溫和,對設備無特殊要求,反應過程中產生的副產物較少,但是酶處理所需反應時間較長,且對酶的純度要求較高,大大提高了生產成本,不利于工業化使用[11];酸解法過程簡單,反應時間短,生產成本低,是目前較為常用的處理方法,但是傳統酸水解是通過熱對流或熱傳導進行加熱,加熱效率較低[12];微波降解法是一種綠色環保、方便簡單的加熱方式,具有加熱速率快、可選擇性加熱、對熱能消耗量少及反應副產物少、所得產物純度高等優點[13],但是單一的微波處理大多限于實驗室研究階段。因此,將酸處理與微波處理相結合,既能彌補傳統酸處理過程中加熱效率低的不足,又能夠在一定程度上實現工業化應用。
本研究以桉木預水解液為原料,基于預水解液中低聚木糖主要成分為木二糖、木三糖及木四糖,首先通過Ca(OH)2處理和活性炭吸附去除預水解液中木素、糠醛等雜質,得到二級處理預水解液,然后對二級處理預水解液進行微波輔助酸處理制備富含低聚木糖DP2~4(聚合度為2~4的低聚木糖)的三級處理預水解液。探討了微波輔助酸處理過程中酸類型、酸用量、處理溫度及處理時間對三級處理預水解液中低聚木糖DP2~4含量的影響,以優化工藝條件;并將酸處理后所制備的低聚木糖與目前市場上的低聚木糖產品進行了對比分析,為后續預水解液的高值化利用提供技術支持與理論指導。
1 實 驗
1.1 原料及試劑
桉木預水解液,由山東太陽紙業有限公司提供;活性炭(磷酸活化、木質、過200目),購于廣東海燕活性炭有限公司;Ca(OH)2、硫酸(H2SO4)、鹽酸(HCl)及乙酸(CH3COOH),均為分析純,購于天津恒興試劑有限公司;H3PO4(色譜純)、KBr(光譜純),購于天津科密歐化學試劑有限公司;液體NaOH(色譜純,純度50%),由美國Thermo?Fisher公司提供;標準品木糖、木二糖(X2)、木三糖(X3)及木四糖(X4),購于上海意果科技有限公司;透析袋(直徑22 mm,壓平寬度34 mm,長度5 m,相對分子質量200,購于美國邁姆生物科技有限公司;商品低聚木糖(食品級,XOS?95),購于山東龍力公司。
1.2 實驗方法
1.2.1 桉木二級處理預水解液的制備
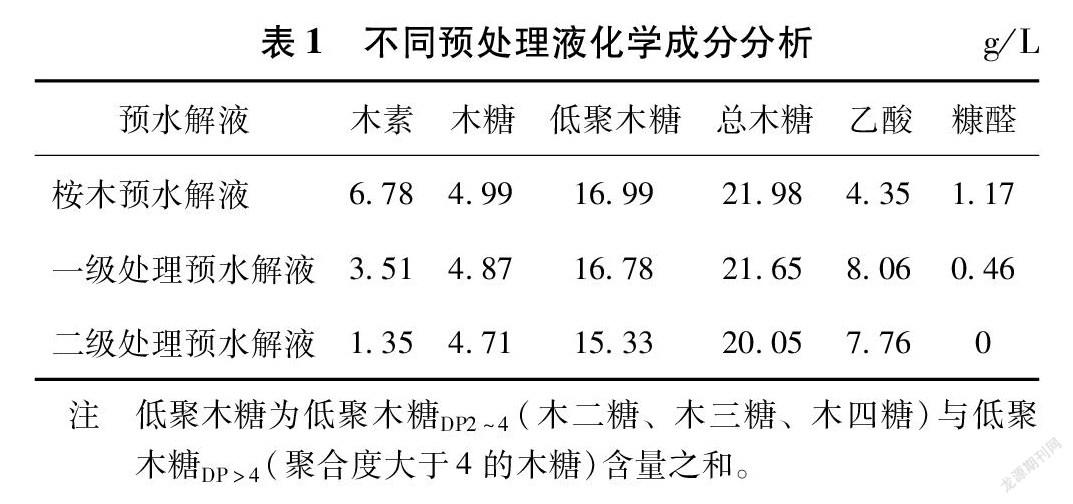
向桉木預水解液中加入1%(以預水解液質量計)的Ca(OH)2,處理10 min后離心,取上清液,稱為一級處理預水解液;向一級處理預水解液中加入用量0.8%(以一級處理液質量計)的活性炭,吸附5 min后離心,取上層清液,稱為二級處理預水解液。各級處理液中木素、木糖及乙酸的含量如表1所示。
由表1中數據可知,經過二級處理后,預水解液中木素及糠醛脫除率分別為80.1%和100%,總木糖損失率為8.8%,乙酸含量提高為原來的1.78倍。二級處理預水解液中木糖及低聚木糖DP2~4的含量如表2所示。
1.2.2 微波輔助酸處理制備三級處理預水解液
微波輔助酸處理制備三級處理預水解液(即富含低聚木糖DP2~4的預水解液)的反應在微波反應器(MicroSYNTH)中進行,該反應器是變功率可控溫儀器,設定升溫時間為2 min。固定反應條件二級處理預水解液用量20 g不變,探討不同酸類型(乙酸、磷酸、鹽酸、硫酸)、不同硫酸用量(1.0%、1.4%、1.8%、2.2%,基于二級處理預水解液質量計)、不同處理溫度(100、110、120 、130℃)和不同處理時間(10、20、30 min)對三級處理預水解液中低聚木糖DP2~4含量的影響。反應完成后,將三級處理預水解液離心過濾,取上層清液用于木糖及低聚木糖DP2~4含量的檢測。
1.2.3 低聚木糖的純化
將在較優的微波輔助酸處理工藝條件下得到的三級處理預水解液置入透析袋中透析處理48 h,以除去其中剩余的小分子木素及酸根離子等雜質,透析完成后,將透析液進行旋轉蒸發除去部分水分,然后將濃縮糖液進行冷凍干燥得到低聚木糖產品,用于后續紅外光譜與熱穩定性分析。
1.3 檢測
1.3.1 預水解液中木糖、低聚木糖DP2~4及總木糖含量的檢測
將預水解液稀釋適宜倍數,采用離子色譜儀(ICS?5000型,美國Thermofisher公司)直接測定預水解液中木糖、低聚木糖DP2~4的濃度。測試過程的色譜條件[14]:分析柱為DionexCarboPacTM PA200(3 mm×250 mm),保護柱為CarboPacTM PA200(3 mm×50 mm);EC檢測器;進樣量為25 L;柱溫 30℃;流動相為100 mmol/L NaOH與500 mmol/L NaOAc溶液。
總木糖含量測定:將經過酸水解之后的預水解液稀釋適宜倍數,采用ICS?5000型離子色譜測定儀測定木糖含量,即為上清液中總木糖含量。
酸水解方法[15]:取5 mL上清液放入耐壓瓶中,加入174 L、質量分數為72%的硫酸,將耐壓瓶密封后放入油浴中,121℃下反應60 min。
1.3.2 預水解液中糠醛含量的檢測
將預水解液稀釋適宜倍數,采用高效液相色譜(LC?20AT,日本島津公司)測定預水解液中糠醛的含量。檢測條件:色譜柱為SUPELCOGEL C?610H(30 cm×7.8 mm),紫外檢測器(SPD?20A),檢測波長210 nm,柱溫30℃;0.1%的磷酸淋洗,淋洗速度為0.7 mL/min。
1.3.3 紅外光譜(FT?IR)分析
取1 mg低聚木糖樣品,與100 mg干燥KBr經瑪瑙研缽研磨后壓片,置于Vertex70傅里葉變換紅外光譜分析儀(Vertex70型,德國布魯克公司)中測試,掃描范圍為250~4250 cm-1,掃描次數為16次。
1.3.4 熱穩定性(TGA)分析
取5~10 mg低聚木糖樣品置于坩堝中,在熱重分析儀(Q50型,美國TA儀器公司)中進行測試。測試條件為:從室溫開始,在氮氣環境中以10℃/min的升溫速率升溫至600℃。
2 結果與討論
2.1 不同類型酸處理對三級處理預水解液中木糖、低聚木糖DP2~4及糠醛含量的影響
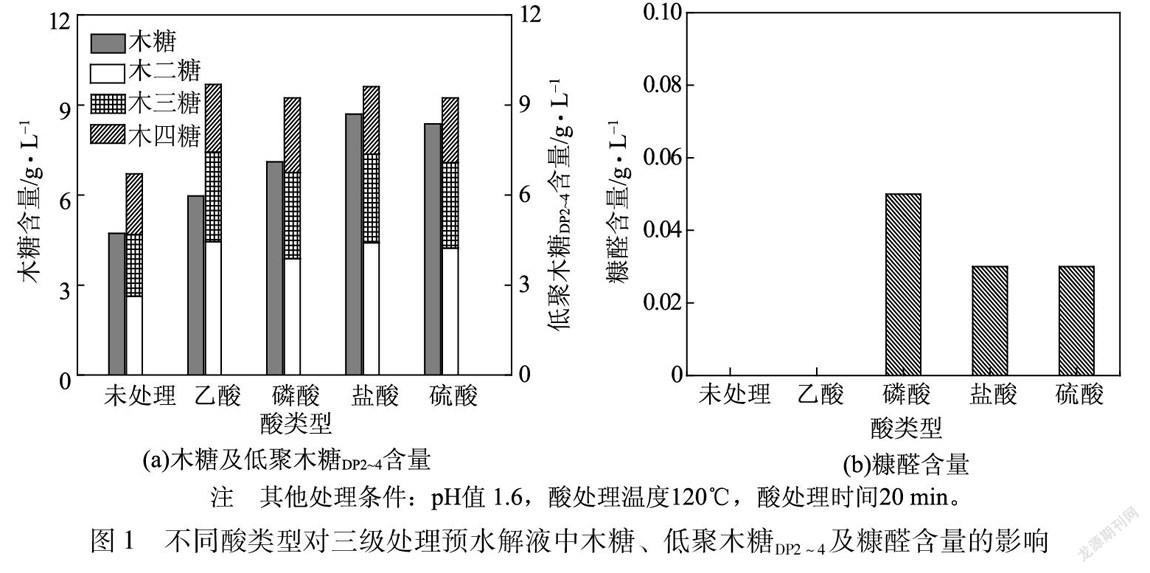
酸處理過程中不同類型酸處理對三級處理預水解液中木糖、低聚木糖DP2~4及糠醛含量的影響見圖1。由圖1可以看出,在相同的處理條件下,經過乙酸處理所制備的低聚木糖DP2~4含量最高為9.67 g/L,木糖含量較低為5.96 g/L,且無糠醛等副產物產生(見圖1(b)),表明在此條件下,仍有部分木糖以低聚木糖(聚合度>4)的形式存在。經過鹽酸處理所制備的低聚木糖DP2~4含量為9.60 g/L,木糖含量高達8.70 g/L。另外圖1顯示,經過磷酸和硫酸處理所制備的低聚木糖DP2~4含量相似,但硫酸處理所得木糖含量高于磷酸處理。出現上述現象可能與酸自身的性質有關。乙酸、磷酸、鹽酸和硫酸加入到二級處理預水解液中,分別被電解為CH3COO-、H2PO-4、Cl-及SO2-4,而不同的酸根離子具有不同的處理行為[16]。圖1表明,乙酸是較為有效的酸處理劑。但是在本實驗中,利用乙酸調節三級處理預水解液pH值至1.6,相當于乙酸用量為280%(基于二級處理預水解液質量計),而過高的乙酸用量會降低三級處理預水解液中低聚木糖DP2~4的含量,不利于低聚木糖DP2~4的純化及乙酸的回收。另外,鹽酸處理所得低聚木糖DP2~4含量略高于硫酸處理所得低聚木糖DP2~4含量,但鹽酸易揮發,不利于工業化使用。因此,考慮到工業實際生產,硫酸是較為理想的酸處理劑,后續實驗均以硫酸為處理劑進行。
2.2 硫酸用量對三級處理預水解液中木糖、低聚木糖DP2~4及糠醛含量的影響
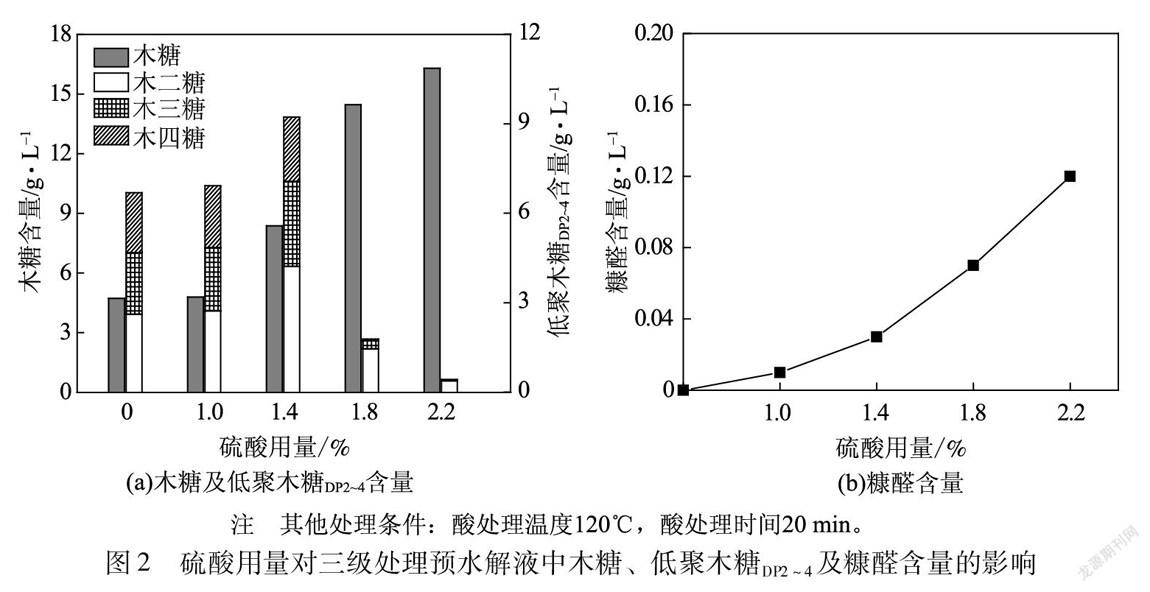
酸處理過程中硫酸用量對三級處理預水解液中木糖、低聚木糖DP2~4及糠醛含量的影響見圖2。
由圖2(a)可以看出,硫酸用量對三級處理預水解液中木糖及低聚木糖DP2~4含量的影響較大。當硫酸用量小于1.0%時,三級處理預水解液中木糖及低聚木糖DP2~4含量變化不明顯;進一步提高硫酸用量至1.4%,低聚木糖DP2~4含量不斷增加,且在硫酸用量為1.4%時達到最大值9.25 g/L,在此條件下,木糖、木二糖、木三糖及木四糖含量分別為8.38、4.23、2.85及2.17 g/L。原因可能是隨著酸用量的增加,反應體系中酸性活性位點增多,使聚合度較高的低聚木糖降解為木糖、木二糖和木三糖等聚合度較低的低聚木糖。之后,進一步提高硫酸用量至2.2%,木二糖、木三糖及木四糖含量均開始減少,低聚木糖DP2~4含量快速降低,而木糖含量快速增加。在硫酸用量為2.2%時,木糖及低聚木糖DP2~4含量分別為16.30 g/L和0.42 g/L,低聚木糖DP2~4幾乎完全降解。這是由于過量酸的加入,使溶液酸性過強,導致低聚木糖DP2~4進一步降解為木糖。另外,由圖2(b)可知,隨著硫酸用量的不斷增加,三級處理預水解液中的糠醛含量呈現一直增加的趨勢,原因可能是在較強的酸性環境下,木糖進一步被催化降解為糠醛等小分子產物[16]。然而即使在2.2%的硫酸用量下,糠醛含量仍然較低,僅為0.12 g/L。由上述分析可知,較優的硫酸用量為1.4%。
2.3 處理溫度對三級處理預水解液中木糖、低聚木糖DP2~4及糠醛含量的影響
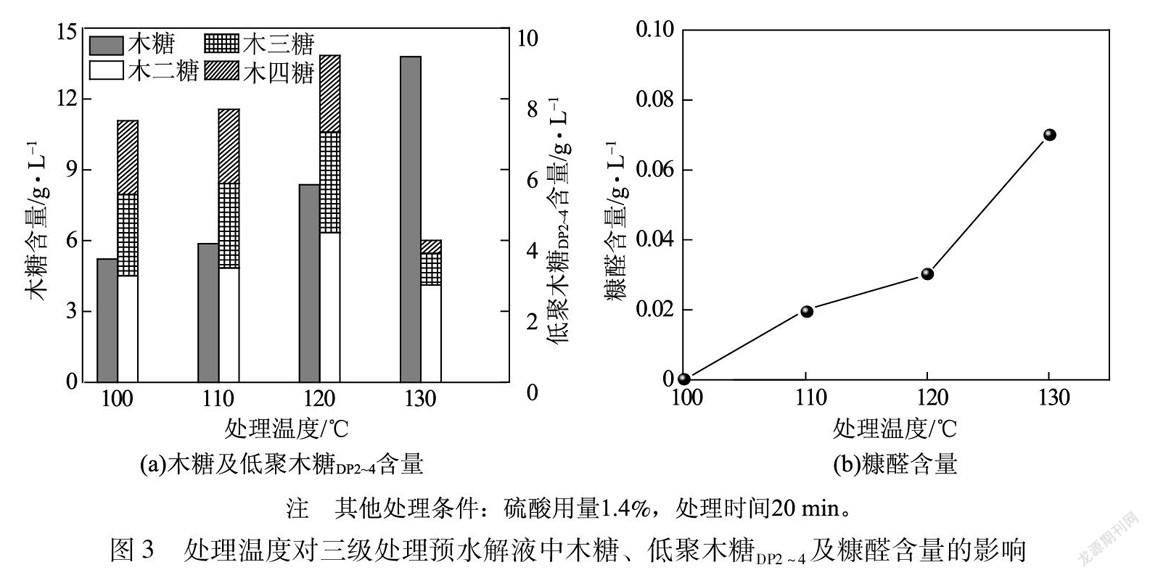
酸處理過程中處理溫度對三級處理預水解液中木糖、低聚木糖DP2~4及糠醛含量的影響見圖3。
由圖3(a)可以看出,隨著處理溫度的不斷提高,三級處理預水解液中低聚木糖DP2~4的含量呈現先增加后迅速降低的趨勢,而木糖含量呈現持續增加的趨勢。在處理溫度低于110℃時,木糖及低聚木糖DP2~4含量提高不明顯,這表明三級處理預水解液中(低)聚木糖的降解反應在相對較高的溫度下才能進行。繼續提高處理溫度至120℃,低聚木糖DP2~4含量提高至9.25 g/L,木糖、木二糖及木三糖含量明顯增加,而木四糖含量變化不明顯,這說明高溫有利于聚木糖降解為低聚木糖DP2~4。進一步提高處理溫度至130℃,木糖含量達到13.79 g/L,木二糖、木三糖及木四糖含量均降低,低聚木糖DP2~4含量降低為4.03 g/L,這表明過高的處理溫度會使低聚木糖DP2~4進一步降解為木糖。因此,酸水解制備低聚木糖DP2~4時溫度不宜過高。另外,由圖3(b)可知,隨著處理溫度的升高,糠醛含量不斷增加,在溫度為130℃時,糠醛含量仍較低,約為0.07 g/L,這說明該反應過程中產生的副產物較少。由上述分析可知,通過微波輔助酸處理桉木預水解液制備低聚木糖DP2~4的較優溫度為120℃。
2.4 處理時間對三級處理預水解液中木糖、低聚木糖DP2~4及糠醛含量的影響
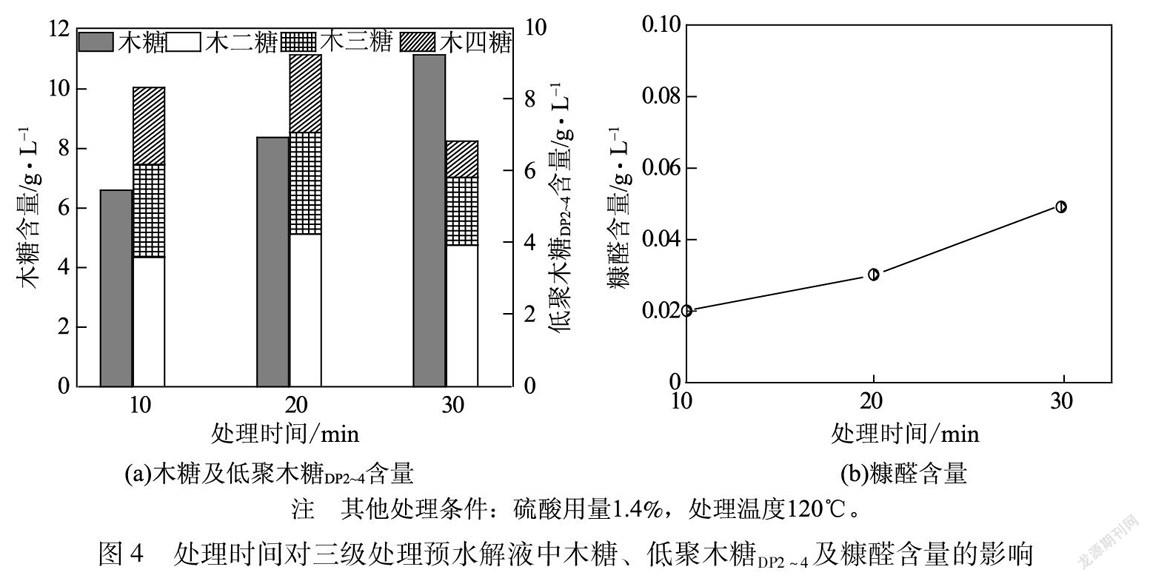
酸處理過程中處理時間對三級處理預水解液中木糖、低聚木糖DP2~4及糠醛含量的影響見圖4。
由圖4(a)可以看出,隨著處理時間的不斷增加,三級處理預水解液中低聚木糖DP2~4含量呈現先增加后下降的趨勢,而木糖含量呈現一直增加的趨勢。當處理時間增加至20 min時,低聚木糖DP2~4含量達到最大值9.25 g/L,木糖含量增加為8.38 g/L,木二糖和木三糖含量均有不同程度的增加,而木四糖含量沒有明顯變化。原因可能是聚合度>4的低聚木糖經過酸降解為木四糖的反應與木四糖降解轉化為木糖、木二糖或木三糖的反應達到了動態平衡。繼續增加反應時間至30 min,木糖含量增加為11.15 g/L,低聚木糖DP2~4含量降低為6.82 g/L。這表明在硫酸用量為1.4%、處理溫度為120℃時,較短的反應時間(20 min)即可使低聚木糖DP2~4含量較高,而增加處理時間會使低聚木糖DP2~4進一步降解為木糖。因此,通過酸處理制備低聚木糖DP2~4時需要嚴格控制處理時間。另外,由圖4(b)可知,處理時間對糠醛含量影響較小,在處理時間為30 min時,糠醛含量仍較低約為0.05 g/L。綜上所述,酸處理過程中較優的處理時間為20 min。
2.5 較優處理工藝條件下木糖及低聚木糖DP2~4含量
由2.1~2.4分析可知,微波輔助酸處理二級處理預水解液制備低聚木糖DP2~4的較優工藝條件為:硫酸用量1.4%、處理溫度120℃和處理時間20 min。在此條件下,三級處理預水解液中木糖及低聚木糖DP2~4含量如表3所示。
由表3可知,與二級處理預水解液相比,經過微波輔助酸處理后所得三級處理預水解液中木糖、木二糖和木三糖含量分別提高了3.65、1.62和0.78 g/L,而木四糖含量無明顯變化,低聚木糖DP2~4含量由原來6.70 g/L上升到9.25 g/L,提高了38.1%。
2.6 紅外光譜(FT?IR)分析
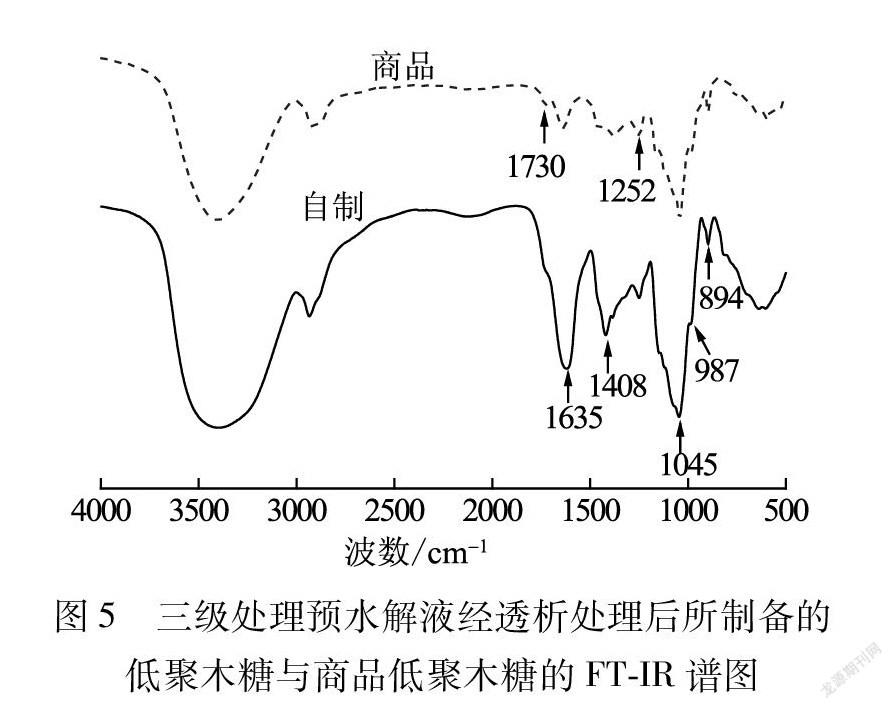
圖5為由三級處理預水解液經過透析純化處理后所制備的低聚木糖與商品低聚木糖的FT?IR譜圖。
由圖5可以看出,三級處理預水解液經透析處理后所制備的低聚木糖與商品低聚木糖樣品的FT?IR譜圖相似。兩種低聚木糖均在1045 cm-1處出現較強的吸收峰,該處是由C—O的伸縮振動引起,是聚木糖主鏈的典型特征峰[17];在894 cm-1處出現的吸收峰是由糖單元間顯性β?糖苷鍵的振動引起;987 cm-1處出現較弱的吸收峰主要是木糖殘基C—3上的阿拉伯糖取代基,是阿拉伯聚木糖型低聚物的典型吸收峰[18];1635 cm-1處出現的吸收峰是由吸附水的彎曲振動引起[19];在1408 cm-1處出現的吸收峰是由—COO-的對稱伸縮振動引起,為糖醛酸的特征吸收峰[20]。上述分析結果表明,經過硫酸處理桉木預水解液所制備的低聚木糖與商品低聚木糖所含官能團相似,均含有部分阿拉伯糖及糖醛酸側鏈。另外圖5顯示,商品低聚木糖樣品在1730 cm-1處出現較弱的吸收峰,該處是乙酰基的特征吸收峰,而經過硫酸處理預水解液所制備的低聚木糖樣品在該處沒有出現吸收峰,這表明在酸處理制備低聚木糖的過程中,連接在聚木糖側鏈上的乙酰基脫落下來,這是由堿性條件下乙酰基脫落形成乙酸所導致的[21],與Ca(OH)2處理過程中乙酸含量的增加一致(見表1)。
2.7 熱重(TGA)分析
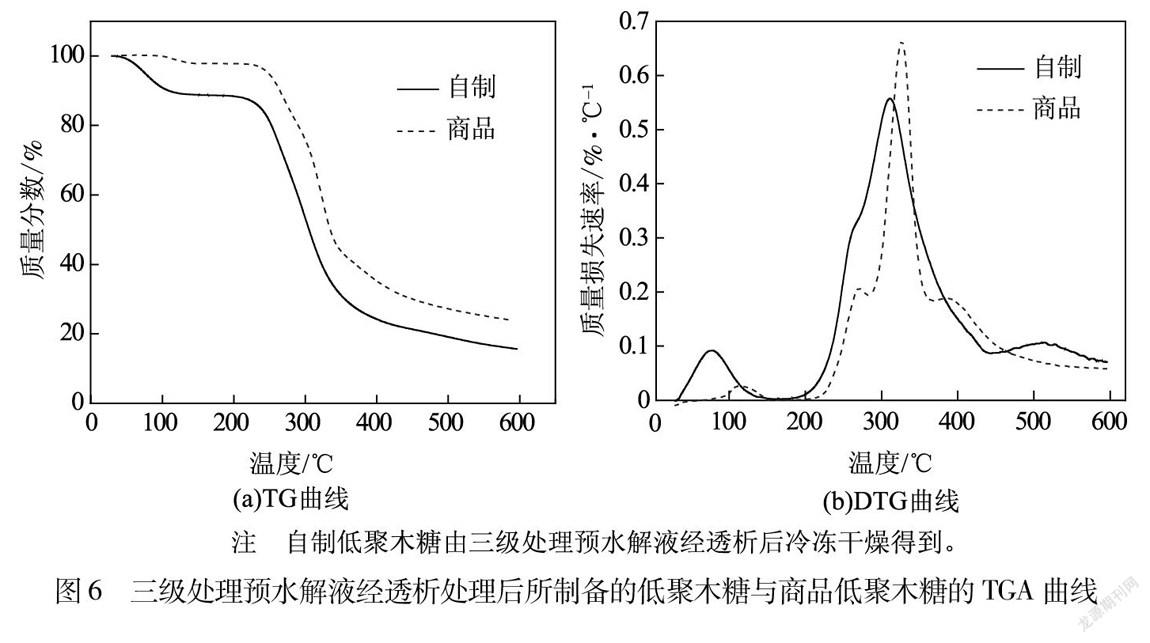
圖6為由三級處理預水解液經過透析處理后所制備的低聚木糖與商品低聚木糖的TGA曲線。
由圖6(a)可知,經過硫酸處理所制備的低聚木糖與商品低聚木糖的熱穩定性曲線相似。將溫度升高至600℃,自制低聚木糖與商品低聚木糖質量分別損失了83%和78%。圖6(b)顯示,兩種低聚木糖在150℃前均出現一個較小峰,這是由樣品中水分蒸發所致。自制低聚木糖從200℃左右開始分解,同時在310℃左右出現最大峰,質量損失過程在600℃結束。與自制低聚木糖不同,商品低聚木糖在325℃左右出現最大峰,由此可知商品低聚木糖的熱穩定性略高于自制低聚木糖。由上述分析可知,兩種低聚木糖的熱解過程主要分為4個階段:25~150℃為第一個階段,隨著處理溫度的不斷升高,樣品吸熱使樣品中的水分蒸發,這一階段只發生物理變化;200~310℃(或325℃)為第二階段,在此階段內,自制(或商品)低聚木糖開始發生質量損失,生成不燃性氣體如CO、CO2、甲酸和乙酸等[19];第三階段為310(或325)~440℃,在此階段內,不燃性氣體生成為可燃性氣體;第四階段(>440℃)主要為炭化階段,是由C—O和C—H鍵的進一步裂解造成的[22]。另外,圖6顯示,樣品熱重曲線溫度范圍較寬,原因可能是樣品中所含低聚木糖的聚合度范圍較寬,而不同聚合度的低聚木糖具有不同的熱重行為。由上述分析可知,經過微波輔助酸處理桉木預水解液所制備的低聚木糖與商品低聚木糖的性質相近,均具有較高的熱穩定性。
3 結 論
為利用桉木預水解液制備低聚木糖,對經過Ca(OH)2和活性炭處理的二級處理預水解液進行微波輔助酸處理,探討了處理過程中酸類型、酸用量、處理溫度和處理時間對預水解液中木糖及聚合度為2~4 低聚木糖(低聚木糖DP2~4)含量的影響,并對處理后預水解液中的低聚木糖進行了分析與表征。
3.1 酸類型、酸用量、處理溫度及處理時間對低聚木糖的含量均有較大影響,其中硫酸是一種較優的酸處理劑;硫酸處理二級處理預水解液制備低聚木糖的較優工藝條件為:硫酸用量1.4%、處理溫度120℃和處理時間20 min,在此條件下,經過酸處理后所得三級處理預水解液中低聚木糖DP2~4的含量為9.25 g/L,與二級處理預水解液相比,低聚木糖DP2~4含量提高了38.1%,預水解液中低聚木糖組分得到了進一步純化。
3.2 傅里葉變換紅外光譜(FT?IR)分析和熱重(TGA)分析結果表明,通過微波輔助酸處理預水解液所制備的低聚木糖與目前商品低聚木糖的性質相似,兩者均含有部分阿拉伯糖及糖醛酸側鏈,且均具有較高的熱穩定性。
參 考 文 獻
[1] TIAN Chao, HUANG Yan, YANG Xiaobo, et al. The Reactivity of Dissolving Pulp and Its Research Progress: A Review[J]. China Pulp & Paper, 2015, 34(1): 61.
田 超, 黃 雁, 楊小博, 等. 溶解漿的反應性能及相關研究進展[J]. 中國造紙, 2015, 34(1): 61.
[2] DONG Jiran, CHEN Jiachuan, JI Xingxiang, et al. Study on the Removal of Lignin from Eucalyptus Pre?hydrolysis Liquid by Laccase Combined with Activated Carbon Treatment[J]. China Pulp & Paper, 2018, 37(9): 9.
董吉冉, 陳嘉川, 吉興香, 等. 漆酶協同活性炭處理脫除桉木預水解液中木素的研究[J]. 中國造紙, 2018, 37(9): 9.
[3] CHEN Jia?chuan, DONG Ji?;ran, YANG Gui?hua, et al. A Process for Purifying Xylosugars of Pre?hydrolysis Liquor from Kraft?based Dissolving Pulp Production Process[J]. Biotechnology for Biofuels, 2018, 11(1): 337.
[4] XU Feng, YANG Guihua, JI Xingxiang, et al. Effect of P Factor on Dissolution of Poplar Hemicellulose During the Hydrothermal Pretreatment Process[J]. China Pulp & Paper, 2018, 37(8): 1.
徐 豐, 楊桂花, 吉興香, 等. 熱水預處理過程中P因子對楊木半纖維素溶出效果的影響[J]. 中國造紙, 2018, 37(8): 1.
[5] Caparros S, Garrote G, Ariza J, et al. Xylooligosaccharides Production from Arundo Donax[J]. J. Agric. Food Chem, 2007, 55(14): 5536.
[6] Chapla D, Pandit P, Shah A. Production of Xylooligosaccharides from Corncob Xylan by Fungal Xylanase and Their Utilization by Probiotics[J]. Bioresource Technology, 2012, 115(5): 215.
[7] Moniz P, Ailing H, Duarte L C, et al. Assessment of the Bifidogenic Effect of Substituted Xylo?oligosaccharides Obtained from Corn Straw[J]. Carbohydrate Polymers, 2016, 136: 466.
[8] Yang Z Y, Wu D T, Chen C W, et al. Preparation of Xylooligosaccharides from Xylan by Controlled Acid Hydrolysis and Fast Protein Liquid Chromatography Coupled with Refractive Index Detection[J]. Separation & Purification Technology, 2016, 171: 151.
[9] YANG Dou, ZHANG Wei?bo, ZHAO Qian?yun, et al. Study on the Technology of Xylooligosaccharide Preparation[J]. Cereal and Food Industry, 2017, 24(1): 53.
楊 豆, 張衛波, 趙倩蕓. 制備低聚木糖的工藝研究[J]. 糧食與食品工業, 2017, 24(1): 53.
[10] Yang B, Wang B B, Wang G H, et al. Integrated Forest Biorefinery: Value?added Utilization of Dissolved Organics in the Prehydrolysis Liquor of Prehydrolysis Kraft (PHK) Dissolving Pulp Production Proces[J]. Paper and Biomaterials, 2018, 3(3):47.
[11] Samanta A K, Jayapal N, Kolte A P, et al. Enzymatic Production of Xylooligosaccharides from Alkali Solubilized Xylan of Natural Grass(Sehima Nervosum)[J]. Bioresource Technology, 2012, 112(3): 199.
[12] Warrand J, Janssen H G. Controlled Production of Oligosaccharides from Amylose by Acid?hydrolysis Under Microwave Treatment: Comparison with Conventional Heating[J]. Carbohydrate Polymers, 2007, 69(2): 353.
[13] Delazar A, Nahar L, Hamedeyazdan S, et al. Microwave?assisted Extraction in Natural Products Isolation[J]. Methods MolBiol, 2012, 864: 89.
[14] FAN Li, XU Yong, LIAN Zhi?na, et al. Quantitative Determination of Xylo?oligosaccharides in Xylo?oligosaccharides Products with High Performance Anion?exchange Chromatography Coupled with Pulsed Amperometric Detection[J]. Chinese Journal of Chromatography, 2011, 29(1): 75.
范 麗, 徐 勇, 連之娜, 等. 高效陰離子交換色譜?脈沖安培檢測法定量測定低聚木糖樣品中的低聚木糖[J]. 色譜, 2011, 29(1): 75.
[15] Yang Guihua, Sarwar Jahan M, Liu Haitang, et al. Acid Hydrolysis of Prehydrolysis Liquor Produced from the Kraft?based Dissolving Pulp Production Process[J]. Industrial & Engineering Chemistry Research, 2012, 51(43): 13902.
[16] Yemis O, Mazza G, et al. Acid?catalyzed Conversion of Xylose, Xylan and Straw into Furfural by Microwave?assisted Reaction[J]. Bioresource Technology, 2011, 102: 7371.
[17] BIAN J, PENG P, PENG F, et al. Microwave?assisted Acid Hydrolysis to Produce Xylooligosaccharides from Sugarcane Bagasse Hemicelluloses[J]. Food Chemistry, 2014, 156(156): 7.
[18] CHEN Qing?qing, JIANG Hua, ZHANG Yang, et al. Optimization of Extraction and Characterization of Hemicelluloses from Hybrid Poplar Residues[J]. Biomass Chemical Engineering, 2013, 47(3): 39.
陳清清, 江 華, 張 洋, 等. 速生楊半纖維素堿法提取工藝的優化和表征[J]. 生物質化學工程, 2013, 47(3): 39.
[19] Peng F, Ren J L, XU F, et al. Comparative Study of Hemicelluloses Obtained by Graded Ethanol Precipitation from Sugarcane Bagasse[J]. Journal of Agricultural & Food Chemistry, 2009, 57(14): 6305.
[20] Patricia G, Maria J. Structural Features and Properties of Soluble Products Derived from Eucalyptus Globulus Hemicelluloses[J]. Food Chemistry, 2011, 127(4): 1798.
[21] Shen J, Fathei P, Soleiman P, et al. Lime Treatment of Prehydrolysis Liquor from the Kraft?based Dissolving Pulp Production Process[J]. Industrial & Engineering Chemistry Research, 2012, 51(2): 662.
[22] Maschio G, Koufopanos C, Lucchesi A. Pyrolysis, A Promising Route for Biomass Utilization[J]. Bioresource Technology, 1992, 42(3): 219.CPP

