呼吸指數及氧合指數在兒童ARDS中的臨床意義
鄭 茂,張玉鳳,張曉芳,安 媛,王 瑩,陳 瑤,符 佳
(西安市兒童醫院,陜西 西安 710003)
急性呼吸窘迫綜合征(acute respiratory distress syndrome,ARDS)是一種急性缺氧性呼吸衰竭,主要是由機體遭受各種侵襲導致,比如創傷、感染及休克等,其主要表現為低氧血癥和急性呼吸窘迫,隨著病情發展,很容易造成多臟器功能衰竭的發生,威脅患者生命安全[1]。兒童ARDS具有發病迅速,死亡率高的特點,若不能及時進行救治,很容易導致患兒死亡,即使挽救了患兒生命,其往往會存在預后不良等情況,對患兒生長發育及生活質量造成影響[2]。為了提高ARDS的早期診斷準確率,尋找更有參考價值的血氣分析指標非常關鍵[3]。本次研究選取了西安市兒童醫院重癥監護室的ARDS患兒為研究對象,對其在進行機械通氣期間的呼吸指數(RI)和氧合指數(OI)進行觀察,分析其在ARDS診斷中的參考價值。
1資料與方法
1.1一般資料
研究組:選取2017年1月至2018年12月西安市兒童醫院重癥監護病房收治的需要進行機械通氣治療的ARDS患兒20例為研究對象,其中男性12例,女性8例,年齡為3~12歲,平均年齡為(7.3±2.1)歲;原發病:血液系統腫瘤或白血病13例,重癥肺炎2例,病毒性感染5例。本次研究所納入的20例患者均接受呼吸機進行機械通氣治療,帶機時間為5~28天,平均帶機時間為(10.3±2.1)天;治療期間共發生死亡6例,死亡原因:重癥病毒感染合并多臟器功能衰竭2例,帶機時間分別為5天、6天,血液系統腫瘤患兒因化療后骨髓抑制感染,導致多臟器功能衰竭死亡4例,帶機時間分別為5天、6天、6天、8天。納入標準:①患兒在原發病癥的基礎上突然出現氣促、呼吸窘迫等情況,且經常規吸氧無法進行癥狀改善;②患者的OI在200mmHg以下;③為患兒進行X線照射,可觀察到雙肺紋理增多且變得模糊,存在網狀陰影或斑片狀陰影,具有擴張、融合迅速的特點;④患兒家屬對本次研究知情并同意。排除標準:①患兒存在肺部腫瘤;②患兒存在心源性肺水腫;③患兒存在中樞性呼吸抑制;④患兒伴有肺栓塞或肺部手術治療史;⑤患兒存在肌無力或胸廓畸形;⑥患兒伴氣胸、血胸等情況。
對照組:選取同期本院收治的肺炎合并急性呼吸衰竭患兒20例,其中男性12例,女性8例,年齡為3~11歲,平均年齡為(7.2±2.2)歲;其中1例患兒合并青紫型先天性心臟病。本次研究所納入的20例患者均接受呼吸機進行機械通氣治療,帶機時間為4~19天,平均帶機時間為(10.1±2.3)天;本組患兒未出現死亡病例。納入標準:①入組患兒均符合重癥肺炎的臨床診斷;②患兒須接受機械通氣治療;③患兒家屬對本次研究知情并同意。排除標準:①患兒存在肺部腫瘤;②患兒存在中樞性呼吸抑制;③患兒伴有肺栓塞或肺部手術治療史;④患兒存在肌無力或胸廓畸形;⑤患兒伴氣胸、血胸等情況。
本次研究已獲得西安市兒童醫院倫理委員會批準。
1.2方法
采用血氣分析儀(prem ire 9000)對兩組患兒進行血氣相關指標的分析。對患兒進行動脈血采集,采血點為股動脈或橈動脈。對兩組患兒進行機械通氣治療,使用呼吸機(德國:GragerEV ITA4機型)進行機械通氣,對兩組患兒不同機械通氣階段的血氣變化情況進行監測。監測時間分別為機械通氣早期(建立機械通氣后2小時以內)、機械通氣中期(建立機械通氣后48~72小時之間)及機械通氣撤機前(在撤機前2小時至撤機前30分鐘以內);檢測指標包含動脈血氧分壓(PaO2)、血氧飽和度(SaO2)、肺泡-動脈血氧分壓[P(A-a)O2]、RI及OI,根據SaO2、PaO2、氧吸入濃度(FiO2)、飽和水蒸氣壓(PH2O)、大氣壓(Pa)、動脈血二氧化碳分壓(PaCO2)及P(A-a)O2的檢測情況進行RI和OI的計算,計算公式為P(A-a)O2=(Pa-PH2O)×FiO2-PaO2-PaCO2;OI=(PaO2)/FiO2,RI=P(A-a)O2/PaO2。在標準狀態下Pa的數值為760mmHg,在標準狀態下PH2O的數值為47mmHg。
1.3觀察指標
觀察兩組患兒在不同機械通氣期間SaO2、PaO2、P(A-a)O2、RI及OI值的變化情況,并對P(A-a)O2、RI及OI值之間的相關性進行分析。
1.4統計學方法
應用SPSS 18.0進行數據分析,計數采用χ2檢驗,計量采用t檢驗,以P<0.05提示差異有統計學意義。
2結果
2.1機械通氣早期相關指標的分析
在機械通氣早期階段患兒中,研究組的RI、P(A-a)O2均明顯高于對照組(均P<0.05),研究組的OI明顯低于對照組(P<0.05),研究組的SaO2、PaO2與對照組比較差異均無統計學意義(均P>0.05),見表1。
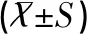
表1 機械通氣早期患兒相關指標的比較結果
2.2機械通氣中期相關指標的分析
在機械通氣中期階段患兒中,研究組的RI、P(A-a)O2均明顯高于對照組(均P<0.05),研究組的OI明顯低于對照組(P<0.05),研究組的SaO2、PaO2與對照組比較差異均無統計學意義(均P>0.05),見表2。
2.3機械通氣撤機前相關指標的分析
在機械通氣撤機前階段患兒中,研究組的RI、P(A-a)O2、OI、SaO2及PaO2與對照組比較差異均無統計學意義(均P>0.05),見表3。
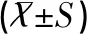
表2 機械通氣中期患兒相關指標的比較結果

表3 機械通氣撤機前患兒相關指標對比
2.4患兒的OI、RI及P(A-a)O2相關性分析
研究組患兒的RI與P(A-a)O2呈正相關性,r=0.894,P<0.05;研究組患兒RI與OI呈負相關性,r=-0.621,P<0.05;對照組患兒RI與P(A-a)O2呈正相關性,r=0.804,P<0.05;對照組患兒RI與OI呈負相關性,r=-0.712,P<0.05。
3討論
3.1急性呼吸窘迫的疾病特點
目前臨床治療ARDS的主要手段就是進行機械通氣治療,進而為原發病的治療提供時間支持。對于ARDS的病情變化可以采用RI進行客觀評價,在臨床上對ARDS患者的救治過程中起到了非常重要的指導作用[4]。ARDS屬于急性呼吸衰竭,是由原發病及多種因素誘導下發生的,其主要疾病特點為頑固性低氧血癥及非心源性肺水腫,患者以呼吸窘迫、呼吸困難為主要臨床表現,急性肺損傷是其病理基礎,屬于全身炎癥反應綜合征在肺部的表現[5]。有學者在研究中指出,當機體氣體交換功能及肺通氣功能受到影響時,RI可以對其發生的變化進行反應,其變化會受到肺內分流、心輸出量、彌散功能、混合靜脈血氧分壓及通氣狀態等影響[6];但FiO2及呼吸方式并不會對RI造成影響。
3.2急性呼吸窘迫臨床特點與各指標間的關系
因RI是P(A-a)O2與PaO2的比值,因此可對患兒氧合狀態進行比較客觀的評價[7]。RI比較容易計算,在重癥監護室患兒中應用比較方便,且可隨時進行計算。但是,ARDS患兒往往需要進行機械通氣治療,FiO2及機械通氣均會對PaO2造成影響,而且地理差異、年齡等因素也會對PaO2造成一定程度的影響[8]。PaO2下降存在于多種呼吸衰竭類型中,因此若單純使用PaO2作為對ARDS早期診斷的依據仍存在諸多的不足[9]。FiO2會對PaO2值造成影響,當FiO2值較高或在良好的機械通氣條件下,PaO2不會出現明顯的下降狀況,甚至在患兒肺部炎癥已出現影像學早期改變的情況下,其PaO2值仍可保持在60mmHg左右。因此,單純觀察患兒PaO2指標并不能對其病情進行準確判斷,進而導致診斷延遲[10]。當P(A-a)O2明顯升高時,則表示患兒存在換氣功能障礙,P(A-a)O2與PaO2相比,P(A-a)O2的下降情況更為敏感,可早期反映肺部的氧攝取情況;但是,FiO2同樣會影響P(A-a)O2,因此,當患兒在接受吸氧治療時,其參考性明顯降低。目前已有研究證實,FiO2不會影響PaO2與肺泡氣氧分壓(PAO2)的比值[11]。PaO2與PAO2的比值倒數減去1則是RI,FiO2及通氣方式對RI的影響并不明顯。因此,在對ARDS患兒早期肺功能進行診斷時,可以通過RI進行分析,進而實現ARDS的早期診斷,及時進行有效的治療[12]。本研究結果顯示,在ARDS發展的早期及中期,RI明顯升高,與肺炎合并呼吸衰竭患兒相比,差異具有統計學意義,但是SaO2、PaO2值兩組患兒并無明顯差異。這一結果說明,通過檢測RI的方式,可以有效地區分肺炎合并呼吸衰竭患兒與ARDS患兒,實現ARDS的早期診斷,進而為有效治療方案的制定提供時間支持。
3.3 OI和RI對疾病診斷的意義
肺氧交換是否正常可采用P(A-a)O2進行評估,彌散功能、通氣/血流及解剖分流是其主要影響因素,心排量、體位、氧離曲線、年齡及閉合器量等為次要影響因素[13]。本研究結果顯示,RI與P(A-a)O2呈正相關性,但是FiO2可以對P(A-a)O2造成影響,因此,在對ARDS患兒進行臨床早期診斷時,RI的參考性更強。目前已有大量研究證實,除RI外,OI在ARDS診斷中同樣具有非常高的參考性[14]。OI是PaO2與FiO2的比值,計算比較容易,可反映患兒在吸氧條件下的缺氧狀態,而且該數值與肺內血液分流量密切相關。但是給氧濃度及給氧方式會對OI的數值造成影響,特別是ARDS患兒多伴有多器官功能障礙情況。因此認為OI可作為肺泡損傷和肺血管床損傷的診斷指標。嚴重低氧血癥屬于ARDS的常見臨床表現,因此在對ARDS患兒進行診斷時常將PaO2指標的下降作為診斷依據,但該數值受地區等因素的影響比較明顯[15]。本研究結果顯示,ARDS患兒的OI值明顯降低,且RI與OI呈負相關,這說明OI在ARDS的診斷過程中同樣具有非常高的參考性。本研究結果顯示,在撤機前,ARDS患兒與肺炎合并呼吸衰竭患兒相比,各指標并無明顯差異。因此,可通過檢測OI及RI指標的方式,對患兒機械通氣時間進行評估。
綜上所述,在兒童ARDS患兒中,存在RI明顯升高,OI明顯降低的情況,因此在對兒童ARDS患兒進行診斷時可將其作為參考指標。

