納氏試劑分光光度法對水中氨氮的測定研究
王作芬
(浙江中環檢測科技股份有限公司,浙江溫州325016)
水中氨氮是以銨鹽、游離氮作為主要存在形式,而以存在于生活污水中的銨鹽和游離氮關系著水中含氮有機物,含氮有機物在微生物作用下會產生分解,如此一來水中也就存在了氨氮[1]。水中含量過高的氨氮會在一定程度上損害人體,借助納氏試劑分光光度法監測、評價,可有效處理污水。水中氨氮測定期間,溫度控制這一環節十分重要,能直接影響到納氏試劑及氨氮反應速度。具體測定實踐中,針對試驗環境、器具、用水和顯色時間等因素必須予以重視,以實際情況為根據對反應條件合理控制,為實驗數據提供準確、高精密度保障。
1 實驗部分
1.1 實驗原理
該方法的原理為:以銨鹽或游離氮形式存在的氨氮在與納氏試劑反應之后,有淡紅色的絡合物產生,該絡合物吸光度和氨氮含量之間的關系為正比,在波長420nm 處對其吸光度展開測量。該方法具有高準確度、便捷等優點,得到了廣泛運用。
1.2 實驗試劑
配制試劑用水均應為無氨水。
1.2.1 納氏試劑
稱取16g 氫氧化鈉并以50mL 純水溶解,冷卻至室溫。另稱取7g 碘化鉀、10g 碘化汞,置于少量純水中溶解后不斷攪拌并將氫氧化鈉溶液逐一注入其內[2]。添加純水稀釋至100mL 后密封保存于聚乙烯瓶中。
1.2.2 銨標準貯備溶液
稱取優級純氯化銨3.819g 置于純水中溶解后轉至容量瓶(1000mL)內,添加純水稀釋至標線,氨氮含量為1.00mg/mL。
1.2.3 銨標準使用溶液
將銨標準貯備溶液5.00mL 移至容量瓶(500mL)內,添加純水稀釋至標線,氨氮含量為0.010mg/mL。
1.2.4 酒石酸鉀鈉溶液
稱取酒石酸鉀鈉50g 置于100mL 純水中,溶解后加熱、煮沸除氨、冷卻至室溫后定容至100mL。
1.3 儀器設備
1000 mL 全玻璃蒸餾器;50mL 具塞比色管;電子天平;分光光度計。
1.4 標準曲線的繪制
吸取銨標準使用液 0、0.50mL、1.00mL、3.00mL、5.00mL、7.00mL 和10.0mL 置于比色管(50mL)內,添加純水稀釋至標線,添入酒石酸鉀鈉溶液1.0mL,混勻、放置10min。采取光程10mm 比色皿,在420nm 波長處對其吸光度進行測定,參比對象為水。以所測吸光度為依據,校正吸光度為減去零濃度空白管吸光度后的值。
1.5 水樣測定
在比色管(50mL)內添加50mL 純水。吸取銨標準使用溶液0、0.50mL、1.00mL、3.00mL、5.00mL、7.00mL 和10.0mL 置于比色管(50mL)內,添加無氨水稀釋至刻度[3]。分別將1mL 酒石酸鉀鈉溶液加入水樣及標準管內并搖勻,隨后將1mL 納氏試劑加入,再次搖勻。用1cm 比色皿在420nm 波長處對其吸光度值進行測定,繪制標準曲線。以相同步驟測定水樣吸光度,依據標準曲線獲取氨氮含量。
2 結果與討論
2.1 結果
以表1 結果為根據完成標準曲線的繪制,其中縱坐標為凈吸光度、橫坐標為氨氮含量,下圖1為標準曲線。

表1 實際檢測結果
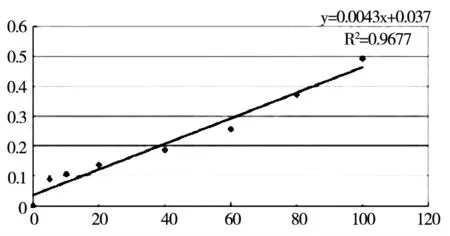
圖1
由此可知氨氮含量與凈吸光度可將滿足。
依據實驗結果得知,高達0.9677 的具有較高的擬合程度。完成標準曲線的繪制后,僅需將水樣吸光度測出,便可獲取水樣中氨氮濃度。
2.2 水樣中物質的影響
氨氮測定期間,若是水樣帶有顏色、渾濁等,測量結果會有一定的誤差產生。具體測定過程中,針對水樣需實施預處理,若是水樣具有相對較高的清潔度,可采用絮凝沉淀法;針對污染嚴重的工業廢水等,可采取蒸餾法消除干擾[4]。而在酸性條件下,有機廢水中因有機物分解的緣故,有機氮會朝著氨氮轉化,如此一來在放置時間的不斷延長下,氨氮測定結果也會變大,鑒于此,在完成采樣后需盡快開展測定工作。無機廢水中的氨氮在酸性條件下朝著酸鹽氨、亞硝酸鹽氨轉化時,存在相對緩慢的速度,測定結果幾乎不會受到保存數日的影響。就地表水樣而言,將硫酸加入水樣使其pH 值因酸化而不超過2h,室溫條件下放置15d 相對穩定。
2.3 顯色時間的影響
具體測量過程中,由于各類原因的影響,比色時間通常會出現提前或延后的狀況,故而顯色時間的合理確定十分關鍵[5]。在25℃室溫下,將酒石酸鉀鈉、納氏試劑加入含有0.05mg/L、0.50mg/L、1.00mg/L 的氨氮樣品中顯色后,在不同放置時間下對其吸光度進行測定,下表2 為具體結果。

表2 顯色時間對吸光度的影響(A)
依據上表2 不難發現,顯色時間不超過5min由于反應不完全,存在較低的吸光度值;顯色時間在10~30min 內,具有較為穩定的顯色及最大的吸光度值;顯色大于40min 后,吸光度值會隨著褪色而降低。鑒于此,水中氨氮測定中,采用納氏試劑分光光度法時應選擇10~30min 的顯色時間。
2.4 顯色溫度的影響
對于納氏試劑、氨氮反應速度而言,溫度能對其造成一定的影響,測定結果也會受到相應的影響[6]。故而,在具體實驗中以5℃、10℃、15℃、20℃、25℃、30℃、35℃等不同室溫下,選擇10min 顯色時間展開測定,在5~15℃溫度內,出現不完全顯色;20~25℃溫度,具有較為完全的顯色;超過30℃的溫度,吸光度會隨溫度上升而下降。故而,應以20~25℃的實驗室溫度為宜。而當實驗室溫度相對較低時,要想確保該方法的靈敏度,可適當延長顯色時間。
2.5 水樣pH 的影響
納氏試劑顯色反應的反應式如下:
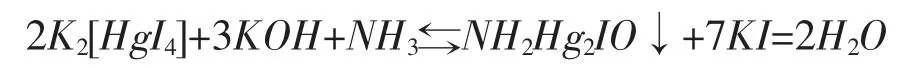
依據反應式不難發現,顯色體系pH、分析結果準確性會在一定程度上受到顯色程度的影響。加入納氏試劑后,溶液顯色pH 值以11.8~12.4 為佳。當pH<11.8 時,反應為逆反應,會有紅色沉淀形成;pH>12.4 時,溶液渾濁且無法比色,同時還會形成大量的。25℃室溫下,改變同一水樣的pH值并加入納氏試劑1.0mL,放置10min 后對其吸光度進行測定,下表3 為具體測定結果。

表3 pH 值與吸光度關系
依據表3 不難發現,水樣具備最高吸光度值時pH 約為7,故而水樣保存運輸中進行加酸酸化處理時,測定樣品前需調整pH 為中性。
3 結語
依據實驗完成氨氮標準曲線的繪制,以供不同水樣中氨氮含量的有效、快速檢測。廢水污染物中,氨氮十分常見,其含量是對水環境質量進行評價的重要指標之一。飲用水中出現過高的氨氮含量時,亞硝酸鹽結合蛋白質會構成具有強致癌性的亞硝胺物質,嚴重威脅到人體健康。同時,氨氮也會在一定程度上影響水生生物,隨著水中氨氮含量的升高,pH 值及毒性也會相應的上升,進而對水生生物造成更大的危害。故而,就水中氨氮含量測定工作而言,對于水質評價、水體凈化有著極為關鍵的意義。

