耦合發酵產氫尾液處理的微生物電化學系統研究
盧建宏,李 卓,孫馳賀,付 乾*,李 俊,張 亮,廖 強,朱 恂
耦合發酵產氫尾液處理的微生物電化學系統研究
盧建宏1,2,李 卓1,2,孫馳賀1,2,付 乾1,2*,李 俊1,2,張 亮1,2,廖 強1,2,朱 恂1,2
(1.重慶大學低品位能源利用技術及系統教育部重點實驗室,重慶 400030;2.重慶大學工程熱物理研究所,能源與動力工程學院,重慶 400030)
區別于傳統的稀釋或加緩沖劑調節pH值的方法,本文提出采用微生物電解池(MEC)電調控暗發酵尾液pH值,并進一步采用微生物電合成系統(MES)降解廢液產甲烷.結果表明,在MEC處理產氫暗發酵尾液過程中,伴隨著陰極側氫氣的產生,暗發酵尾液中大量H+被消耗,溶液pH值從4.5升高到8.7;隨后在MES中,產氫發酵尾液中有機物被進一步降解產生甲烷,其平均產甲烷速率達到4.5mmol/(L?d),且在21d內化學需氧量(COD)去除率達到89%,遠優于沒有經過pH調控的產氫發酵尾液MES中的產甲烷性能.
微生物電化學系統;暗發酵尾液;pH調控;有機物降解;甲烷
隨著工業化進程的不斷推進,化石燃料消耗所帶來的環境污染,溫室效應及能源短缺等問題日益凸顯,尋找新型清潔可再生能源迫在眉睫[1],生物能源作為一種生產安全、制備簡單的清潔能源被認為是最具潛力的新型能源之一[2-4].目前,通過對有機物進行發酵而產生氫氣,是最為常見的生物能源方法之一,由于氫氣具有熱值高、燃燒后無污染、容易分離等優點,發酵產氫正受到國內外研究者的廣泛關注[5-7].
發酵產氫以秸稈或高濃度有機廢液為原料產生氫能,是一種極具應用前景的生物能源技術.然而,發酵產氫過程中產生的脂肪酸積累可導致pH值過低,抑制產氫微生物活性,從而迫使產氫中斷.
發酵產氫主要可分為兩個過程:首先是大分子有機物(纖維素,木質纖維素等)在微生物的催化下水解成單糖(如葡萄糖等)[7],其次是單糖進一步被微生物利用,水解形成脂肪酸以及脂肪酸進一步水解成乙酸,過程中伴隨氫氣的產生,產生的脂肪酸主要由乙酸、丙酸,丁酸、戊酸等小分子有機物組成[5,8].
同時,在有機物的水解過程中,發酵液累積了大量脂肪酸,溶液pH將明顯下降,有研究表明積累的脂肪酸可使發酵液pH降低至4.5以下[8-10];這不僅抑制了發酵產氫,也會導致發酵產甲烷(徹底降解)過程緩慢[8,10].為了解決上述問題,Cai[11]和Ghimire[12]等學者用連續流動及定期更換發酵液的運行模式及時移除溶液中的脂肪酸,但由于水力停留時間較短,溶液中的有機物不能充分被降解,導致尾液中殘留大量有機物,直接排放將對環境造成二次污染. Tao等[13]在實驗過程中,對發酵尾液進行稀釋雖然能夠提高溶液pH,使低pH條件下失活的微生物恢復活性,進而繼續降解有機物,提高能量回收率,但稀釋過程將消耗大量潔凈水,且由于熱力學限制等因素,尾液中依然殘留大量有機物;Dou等[14]和Cai等[11]在發酵液中加入大量緩沖液,使溶液pH值始終保持在近中性條件,雖然在長時間運行后能夠將有機物徹底地水解為氫氣和甲烷,但在工業應用中該方法將極大增加運行成本.
綜上所述,目前對于發酵尾液pH值的控制存在著各種不足,通過移除溶液中的H+來調節pH值可有效解決發酵尾液中pH值過低的問題.微生物電化學系統(BES)是一種新型的生物能源轉換裝置,其主要特點是以具有電化學活性的微生物來催化電極表面的氧化還原反應,從來可以在降解溶液中有機物的同時進行產電、產H2或者還原CO2產CH4.按其產物及工作原理,可分為微生物燃料電池(MFC)、微生物電解池(MEC)和微生物電合成系統(MES).
MEC可以在降解有機物的同時產生氫氣,從而實現溶液中H+的移除,是一種十分理想的調控發酵尾液pH的能源轉化裝置[15]. MEC主要由陽極、陰極及電解質組成,在生物陽極側,微生物在降解有機物(如乙酸根)的同時將其電子轉移到陽極表面. 電子經過外電路到達陰極表面,在陰極表面微生物催化劑的作用下,與H+結合反應生成H2,與此同時, MEC反應的進行需要外部輸入一定的電壓.對于MEC與發酵產氫的耦合系統來說,因為在移除H+的過程中,溶液pH不斷提高,在低pH條件下失活的微生物將恢復活性,進一步提高該系統降解有機物效率及燃料產率;但由于熱力學的限制,最終的小分子有機物無法繼續降解為氫氣[16],因此本文利用MES對近中性尾液徹底降解,同時將二氧化碳還原成甲烷.
MES結構及工作原理與MEC類似,主要區別是在其陰極側,具有電化學活性的微生物(以產甲烷菌為主)可從其電極表面汲取電子,并將CO2還原成CH4.同樣的,MES反應的進行需要外部輸入一定的電壓[16].相比于發酵產氫過程,由于外加能源的輸入,MES能夠將發酵尾液中不能繼續被微生物自發降解的小分子有機物徹底降解;又由于該系統生成的物質都為氣態的生物燃料,因此既實現了燃料的氣液分離,又實現了溶液中H+的移除,因此將厭氧發酵過程與MES相結合是一種十分具有前景的生物能源轉化技術.
本文利用MEC的優勢,首先利用雙室型MECs將暗發酵尾液中溶液中的大部分H+還原為H2,使得溶液pH值升高;然后利用單室MES將已調控pH值的產氫發酵尾液進行進一步降解,以去除溶液中有機物并生成CH4等燃料;同時研究了該系統中產氫發酵尾液中有機物的降解率、pH調控范圍及生物燃料產量.
1 材料與方法
1.1 MEC反應器構建及啟動
雙室MEC反應器示意圖如圖1左圖所示,主要包括陰陽兩極腔室,其腔室容量均為340mL,中間通過陽離子交換膜(AEM)(直徑5cm, CMI700,安德膜,北京,中國)分隔開來,并用鉸鏈固定.陰陽極均采用碳布(5′4.5cm, TMIL Ltd.,茨城,日本)制成,并經過丙酮和超純水沖洗3次以去除表面可能存在的有機物等雜質.為減小電極電阻,采用鈦絲連接碳布電極以引出電流,并確保電極電阻小于3歐姆.反應器開口處均采用丁基膠塞及鋁蓋密封.陰極腔室插入Ag/AgCl參比電極(飽和KCl溶液)以監測陰極電位.
單室MES反應器結構示意圖如圖1右圖所示,與雙室MEC反應器相比去除了陽離子交換膜,其容積為300mL.電極與雙室MEC中所采用電極一致,反應器開口處均采用丁基膠塞及鋁蓋密封以保持反應器厭氧狀態.運行過程中插入Ag/AgCl參比電極(飽和KCl溶液)來監測陰陽極電位.
1.2 暗發酵產氫尾液樣品
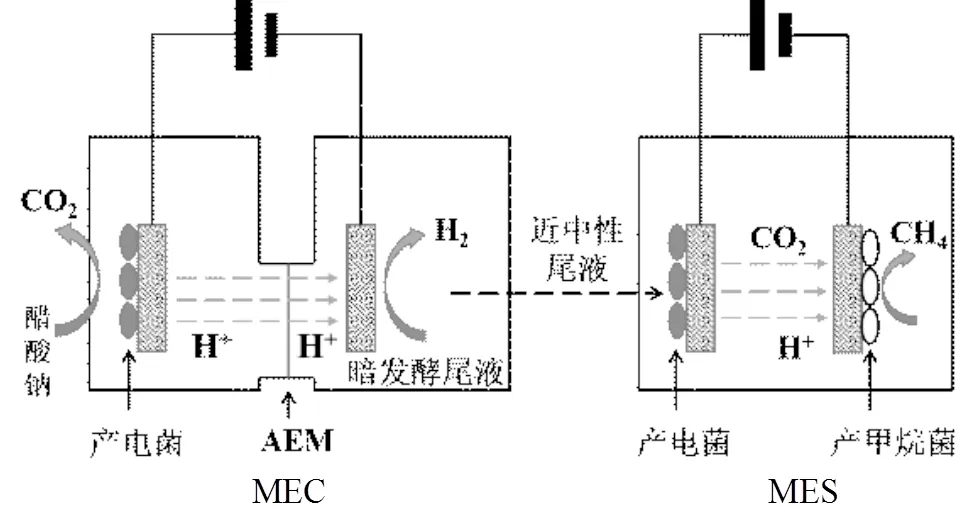
圖1 BES處理暗發酵尾液流程示意
實驗中所用暗發酵產氫尾液取自容積為400mL的發酵罐,其接種產氫細菌80mL(沼泥在121℃高壓滅菌鍋中滅菌15min后剩下的細菌即為產氫菌),以1:1物質的量比的葡萄糖和甘氨酸作為底物(每天加載10g/L 的COD量)進行暗發酵,整個暗發酵過程的水力停留時間(HRT)為2d.由于在暗發酵過程中累積了大量的脂肪酸,本研究中所采用暗發酵尾液pH值為4.5.通過對尾液進行測量后,得到其主要脂肪酸濃度依次為乙酸(28.32±1.83)mmol/L,丙酸(0.93±0.0)mmol/L,丁酸(29.05±2.67)mmol/L,戊酸(1.55±0.41)mmol/L.實驗開始前,為了確保發酵產氫徹底停止,先將該暗發酵產氫尾液靜置2d,期間保持嚴格厭氧狀態,并防止細菌污染.
1.3 實驗操作流程
實驗中先啟動雙室型MEC,隨后將pH值為4.5的產氫暗發酵尾液通入到雙室MEC陰極腔室,通過陰極側反應消耗H+(2H++2e-=H2↑)以調控其pH值;隨后將暗發酵尾液轉移到單室MES中,伴隨著陽極將尾液中有機物的降解,陰極發生二氧化碳還原成甲烷的反應,最后實現降解有機物和生成燃料的目的.整個流程圖如圖1所示.
雙室MEC啟動過程中,在雙室MEC陰極腔室內加入250mL pH為4.5的暗發酵尾液,陽極腔室加入100mL具有電化學活性的菌液(COD 2000mg/L)和140mL培養基.為保證嚴格厭氧,上述操作均在厭氧手套箱內完成.實驗中所采用電化學活性菌液取自實驗室內長期運行的MEC反應器,原始菌種為重慶郊區養豬場的厭氧活性污泥.培養基成分為醋酸鈉溶液(COD 500mg/L)(11.82g/L Na2HPO4×12H2O, 2.64g/L KH2PO4, 1.17g/L CH3COONa×3H2O)進行高溫滅菌后,再加入2.5mL Wolfe礦物溶液[17].上述操作完成后,對陰陽極腔室依次持續鼓入20min高純氮氣(純度99.99%)以去除溶解氧,通過加載0.9V外電壓來啟動雙室MEC(電源正極接MEC陽極,負極接MEC陰極).
單室MES啟動過程中,在其反應腔室內依次加入80mL菌液和120mL pH值已經調控的暗發酵產氫尾液,通過持續鼓入純二氧化碳(99.999%)20min,使得氣相初始為純二氧化碳構成,操作完成后加載0.9V外電源啟動(電源正極接MES陽極,負極接MES陰極).
1.4 測試方法
為監測電流,在電路中串聯1Ω的電阻,通過安捷倫數據采集儀(34970A, Agilent Technology, Santa Clara, CA, US) 每隔60s記錄電阻兩端電壓,并通過歐姆定律()計算出電流,同時通過安捷倫數據采集記錄下陰極相對于參比電極的電勢.
采用氣相色譜(Thermo Scientific, Waltham, MA, USA)測定在電解池氣室中氫氣和甲烷的峰面積(氣密進樣針分別抽取3次,每次抽取0.2mL),接著通過標準曲線計算氫氣和甲烷氣體含量[18].通過電化學工作站(Bio-Logic, VMP3,法國)掃描獲取電極循環伏安(CV)曲線.生物陽極的掃描區間為-0.6到0.4V vs. Ag/AgCl,掃速為1mV/s,重復掃描3次.
電極表面生物膜形貌特征可通過掃描電子顯微鏡(SEM)(SU8020,中科百測, 北京,中國)進行表征.拍攝前需要先將樣品放進2.5%的戊二醛固定液進行生物膜固定,然后進行酒精和叔丁醇脫水,最后使用噴金設備進行噴金處理.電極表面生物膜上活性生物量的計算主要依據Findlay等[19]提出的磷脂法進行測算.
2 結果與討論
2.1 雙室MEC系統產氫運行模式
由圖2A可知,在接種啟動之后,雙室MEC系統電流隨時間呈現指數上升趨勢,這主要是因為接種啟動之后,具有電化學活性的微生物開始在陽極表面附著并繁殖;且由于微生物繁殖為分裂繁殖,所以電流呈現指數上升趨勢.在1.2d之后,MEC電流開始達到穩定值,主要是因為電極表面電化學活性微生物的增長和營養物質的供給開始達到一個平衡狀態.在2.5d之后,電流開始逐漸下降,根本原因是從陽極至陰極室的陽離子(包括H+)遷移數下降.
在為期6d的實驗周期中,該雙室MEC的電流密度呈現先增加后下降的趨勢,最大電流密度約為2.0A/m2.氫氣最大產量約為3.65mmol.由圖2B可知,MEC陰極腔室內產氫發酵尾液的原始pH為4.5,而經過MEC處理后,其pH值增至8.7,表明通過MEC將H+還原為H2,是一種有效調控產氫發酵尾液pH值的方法.
在陰極腔室中,氫離子來源分為兩部分,一部分是陽極有機物降解產生H+傳遞到陰極;另外一部分是暗發酵尾液含有H+以及有機物進一步水解產生含有H+的脂肪酸.在第1d內,由于微生物的繁殖,陰極發生H+還原成H2的反應逐漸變得劇烈,并伴隨氫氣產量提升,這也導致電流增大,溶液pH不斷增大,由此進一步使得在低pH(<4.5)尾液中活性受到抑制的微生物在中性及偏堿性的溶液環境中恢復活性[20],進而繼續參與陰極液中有機物水解活動,水解過程中產生脂肪酸及氫氣.從第2.5d開始,由于陽極底物逐漸消耗殆盡,導致陽極氧化有機物產生的電子和H+逐漸減少,因此傳遞到陰極的電子和H+逐漸減少;而另一方面,在陰極尾液中,有機物水解成脂肪酸的反應也由于底物消耗而逐漸停止;兩方面原因導致陰極液中的H+迅速減少,進而導致H+還原成H2的反應劇烈程度逐漸減緩,氫氣產率開始減緩,故而電流逐漸減小,但是陰極液pH和陰極產氫量依舊在增長.然而,在為期6d的實驗周期中,發酵產氫尾液的pH值并未降低至酸性,表明電化學消耗H+的速率比產生H+的速率更快,因此發生在電極表面生物電化學反應是該系統內的主要反應過程.
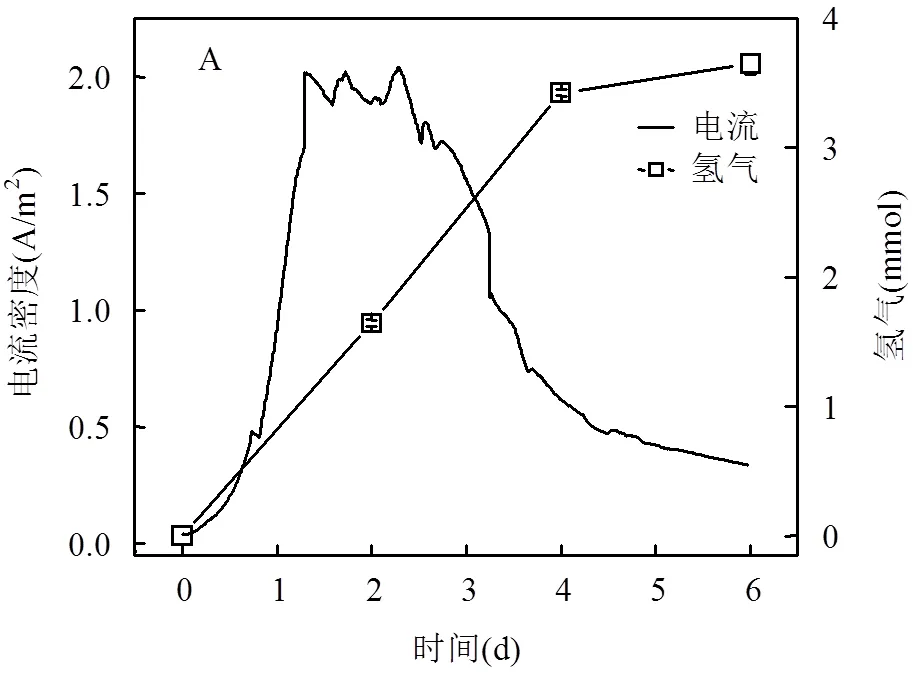
圖3A為MEC陽極表面微生物形貌特征,可見在生物陽極表面形成了一層致密的生物膜,可推斷生物陽極在經過6d的生長后變得相對成熟穩定.作為對比,陰極表面的微生物比較稀疏,這主要是因為相對于陽極測的產電菌,陰極側的產氫功能菌群生長速度相對緩慢[21-22].

圖3 MEC陽極(A)和陰極(B)SEM圖
2.2 單室MES系統產甲烷性能特性
2.2.1 單室MES啟動特性 由圖4A可知,在為期21d的實驗周期中,實驗樣的電流密度呈現先增加后降低的趨勢,將經過pH調控的產氫發酵尾液加入單室MES中并運行8d后,實驗樣電流密度開始增長,并在15d時達到最大電流密度6.1A/m2,隨后其電流密度降低至0.3A/m2,實驗樣2也呈現了相同趨勢.然而,對照樣在整個實驗周期中幾乎沒有電流產生,表明對照樣中沒有電化學反應的發生.這主要因為對照樣中pH值過低(~4.5),溶液中的微生物活性受到抑制,難以啟動成功[8].由于微生物電合成系統中外電路的電子來源于陽極表面電化學活性微生物對有機物的氧化,因此上述結果表明,產氫發酵尾液中的確存在大量未降解有機物,其主要以小分子有機酸形式存在[5].由圖4B可知,對照樣在整個實驗周期中沒有甲烷產生,進一步證實了較低的pH值對具有電化學活性的微生物起到抑制作用.
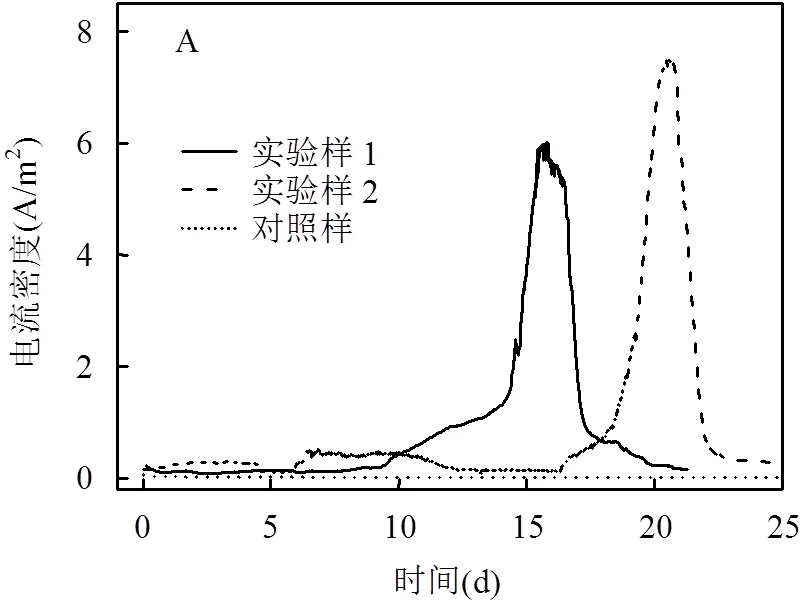
實驗樣:采用單室MES處理經過pH值調控的暗發酵尾液(初始pH=8.7);對照樣:采用單室MES處理未經pH調控的暗發酵尾液(初始pH=4.5);厭氧發酵:采用發酵處理未經pH值調控的尾液(初始pH=4.5)
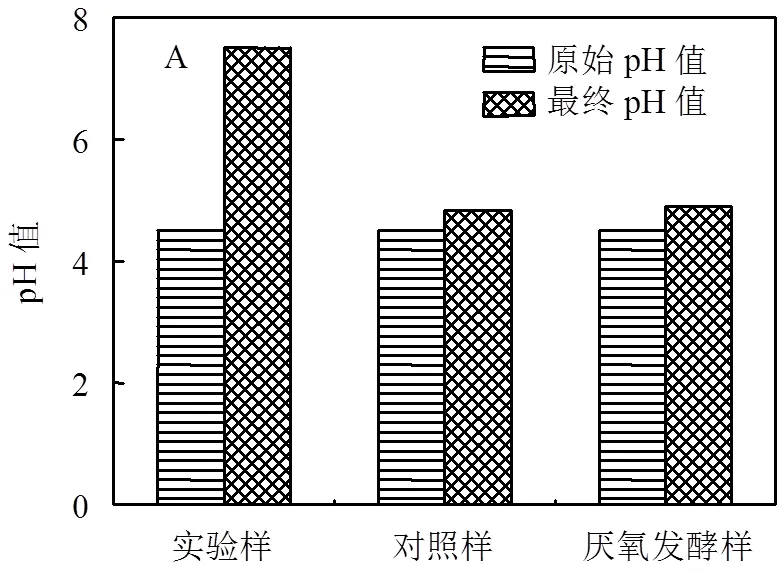
2.2.2 單室MES反應器性能特性 為了進一步研究通過MEC調控pH值是一種有效的降解暗發酵尾液并提高產甲烷率的方式,實驗對暗發酵尾液經過微生物電解池處理前后的pH值、COD及COD移除率進行了研究.由圖5A可知,初始暗發酵尾液的pH值為4.5,暗發酵尾液經過雙室MEC陰極產氫,接著轉移到單室MES進行降解并伴隨著甲烷的生成,經過降解后尾液最終的pH為7.5,而厭氧發酵樣和對照樣的暗發酵尾液pH基本沒有變化.由圖5B與C可知,實驗樣在反應前后的21d內, COD由5889mg/L顯著降低至670mg/L,COD移除率高達89%.作為對比,在60d內對照樣和單純厭氧發酵樣(AD)的COD從5889mg/L依次降低到5210mg/ L,5063mg/L,COD移除率依次為11%和14%.通過對比可見,實驗樣比厭氧發酵和對照樣在單位時間內具有更加快速的產氣速率級更高COD移除效率.上述結果表明,經過MEC調控pH值后再通過MES降解處理尾液產甲烷確有利于溶液中有機物的移除.
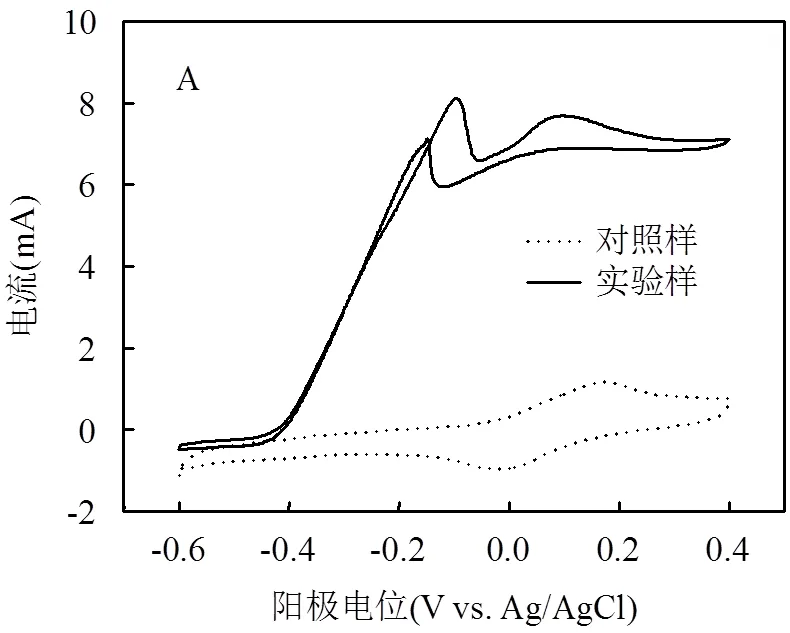
2.2.3 MES電極特性表征 從圖6A可見,實驗樣開始出現氧化反應的起始電位是-0.4V,隨著電位增加到-0.1V,出現氧化峰,此時電流達到最大為8.4mA.然而,在未經pH調控的對照樣CV中開始出現氧化反應的起始電位為-0.1V,且直到0.2V才出現氧化峰,此時峰值電流只有1.2mA.可見,pH值對MES中電化學微生物影響很大. 圖6B為MES陰極CV特性曲線,圖中實驗樣和對照樣陰極都是在-0.7V時開始發生還原反應,隨著電位變得更負,還原反應更加劇烈.
為進一步研究電極表面生物膜情況,對MES陰陽兩極進行SEM表征,如圖6C, D, E, F所示.可見,對照樣陰陽兩極表面附著比較稀疏的生物膜,而實驗樣的陰陽兩極表面均形成了致密的生物膜. 對于陽極表面微生物主要是長條橢圓形和短粗橢圓形構成的成片致密膜層,而陰極微生物主要是長條橢圓形微生物構成團簇分布在電極表面.
通過圖6實驗樣和對照樣的對比發現,低pH值(4.5)的產氫發酵尾液嚴重抑制微生物在MES中活性,即使經過60d培養,微生物在電極上的生長依舊極為緩慢;而經過產氫移除質子后的尾液,適合微生物生長,僅僅21d,在電極上形成了致密的生物膜,其電極也具有更好性能.
3 結論
3.1 在MEC中,隨著陰極不斷將H+還原為H2,發酵尾液pH值逐漸從4.5上升到8.7,pH的提高使得微生物活性恢復,這促進有機物進一步水解并伴隨氫氣產生,整個過程既實現調控暗發酵尾液pH值的目的,還實現氫氣的回收(產氫3.65mmol).
3.2 使用厭氧發酵與MES構成的耦合系統處理調控后的尾液,在21d的降解處理時間內,甲烷產量達到18.8mmol,COD去除率達89%;反之,未經pH調控的暗發酵尾液在該系統中,60d內幾乎無法被降解,甲烷產量幾乎為零.與此同時,實驗樣也表現出更好的電流、電極性能,這一系列結果表明,經過pH調控后的尾液,更適合微生物生長,使得耦合系統具有更高的降解效率和產甲烷速率.
[1] Zhang D, Wang J, Lin Y, et al., Present situation and future prospect of renewable energy in China [J]. Renewable and Sustainable Energy Reviews, 2017,76:865-871.
[2] Chu S, Majumdar A, Opportunities and challenges for a sustainable energy future [J]. Nature, 2012,488(7411):294-303.
[3] 劉晶晶,孫永明,孔曉英,等.不同接種條件下微生物燃料電池產電特性分析 [J]. 中國環境科學, 2011,31(10):1651-1656. Liu J J, Sun Y M, Kong X Y, et al. Power-generation performance of microbial fuel cells with different inoculations [J]. China Environmental Science, 2011,31(10):1651-1656.
[4] 馮雅麗,于 蓮,李浩然,等.微生物燃料電池降解焦化廢水過程研究 [J]. 中國環境科學, 2018,38(11):4099-4105. Feng Y L, Yu L, Li H R, et al. The degradation process of coking wastewater by microbial fuel cells [J]. China Environmental Science, 2018,38(11):4099-4105.
[5] Kumar G, Shobana S, Nagarajan D, et al., Biomass based hydrogen production by dark fermentation-recent trends and opportunities for greener processes [J].Current Opinion in Biotechnology, 2018,50: 136-145.
[6] Seifert K, Zagrodnik R, Stodolny M, et al., Biohydrogen production from chewing gum manufacturing residue in a two-step process of dark fermentation and photofermentation [J]. Renewable Energy, 2018,122:526-532.
[7] Himmel M E, Ding S-Y, Johnson D K, et al., Biomass recalcitrance: engineering plants and enzymes for biofuels production [J]. Science, 2007,315(5813):804-807.
[8] Hwang M H, Jang N J, Hyun S H, et al., Anaerobic bio-hydrogen production from ethanol fermentation: the role of pH [J]. Journal of Biotechnology, 2004,111(3):297-309.
[9] Chen Y, Cheng J J, Creamer K S. Inhibition of anaerobic digestion process: a review [J]. Bioresource Technology, 2008,99(10):4044- 4064.
[10] Hanaki K, Hirunmasuwan S, Matsuo T, Protection of methanogenic bacteria from low pH and toxic materials by immobilization using polyvinyl alcohol [J]. Water Research, 1994,28(4):877-885.
[11] Cai W, Han T, Guo Z, et al. Methane production enhancement by an independent cathode in integrated anaerobic reactor with microbial electrolysis [J]. Bioresource Technology, 2016,208:13-18.
[12] Ghimire A, Valentino S, Frunzo L, et al. Biohydrogen production from food waste by coupling semi-continuous dark-photofermentation and residue post-treatment to anaerobic digestion: A synergy for energy recovery [J]. International Journal of Hydrogen Energy, 2015,40(46): 16045-16055.
[13] Tao B, Passanha P, Kumi P, et al. Recovery and concentration of thermally hydrolysed waste activated sludge derived volatile fatty acids and nutrients by microfiltration, electrodialysis and struvite precipitation for polyhydroxyalkanoates production [J]. Chemical Engineering Journal, 2016,295:11-19.
[14] Dou Z, Dykstra C M, Pavlostathis S G. Bioelectrochemically assisted anaerobic digestion system for biogas upgrading and enhanced methane production [J]. Science of the Total Environment, 2018,633: 1012-1021.
[15] Park J, Lee B, Tian D, et al. Bioelectrochemical enhancement of methane production from highly concentrated food waste in a combined anaerobic digester and microbial electrolysis cell [J]. Bioresource Technology, 2018,247:226-233.
[16] Rabaey K, Rozendal R A. Microbial electrosynthesis - revisiting the electrical route for microbial production [J]. Nature Reviews Microbiology, 2010,8(10):706-716.
[17] Balch W, Fox G, Magrum L, et al. Methanogens: reevaluation of a unique biological group [J]. Microbiological reviews, 1979,43(2):260.
[18] Nichols E M, Gallagher J J, Liu C, et al. Hybrid bioinorganic approach to solar-to-chemical conversion [J]. Proceedings of the National Academy of Sciences of the United States of America, 2015,112(37): 11461-11466.
[19] Findlay R H, King G M, Watling L. Efficacy of phospholipid analysis in determining microbial biomass in sediments [J]. Applied and Environmental Microbiology, 1989,55(11):2888-2893.
[20] Lee Y J, Miyahara T, Noike T. Effect of pH on microbial hydrogen fermentation [J]. Journal of Chemical Technology & Biotechnology, 2002,77(6):694-698.
[21] Jourdin L, Freguia S, Donose B C, et al. Autotrophic hydrogen- producing biofilm growth sustained by a cathode as the sole electron and energy source [J]. Bioelectrochemistry, 2015,102:56-63.
[22] Katuri K, Ferrer M L, Gutiérrez M C, et al. Three-dimensional microchanelled electrodes in flow-through configuration for bioanode formation and current generation [J]. Energy & Environmental Science, 2011,4(10):4201.
Degradation of dark fermentation effluents for biogas production using bioelectrochemical systems.
LU Jian-hong1,2, LI Zhuo1,2, SUN Chi-He1,2, FU Qian1,2*, LI Jun1,2, ZHANG Liang1,2, LIAO Qiang1,2, ZHU Xun1,2
(1.Key Laboratory of Low-grade Energy Utilization Technologies and Systems, Ministry of Education, Chongqing University, Chongqing 400030, China;2.Institute of Engineering Thermophysics, School of Energy and Power Engineering, Chongqing University, Chongqing 400030, China)., 2019,39(10):4157~4163
Dark fermentation for H2production was a promising bioenergy, as it could use straw and/or wastewater containing high organics as raw materials. The accumulated volatile fatty acids (VFAs), which were produced during the process of hydrogen fermentation, significantly inhibit the process of hydrogen production in the dark fermentation. Herein, bioelectrochemical system (BES) was used to treat the effluent of dark fermentation. A microbial electrolysis cell (MEC) was firstly used to treat the effluents of dark fermentation. Accompanied with hydrogen production in MEC, the pH value of the effluents increased from 4.5 to 8.7. Then the near-neutral effluents were used for methane production using a single-chamber microbial electrosynthesis system (MES), in which methanogens acted as biocatalysts to reduce CO2to CH4. The results showed that the chemical oxygen demand (COD) removal efficiency and CH4production rate of single-chamber MES were 89% and 4.5mmol/(L×d), respectively, significantly higher than that without any treatment.
bioelectrochemical system;dark fermentation effluents;adjusting pH;degradation of organic solutions;methane
X703
A
1000-6923(2019)10-4157-07
盧建宏(1991-),男,廣西桂林人,重慶大學碩士研究生,主要從事微生物電化學系統陰極還原二氧化碳成甲烷的研究.
2019-03-18
國家自然科學基金資助項目(51776025,51622602,51606022);重慶市留學人員創業創新支持計劃(cx2017017);中央高校基本科研業務經費項目(2018CDXYDL0001)
* 責任作者, 研究員, fuqian@cqu.edu.cn

