月桂酰單乙醇酰胺硫酸鈉分子有序組合體的研究
萬笑可 肖華英 許虎君
(江南大學化學與材料工程學院, 江蘇無錫,214122)
傳統的表面活性劑是具有單一親水基和親油基的雙親分子結構的物質,在水溶液中,其分子易吸附在界(表) 面上,并定向排列,降低體系的界(表) 面張力。同時,分子中的非極性基團(親油基)易于相互吸引,并締合成分子有序組合體——膠束。近年來,表面活性劑的分子有序組合體在科學研究及工業應用上得到了很大的發展。表面活性劑的締合特性對很多外界因素非常敏感。而表面活性劑濃度、醇和無機鹽作為添加劑,通常強烈影響表面活性劑的自組織行為,在學術研究和工業上使用的各類表面活性劑均來源于含有醇等雜質的原材料。因此,進行這些物質對表面活性劑分子有序組合體的影響研究變得十分重要。本文研究了月桂酰單乙醇酰胺硫酸鈉表面活性劑水溶液膠束聚集行為,為應用工作提供參考。
1 實驗
1.1 試劑與儀器
C12MSN為本實驗室合成,含量98.4%,30℃時臨界膠束濃度是2.79×10-3mol/L;丙醇、丁醇、戊醇、氯化鈉均為分析純,上海化學試劑有限公司;芘(Aldrich產品,99.0%);二苯甲酮(CP級,上海群力化工廠);超純水(無錫新中亞微電子研究所,電導率7.8×10-7S/㎝)。K10T表面張力儀;島津RF-530PC熒光光度計;KQ-100B型超聲波清洗器。
表面活性劑溶液(或加入一定的醇溶液)以芘的飽和水溶液為溶劑配制;猝滅劑二苯甲酮用無水甲醇配制成一定濃度的溶液備用:在潔凈干燥的具塞三角瓶中準確移取一定量的二苯甲酮的甲醇溶液用純氮氣吹趕甲醇至干,用移液管精確移入配制好的表面活性劑溶液,在超聲波浴槽中分散10min后置于恒溫水浴中恒溫16h。 熒光光度計的激發波長為335 nm,在372 nm波長處讀取熒光讀數I372。
根據公式:
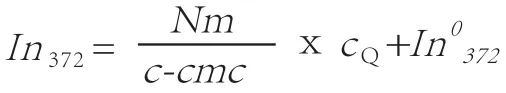
用作圖法求取膠束聚集數(Nm),上式中cQ為猝滅劑濃度,In0372為猝滅劑濃度為0時的In372。
2 結果與討論
2.1 合適的探針濃度[1]
熒光探針芘在膠束中的分布遵循poisson分布規律。當cP/cQ≤1時可以確保每個膠束中增溶一個芘分子。芘在水中的溶解度極小,約為7.0×10-7mol/L。用芘的飽和水溶液為溶劑配制表面活性劑溶液。由于芘在飽和水溶液中已經以分子狀態存在,從而極大地改善了芘在表面活性劑膠束溶液中的分散和分布狀況。這樣既可以滿足cP/cQ≤1又可以保證在測試液中I372值恒定,使得In372~cQ線性關系良好。因此,芘應為飽和濃度。
2.2 合適的猝滅劑濃度
在表面活性劑濃度為5倍cmc濃度時,在猝滅劑濃度為0~4mmol/L范圍內測定I372, 以相鄰五個cQ值點與In372進行線性回歸,求得一個Nm, 將Nm對cQ值作圖,結果見圖1。
從圖1中找出Nm隨cQ變化緩慢的區域其所對應的范圍即為猝滅劑合適濃度范圍。熒光探針法測定膠束聚集數時,探針和猝滅劑均被膠束增溶,從而引起膠束大小和形狀改變。因此,探針濃度確定后,在保證cP/cQ<1的前提下猝滅劑濃度不宜過高。從圖1中可以看到的合適猝滅劑濃度范圍為小于1.0mmol/L。

圖1 C12MSN的Nm與cQ的關系
2.3 Nm的C12MSN濃度效應
以芘的飽和溶液配制不同濃度的C12MSN系列溶液,用穩態熒光法測定不同濃度C12MSN溶液的Nm,并做Nm~c圖,如圖2所示。
從圖2可以看出:Nm不是一個常量,而是一個變量。并且,它隨表面活性劑濃度的增大而增大。傳統表面活性劑濃度在10倍cmc以內可測得其球形膠束合適的Nm。但MSN在較低濃度時,測得的Nm很小。分析其原因:是由于表面活性劑在分子有序組合體中的排列受兩種作用力的控制,一種是烷烴鏈間的疏水相互作用,它是表面活性劑自發組成分子有序組合體的驅動力;另一種是頭基間由于靜電斥力或水化層阻力造成的彼此之間的排斥。對于C12MSN而言,后者的作用力遠大于前者,故不利于緊密組合體的生成。因此,在較低濃度時,由于膠束中表面活性劑分子間比較疏松,導致表面活性劑自發組成分子有序聚集體驅動力的烷烴間疏水相互作用力比較低,并且,不能增溶足夠的探針和猝滅劑,影響了探針和猝滅劑在膠束中的Poisson分布,所以,測得的結果比較低。當表面活性劑的濃度大于10倍cmc時,測定的結果較高,可能是由于表面活性劑濃度不斷增加,原來較規整的球狀膠束不能再融入表面活性劑單體,因此,更多的表面活性劑通過纏繞、扭曲在原來的球狀膠束上聚集,形成不規整的棒狀、層狀及囊泡狀結構,導致膠束聚集數測定結果較高。在4~9倍cmc區間內,膠束聚集數Nm隨表面活性劑濃度C線性增大,變化規律遵循方程:
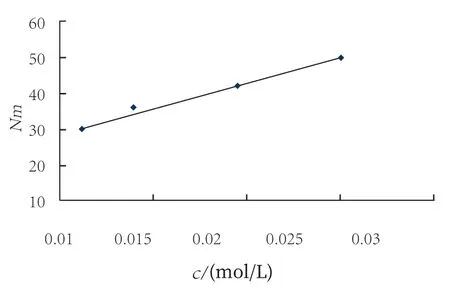
圖2 C12MSN的Nm與cC12MSN濃度的關系
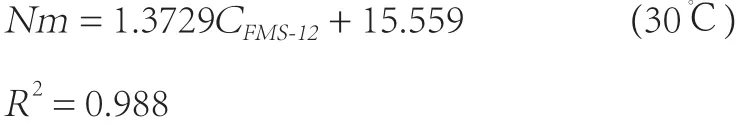
可見膠束聚集數具有濃度依賴性。在一定表面活性劑濃度范圍內,膠束聚集數隨濃度增大而線性增大,并不是定值。
2.4 Nm的醇效應
以5倍cmc的表面活性劑飽和芘溶液加入不同的醇(丙醇,丁醇,戊醇)中,用穩態熒光法測定膠束聚集數。
從圖3中看出:膠束聚集數隨醇濃度的增大而減小,醇的碳鏈越短其減小得越明顯。這可能是由于醇參與組成了混合膠束,即:醇將烷烴鏈插入膠束內核中,羥基則位于膠束表面的柵欄層間,從而,降低了膠束表面柵欄層中表面活性劑分子頭基間的靜電斥力,也可能是降低了介質的介電常數,從而,提高了溶液中的靜電相互作用,使膠束聚集數減小。
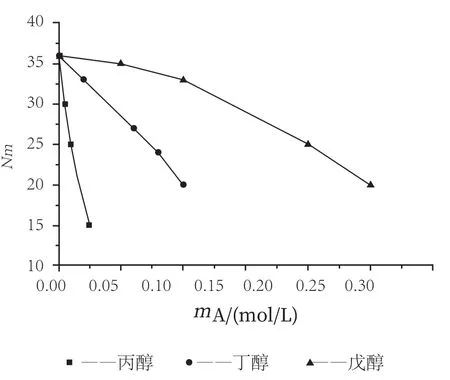
圖3 Nm 隨醇的變化
2.5 Nm的鹽效應
在表面活性劑濃度為5倍cmc時測定。
傳統的單親水基離子型表面活性劑形成的膠束,由于電荷的存在,膠束/水界面存在雙電層,水分子形成了親水基的水化膜,無機鹽NaCl的加入,部分破壞了水化膜,壓縮了離子基團周圍的擴散雙電層,屏蔽了電荷之間的排斥力,導致其膠束的Nm值顯著提高。從圖4中可以看出:C12MSN的膠束聚集數隨鹽的濃度增大而增大,但由于引入了酰胺基,Nm值的提高并不是特別顯著。

圖4 Nm隨NaCl濃度的變化
2.6 膠束內核的微極性
在芘的熒光圖譜上檢出I1和I3,其比值反映探針芘周圍環境膠束內核的微極性。
從表1中可以看出:膠束內核的微極性隨表面活性劑濃度和無機鹽濃度的增大而減小。表面活性劑形成的膠束中,芘應增溶在靠近表面活性劑極性頭的柵欄層之間。C12MSN濃度及膠束聚集數的增大勢必造成表面活性劑分子排列更加緊密,迫使原本滲透到柵欄層中的水進入本體中去,同時芘分子也向膠束內部轉移,使其所處微環境的極性變小,所以I1/ I3值隨濃度的增大而變小;在c(C12MSN)大于其cmc時,芘處于C12MSN的膠束中,當沒有無機鹽存在時,芘增溶到膠團靠近極性頭的柵欄層之間,此處由于存在部分水分子而具有較強的極性,而無機鹽的加入, 破壞了膠束周圍的水化膜,更重要的是壓縮了離子基團周圍的擴散雙電層,屏蔽了電荷之間的斥力,表面活性劑分子之間排列得更加緊密,迫使原本滲透到柵欄層中的水分子進入本體水中,同時芘分子向膠團內部移動,所處含無機鹽的環境極性變小。

表1 芘的I1/ I3隨表面活性劑濃度及加入鹽濃度的變化關系

3 結論
C12MSN的膠束聚集數隨其濃度的增大而增大;醇的加入使膠束聚集數減小,并且隨著烷烴鏈的減小降低幅度更加明顯;C12MSN的膠束聚集數隨鹽的濃度增大而增大。膠束內核的微極性隨表面活性劑濃度和無機鹽濃度的增大而減小。

